कोशिका-नाशक कीमोथेरेपी
5-FU : अश्रुपात (अश्रु वाहिनी संकुचन), नेत्रश्लेष्मलाशोथ, कॉर्नियल उपकला विकार1)
सिस्प्लैटिन : ऑप्टिक न्यूरोपैथी, रंग दृष्टि विकार (दुर्लभ)1)
टैक्सेन (डोसेटैक्सेल, पैक्लिटैक्सेल) : अश्रुपात, सिस्टॉइड मैक्यूलर एडिमा4)

कैंसर रोधी दवाओं और लक्षित चिकित्सा के कारण होने वाले नेत्र दुष्प्रभाव उन रोग स्थितियों का सामूहिक नाम है जिनमें कैंसर उपचार और प्रतिरक्षा रोग उपचार में उपयोग की जाने वाली दवाएं नेत्र ऊतकों में प्रतिकूल घटनाएं उत्पन्न करती हैं।
संबंधित दवा श्रेणियां व्यापक हैं।
कैंसर उपचार में प्रगति के साथ जीवित रहने की अवधि बढ़ गई है, और दीर्घकालिक उपचार के दौरान नेत्र दुष्प्रभावों के प्रबंधन का महत्व बढ़ गया है1)। नेत्र दुष्प्रभाव हल्की असुविधा से लेकर अपरिवर्तनीय दृष्टि हानि तक हो सकते हैं, और उचित जांच एवं शीघ्र हस्तक्षेप दृष्टि पूर्वानुमान से सीधे जुड़ा हुआ है।
यदि दृष्टि में कमी, लालिमा, आँख में दर्द, मक्खियाँ उड़ना, रोशनी की चमक, या विकृति (चीज़ें टेढ़ी दिखना) जैसे लक्षण दिखाई दें, तो तुरंत नेत्र चिकित्सक से परामर्श लें। हल्के लक्षणों को भी नज़रअंदाज़ करने से अपरिवर्तनीय क्षति हो सकती है, इसलिए उपचार करने वाले चिकित्सक (ऑन्कोलॉजिस्ट) को भी सूचित करें और नेत्र चिकित्सक के साथ समन्वय करना महत्वपूर्ण है।
दवा श्रेणी के अनुसार नेत्र दुष्प्रभाव भिन्न होते हैं। नीचे मुख्य दवाएँ और उनके नेत्र लक्षण दिए गए हैं।
कोशिका-नाशक कीमोथेरेपी
5-FU : अश्रुपात (अश्रु वाहिनी संकुचन), नेत्रश्लेष्मलाशोथ, कॉर्नियल उपकला विकार1)
सिस्प्लैटिन : ऑप्टिक न्यूरोपैथी, रंग दृष्टि विकार (दुर्लभ)1)
टैक्सेन (डोसेटैक्सेल, पैक्लिटैक्सेल) : अश्रुपात, सिस्टॉइड मैक्यूलर एडिमा4)
हार्मोन थेरेपी और इम्यूनोमॉड्यूलेटर
टैमॉक्सिफ़ेन : पेरीमैक्यूलर क्रिस्टलीय जमाव, कॉर्नियल व्होरल अपारदर्शिता, सिस्टॉइड मैक्यूलर एडिमा। घटना दर: विदेश में 3-6%, जापान में 0.2%।
HCQ/क्लोरोक्वीन : बुल्स आई मैकुलोपैथी (वलयाकार शोष), दृष्टि में कमी, रतौंधी, रंग दृष्टि असामान्यताएँ। 5 वर्षों से अधिक उपचार पर लगभग 0.5%।
इंटरफेरॉन : फंडस के पश्च ध्रुव पर छोटे रक्तस्राव और कॉटन-वूल स्पॉट। प्रशासन के 2-3 महीनों के भीतर। अधिकांश लक्षणहीन और स्वतः ठीक हो जाते हैं।
आणविक लक्षित दवाएं
MEK अवरोधक (ट्रामेटिनिब आदि) : सीरस रेटिनल डिटेचमेंट, PED। घटना दर लगभग 10-25%2)
EGFR अवरोधक (जेफिटिनिब आदि) : ट्राइकियासिस, ब्लेफेराइटिस, कॉर्नियल एपिथेलियल विकार5)
BRAF अवरोधक (वेमुराफेनिब आदि) : यूवाइटिस, सीरस रेटिनल डिटेचमेंट6)
ALK अवरोधक (क्रिज़ोटिनिब आदि) : फोटोप्सिया, धुंधली दृष्टि। लगभग 60% में दृश्य हानि होती है7)
इम्यून चेकपॉइंट अवरोधक (ICI)
यूवाइटिस (पूर्वकाल, पश्च, पैनुवाइटिस) : घटना दर लगभग 1%3)
VKH जैसा सिंड्रोम : गंभीर रूप जिसमें उच्च खुराक स्टेरॉयड की आवश्यकता होती है3)
ड्राई आई, कंजक्टिवाइटिस, ऑर्बिटल इंफ्लेमेटरी रोग, एक्स्ट्राओकुलर मायोसाइटिस8)
ADC (T-DXd आदि) : कॉर्नियल विकार (सतही पंक्टेट केराटोपैथी, कॉर्नियल स्ट्रोमल ओपेसिटी)10)
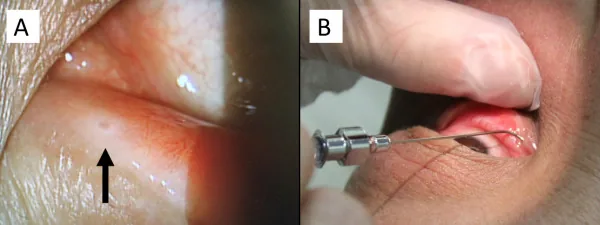
मल्टीपल स्केलेरोसिस के रिलैप्स को रोकने के लिए उपयोग किया जाने वाला फिंगोलिमोड (इमुसेरा/गिलेनिया) मैक्यूलर एडिमा का कारण बन सकता है। मैक्यूलर एडिमा की घटना दर फिंगोलिमोड 0.5 मिलीग्राम/दिन पर 0.2% और 1.25 मिलीग्राम/दिन पर 1.4% है, जो अधिकतर उपचार शुरू करने के 3-4 महीनों के भीतर होती है।
दवा श्रेणी के अनुसार नेत्र संबंधी दुष्प्रभावों के जोखिम कारक भिन्न होते हैं।
| दवा श्रेणी | प्रमुख जोखिम कारक |
|---|---|
| HCQ/क्लोरोक्वीन | 5 वर्ष से अधिक उपचार अवधि, CQ >3.0 mg/kg/दिन या HCQ >6.5 mg/kg/दिन, वृद्धावस्था, गुर्दे/यकृत की शिथिलता, रेटिना रोग सहवर्ती |
| टैमोक्सीफेन | उच्च खुराक और दीर्घकालिक उपयोग (संचयी खुराक में वृद्धि) |
| इंटरफेरॉन | उच्च प्रारंभिक खुराक, वृद्धावस्था, मधुमेह, उच्च रक्तचाप, एनीमिया |
| MEK अवरोधक | खुराक पर निर्भर (उच्च खुराक पर आवृत्ति बढ़ जाती है) 2) |
| ICI | प्रणालीगत irAE (थायरॉयडिटिस, कोलाइटिस आदि) वाले रोगियों में नेत्र irAE भी आसानी से होते हैं 3) |
| ADC | दवा-विशिष्ट कॉर्नियल विषाक्तता तंत्र 10) |
HCQ रेटिनोपैथी के विशिष्ट जोखिम कारक निम्नलिखित हैं:
इंटरफेरॉन रेटिनोपैथी मधुमेह, उच्च रक्तचाप, एनीमिया जैसी प्रणालीगत बीमारियों की उपस्थिति में अधिक बार और गंभीर होती है, और उपचार-प्रतिरोधी या पुनरावर्ती मामलों में भी अधिक आसानी से होती है।
AAO (अमेरिकन एकेडमी ऑफ ऑप्थैल्मोलॉजी) की सिफारिशों9) के आधार पर, निम्नलिखित स्क्रीनिंग की जाती है:
उपयोगी जांचों में हम्फ्री 10-2 केंद्रीय दृश्य क्षेत्र परीक्षण, SD-OCT, फंडस ऑटोफ्लोरेसेंस, मल्टीफोकल ERG और फुल-फील्ड ERG शामिल हैं। बुल्स आई (वलयाकार शोष) उन्नत HCQ रेटिनोपैथी का एक विशिष्ट फंडस निष्कर्ष है।
| दवा | स्क्रीनिंग का समय और जांच |
|---|---|
| HCQ/क्लोरोक्वीन | उपचार शुरू करने पर आधार रेखा + 5 वर्षों के बाद वार्षिक (SD-OCT, 10-2 दृश्य क्षेत्र, FAF) 9) |
| टैमोक्सीफेन | लक्षण प्रकट होने पर और नियमित रूप से फंडस जांच और SD-OCT |
| इंटरफेरॉन | उपचार शुरू करने के 2-3 महीने बाद फंडस जांच। लक्षण होने पर तुरंत नेत्र चिकित्सक से परामर्श |
| MEK अवरोधक | दृष्टि में कमी या विकृति दृष्टि होने पर OCT द्वारा सीरस रेटिना डिटेचमेंट की पुष्टि 2) |
| ICI | दृष्टि में कमी, लालिमा या आंख में दर्द होने पर तुरंत नेत्र चिकित्सक से परामर्श 3) |
| फिंगोलिमॉड | उपचार से पहले आधार रेखा फंडस जांच + उपचार के 3-4 महीने बाद अनुवर्ती |
ICI उपयोगकर्ताओं में दृष्टि में कमी, लालिमा या आंख में दर्द होने पर, पूर्वकाल कक्ष में सूजन कोशिकाएं, कांच का धुंधलापन और कोरॉइडल घावों का मूल्यांकन करें, और irAE के रूप में यूवाइटिस या VKH जैसे सिंड्रोम की संभावना पर विचार करें 3).
उपचार शुरू करते समय आधार रेखा के रूप में दृश्य तीक्ष्णता, फंडस और एसडी-ओसीटी सहित नेत्र परीक्षण कराने की सिफारिश की जाती है। इसके बाद, यदि कोई जोखिम कारक (5 वर्ष से अधिक उपचार अवधि, उच्च खुराक, वृद्धावस्था, गुर्दे की शिथिलता आदि) नहीं हैं, तो 5 वर्ष के बाद से वार्षिक जांच शुरू करें। यदि जोखिम कारक मौजूद हैं, तो पहले और अधिक बार जांच की आवश्यकता होती है। मुख्य जांच में एसडी-ओसीटी, हम्फ्री 10-2 दृश्य क्षेत्र परीक्षण और फंडस ऑटोफ्लोरेसेंस शामिल हैं।
दवा बंद करना ही एकमात्र उपचार है। शरीर से निष्कासन धीमा होने के कारण, दवा बंद करने के बाद भी घाव बढ़ और बिगड़ सकते हैं। इसलिए शीघ्र पहचान अत्यंत महत्वपूर्ण है, और अपरिवर्तनीय क्षति होने से पहले दवा बंद करने का निर्णय दृष्टि के पूर्वानुमान को निर्धारित करता है।
अधिकांश मामलों का पूर्वानुमान अच्छा होता है; यदि कोई लक्षण नहीं हैं, तो मूल रूप से आईएफएन थेरेपी समाप्त होने तक प्रतीक्षा करें। गंभीर मामलों या दृष्टि हानि में, आईएफएन की खुराक कम करने या बंद करने पर विचार करें। मधुमेह या उच्च रक्तचाप के साथ मामलों में शीघ्र उपचार आवश्यक है।
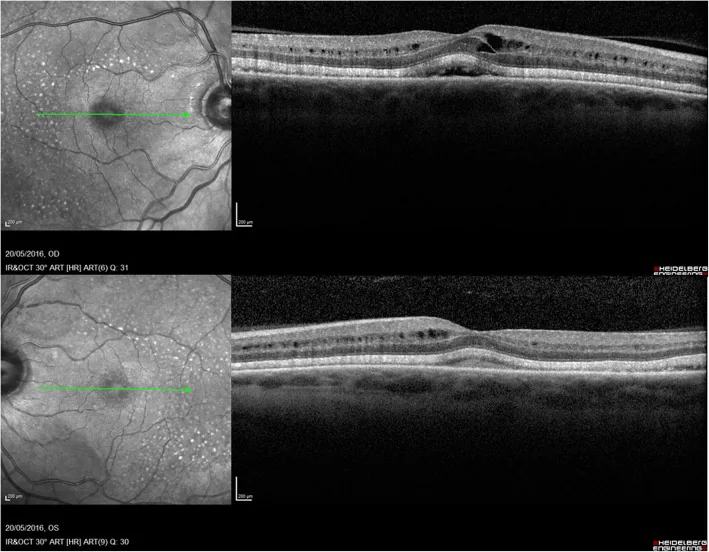
CTCAE ग्रेड के आधार पर प्रबंधन करें 3)।
अधिकांश मामलों में दवा बंद करने से सुधार होता है। आवश्यकतानुसार NSAIDs आई ड्रॉप या स्टेरॉयड आई ड्रॉप का उपयोग किया जा सकता है।
हमेशा उपचार बंद करना आवश्यक नहीं है। आंखों के दुष्प्रभावों की गंभीरता (CTCAE ग्रेड) और दवा के प्रकार के अनुसार प्रबंधन भिन्न होता है। कुछ मामलों में, जैसे HCQ रेटिनोपैथी या टैमोक्सीफेन रेटिनोपैथी, दवा बंद करना मूल नियम है, जबकि MEK अवरोधकों के कारण हल्के सीरस रेटिनल डिटेचमेंट या EGFR अवरोधकों के कारण ट्राइकियासिस में, लक्षणात्मक उपचार के साथ दवा जारी रखने का विकल्प चुना जा सकता है। ऑन्कोलॉजिस्ट और नेत्र रोग विशेषज्ञ के बीच समन्वय से प्रत्येक स्थिति के अनुसार निर्णय लेना महत्वपूर्ण है।
दवा श्रेणी के अनुसार आंखों के ऊतकों को क्षति पहुंचाने के तंत्र भिन्न होते हैं।
CQ और HCQ में मेलेनिन के प्रति उच्च आकर्षण होता है और ये रेटिनल पिगमेंट एपिथेलियम (RPE) कोशिकाओं के मेलेनिन ग्रैन्यूल से जुड़कर कोशिकाओं में जमा हो जाते हैं। संचित CQ/HCQ लाइसोसोम में ले जाया जाता है, जिससे लाइसोसोम का pH बढ़ जाता है और लाइसोसोमल एंजाइमों की गतिविधि बाधित होती है। RPE के एंजाइमेटिक चयापचय कार्य में बाधा आने पर फोटोरिसेप्टर बाहरी खंडों का विघटन और नवीनीकरण बाधित होता है, जिससे फोटोरिसेप्टर अध:पतन होता है। शरीर में संचय की अधिक मात्रा के कारण, दवा बंद करने के बाद भी क्षति बढ़ सकती है।
तंत्रिका फाइबर परत और आंतरिक प्लेक्सीफॉर्म परत में गोलाकार घाव (तंत्रिका फाइबर अध:पतन और अक्षीय सूजन) बनते हैं। क्रिस्टलीय जमा को कैल्शियम और जटिल कार्बोहाइड्रेट युक्त अध:पतन उत्पाद माना जाता है जो तंत्रिका फाइबर के अंदर जमा होते हैं। सिस्टॉइड मैक्यूलर एडिमा (CME) मुलर कोशिकाओं की शिथिलता और द्रव संचय के कारण होता है।
IFN वाहिकासंकुचन, श्वेत रक्त कोशिका घुसपैठ और संवहनी एंडोथेलियल क्षति को प्रेरित करता है। प्रतिरक्षा कॉम्प्लेक्स केशिकाओं में जमा हो जाते हैं, जिससे केशिका अवरोध होता है। अवरुद्ध केशिकाओं के आगे (धमनी की ओर) कपास-ऊन के धब्बे (तंत्रिका फाइबर परत रोधगलन) दिखाई देते हैं, और अवरोध स्थल पर रक्तस्राव छोटे रक्तस्राव के रूप में देखा जाता है। अधिकांश मामलों में ये क्षणिक होते हैं और IFN बंद करने के बाद गायब हो जाते हैं।
MEK अवरोधक MAPK/ERK मार्ग (कोशिका प्रसार और उत्तरजीविता संकेत) को अवरुद्ध करते हैं। RPE ERK संकेत द्वारा सक्रिय परिवहन (आयन और पानी) बनाए रखता है, इसलिए ERK अवरोध से RPE के आयन परिवहन और पंप कार्य में बाधा आती है। इसके परिणामस्वरूप रेटिना के नीचे द्रव संचय होता है, जो सीरस रेटिनल डिटेचमेंट और रेटिनल पिगमेंट एपिथेलियल डिटेचमेंट (PED) के रूप में प्रकट होता है2)।
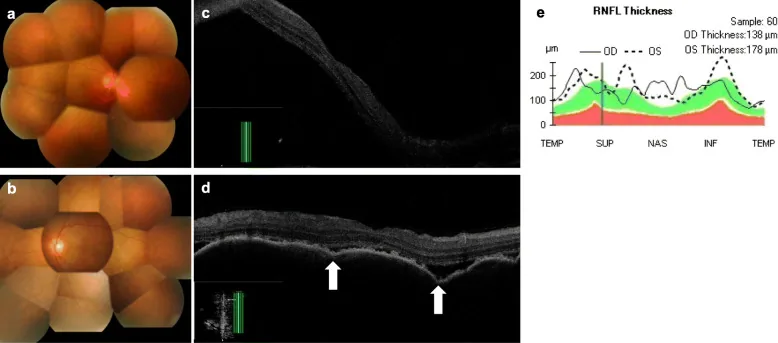
ICI (PD-1/PD-L1 अवरोधक, CTLA-4 अवरोधक) टी कोशिकाओं के इम्यून चेकपॉइंट को हटाकर एंटीट्यूमर प्रतिरक्षा को बढ़ाते हैं। लेकिन यह तंत्र ऑटोइम्यून दमन तंत्र को भी हटा देता है, जिससे आंख के ऊतकों (यूविया, स्क्लेरा, कक्षा, लैक्रिमल ग्रंथि) में ऑटोइम्यून प्रतिक्रिया उत्पन्न होती है। VKH जैसे सिंड्रोम में मेलानोसाइट्स (कोरॉइड, सिलिअरी बॉडी, आइरिस) के प्रति ऑटोरिएक्टिव टी कोशिकाएं सक्रिय हो जाती हैं, जिससे पैनुवाइटिस, सीरस रेटिनल डिटेचमेंट और डिपिग्मेंटेशन घाव होते हैं 3)।
ICI-संबंधित ओकुलर irAE की समग्र तस्वीर प्राप्त करने के लिए अंतरराष्ट्रीय बहु-केंद्रीय रजिस्ट्री अध्ययन चल रहे हैं 3)। यूवाइटिस, VKH जैसे सिंड्रोम, एक्स्ट्राओकुलर मायोसिटिस आदि विविध ओकुलर irAE के स्पेक्ट्रम, आवृत्ति और परिणामों को स्पष्ट करके, जोखिम स्तरीकरण और प्रोटोकॉल स्थापना की उम्मीद है।
ट्रैस्टुज़ुमैब डेरक्सटेकन (T-DXd) सहित ADC अगली पीढ़ी की कैंसर चिकित्सा के रूप में फैल रहे हैं, लेकिन कॉर्नियल विषाक्तता (पंक्टेट सुपरफिशियल केराटोपैथी, कॉर्नियल स्ट्रोमल ओपेसिटी) को प्रतिकूल घटना के रूप में पहचाना गया है 10)। दवा निगरानी अध्ययनों द्वारा मामलों का संग्रह और कॉर्नियल सुरक्षा रणनीतियों की स्थापना चुनौतीपूर्ण है।
अनुकूली प्रकाशिकी OCT और मल्टीस्पेक्ट्रल फंडस इमेजिंग द्वारा पारंपरिक तरीकों से अज्ञात प्रारंभिक RPE संरचना परिवर्तनों के दृश्यीकरण का प्रयास किया जा रहा है 11)। इसके अलावा, कृत्रिम बुद्धिमत्ता (AI) का उपयोग करके OCT छवि विश्लेषण द्वारा स्वचालित स्क्रीनिंग का विकास भी प्रगति पर है, जिससे छूटने के जोखिम में कमी की उम्मीद है 11)।
ICI और लक्षित चिकित्सा के प्रसार के साथ, नेत्र विज्ञान और ऑन्कोलॉजी के बीच मानकीकृत सहयोग प्रोटोकॉल की स्थापना आवश्यक है 8)। CTCAE ग्रेडिंग पर आधारित ओकुलर साइड इफेक्ट प्रबंधन एल्गोरिदम के दिशानिर्देशीकरण की प्रक्रिया चल रही है।
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.