Kemoterapi sitotoksik
5-FU: Lakrimasi (stenosis duktus lakrimalis), konjungtivitis, gangguan epitel kornea1)
Sisplatin: Neuropati optik, gangguan penglihatan warna (jarang)1)
Taksan (dosetaksel, paklitaksel): Lakrimasi, edema makula kistoid4)

Efek samping mata akibat obat antikanker dan obat target molekuler adalah istilah umum untuk kondisi di mana obat yang digunakan untuk pengobatan kanker dan penyakit imun menyebabkan efek samping pada jaringan mata.
Kategori obat yang terlibat sangat luas.
Seiring kemajuan pengobatan kanker, masa bertahan hidup meningkat, dan manajemen efek samping okular selama pengobatan jangka panjang menjadi semakin penting1). Efek samping okular berkisar dari ketidaknyamanan ringan hingga gangguan penglihatan ireversibel, dan skrining yang tepat serta intervensi dini berhubungan langsung dengan prognosis penglihatan.
Jika muncul gejala seperti penurunan penglihatan, mata merah, nyeri mata, floaters, kilatan cahaya, metamorphopsia (benda terlihat terdistorsi), segera konsultasikan ke dokter mata. Meskipun gejalanya ringan, mengabaikannya dapat menyebabkan kerusakan ireversibel, oleh karena itu penting untuk melaporkan ke dokter utama (onkologi) dan berkoordinasi dengan dokter mata.
Efek samping okular berbeda tergantung kategori obat. Berikut adalah obat utama dan gejala okularnya.
Kemoterapi sitotoksik
5-FU: Lakrimasi (stenosis duktus lakrimalis), konjungtivitis, gangguan epitel kornea1)
Sisplatin: Neuropati optik, gangguan penglihatan warna (jarang)1)
Taksan (dosetaksel, paklitaksel): Lakrimasi, edema makula kistoid4)
Terapi hormon dan obat imunomodulator
Tamoksifen: Deposit kristalin perimakula, kekeruhan kornea spiral, edema makula kistoid. Insidensi: 3-6% di luar negeri, 0,2% di dalam negeri
HCQ/klorokuin: Makulopati bull’s eye (atrofi annular), penurunan penglihatan, rabun senja, abnormalitas penglihatan warna. Sekitar 0,5% setelah penggunaan 5 tahun
Interferon: Perdarahan kecil dan bercak putih seperti kapas di kutub posterior fundus. Terjadi dalam 2-3 bulan setelah pemberian. Sebagian besar tanpa gejala dan sembuh spontan.
Obat Target Molekuler
Inhibitor MEK (misalnya trametinib): Ablasi retina serosa dan PED. Insidensi sekitar 10-25%2)
Inhibitor EGFR (misalnya gefitinib): Trikiasis, blefaritis, gangguan epitel kornea5)
Inhibitor BRAF (misalnya vemurafenib): Uveitis, ablasi retina serosa6)
Inhibitor ALK (misalnya krizotinib): Fotopsia, penglihatan kabur. Sekitar 60% mengalami gangguan penglihatan7)
Inhibitor Checkpoint Imun (ICI)
Uveitis (anterior, posterior, panuveitis): Insidensi sekitar 1%3)
Sindrom mirip VKH: Bentuk berat yang memerlukan steroid dosis tinggi3)
Mata kering, konjungtivitis, penyakit inflamasi orbita, miositis ekstraokular8)
ADC (misalnya T-DXd): Gangguan kornea (keratopati punctata superfisial, kekeruhan stroma kornea)10)
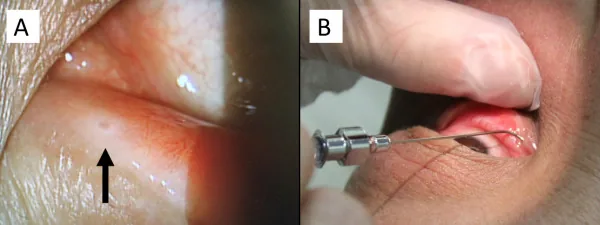
Fingolimod (Imusera/Gilenya) yang digunakan untuk pencegahan kekambuhan multiple sclerosis diketahui menyebabkan edema makula. Insidensi edema makula adalah 0,2% untuk fingolimod 0,5 mg/hari dan 1,4% untuk 1,25 mg/hari, dan sebagian besar terjadi dalam 3-4 bulan setelah memulai pengobatan.
Faktor risiko efek samping mata berbeda untuk setiap kategori obat.
| Kategori Obat | Faktor Risiko Utama |
|---|---|
| HCQ/Klorokuin | Durasi pemberian >5 tahun, CQ >3,0 mg/kg/hari atau HCQ >6,5 mg/kg/hari, usia lanjut, gangguan ginjal/hati, penyakit retina penyerta |
| Tamoksifen | Dosis tinggi dan penggunaan jangka panjang (peningkatan dosis kumulatif) |
| Interferon | Dosis awal tinggi, usia lanjut, diabetes, hipertensi, anemia |
| Inhibitor MEK | Tergantung dosis (frekuensi meningkat pada dosis tinggi) 2) |
| ICI | Pasien dengan irAE sistemik (misalnya tiroiditis, kolitis) lebih rentan mengalami irAE mata 3) |
| ADC | Mekanisme toksisitas kornea spesifik obat 10) |
Faktor risiko spesifik untuk retinopati HCQ meliputi:
Retinopati interferon lebih sering terjadi dan lebih parah pada pasien dengan penyakit sistemik seperti diabetes, hipertensi, dan anemia, serta sering terjadi pada kasus refrakter atau rekuren.
Berdasarkan rekomendasi AAO (American Academy of Ophthalmology)9), dilakukan skrining sebagai berikut:
Pemeriksaan yang berguna meliputi: Humphrey 10-2 lapang pandang sentral, SD-OCT, autofluoresensi fundus, ERG multifokal, dan ERG lapang penuh. Gambaran bull’s eye (atrofi sirkumferensial) merupakan temuan fundus khas pada retinopati HCQ lanjut.
| Obat | Waktu Skrining dan Pemeriksaan |
|---|---|
| HCQ/Klorokuin | Baseline saat awal pemberian + tahunan setelah 5 tahun (SD-OCT, lapang pandang 10-2, FAF) 9) |
| Tamoksifen | Saat muncul gejala dan pemeriksaan fundus rutin serta SD-OCT |
| Interferon | Pemeriksaan fundus 2-3 bulan setelah mulai pemberian. Jika ada gejala, segera periksa ke dokter mata |
| Inhibitor MEK | Saat terjadi penurunan visus atau metamorphopsia, konfirmasi ablasi retina serosa dengan OCT 2) |
| ICI | Saat terjadi penurunan visus, kemerahan, atau nyeri mata, segera periksa ke dokter mata 3) |
| Fingolimod | Pemeriksaan fundus baseline sebelum pemberian + follow-up 3-4 bulan setelah pemberian |
Pada pasien pengguna ICI yang mengalami penurunan visus, kemerahan, atau nyeri mata, lakukan evaluasi sel inflamasi bilik anterior, kekeruhan vitreus, dan lesi koroid, serta pertimbangkan kemungkinan uveitis atau sindrom mirip VKH sebagai irAE 3).
Pada awal pemberian, dianjurkan untuk menjalani pemeriksaan mata yang meliputi visus, fundus, dan SD-OCT sebagai baseline. Setelah itu, jika tidak ada faktor risiko (durasi pemberian >5 tahun, dosis tinggi, usia lanjut, gangguan fungsi ginjal, dll.), skrining tahunan dimulai setelah 5 tahun. Jika ada faktor risiko, pemeriksaan lebih awal dan lebih sering diperlukan. Pemeriksaan utama meliputi SD-OCT, perimetri Humphrey 10-2, dan autofluoresensi fundus.
Satu-satunya terapi adalah penghentian obat. Karena eliminasi dari tubuh lambat, lesi dapat berkembang dan memburuk bahkan setelah penghentian obat. Oleh karena itu, deteksi dini sangat penting, dan keputusan untuk menghentikan obat sebelum terjadi kerusakan ireversibel menentukan prognosis penglihatan.
Sebagian besar kasus memiliki prognosis baik, dan jika asimtomatik, pada dasarnya menunggu hingga terapi IFN selesai. Pada kasus berat atau dengan penurunan visus, pertimbangkan pengurangan dosis atau penghentian IFN. Pada kasus dengan diabetes atau hipertensi, diperlukan penanganan dini.
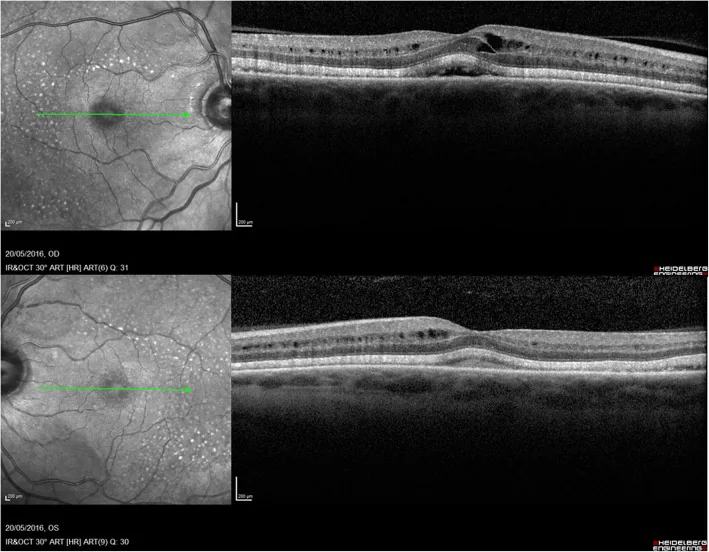
Tata laksana berdasarkan grade CTCAE 3).
Pada banyak kasus, kondisi membaik setelah penghentian pemberian. Jika perlu, dapat diberikan tetes mata NSAID atau steroid.
Tidak selalu harus dihentikan. Penanganan berbeda tergantung pada tingkat keparahan efek samping mata (grade CTCAE) dan jenis obat. Pada beberapa kasus seperti retinopati HCQ atau tamoksifen, penghentian obat adalah dasar, sementara pada kasus lain seperti ablasi retina serosa ringan akibat inhibitor MEK atau trikiasis bulu mata akibat inhibitor EGFR, pengobatan dapat dilanjutkan sambil melakukan terapi simtomatik. Penting bagi dokter onkologi dan dokter mata untuk bekerja sama dalam menentukan keputusan sesuai kondisi masing-masing.
Mekanisme kerusakan jaringan mata berbeda untuk setiap kategori obat.
CQ dan HCQ memiliki afinitas tinggi terhadap melanin, berikatan dengan granula melanin di sel epitel pigmen retina (RPE) dan terakumulasi di dalam sel. Akumulasi CQ/HCQ menyebabkan peningkatan pH lisosom, mengganggu aktivitas enzim lisosom. Ketika fungsi metabolisme enzim RPE terganggu, degradasi dan pembaruan segmen luar fotoreseptor terganggu, menyebabkan degenerasi fotoreseptor. Karena jumlah akumulasi dalam tubuh besar, kerusakan dapat berlanjut bahkan setelah penghentian obat.
Terbentuk lesi bulat (degenerasi serabut saraf dan pembengkakan akson) di lapisan serabut saraf dan lapisan pleksiform dalam. Endapan kristalin dianggap sebagai produk degenerasi yang mengandung kalsium dan karbohidrat kompleks yang mengendap di dalam serabut saraf. Edema makula kistoid (CME) terjadi akibat disfungsi sel Müller dan akumulasi cairan.
IFN menginduksi vasospasme, infiltrasi leukosit, dan kerusakan endotel vaskular, menyebabkan deposisi kompleks imun di kapiler yang mengakibatkan oklusi kapiler. Di sisi arteri dari kapiler yang tersumbat, muncul bercak putih seperti kapas (infark lapisan serabut saraf), dan perdarahan kecil terlihat sebagai perdarahan titik. Sebagian besar bersifat sementara dan menghilang setelah penghentian IFN.
Inhibitor MEK memblokir jalur MAPK/ERK (sinyal proliferasi dan kelangsungan hidup sel). RPE mempertahankan transpor aktif (ion dan air) melalui sinyal ERK, sehingga inhibisi ERK mengganggu fungsi transpor ion dan pompa RPE. Akibatnya, terjadi akumulasi cairan subretina, yang bermanifestasi sebagai ablasi retina serosa dan ablasi epitel pigmen retina (PED)2).
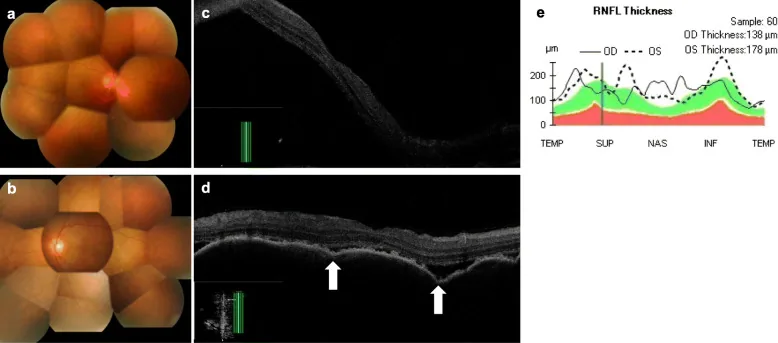
ICI (inhibitor PD-1/PD-L1, inhibitor CTLA-4) membebaskan checkpoint imun sel T dan meningkatkan imunitas antitumor. Namun, mekanisme ini juga membebaskan mekanisme supresi autoimun, memicu reaksi autoimun pada jaringan mata (uvea, sklera, orbita, kelenjar lakrimal). Pada sindrom mirip VKH, sel T autoreaktif terhadap melanosit (koroid, badan siliaris, iris) diaktifkan, menyebabkan panuveitis, ablasi retina serosa, dan lesi depigmentasi 3).
Untuk memahami gambaran keseluruhan efek samping okular terkait imun ICI, studi registri internasional multisenter sedang dilakukan 3). Dengan memperjelas spektrum, frekuensi, dan hasil dari berbagai efek samping okular seperti uveitis, sindrom mirip VKH, dan miositis ekstraokular, diharapkan stratifikasi risiko dan penetapan protokol dapat tercapai.
ADC seperti trastuzumab deruxtecan (T-DXd) semakin populer sebagai terapi antikanker generasi berikutnya, namun gangguan kornea (keratitis epitelial superfisial, kekeruhan stroma kornea) diakui sebagai efek samping 10). Akumulasi kasus melalui studi farmakovigilans dan pengembangan strategi perlindungan kornea menjadi tantangan.
Dengan OCT adaptif dan fotografi fundus multispektral, upaya dilakukan untuk memvisualisasikan perubahan struktur awal RPE yang tidak terdeteksi dengan metode konvensional 11). Selain itu, pengembangan skrining otomatis menggunakan AI untuk analisis gambar OCT juga berlangsung, diharapkan dapat mengurangi risiko terlewat 11).
Dengan meluasnya penggunaan ICI dan obat target molekuler, diperlukan penetapan protokol kolaborasi standar antara oftalmologi dan onkologi 8). Pedoman algoritma manajemen efek samping okular berdasarkan grading CTCAE sedang dikembangkan.
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.