細胞毒性化療

抗癌藥物與分子標靶藥物的眼部副作用
1. 什麼是抗癌藥和分子標靶藥的眼部副作用?
Section titled “1. 什麼是抗癌藥和分子標靶藥的眼部副作用?”抗癌藥和分子標靶藥的眼部副作用是指用於癌症治療和免疫疾病治療的藥物對眼組織引起不良事件的總稱。
涉及的藥物類別非常廣泛。
- 細胞毒性化療(5-FU、順鉑、紫杉烷類等):溢淚、角膜上皮病變、視神經病變等1)
- 荷爾蒙治療(泰莫西芬等):結晶樣黃斑沉積物、CME、角膜渦狀混濁
- 免疫調節藥(氯奎寧、羥氯奎寧、干擾素):視網膜病變、眼底出血、棉絮狀白斑
- 分子標靶藥物(MEK抑制劑、EGFR抑制劑、BRAF抑制劑、ALK抑制劑等):每種藥物有特有的眼部副作用2)
- 免疫檢查點抑制劑(ICI)(nivolumab、pembrolizumab等):作為irAE的葡萄膜炎、VKH樣症候群3)
- 抗體藥物複合體(ADC)(trastuzumab deruxtecan等):角膜損傷10)
隨著癌症治療的發展,存活期延長,長期治療中眼部副作用管理的重要性日益增加1)。眼部副作用從輕微不適到不可逆的視力障礙範圍廣泛,適當的篩檢和早期介入直接關係到視力預後。
2. 依藥物類別的症狀和臨床所見
Section titled “2. 依藥物類別的症狀和臨床所見”不同藥物類別的眼部副作用不同。以下列出主要藥物及其眼部症狀。
荷爾蒙療法和免疫調節劑
tamoxifen:黃斑周圍結晶樣沉積物、角膜渦狀混濁、CME。發生率:海外3~6%,國內0.2%
HCQ/chloroquine:牛眼黃斑病變(環狀萎縮)、視力下降、夜盲、色覺異常。使用5年以上約0.5%
干擾素:眼底後極部小出血、棉絮狀白斑。給藥後2~3個月內出現。多數無症狀、自然消退。
分子標靶藥物
免疫檢查點抑制劑(ICI)
芬戈莫德引起的黃斑水腫
Section titled “芬戈莫德引起的黃斑水腫”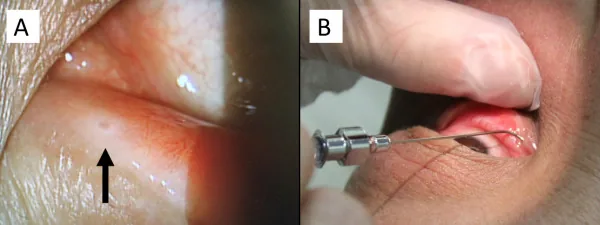
用於預防多發性硬化復發的芬戈莫德(伊姆塞拉/吉列尼亞)已知可引起黃斑水腫。黃斑水腫的發生率在芬戈莫德0.5 mg/天時為0.2%,1.25 mg/天時為1.4%,多數在開始治療後3~4個月內出現。
3. 原因與風險因素
Section titled “3. 原因與風險因素”不同藥物類別的眼部副作用風險因素不同。
| 藥物類別 | 主要風險因素 |
|---|---|
| 羥氯喹/氯喹 | 用藥時間超過5年、CQ >3.0 mg/kg/日或HCQ >6.5 mg/kg/日、高齡、腎/肝功能不全、合併視網膜疾病 |
| 他莫昔芬 | 高劑量和長期使用(累積劑量增加) |
| 干擾素 | 高初始劑量、高齡、糖尿病、高血壓、貧血 |
| MEK抑制劑 | 劑量依賴性(高劑量時頻率增加)2) |
| 免疫檢查點抑制劑 | 合併全身irAE(如甲狀腺炎、結腸炎)的患者更易發生眼部irAE 3) |
| 抗體藥物複合體 | 藥物特異性角膜毒性機制 10) |
HCQ視網膜病變的具體危險因子包括以下各項。
- 用藥期間:長期用藥5年以上(累積劑量:CQ >460 g,HCQ >1,000 g)
- 每日劑量:CQ >3.0 mg/kg/日,HCQ >6.5 mg/kg/日
- 全身風險:高齡、腎功能下降(HCQ排泄延遲)、肝功能異常
- 眼部局部風險:合併既有的視網膜疾病或黃斑部病變
干擾素視網膜病變在患有糖尿病、高血壓、貧血等全身性疾病時更常見且更嚴重,也更容易發生在治療頑抗或復發的病例中。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”HCQ篩檢方案
Section titled “HCQ篩檢方案”根據美國眼科學會(AAO)的建議9),進行以下篩檢。
- 開始用藥時(基線):視力、眼底和SD-OCT檢查
- 用藥5年後:若無高風險因子,開始每年一次篩檢
- 有風險因子:不等5年,儘早開始篩檢,並縮短間隔
- 建議最大劑量:按實際體重不超過5 mg/kg/日9)
有用的檢查包括Humphrey 10-2中心視野檢查、SD-OCT、眼底自發螢光、多焦ERG和全視野ERG。牛眼狀黃斑部病變(環狀萎縮)是晚期HCQ視網膜病變的特徵性眼底表現。
依藥物的篩檢建議
Section titled “依藥物的篩檢建議”| 藥物 | 篩檢時機與檢查 |
|---|---|
| HCQ/氯奎寧 | 治療開始時基準線 + 5年後每年一次(SD-OCT、10-2視野、FAF)9) |
| 泰莫西芬 | 出現症狀時及定期眼底檢查、SD-OCT |
| 干擾素 | 開始治療後2~3個月進行眼底檢查。如有症狀,立即就診眼科 |
| MEK抑制劑 | 出現視力下降或視物變形時,以OCT確認漿液性視網膜剝離2) |
| ICI | 出現視力下降、充血或眼痛時,立即就診眼科3) |
| 芬戈莫德 | 治療前基準線眼底檢查 + 治療後3~4個月追蹤 |
使用ICI的患者出現視力下降、充血或眼痛時,應評估前房發炎細胞、玻璃體混濁和脈絡膜病變,並考慮irAE引起的葡萄膜炎或VKH樣症候群的可能性3)。
建議在開始用藥時進行基線眼科檢查,包括視力、眼底和SD-OCT。之後,如果沒有危險因子(用藥時間≥5年、高劑量、高齡、腎功能障礙等),從5年後開始每年篩查一次。如果有危險因子,則需要更早、更頻繁的檢查。主要檢查項目包括SD-OCT、Humphrey 10-2視野檢查和眼底自發螢光。
5. 標準治療方法
Section titled “5. 標準治療方法”羥氯喹/氯喹視網膜病變
Section titled “羥氯喹/氯喹視網膜病變”停藥是唯一的治療方法。由於藥物從體內排出緩慢,停藥後病變仍可能進展或惡化。因此,早期發現極為重要,在發生不可逆損傷之前決定停藥對視力預後至關重要。
他莫昔芬眼部副作用
Section titled “他莫昔芬眼部副作用”干擾素視網膜病變
Section titled “干擾素視網膜病變”多數病例預後良好,無症狀者基本等待IFN治療結束。重症或視力下降者考慮減量或停用IFN。合併糖尿病或高血壓者需早期處理。
MEK抑制劑引起的漿液性視網膜剝離
Section titled “MEK抑制劑引起的漿液性視網膜剝離”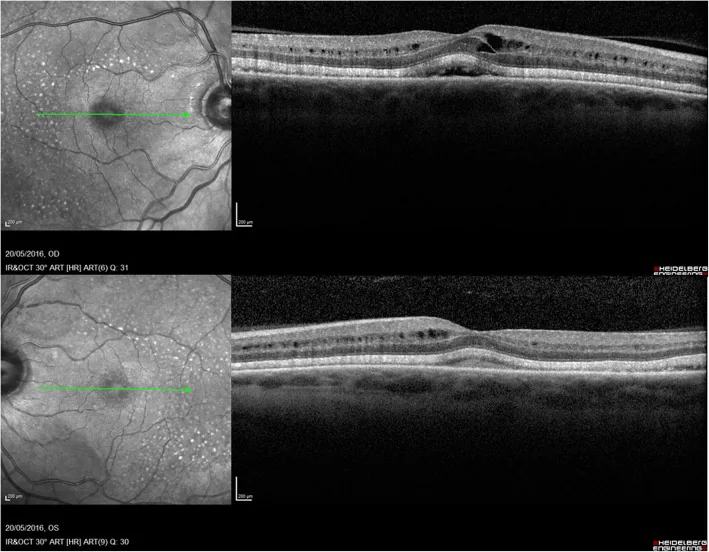
- 對於中度至重度漿液性視網膜剝離,應停藥或減量2)
- 輕度病例可在觀察下繼續用藥,多數可自然緩解2)
- 停藥或減量後確認視網膜下液消退
EGFR抑制劑引起的眼部副作用
Section titled “EGFR抑制劑引起的眼部副作用”- 睫毛亂生(trichiasis):拔除變形的睫毛5)
- 眼瞼炎:局部使用類固醇或抗生素軟膏5)
- 角膜上皮障礙:使用不含防腐劑的人工淚液和角膜保護眼藥水
ICI相關葡萄膜炎
Section titled “ICI相關葡萄膜炎”根據CTCAE分級進行管理3)。
- 第1級(輕度):使用類固醇眼藥水管理。可繼續ICI治療
- 第2級(中度):全身使用類固醇(prednisolone)。考慮暫停ICI
- 第3~4級(重度):高劑量全身類固醇。考慮暫停或永久停用ICI
- VKH樣症候群:methylprednisolone 1克/日×3天脈衝治療,隨後口服類固醇逐漸減量8)
芬戈莫德黃斑水腫
Section titled “芬戈莫德黃斑水腫”多數病例在停藥後改善。必要時可併用NSAIDs眼藥水或類固醇眼藥水。
並非必須停藥。根據眼部副作用的嚴重程度(CTCAE分級)和藥物種類,處理方式不同。對於HCQ視網膜病變和他莫昔芬視網膜病變,停藥是基本原則;而對於MEK抑制劑引起的輕度漿液性視網膜剝離或EGFR抑制劑引起的睫毛粗長,有時會選擇對症治療的同時繼續用藥。重要的是腫瘤內科主治醫師與眼科醫師協作,根據個體情況做出判斷。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”不同藥物類別對眼組織的損傷機轉不同。
氯喹和HCQ的視網膜毒性
Section titled “氯喹和HCQ的視網膜毒性”CQ和HCQ對黑色素有高親和力,與視網膜色素上皮(RPE)細胞的黑色素顆粒結合並在細胞內蓄積。蓄積的CQ/HCQ被溶酶體攝取,導致溶酶體pH升高,損害溶酶體酶活性。當RPE的酶代謝功能受損時,光感受器外節的降解和更新受阻,進而發展為光感受器變性。由於體內蓄積量大,停藥後損傷仍可能進展。
他莫昔芬視網膜病變的機轉
Section titled “他莫昔芬視網膜病變的機轉”在神經纖維層和內叢狀層形成球狀病灶(神經纖維變性和軸索腫脹)。結晶樣沉積物被認為是含有鈣和複合糖類的變性產物沉積在神經纖維內。囊樣黃斑水腫(CME)由Müller細胞功能障礙和液體滯留引起。
干擾素視網膜病變的機轉
Section titled “干擾素視網膜病變的機轉”IFN誘導血管痙攣、白血球浸潤和血管內皮損傷,免疫複合物沉積在毛細血管中,導致毛細血管閉塞。閉塞毛細血管的前方(動脈側)出現棉絮斑(神經纖維層梗塞),閉塞部位出血表現為小出血。多為一過性,停藥後消退。
MEK抑制劑引起的漿液性視網膜剝離
Section titled “MEK抑制劑引起的漿液性視網膜剝離”MEK抑制劑阻斷MAPK/ERK路徑(細胞增殖和生存信號)。由於RPE通過ERK信號維持主動運輸(離子和水分),ERK抑制導致RPE的離子運輸和泵功能受損。結果導致視網膜下液體積聚,表現為漿液性視網膜剝離和視網膜色素上皮剝離(PED)2)。
免疫檢查點抑制劑(ICI)的眼部irAE
Section titled “免疫檢查點抑制劑(ICI)的眼部irAE”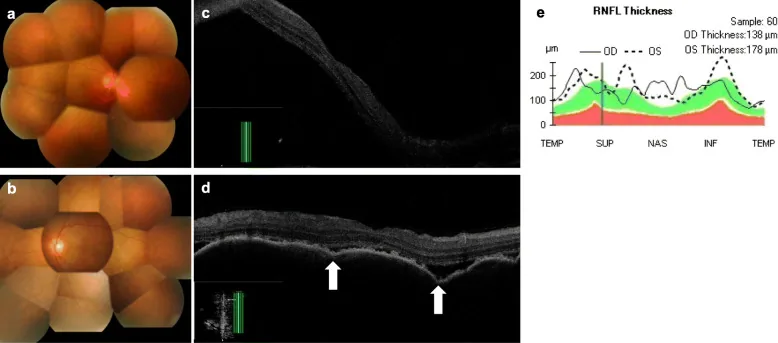
ICI(PD-1/PD-L1抑制劑、CTLA-4抑制劑)解除T細胞的免疫檢查點,增強抗腫瘤免疫。然而,此機制同時也解除自身免疫抑制,引發眼組織(葡萄膜、鞏膜、眼眶、淚腺)的自身免疫反應。在VKH樣症候群中,針對黑色素細胞(脈絡膜、睫狀體、虹膜)的自身反應性T細胞被活化,導致全葡萄膜炎、漿液性視網膜剝離與脫色素病變3)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”ICI相關眼部irAE的大規模註冊研究
Section titled “ICI相關眼部irAE的大規模註冊研究”為全面了解ICI相關眼部irAE,國際多中心註冊研究正在進行中3)。透過闡明葡萄膜炎、VKH樣症候群、眼外肌炎等多種眼部irAE的譜系、頻率與轉歸,有望實現風險分層與方案確立。
抗體藥物複合體(ADC)的角膜毒性
Section titled “抗體藥物複合體(ADC)的角膜毒性”以Trastuzumab deruxtecan(T-DXd)為代表的ADC作為下一代抗癌療法正在普及,但角膜毒性(點狀角膜病變、角膜基質混濁)已被確認為不良事件10)。透過藥物警戒研究累積病例並建立角膜保護策略是當前的課題。
HCQ視網膜病變的超早期檢測
Section titled “HCQ視網膜病變的超早期檢測”自適應光學OCT與多光譜眼底攝影正在嘗試可視化傳統方法無法檢測的早期RPE結構變化11)。此外,利用人工智慧(AI)分析OCT影像進行自動篩檢的開發也在進行中,有望降低漏診風險11)。
眼科與腫瘤內科協作方案的建立
Section titled “眼科與腫瘤內科協作方案的建立”隨著ICI與分子標靶藥物的普及,需要建立眼科與腫瘤內科之間的標準化協作方案8)。基於CTCAE分級的眼部副作用管理演算法的指引化正在推進中。
8. 參考文獻
Section titled “8. 參考文獻”-
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
-
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
-
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
-
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
-
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
-
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
-
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
-
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
-
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
-
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
-
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.
