เคมีบำบัดแบบฆ่าเซลล์
5-FU: น้ำตาไหล (ท่อน้ำตาตีบ), เยื่อบุตาอักเสบ, ความผิดปกติของเยื่อบุกระจกตา1)
ซิสพลาติน: โรคเส้นประสาทตา, ความผิดปกติของการมองเห็นสี (พบน้อย)1)
แท็กเซน (โดเซแทกเซล, แพคลิแทกเซล): น้ำตาไหล, จุดรับภาพบวมแบบถุงน้ำ4)

ผลข้างเคียงทางตาจากยาเคมีบำบัดและยามุ่งเป้าระดับโมเลกุลเป็นคำรวมสำหรับภาวะที่ยาใช้รักษามะเร็งและโรคภูมิคุ้มกันทำให้เกิดเหตุการณ์ไม่พึงประสงค์ต่อเนื้อเยื่อตา
ประเภทของยาที่เกี่ยวข้องมีหลากหลาย
ด้วยความก้าวหน้าของการรักษามะเร็ง ทำให้ระยะเวลารอดชีวิตยาวนานขึ้น และการจัดการผลข้างเคียงทางตาในระหว่างการรักษาระยะยาวมีความสำคัญเพิ่มขึ้น1) ผลข้างเคียงทางตามีตั้งแต่ความรู้สึกไม่สบายเล็กน้อยไปจนถึงการสูญเสียการมองเห็นแบบถาวร และการตรวจคัดกรองที่เหมาะสมรวมถึงการแทรกแซงตั้งแต่เนิ่นๆ ส่งผลโดยตรงต่อพยากรณ์โรคทางการมองเห็น
หากมีอาการเช่น การมองเห็นลดลง ตาแดง ปวดตา ภาพลอย ภาพแสงวาบ ภาพบิดเบี้ยว (เห็นวัตถุผิดรูป) ควรไปพบจักษุแพทย์ทันที แม้ว่าอาการจะเล็กน้อย การปล่อยทิ้งไว้อาจนำไปสู่ความเสียหายถาวร ดังนั้นจึงสำคัญที่จะรายงานให้แพทย์ผู้รักษา (อายุรศาสตร์มะเร็งวิทยา) ทราบและประสานงานกับจักษุแพทย์
ผลข้างเคียงทางตาแตกต่างกันไปตามประเภทของยา ด้านล่างนี้คือยาหลักและอาการทางตาของยาเหล่านั้น
เคมีบำบัดแบบฆ่าเซลล์
5-FU: น้ำตาไหล (ท่อน้ำตาตีบ), เยื่อบุตาอักเสบ, ความผิดปกติของเยื่อบุกระจกตา1)
ซิสพลาติน: โรคเส้นประสาทตา, ความผิดปกติของการมองเห็นสี (พบน้อย)1)
แท็กเซน (โดเซแทกเซล, แพคลิแทกเซล): น้ำตาไหล, จุดรับภาพบวมแบบถุงน้ำ4)
การรักษาด้วยฮอร์โมนและยาปรับภูมิคุ้มกัน
ทามอกซิเฟน: การสะสมผลึกบริเวณรอบจุดรับภาพ, กระจกตาขุ่นเป็นเกลียว, จุดรับภาพบวมแบบถุงน้ำ อุบัติการณ์: 3-6% ในต่างประเทศ, 0.2% ในประเทศ
HCQ/คลอโรควิน: จอประสาทตาเสื่อมแบบตาวัว (ฝ่อเป็นวงแหวน), การมองเห็นลดลง, ตาบอดกลางคืน, ความผิดปกติของการมองเห็นสี ประมาณ 0.5% หลังจากใช้ 5 ปี
อินเตอร์เฟียรอน: เลือดออกเล็กน้อยและจุดขาวคล้ายสำลีที่ขั้วหลังของจอตา เกิดขึ้นภายใน 2-3 เดือนหลังให้ยา ส่วนใหญ่ไม่มีอาการและหายได้เอง
ยามุ่งเป้าระดับโมเลกุล
สารยับยั้ง MEK (เช่น trametinib): จอตาลอกชนิดมีน้ำใต้จอตา และการลอกของชั้น pigment epithelium อุบัติการณ์ประมาณ 10-25%2)
สารยับยั้ง EGFR (เช่น gefitinib): ขนตางอกผิดปกติ เปลือกตาอักเสบ ความผิดปกติของเยื่อบุกระจกตา5)
สารยับยั้ง BRAF (เช่น vemurafenib): ม่านตาอักเสบ จอตาลอกชนิดมีน้ำใต้จอตา6)
สารยับยั้ง ALK (เช่น crizotinib): เห็นแสงวาบ ตาพร่า ประมาณ 60% มีความผิดปกติทางการมองเห็น7)
สารยับยั้งภูมิคุ้มกัน checkpoint (ICI)
ม่านตาอักเสบ (ส่วนหน้า ส่วนหลัง หรือทั้งลูกตา): อุบัติการณ์ประมาณ 1%3)
กลุ่มอาการคล้าย VKH: รูปแบบรุนแรงที่ต้องใช้สเตียรอยด์ขนาดสูง3)
ตาแห้ง เยื่อบุตาอักเสบ โรคอักเสบของเบ้าตา กล้ามเนื้อนอกลูกตาอักเสบ8)
ADC (เช่น T-DXd): ความผิดปกติของกระจกตา (กระจกตาอักเสบแบบจุดตื้น, กระจกตาขุ่นในชั้นสโตรมา)10)
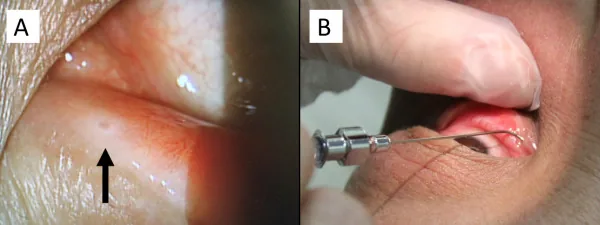
เป็นที่ทราบกันว่า fingolimod (Imusera/Gilenya) ซึ่งใช้ป้องกันการกลับเป็นซ้ำของโรคปลอกประสาทเสื่อมแข็ง ทำให้เกิดจอประสาทตาบวมน้ำ อุบัติการณ์ของจอประสาทตาบวมน้ำคือ 0.2% สำหรับ fingolimod ขนาด 0.5 มก./วัน และ 1.4% สำหรับขนาด 1.25 มก./วัน และส่วนใหญ่เกิดขึ้นภายใน 3-4 เดือนหลังจากเริ่มการรักษา
ปัจจัยเสี่ยงของผลข้างเคียงทางตาจะแตกต่างกันไปตามประเภทของยา
| ประเภทของยา | ปัจจัยเสี่ยงหลัก |
|---|---|
| HCQ/คลอโรควิน | ระยะเวลาการใช้ยา >5 ปี, CQ >3.0 มก./กก./วัน หรือ HCQ >6.5 มก./กก./วัน, อายุมาก, การทำงานของไต/ตับบกพร่อง, โรคจอประสาทตาร่วม |
| ทามอกซิเฟน | ขนาดสูงและการใช้ระยะยาว (เพิ่มขนาดสะสม) |
| อินเตอร์เฟอรอน | ขนาดเริ่มต้นสูง, อายุมาก, เบาหวาน, ความดันโลหิตสูง, โลหิตจาง |
| สารยับยั้ง MEK | ขึ้นกับขนาดยา (ความถี่เพิ่มขึ้นเมื่อใช้ขนาดสูง) 2) |
| ICI | ผู้ป่วยที่มี irAE ทั่วร่างกาย (เช่น ต่อมไทรอยด์อักเสบ, ลำไส้ใหญ่อักเสบ) มีแนวโน้มเกิด irAE ทางตาได้ง่าย 3) |
| ADC | กลไกความเป็นพิษต่อกระจกตาที่จำเพาะต่อยา 10) |
ปัจจัยเสี่ยงเฉพาะของจอประสาทตาเสื่อมจาก HCQ ได้แก่:
จอประสาทตาเสื่อมจากอินเตอร์เฟอรอนพบได้บ่อยและรุนแรงกว่าในผู้ที่มีโรคทางระบบ เช่น เบาหวาน ความดันโลหิตสูง และโลหิตจาง และมักเกิดในกรณีที่ดื้อต่อการรักษาหรือกลับเป็นซ้ำ
ตามคำแนะนำของ AAO (สมาคมจักษุแพทย์อเมริกัน)9) ให้ทำการตรวจคัดกรองดังนี้:
การตรวจที่มีประโยชน์ ได้แก่: การตรวจลานสายตาส่วนกลาง Humphrey 10-2, SD-OCT, การเรืองแสงอัตโนมัติของจอตา, การตรวจคลื่นไฟฟ้าจอตาหลายจุด และการตรวจคลื่นไฟฟ้าจอตาทั้งลาน ภาพตาวัว (ฝ่อเป็นวงแหวน) เป็นลักษณะเฉพาะของจอประสาทตาเสื่อมจาก HCQ ระยะลุกลาม
| ยา | ระยะเวลาในการตรวจคัดกรองและการตรวจ |
|---|---|
| HCQ/คลอโรควิน | ตรวจพื้นฐานเมื่อเริ่มให้ยา + รายปีหลังจาก 5 ปี (SD-OCT, ลานสายตา 10-2, FAF) 9) |
| ทามอกซิเฟน | เมื่อมีอาการและตรวจอวัยวะภายในตาเป็นระยะร่วมกับ SD-OCT |
| อินเตอร์เฟอรอน | ตรวจอวัยวะภายในตา 2-3 เดือนหลังจากเริ่มให้ยา หากมีอาการ ให้ไปพบจักษุแพทย์ทันที |
| ยายับยั้ง MEK | เมื่อเกิดการมองเห็นลดลงหรือภาพบิดเบือน ให้ยืนยันจอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตาด้วย OCT 2) |
| ICI | เมื่อเกิดการมองเห็นลดลง ตาแดง หรือปวดตา ให้ไปพบจักษุแพทย์ทันที 3) |
| ฟิงโกลิโมด | ตรวจอวัยวะภายในตาพื้นฐานก่อนให้ยา + ติดตามผล 3-4 เดือนหลังจากให้ยา |
ในผู้ป่วยที่ใช้ ICI ซึ่งมีการมองเห็นลดลง ตาแดง หรือปวดตา ควรประเมินเซลล์อักเสบในช่องหน้าตา ความขุ่นของวุ้นตา และรอยโรคคอรอยด์ โดยพิจารณาถึงความเป็นไปได้ของม่านตาอักเสบหรือกลุ่มอาการคล้าย VKH ในฐานะ irAE 3).
แนะนำให้ตรวจตาซึ่งรวมถึงการวัดสายตา ตรวจจอประสาทตา และ SD-OCT เป็นพื้นฐานเมื่อเริ่มให้ยา หลังจากนั้น หากไม่มีปัจจัยเสี่ยง (ระยะเวลาให้ยา >5 ปี ขนาดสูง อายุมาก การทำงานของไตบกพร่อง ฯลฯ) ให้เริ่มตรวจคัดกรองปีละครั้งหลังจาก 5 ปี หากมีปัจจัยเสี่ยง จำเป็นต้องตรวจเร็วขึ้นและบ่อยขึ้น การตรวจหลักได้แก่ SD-OCT การตรวจลานสายตา Humphrey 10-2 และการเรืองแสงอัตโนมัติของจอประสาทตา
การรักษาเพียงอย่างเดียวคือการหยุดยา เนื่องจากการขับยาออกจากร่างกายช้า รอยโรคอาจดำเนินและแย่ลงแม้หลังจากหยุดยา ดังนั้นการตรวจพบตั้งแต่เนิ่นๆ จึงสำคัญอย่างยิ่ง และการตัดสินใจหยุดยาก่อนเกิดความเสียหายที่ไม่สามารถกลับคืนได้จะเป็นตัวกำหนดพยากรณ์การมองเห็น
กรณีส่วนใหญ่มีการพยากรณ์โรคที่ดี และหากไม่มีอาการ โดยพื้นฐานแล้วให้รอจนกว่าการรักษาด้วย IFN จะสิ้นสุด ในกรณีรุนแรงหรือมีสายตาลดลง ให้พิจารณาลดขนาดหรือหยุด IFN ในกรณีที่มีโรคร่วมเช่นเบาหวานหรือความดันโลหิตสูง จำเป็นต้องจัดการตั้งแต่เนิ่นๆ
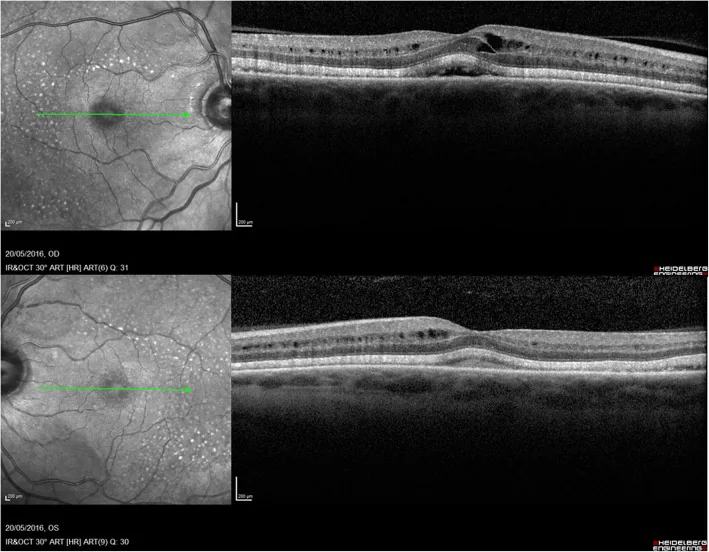
จัดการตามระดับ CTCAE 3).
ในหลายกรณีอาการดีขึ้นเมื่อหยุดยา หากจำเป็นอาจใช้ยาหยอดตา NSAID หรือสเตียรอยด์ร่วมด้วย
ไม่จำเป็นต้องหยุดเสมอไป การจัดการขึ้นอยู่กับความรุนแรงของผลข้างเคียงทางตา (grade CTCAE) และชนิดของยา ในบางกรณีเช่น จอประสาทตาเสื่อมจาก HCQ หรือ tamoxifen การหยุดยาเป็นหลักการพื้นฐาน ในขณะที่กรณีอื่นๆ เช่น จอประสาทตาลอกชนิดเซรุ่มเล็กน้อยจากยา MEK inhibitor หรือขนตางอกผิดปกติจากยา EGFR inhibitor อาจเลือกให้รักษาต่อไปพร้อมกับการรักษาตามอาการ สิ่งสำคัญคือแพทย์มะเร็งวิทยาและจักษุแพทย์ต้องทำงานร่วมกันเพื่อตัดสินใจตามสถานการณ์เฉพาะของผู้ป่วย
กลไกการทำลายเนื้อเยื่อตาแตกต่างกันไปตามประเภทของยา
CQ และ HCQ มีความสัมพันธ์สูงกับเมลานิน โดยจับกับเม็ดเมลานินในเซลล์เยื่อบุผิวรงควัตถุจอตา (RPE) และสะสมภายในเซลล์ การสะสมของ CQ/HCQ ทำให้ pH ในไลโซโซมสูงขึ้น ขัดขวางการทำงานของเอนไซม์ในไลโซโซม เมื่อการทำงานของเอนไซม์เมตาบอลิซึมของ RPE ถูกทำลาย การย่อยสลายและสร้างใหม่ของส่วนนอกของเซลล์รับแสงจะถูกขัดขวาง นำไปสู่การเสื่อมของเซลล์รับแสง เนื่องจากการสะสมในร่างกายมีปริมาณมาก ความเสียหายอาจดำเนินต่อไปแม้หลังจากหยุดยา
เกิดรอยโรคทรงกลม (การเสื่อมของเส้นใยประสาทและแอกซอนบวม) ในชั้นเส้นใยประสาทและชั้นข่ายประสาทชั้นใน ตะกอนผลึกถือเป็นผลิตภัณฑ์จากการเสื่อมที่ประกอบด้วยแคลเซียมและคาร์โบไฮเดรตเชิงซ้อนที่สะสมภายในเส้นใยประสาท จอประสาทตาบวมชนิดซีสตอยด์ (CME) เกิดจากความผิดปกติของเซลล์ Müller และการสะสมของของเหลว
IFN กระตุ้นให้เกิดการหดเกร็งของหลอดเลือด การแทรกซึมของเม็ดเลือดขาว และความเสียหายต่อเยื่อบุผนังหลอดเลือด ทำให้เกิดการสะสมของอิมมูนคอมเพล็กซ์ในเส้นเลือดฝอย ส่งผลให้เส้นเลือดฝอยอุดตัน ด้านหน้าของเส้นเลือดฝอยที่อุดตัน (ด้านหลอดเลือดแดง) จะเกิดจุดขาวคล้ายสำลี (เนื้อตายของชั้นเส้นใยประสาท) และมีเลือดออกเล็กน้อยเป็นจุดเลือดออก ส่วนใหญ่เกิดขึ้นชั่วคราวและหายไปหลังจากหยุด IFN
ยา MEK inhibitor ขัดขวางเส้นทาง MAPK/ERK (สัญญาณการเพิ่มจำนวนและการอยู่รอดของเซลล์) RPE รักษาการลำเลียงแบบแอคทีฟ (ไอออนและน้ำ) ผ่านสัญญาณ ERK ดังนั้นการยับยั้ง ERK จึงทำให้การทำงานของปั๊มไอออนและการลำเลียงของ RPE ผิดปกติ ผลที่ตามมาคือการสะสมของของเหลวใต้จอประสาทตา ซึ่งแสดงออกเป็นจอประสาทตาลอกชนิดเซรุ่มและการลอกของเยื่อบุผิวรงควัตถุจอตา (PED)2)
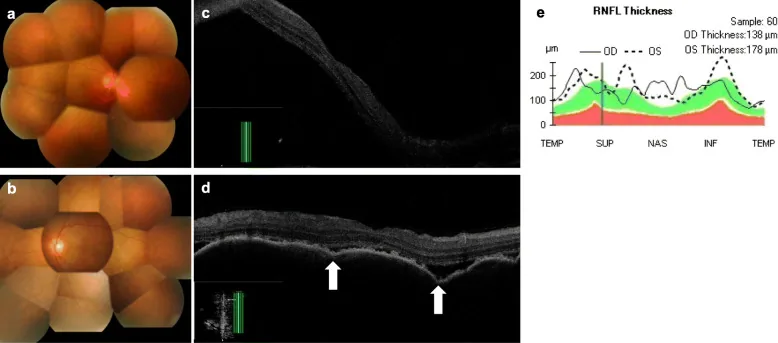
ยายับยั้งจุดตรวจสอบภูมิคุ้มกัน (ยายับยั้ง PD-1/PD-L1, ยายับยั้ง CTLA-4) จะปลดปล่อยจุดตรวจสอบภูมิคุ้มกันของทีเซลล์และเพิ่มภูมิคุ้มกันต้านมะเร็ง อย่างไรก็ตาม กลไกนี้ยังปลดปล่อยกลไกการกดภูมิคุ้มกันตนเองพร้อมกัน ทำให้เกิดปฏิกิริยาภูมิคุ้มกันตนเองต่อเนื้อเยื่อตา (ยูเวีย, ตาขาว, เบ้าตา, ต่อมน้ำตา) ในกลุ่มอาการคล้าย VKH ทีเซลล์ที่ตอบสนองต่อตนเองต่อเมลาโนไซต์ (คอรอยด์, ซิลิอารีบอดี, ม่านตา) จะถูกกระตุ้น ทำให้เกิดม่านตาอักเสบทั้งลูกตา จอตาลอกแบบมีน้ำใต้จอตา และรอยโรคที่สูญเสียเม็ดสี 3)
เพื่อทำความเข้าใจภาพรวมของผลข้างเคียงทางตาที่เกี่ยวข้องกับภูมิคุ้มกันจาก ICI กำลังมีการศึกษาทะเบียนระหว่างประเทศแบบหลายศูนย์ 3) โดยการทำให้ชัดเจนถึงสเปกตรัม ความถี่ และผลลัพธ์ของผลข้างเคียงทางตาต่างๆ เช่น ม่านตาอักเสบ กลุ่มอาการคล้าย VKH และกล้ามเนื้อนอกตาอักเสบ คาดว่าจะสามารถแบ่งชั้นความเสี่ยงและกำหนดแนวทางปฏิบัติได้
ADC เช่น trastuzumab deruxtecan (T-DXd) กำลังเป็นที่นิยมในฐานะการรักษามะเร็งรุ่นต่อไป แต่ความผิดปกติของกระจกตา (กระจกตาอักเสบแบบจุดที่ผิว, ความขุ่นของสโตรมากระจกตา) ได้รับการยอมรับว่าเป็นผลข้างเคียง 10) การรวบรวมผู้ป่วยผ่านการศึกษาการเฝ้าระวังยาและการกำหนดกลยุทธ์การปกป้องกระจกตาเป็นความท้าทาย
ด้วย OCT แบบปรับตัวและการถ่ายภาพจอตาหลายสเปกตรัม มีความพยายามในการมองเห็นการเปลี่ยนแปลงโครงสร้าง RPE ระยะแรกที่ไม่สามารถตรวจพบด้วยวิธีดั้งเดิม 11) นอกจากนี้ การพัฒนาการคัดกรองอัตโนมัติโดยใช้ AI สำหรับการวิเคราะห์ภาพ OCT ก็กำลังดำเนินไป คาดว่าจะลดความเสี่ยงในการมองข้าม 11)
ด้วยการแพร่หลายของ ICI และยาที่มุ่งเป้าระดับโมเลกุล จึงจำเป็นต้องกำหนดแนวทางปฏิบัติร่วมกันที่เป็นมาตรฐานระหว่างจักษุวิทยาและอายุรศาสตร์มะเร็งวิทยา 8) แนวทางสำหรับอัลกอริทึมการจัดการผลข้างเคียงทางตาตามการจัดระดับ CTCAE กำลังถูกพัฒนาขึ้น
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.