العلاج الكيميائي السام للخلايا
5-FU: الدموع (تضيق القناة الدمعية)، التهاب الملتحمة، اعتلال ظهارة القرنية1)
سيسبلاتين: اعتلال العصب البصري، اضطراب رؤية الألوان (نادر)1)
التاكسانات (دوسيتاكسيل، باكليتاكسيل): الدموع، الوذمة البقعية الكيسية4)

الآثار الجانبية العينية للأدوية المضادة للسرطان والأدوية المستهدفة جزيئيًا هي مصطلح شامل للحالات التي تسبب فيها الأدوية المستخدمة لعلاج السرطان والأمراض المناعية أحداثًا ضارة في أنسجة العين.
تتنوع فئات الأدوية المعنية بشكل واسع.
مع تقدم علاج السرطان، زادت فترة البقاء على قيد الحياة، وأصبحت إدارة الآثار الجانبية العينية أثناء العلاج طويل الأمد أكثر أهمية1). تتراوح الآثار الجانبية العينية من الانزعاج البسيط إلى فقدان البصر غير القابل للعكس، ويرتبط الفحص المناسب والتدخل المبكر ارتباطًا مباشرًا بالنتائج البصرية.
إذا ظهرت أعراض مثل انخفاض الرؤية، احمرار العين، ألم العين، العوائم، ومضات الضوء، تشوه الرؤية (رؤية الأشياء مشوهة)، يجب استشارة طبيب العيون فورًا. حتى لو كانت الأعراض خفيفة، فقد يؤدي إهمالها إلى ضرر غير قابل للعكس، لذلك من المهم إبلاغ الطبيب المعالج (أورام) والتنسيق مع طبيب العيون.
تختلف الآثار الجانبية العينية حسب فئة الدواء. فيما يلي الأدوية الرئيسية وأعراضها العينية.
العلاج الكيميائي السام للخلايا
5-FU: الدموع (تضيق القناة الدمعية)، التهاب الملتحمة، اعتلال ظهارة القرنية1)
سيسبلاتين: اعتلال العصب البصري، اضطراب رؤية الألوان (نادر)1)
التاكسانات (دوسيتاكسيل، باكليتاكسيل): الدموع، الوذمة البقعية الكيسية4)
العلاج الهرموني والأدوية المعدلة للمناعة
تاموكسيفين: رواسب بلورية حول البقعة، عتامة قرنية حلزونية، وذمة بقعية كيسية. معدل الحدوث: 3-6% في الخارج، 0.2% محليًا
هيدروكسي كلوروكين/كلوروكين: اعتلال بقعة عين الثور (ضمور حلقي)، انخفاض الرؤية، العشى الليلي، تشوهات رؤية الألوان. حوالي 0.5% بعد 5 سنوات من الاستخدام
الإنترفيرون: نزيف صغير وبقع صوفية قطنية في القطب الخلفي للشبكية. يحدث خلال 2-3 أشهر بعد العلاج. غالبًا ما يكون بدون أعراض ويختفي تلقائيًا.
الأدوية المستهدفة جزيئيًا
مثبطات MEK (مثل تراميتينيب): انفصال الشبكية المصلي وانفصال الظهارة الصباغية. نسبة الحدوث حوالي 10-25%2)
مثبطات EGFR (مثل جيفيتينيب): نمو غير طبيعي للرموش، التهاب الجفن، اضطراب ظهارة القرنية5)
مثبطات BRAF (مثل فيمورافينيب): التهاب العنبية، انفصال الشبكية المصلي6)
مثبطات ALK (مثل كريزوتينيب): رؤية ضوئية، ضبابية الرؤية. حوالي 60% يعانون من اضطرابات بصرية7)
مثبطات نقاط التفتيش المناعية (ICI)
التهاب العنبية (أمامي، خلفي، شامل): نسبة الحدوث حوالي 1%3)
متلازمة شبيهة بمرض فوجت-كوياناغي-هارادا: شكل حاد يتطلب جرعات عالية من الستيرويدات3)
جفاف العين، التهاب الملتحمة، أمراض التهابية في الحجاج، التهاب العضلات خارج العين8)
ADC (مثل T-DXd): اضطراب القرنية (التهاب القرنية النقطي السطحي، عتامة القرنية)10)
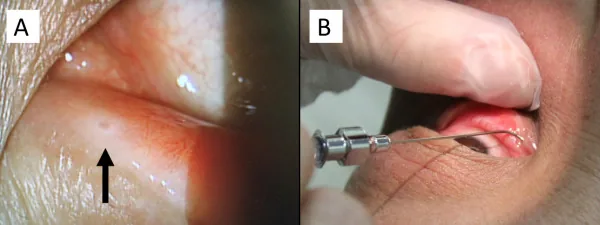
من المعروف أن فينجوليمود (إيموسيرا/جيلينيا) المستخدم للوقاية من انتكاسات التصلب المتعدد يسبب الوذمة البقعية. معدل حدوث الوذمة البقعية هو 0.2% لجرعة 0.5 ملغ/يوم و1.4% لجرعة 1.25 ملغ/يوم، وتحدث غالبًا خلال 3-4 أشهر من بدء العلاج.
تختلف عوامل خطر الآثار الجانبية العينية حسب فئة الدواء.
| فئة الدواء | عوامل الخطر الرئيسية |
|---|---|
| هيدروكسي كلوروكين/كلوروكين | مدة العلاج أكثر من 5 سنوات، جرعة كلوروكين >3.0 ملغم/كغم/يوم أو هيدروكسي كلوروكين >6.5 ملغم/كغم/يوم، التقدم في العمر، اختلال وظائف الكلى أو الكبد، وجود مرض شبكي مصاحب |
| تاموكسيفين | جرعة عالية واستخدام طويل الأمد (زيادة الجرعة التراكمية) |
| إنترفيرون | جرعة أولية عالية، التقدم في العمر، السكري، ارتفاع ضغط الدم، فقر الدم |
| مثبطات MEK | اعتماد على الجرعة (زيادة التكرار مع الجرعات العالية) 2) |
| مثبطات نقاط التفتيش المناعية (ICI) | في حالات الآثار الجانبية المناعية الجهازية المصاحبة (مثل التهاب الغدة الدرقية والتهاب القولون) تكون الآثار الجانبية العينية أكثر شيوعًا 3) |
| الأجسام المضادة الموجهة للأدوية (ADC) | آلية سمية قرنية خاصة بالدواء 10) |
تشمل عوامل الخطر المحددة لاعتلال الشبكية الناتج عن هيدروكسي كلوروكين ما يلي:
اعتلال الشبكية الناتج عن الإنترفيرون يكون أكثر شيوعًا وشدة في حالة وجود أمراض جهازية مثل السكري وارتفاع ضغط الدم وفقر الدم، كما يحدث غالبًا في الحالات المقاومة للعلاج أو المتكررة.
بناءً على توصيات الأكاديمية الأمريكية لطب العيون (AAO)9)، يتم إجراء الفحص التالي:
تشمل الفحوصات المفيدة: فحص المجال البصري المركزي Humphrey 10-2، وSD-OCT، والتصوير الذاتي الفلوري لقاع العين، وتخطيط كهربية الشبكية متعدد البؤر، وتخطيط كهربية الشبكية كامل المجال. يُعد نمط عين الثور (الضمور الحلقي) من العلامات المميزة لاعتلال الشبكية المتقدم الناتج عن هيدروكسي كلوروكين.
| الدواء | توقيت الفحص ونوعه |
|---|---|
| هيدروكسي كلوروكين / كلوروكين | فحص أساسي عند بدء العلاج + سنويًا بعد 5 سنوات (SD-OCT، مجال بصري 10-2، FAF) 9) |
| تاموكسيفين | عند ظهور الأعراض وفحص قاع العين الدوري و SD-OCT |
| إنترفيرون | فحص قاع العين بعد 2-3 أشهر من بدء العلاج. إذا ظهرت أعراض، راجع طبيب العيون فورًا |
| مثبطات MEK | عند حدوث انخفاض الرؤية أو تشوه الرؤية، يتم تأكيد انفصال الشبكية المصلي بواسطة OCT 2) |
| مثبطات نقاط التفتيش المناعية (ICI) | عند حدوث انخفاض الرؤية أو احمرار أو ألم في العين، راجع طبيب العيون فورًا 3) |
| فينجوليمود | فحص قاع العين الأساسي قبل العلاج + متابعة بعد 3-4 أشهر من العلاج |
في المرضى الذين يستخدمون مثبطات نقاط التفتيش المناعية (ICI) ويعانون من انخفاض الرؤية أو احمرار أو ألم في العين، يجب تقييم الخلايا الالتهابية في الغرفة الأمامية، وعتامة الجسم الزجاجي، وآفات المشيمية، مع مراعاة احتمالية التهاب العنبية أو متلازمة شبيهة بمرض VKH كأثر ضار مرتبط بالمناعة (irAE) 3).
يوصى بإجراء فحص عيون يشمل حدة البصر وقاع العين وSD-OCT كخط أساس عند بدء العلاج. بعد ذلك، إذا لم تكن هناك عوامل خطر (مدة علاج تزيد عن 5 سنوات، جرعة عالية، تقدم العمر، ضعف وظائف الكلى، إلخ)، يبدأ الفحص السنوي بعد 5 سنوات. إذا كانت هناك عوامل خطر، يلزم إجراء فحوصات مبكرة وأكثر تواتراً. تشمل الفحوصات الرئيسية SD-OCT، وفحص مجال الرؤية Humphrey 10-2، والتصوير الذاتي الفلوري لقاع العين.
العلاج الوحيد هو إيقاف الدواء. نظراً لبطء التخلص من الدواء من الجسم، قد يتطور المرض ويسوء حتى بعد إيقاف الدواء. لذلك، الكشف المبكر مهم للغاية، واتخاذ قرار إيقاف الدواء قبل حدوث ضرر لا رجعة فيه يحدد تشخيص الرؤية.
معظم الحالات لها تشخيص جيد، وإذا كانت بدون أعراض، فعادةً ما يكون الانتظار حتى انتهاء علاج الإنترفيرون هو النهج المتبع. في الحالات الشديدة أو حالات انخفاض الرؤية، يتم النظر في تقليل جرعة الإنترفيرون أو إيقافه. في حالات الإصابة المصاحبة بداء السكري أو ارتفاع ضغط الدم، يلزم التدخل المبكر.
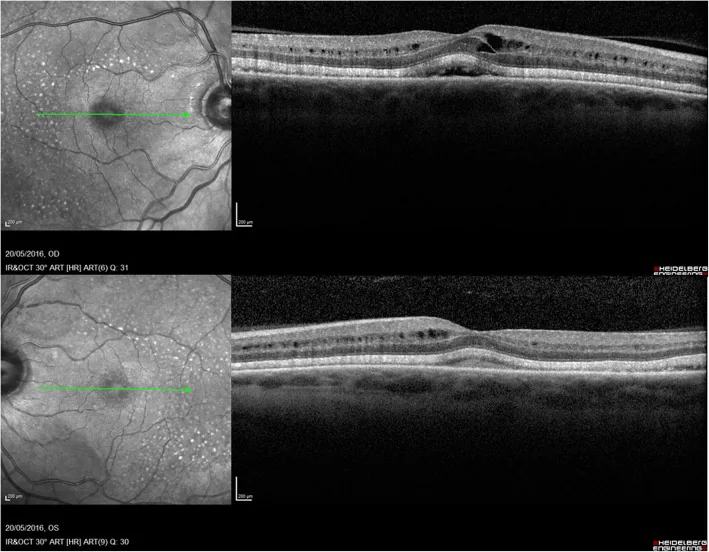
يتم الإدارة بناءً على درجة CTCAE 3).
تتحسن معظم الحالات بعد إيقاف الدواء. يمكن استخدام قطرات مضادات الالتهاب غير الستيرويدية أو الستيرويدية حسب الحاجة.
ليس من الضروري دائمًا إيقاف العلاج. يختلف التعامل حسب شدة الآثار الجانبية العينية (درجة CTCAE) ونوع الدواء. في بعض الحالات مثل اعتلال الشبكية الناتج عن HCQ أو تاموكسيفين، يكون إيقاف الدواء هو الأساس، بينما في حالات أخرى مثل انفصال الشبكية المصلي الخفيف الناتج عن مثبطات MEK أو نمو الرموش غير الطبيعي الناتج عن مثبطات EGFR، يمكن الاستمرار في العلاج مع علاج الأعراض. من المهم التنسيق بين طبيب الأورام وطبيب العيون لاتخاذ القرار المناسب لكل حالة.
تختلف آلية إصابة الأنسجة العينية حسب فئة الدواء.
يتمتع CQ وHCQ بألفة عالية للميلانين، حيث يرتبطان بحبيبات الميلانين في خلايا الظهارة الصبغية للشبكية (RPE) ويتراكمان داخل الخلايا. يؤدي تراكم CQ/HCQ إلى ارتفاع درجة الحموضة في الليزوزومات، مما يعطل نشاط الإنزيمات الليزوزومية. عندما تتعطل وظيفة التمثيل الغذائي للإنزيمات في RPE، يتعطل تحلل وتجديد الأجزاء الخارجية للمستقبلات الضوئية، مما يؤدي إلى تنكس المستقبلات الضوئية. نظرًا لارتفاع كمية التراكم في الجسم، قد يستمر الضرر حتى بعد إيقاف الدواء.
تتشكل آفات كروية (تنكس الألياف العصبية وتورم المحاور) في طبقة الألياف العصبية والطبقة الضفيرية الداخلية. يُعتقد أن الترسبات البلورية هي نواتج تنكسية تحتوي على الكالسيوم والكربوهيدرات المعقدة تترسب داخل الألياف العصبية. تحدث الوذمة البقعية الكيسية (CME) بسبب خلل في وظيفة خلايا مولر وتراكم السوائل.
يحفز IFN تشنج الأوعية الدموية، وتسرب الكريات البيضاء، وتلف بطانة الأوعية الدموية، مما يؤدي إلى ترسب المعقدات المناعية في الشعيرات الدموية مما يسبب انسدادها. ينتج عن انسداد الشعيرات الدموية ظهور بقع بيضاء قطنية (احتشاء طبقة الألياف العصبية) في الجانب الشرياني، ونزيف صغير في موقع الانسداد. غالبًا ما تكون هذه التغيرات مؤقتة وتزول بعد إيقاف IFN.
تعمل مثبطات MEK على إعاقة مسار MAPK/ERK (إشارات تكاثر الخلايا وبقائها). تحافظ RPE على النقل النشط (الأيونات والماء) عبر إشارات ERK، لذا يؤدي تثبيط ERK إلى تعطيل وظيفة النقل الأيوني والمضخة في RPE. ينتج عن ذلك تراكم السوائل تحت الشبكية، مما يظهر على شكل انفصال شبكي مصلي وانفصال ظهارة الشبكية الصبغية (PED)2).
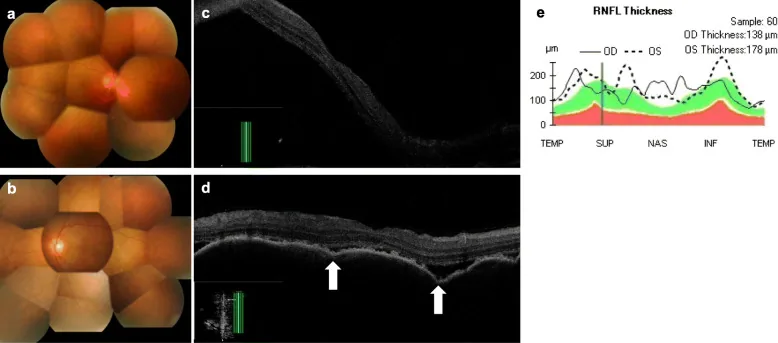
تعمل مثبطات نقاط التفتيش المناعية (مثبطات PD-1/PD-L1 ومثبطات CTLA-4) على تحرير نقاط التفتيش المناعية للخلايا التائية وتعزيز المناعة المضادة للورم. ومع ذلك، فإن هذه الآلية تحرر في الوقت نفسه آليات كبت المناعة الذاتية، مما يؤدي إلى إثارة تفاعلات مناعية ذاتية في أنسجة العين (العنبية، الصلبة، المحجر، الغدة الدمعية). في متلازمة فوغت-كوياناغي-هارادا الشبيهة، يتم تنشيط الخلايا التائية ذاتية التفاعل ضد الخلايا الصباغية (المشيمية، الجسم الهدبي، القزحية)، مما يؤدي إلى التهاب العنبية الشامل، انفصال الشبكية المصلي، وآفات إزالة التصبغ 3).
لفهم الصورة الكاملة للآثار الضارة العينية المرتبطة بالمناعة لمثبطات نقاط التفتيش المناعية، يتم إجراء دراسات سجل دولية متعددة المراكز 3). من خلال توضيح طيف وتواتر ونتائج الآثار الضارة العينية المتنوعة مثل التهاب العنبية، متلازمة فوغت-كوياناغي-هارادا الشبيهة، والتهاب العضلات خارج العين، يُتوقع تحقيق التقسيم الطبقي للمخاطر ووضع بروتوكولات.
تنتشر الأدوية المضادة للجسم المضاد مثل تراستوزوماب ديروكستيكان (T-DXd) كعلاج مضاد للسرطان من الجيل التالي، ولكن يُعترف باعتلال القرنية (التهاب القرنية النقطي السطحي، عتامة حمة القرنية) كحدث ضار 10). يمثل تجميع الحالات من خلال دراسات مراقبة الأدوية ووضع استراتيجيات حماية القرنية تحديًا.
باستخدام التصوير المقطعي التوافقي البصري التكيفي والتصوير متعدد الأطياف لقاع العين، تُبذل محاولات لتصور التغيرات المبكرة في بنية الظهارة الصباغية للشبكية التي لا يمكن اكتشافها بالطرق التقليدية 11). كما يتقدم تطوير الفحص التلقائي باستخدام الذكاء الاصطناعي لتحليل صور التصوير المقطعي التوافقي البصري، مما يُتوقع أن يقلل من خطر الفوات 11).
مع انتشار مثبطات نقاط التفتيش المناعية والأدوية المستهدفة جزيئيًا، يُطلب وضع بروتوكول تعاون موحد بين طب العيون وطب الأورام 8). يتقدم وضع إرشادات لخوارزمية إدارة الآثار الجانبية العينية بناءً على تصنيف CTCAE.
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.