Sitotoksik kemoterapi
5-FU: Göz yaşarması (lakrimal kanal darlığı), konjonktivit, kornea epitel hasarı1)
Sisplatin: Optik nöropati, renk görme bozukluğu (nadir)1)
Taksanlar (dosetaksel, paklitaksel): Göz yaşarması, kistoid makula ödemi4)

Kemoterapi ve hedefe yönelik ilaçların göz yan etkileri, kanser tedavisi ve immün hastalık tedavisinde kullanılan ilaçların göz dokusunda yan etkilere neden olduğu durumların genel adıdır.
İlgili ilaç kategorileri oldukça geniştir.
Kanser tedavisindeki gelişmelerle birlikte sağkalım süresi uzamış ve uzun süreli tedavi sırasında oküler yan etki yönetiminin önemi artmıştır1). Oküler yan etkiler hafif rahatsızlıktan geri dönüşümsüz görme kaybına kadar geniş bir yelpazede olup, uygun tarama ve erken müdahale görme prognozunu doğrudan etkiler.
Görme azalması, kızarıklık, göz ağrısı, uçuşan cisimler, fotopsi (ışık çakmaları) veya metamorfopsi (nesnelerin çarpık görülmesi) gibi belirtiler ortaya çıkarsa derhal bir göz doktoruna başvurun. Belirtiler hafif olsa bile ihmal edilirse geri dönüşümsüz hasara yol açabilir. Bu nedenle, tedaviyi yürüten doktora (onkolog) da bilgi verilmeli ve göz doktoru ile iş birliği yapılması önemlidir.
İlaç kategorisine göre ortaya çıkan oküler yan etkiler farklılık gösterir. Aşağıda başlıca ilaçlar ve gözle ilgili belirtileri sunulmuştur.
Sitotoksik kemoterapi
5-FU: Göz yaşarması (lakrimal kanal darlığı), konjonktivit, kornea epitel hasarı1)
Sisplatin: Optik nöropati, renk görme bozukluğu (nadir)1)
Taksanlar (dosetaksel, paklitaksel): Göz yaşarması, kistoid makula ödemi4)
Hormon tedavisi ve immünomodülatör ilaçlar
Tamoksifen: Makula çevresinde kristalin birikintiler, korneada girdap şeklinde bulanıklık, KME. Görülme sıklığı: yurtdışında %3-6, Japonya’da %0,2
HCQ/klorokin: Bull’s eye makülopati (halka şeklinde atrofi), görme azalması, gece körlüğü, renk görme anormalliği. 5 yıldan uzun kullanımda yaklaşık %0,5
İnterferon: Fundus arka kutbunda küçük kanamalar ve pamuk yünü lekeleri. Genellikle uygulamadan 2-3 ay sonra ortaya çıkar. Çoğu asemptomatiktir ve kendiliğinden geriler.
Hedefe Yönelik İlaçlar
MEK inhibitörleri (trametinib vb.): Seröz retina dekolmanı ve PED. Görülme sıklığı yaklaşık %10-252)
EGFR inhibitörleri (gefitinib vb.): Trikiyazis, blefarit ve kornea epitel hasarı5)
BRAF inhibitörleri (vemurafenib vb.): Üveit ve seröz retina dekolmanı6)
ALK inhibitörleri (krizotinib vb.): Fotopsi ve bulanık görme. Yaklaşık %60’ında görme bozukluğu gelişir7)
İmmün Kontrol Noktası İnhibitörleri (ICI)
Üveit (ön, arka, panüveit): Görülme sıklığı yaklaşık %13)
VKH benzeri sendrom: Yüksek doz steroid gerektiren şiddetli form3)
Kuru göz, konjonktivit, orbital inflamatuar hastalık ve ekstraoküler miyozit8)
ADC (T-DXd vb.): Kornea hasarı (punktat yüzeyel keratopati ve kornea stromal opasitesi)10)
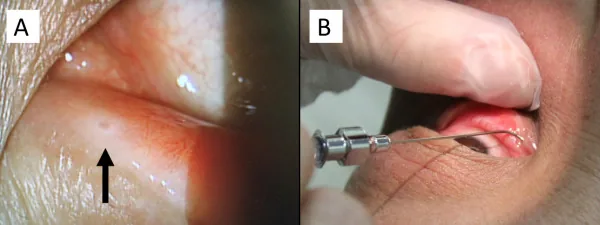
Multipl skleroz nükslerini önlemek için kullanılan fingolimod (Imusera/Gilenya), makula ödemine neden olabilir. Makula ödemi insidansı fingolimod 0.5 mg/gün’de %0.2, 1.25 mg/gün’de %1.4’tür ve çoğu tedavinin başlangıcından sonraki 3-4 ay içinde görülür.
Göz yan etkileri için risk faktörleri ilaç kategorisine göre değişir.
| İlaç Kategorisi | Başlıca Risk Faktörleri |
|---|---|
| HCQ/Klorokin | 5 yıldan uzun süreli kullanım, CQ >3.0 mg/kg/gün veya HCQ >6.5 mg/kg/gün, ileri yaş, böbrek/karaciğer yetmezliği, eşlik eden retina hastalığı |
| Tamoksifen | Yüksek doz ve uzun süreli kullanım (kümülatif doz artışı) |
| İnterferon | Yüksek başlangıç dozu, ileri yaş, diyabet, hipertansiyon, anemi |
| MEK İnhibitörleri | Doz bağımlı (yüksek dozda sıklık artar) 2) |
| ICI | Sistemik irAE (tiroidit, kolit vb.) olan hastalarda oküler irAE de daha sık görülür 3) |
| ADC | İlaca özgü korneal toksisite mekanizması 10) |
HCQ retinopatisi için spesifik risk faktörleri şunlardır:
İnterferon retinopatisi, diyabet, hipertansiyon ve anemi gibi sistemik hastalıkların varlığında daha sık ve şiddetli seyreder; tedaviye dirençli veya tekrarlayan vakalarda da daha sık görülür.
AAO (Amerikan Oftalmoloji Akademisi) önerisine9) dayanarak aşağıdaki tarama yapılır:
Yararlı testler arasında Humphrey 10-2 santral görme alanı testi, SD-OCT, fundus otofloresansı, multifokal ERG ve tam alan ERG bulunur. Bull’s eye (halka şeklinde atrofi) ilerlemiş HCQ retinopatisinin karakteristik fundus bulgusudur.
| İlaç | Tarama Zamanı ve Test |
|---|---|
| HCQ/Klorokin | Tedavi başlangıcında bazal + 5 yıldan sonra yılda bir kez (SD-OCT, 10-2 görme alanı, FAF) 9) |
| Tamoksifen | Semptom ortaya çıktığında ve düzenli fundus muayenesi ve SD-OCT |
| İnterferon | Tedavi başlangıcından 2-3 ay sonra fundus muayenesi. Semptom varsa hemen göz doktoruna başvuru |
| MEK İnhibitörleri | Görme azalması veya metamorfopsi durumunda OCT ile seröz retina dekolmanı doğrulaması 2) |
| ICI | Görme azalması, kızarıklık veya göz ağrısı durumunda hemen göz doktoruna başvuru 3) |
| Fingolimod | Tedavi öncesi bazal fundus muayenesi + tedaviden 3-4 ay sonra takip |
ICI kullanan hastalarda görme azalması, kızarıklık veya göz ağrısı geliştiğinde, ön kamara inflamatuar hücreleri, vitreus bulanıklığı ve koroid lezyonları değerlendirilmeli ve irAE olarak üveit veya VKH benzeri sendrom olasılığı akılda tutulmalıdır 3).
Tedavi başlangıcında temel olarak görme keskinliği, fundus muayenesi ve SD-OCT’yi içeren bir göz muayenesi yapılması önerilir. Daha sonra, risk faktörleri (5 yıldan uzun tedavi süresi, yüksek doz, ileri yaş, böbrek yetmezliği vb.) yoksa, 5. yıldan itibaren yılda bir tarama başlatılır. Risk faktörleri varsa daha erken ve daha sık muayene gerekir. SD-OCT, Humphrey 10-2 görme alanı testi ve fundus otofloresansı başlıca muayene yöntemleridir.
Tek tedavi ilacın kesilmesidir. İlacın vücuttan atılımı yavaş olduğu için, ilaç kesildikten sonra da lezyonlar ilerleyebilir ve kötüleşebilir. Bu nedenle erken tanı son derece önemlidir ve geri dönüşümsüz hasar oluşmadan önce ilacın kesilmesine karar verilmesi görme prognozunu belirler.
Çoğu vakanın prognozu iyidir ve asemptomatikse temel olarak IFN tedavisinin sonlanması beklenir. Şiddetli vakalarda veya görme azalması durumunda IFN dozunun azaltılması veya kesilmesi düşünülür. Diyabet veya hipertansiyon birlikteliğinde erken müdahale gerekir.
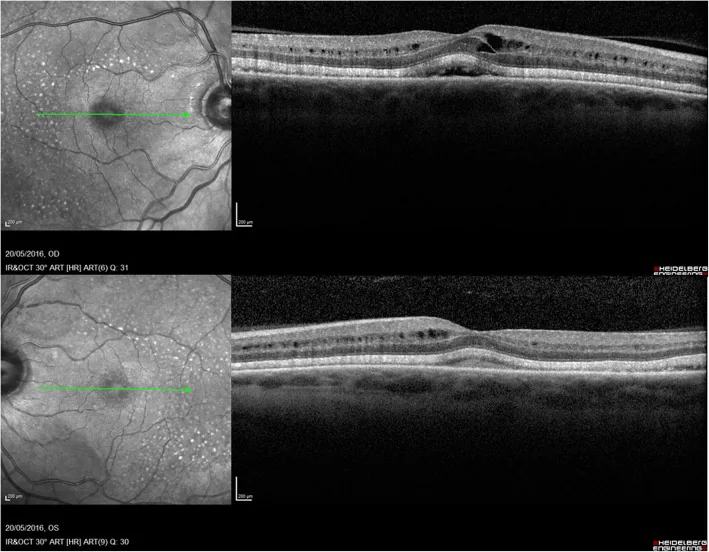
CTCAE derecesine göre yönetilir 3).
Çoğu vakada ilacın kesilmesiyle düzelir. Gerekirse NSAID damla ve steroid damla eklenir.
Her zaman durdurulması gerekmez. Göz yan etkisinin şiddeti (CTCAE derecesi) ve ilaç türüne göre yaklaşım değişir. HCQ retinopatisi veya tamoksifen retinopatisi gibi durumlarda ilacın kesilmesi temel yaklaşım iken, MEK inhibitörlerine bağlı hafif seröz retina dekolmanı veya EGFR inhibitörlerine bağlı trikiyazis gibi durumlarda semptomatik tedavi ile ilaca devam edilebilir. Tıbbi onkolog ve göz doktorunun iş birliği ile her duruma göre karar verilmesi önemlidir.
Her ilaç kategorisi için göz dokusuna hasar mekanizması farklıdır.
CQ ve HCQ melanine yüksek afinite gösterir, retina pigment epitel (RPE) hücrelerindeki melanin granüllerine bağlanarak hücre içinde birikir. Biriken CQ/HCQ lizozomlara alınır ve lizozom pH’sını yükselterek lizozomal enzim aktivitesini bozar. RPE’nin enzimatik metabolik fonksiyonu bozulduğunda, fotoreseptör dış segmentlerinin yıkımı ve yenilenmesi bozulur ve fotoreseptör dejenerasyonuna ilerler. Vücutta birikim miktarı yüksek olduğundan, ilaç kesildikten sonra da hasar ilerleyebilir.
Sinir lifi tabakası ve iç pleksiform tabakada küresel lezyonlar (sinir lifi dejenerasyonu ve aksonal şişme) oluşur. Kristaloid birikintiler, kalsiyum ve kompleks karbonhidratlar içeren dejeneratif ürünlerin sinir lifleri içinde birikmesi olarak düşünülmektedir. Kistoid makula ödemi (CME), Müller hücre fonksiyon bozukluğu ve sıvı birikimi sonucu oluşur.
IFN, vazospazm, lökosit infiltrasyonu ve vasküler endotel hasarını tetikler; immün komplekslerin kılcal damarlara birikmesi kılcal tıkanıklığa yol açar. Tıkalı kılcal damarın önünde (arteryel tarafta) pamuk yünü lekeleri (sinir lifi tabakası enfarktüsü) oluşur ve tıkanıklık kanaması küçük kanamalar olarak gözlenir. Çoğu geçicidir ve IFN kesildikten sonra geriler.
MEK inhibitörleri MAPK/ERK yolunu (hücre çoğalması ve hayatta kalma sinyali) bloke eder. RPE, aktif taşıma (iyon ve su) için ERK sinyaline bağımlıdır; bu nedenle ERK inhibisyonu RPE’nin iyon taşıma ve pompa fonksiyonunu bozar. Sonuç olarak, subretinal sıvı birikimi oluşur ve seröz retina dekolmanı ve retina pigment epitel dekolmanı (PED) olarak ortaya çıkar 2).
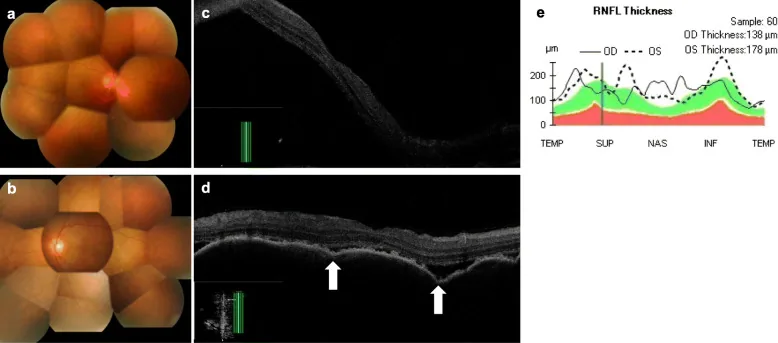
ICI’ler (PD-1/PD-L1 inhibitörleri, CTLA-4 inhibitörleri) T hücrelerinin immün kontrol noktalarını kaldırarak antitümör immüniteyi güçlendirir. Ancak bu mekanizma aynı zamanda otoimmün baskılama mekanizmalarını da ortadan kaldırarak göz dokularına (uvea, sklera, orbita, lakrimal bez) karşı otoimmün reaksiyonu tetikler. VKH benzeri sendromda, melanositlere (koroid, siliyer cisim, iris) karşı oto-reaktif T hücreleri aktive olur ve panüveit, seröz retina dekolmanı ve depigmentasyon lezyonları oluşur 3).
ICI ile ilişkili oküler irAE’nin genel tablosunu anlamak için uluslararası çok merkezli bir kayıt çalışması yürütülmektedir 3). Üveit, VKH benzeri sendrom, ekstraoküler miyozit gibi çeşitli oküler irAE’lerin spektrumu, sıklığı ve sonuçlarının aydınlatılmasıyla risk sınıflandırması ve protokol oluşturulması beklenmektedir.
Trastuzumab derukstekan (T-DXd) başta olmak üzere ADC’ler, yeni nesil kanser tedavileri olarak yaygınlaşmaktadır, ancak kornea toksisitesi (punktat yüzeyel keratopati, korneal stromal opasite) bir advers olay olarak tanınmaktadır 10). İlaç izleme çalışmalarıyla vaka birikimi ve kornea koruma stratejilerinin oluşturulması zorluklar arasındadır.
Adaptif optik OCT ve multispektral fundus görüntüleme ile geleneksel yöntemlerle tespit edilemeyen erken RPE yapısal değişikliklerinin görselleştirilmesi denenmektedir 11). Ayrıca yapay zeka (AI) kullanılarak OCT görüntü analizi ile otomatik taramanın geliştirilmesi ilerlemekte olup, gözden kaçırma riskinin azaltılması beklenmektedir 11).
ICI ve moleküler hedefli ilaçların yaygınlaşmasıyla birlikte, oftalmoloji ve onkoloji arasında standartlaştırılmış işbirliği protokollerinin oluşturulması gerekmektedir 8). CTCAE derecelendirmesine dayalı oküler yan etki yönetim algoritmasının kılavuz haline getirilmesi ilerlemektedir.
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.