세포독성 화학요법

항암제 및 분자표적치료제의 안구 부작용
1. 항암제 및 분자표적약에 의한 눈 부작용이란?
섹션 제목: “1. 항암제 및 분자표적약에 의한 눈 부작용이란?”항암제 및 분자표적약에 의한 눈 부작용은 암 치료 및 면역 질환 치료에 사용되는 약물이 눈 조직에 유해 사건을 일으키는 병태의 총칭입니다.
대상이 되는 약물 범주는 광범위합니다.
- 세포독성 화학요법(5-FU, 시스플라틴, 탁산류 등): 유루, 각막상피장애, 시신경병증 등 1)
- 호르몬 요법(타목시펜 등): 결정형 황반 침착물, CME, 각막 소용돌이 혼탁
- 면역조절제(클로로퀸, 하이드록시클로로퀸, 인터페론): 망막병증, 안저 출혈, 면화반
- 분자표적약물 (MEK 억제제, EGFR 억제제, BRAF 억제제, ALK 억제제 등): 각 약물에 특이적인 안구 부작용2)
- 면역관문억제제(ICI) (니볼루맙, 펨브롤리주맙 등): irAE로서의 포도막염, VKH 유사 증후군3)
- 항체약물접합체(ADC) (트라스투주맙 데룩스테칸 등): 각막 손상10)
암 치료의 발전으로 생존 기간이 연장되면서 장기 치료 중 안구 부작용 관리의 중요성이 증가하고 있습니다1). 안구 부작용은 경미한 불편감에서 비가역적 시력 장애까지 다양하며, 적절한 선별 검사와 조기 개입이 시력 예후에 직접적인 영향을 미칩니다.
2. 약물 범주별 증상 및 임상 소견
섹션 제목: “2. 약물 범주별 증상 및 임상 소견”약물 범주별로 발생하는 안구 부작용이 다릅니다. 아래에 주요 약물과 그 안구 증상을 제시합니다.
호르몬 요법 및 면역조절제
타목시펜: 황반주위 결정형 침착물, 각막 소용돌이 혼탁, CME. 발생률: 해외 3~6%, 국내 0.2%
HCQ/클로로퀸: 황소눈 황반병증(환상 위축), 시력 저하, 야맹증, 색각 이상. 5년 이상 투여 시 약 0.5%
인터페론: 안저 후극부의 소출혈 및 면화반. 투여 후 2~3개월 이내에 발생. 대부분 무증상이며 자연 소실됨.
분자 표적 약물
면역관문억제제(ICI)
핑골리모드에 의한 황반 부종
섹션 제목: “핑골리모드에 의한 황반 부종”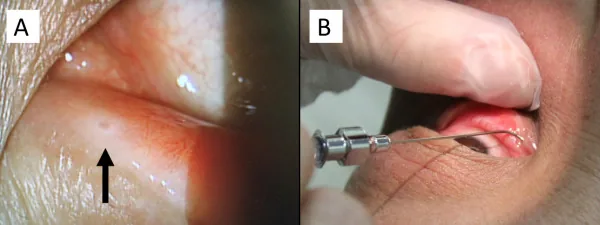
다발성 경화증의 재발 예방에 사용되는 핑골리모드(이무세라/질레니아)는 황반 부종을 일으키는 것으로 알려져 있습니다. 황반 부종의 발현율은 핑골리모드 0.5mg/일에서 0.2%, 1.25mg/일에서 1.4%이며, 대부분 투여 시작 후 3~4개월 이내에 나타납니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”약물 범주별로 안구 부작용의 위험 요인이 다릅니다.
| 약물 범주 | 주요 위험 요인 |
|---|---|
| HCQ/클로로퀸 | 5년 이상 투여, CQ >3.0 mg/kg/일 또는 HCQ >6.5 mg/kg/일, 고령, 신장/간 기능 장애, 망막 질환 동반 |
| 타목시펜 | 고용량·장기 사용 (누적 투여량 증가) |
| 인터페론 | 높은 초기 투여량, 고령, 당뇨병, 고혈압, 빈혈 |
| MEK 억제제 | 용량 의존성 (고용량에서 빈도 증가) 2) |
| ICI | 전신 irAE(갑상선염, 대장염 등) 동반 시 안구 irAE도 발생하기 쉬움 3) |
| ADC | 약물 고유의 각막 독성 메커니즘 10) |
HCQ 망막병증의 구체적인 위험인자는 다음과 같습니다.
- 투여 기간: 5년 이상 장기 투여 (누적: CQ >460 g, HCQ >1,000 g)
- 1일 투여량: CQ >3.0 mg/kg/일, HCQ >6.5 mg/kg/일
- 전신 위험: 고령, 신기능 저하(HCQ 배설 지연), 간기능 장애
- 안구 국소 위험: 기존 망막 질환 또는 황반병증 동반
인터페론 망막병증은 당뇨병, 고혈압, 빈혈 등의 전신 질환이 있는 경우 더 빈번하고 중증화되기 쉬우며, 치료 저항성 또는 재발 사례에서도 발생하기 쉽습니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”HCQ 선별 검사 프로토콜
섹션 제목: “HCQ 선별 검사 프로토콜”미국 안과학회(AAO)의 권고9)에 따라 다음과 같은 선별 검사를 시행합니다.
- 투여 시작 시(기저): 시력, 안저, SD-OCT 검사
- 투여 시작 후 5년: 고위험 인자가 없으면 연 1회 선별 검사 시작
- 위험 인자 있음: 5년을 기다리지 않고 조기에 선별 검사 시작, 간격도 단축
- 권장 투여량 상한: 실제 체중 기준 5 mg/kg/일 이하9)
검사 항목으로는 Humphrey 10-2 중심 시야 검사, SD-OCT, 안저 자가 형광, 다초점 ERG, 전시야 ERG가 유용합니다. 황소눈(윤상 위축)은 진행된 HCQ 망막병증의 특징적인 안저 소견입니다.
약제별 선별 검사 권장
섹션 제목: “약제별 선별 검사 권장”| 약물 | 선별검사 시기와 검사 |
|---|---|
| HCQ/클로로퀸 | 투여 시작 시 기준치 + 5년 이후 매년 1회 (SD-OCT, 10-2 시야, FAF) 9) |
| 타목시펜 | 증상 발생 시 및 정기적인 안저검사, SD-OCT |
| 인터페론 | 투여 시작 후 2~3개월에 안저검사. 증상이 있으면 즉시 안과 진료 |
| MEK 억제제 | 시력 저하 또는 변시증 발생 시 OCT로 장액성 망막박리 확인 2) |
| ICI | 시력 저하, 충혈, 안통 발생 시 즉시 안과 진료 3) |
| 핑골리모드 | 투여 전 기준 안저검사 + 투여 후 3~4개월에 추적 관찰 |
ICI 사용 환자에서 시력 저하, 충혈, 안통이 발생한 경우, 전방 내 염증 세포, 유리체 혼탁, 맥락막 병변을 평가하고 irAE로서의 포도막염 또는 VKH 유사 증후군의 가능성을 염두에 두어야 합니다 3).
투여 시작 시 기저 검사로 시력, 안저, SD-OCT를 포함한 안과 검사를 받는 것이 권장됩니다. 이후 위험 인자(투여 기간 5년 이상, 고용량, 고령, 신기능 장애 등)가 없으면 5년 이후부터 연 1회 선별 검사를 시작합니다. 위험 인자가 있는 경우 더 조기에, 더 자주 검사가 필요합니다. SD-OCT, Humphrey 10-2 시야 검사, 안저 자가형광이 주요 검사 항목입니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”HCQ/클로로퀸 망막병증
섹션 제목: “HCQ/클로로퀸 망막병증”투여 중단이 유일한 치료법입니다. 체내 배출이 느리기 때문에 투약 중단 후에도 병변이 진행·악화될 수 있습니다. 따라서 조기 발견이 매우 중요하며, 비가역적 손상이 발생하기 전 단계에서의 약물 중단 결정이 시력 예후를 좌우합니다.
타목시펜 안구 부작용
섹션 제목: “타목시펜 안구 부작용”- 기본: 가능한 한 투여 중단. 중단으로 진행이 멈추고 때로는 호전됩니다.
- CME: CME가 소실되지 않으면 항VEGF 약물이 효과적입니다.
- 크리스탈린 침착: 투여 중단 후에도 잔존하는 경우가 많으며, 완전한 소실은 기대하기 어렵습니다.
- 각막 소용돌이 혼탁: 경증에서는 경과 관찰. 중증에서는 투여 중단을 고려합니다.
인터페론 망막병증
섹션 제목: “인터페론 망막병증”대부분의 증례는 예후가 좋으며, 무증상이면 기본적으로 IFN 치료 종료를 기다리는 방침입니다. 중증 증례·시력 저하 증례에서는 IFN 감량·중단을 고려합니다. 당뇨병·고혈압 합병 증례에서는 조기 대처가 필요합니다.
MEK 억제제에 의한 장액성 망막박리
섹션 제목: “MEK 억제제에 의한 장액성 망막박리”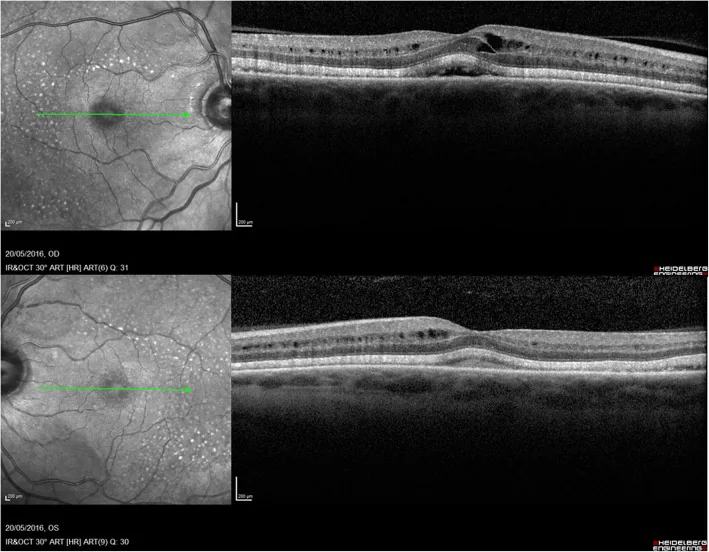
- 중등도 이상의 장액성 망막박리에서는 약물 중단 또는 감량을 시행합니다2)
- 경증의 경우 경과 관찰하면서 투여를 지속할 수 있으며, 대부분 자연적으로 호전됩니다2)
- 중단 또는 감량 후 망막하액의 소실을 확인합니다
EGFR 억제제에 의한 안구 부작용
섹션 제목: “EGFR 억제제에 의한 안구 부작용”- 속눈썹 난생(trichiasis): 변형된 속눈썹은 제거술을 시행합니다5)
- 안검염: 스테로이드 연고·항생제 연고를 외용합니다5)
- 각막 상피 장애: 방부제 없는 인공눈물·각막 보호 점안액
ICI 관련 포도막염
섹션 제목: “ICI 관련 포도막염”CTCAE 등급에 따라 관리합니다3).
- 1등급(경증): 스테로이드 점안액으로 관리. ICI 지속 가능
- 2등급(중등도): 스테로이드 전신 투여(프레드니솔론). ICI 일시 중단 고려
- 3~4등급(중증): 고용량 스테로이드 전신 투여. ICI 중단·영구 중단 고려
- VKH 유사 증후군: 메틸프레드니솔론 1g/일 × 3일간 펄스 요법 후 경구 스테로이드 감량8)
핑골리모드 황반부종
섹션 제목: “핑골리모드 황반부종”투여 중단으로 많은 예에서 호전됩니다. 필요에 따라 NSAIDs 점안액이나 스테로이드 점안액을 병용합니다.
반드시 중단이 필요한 것은 아닙니다. 안구 부작용의 중증도(CTCAE 등급)와 약제 종류에 따라 대응이 다릅니다. HCQ 망막증이나 타목시펜 망막증처럼 투여 중단이 기본이 되는 경우가 있는 반면, MEK 억제제의 경미한 장액성 망막박리나 EGFR 억제제의 속눈썹 난생에서는 대증요법을 시행하면서 투여를 지속하는 경우도 있습니다. 종양내과 주치의와 안과가 협력하여 개별 상황에 맞게 판단하는 것이 중요합니다.
6. 병태생리학·상세한 발병 기전
섹션 제목: “6. 병태생리학·상세한 발병 기전”약제 범주별로 안구 조직에 대한 손상 기전이 다릅니다.
클로로퀸·HCQ의 망막 독성
섹션 제목: “클로로퀸·HCQ의 망막 독성”CQ·HCQ는 멜라닌 친화성이 높아 망막색소상피(RPE) 세포의 멜라닌 과립과 결합하여 세포 내에 축적됩니다. 축적된 CQ/HCQ는 리소좀에 흡수되어 리소좀의 pH 상승을 일으키고 리소좀 효소의 활성을 손상시킵니다. RPE의 효소 대사 기능이 손상되면 광수용체 외절의 분해·갱신이 장애되어 광수용체 변성으로 진행됩니다. 체내 축적량이 많기 때문에 투여 중단 후에도 손상이 진행될 수 있습니다.
타목시펜 망막증의 기전
섹션 제목: “타목시펜 망막증의 기전”신경섬유층·내망상층에 구상 병소(신경섬유의 변성·축삭 종창)가 형성됩니다. 결정형 침착물은 칼슘과 복합당질을 포함하는 변성 산물이 신경섬유 내에 침착된 것으로 생각됩니다. 낭포황반부종(CME)은 뮐러 세포의 기능 장애·액체 저류로 인해 발생합니다.
인터페론 망막증의 기전
섹션 제목: “인터페론 망막증의 기전”IFN은 혈관 연축·백혈구 침윤·혈관 내피 손상을 유발하고, 면역 복합체가 모세혈관에 침착되어 모세혈관 폐쇄를 일으킵니다. 폐쇄된 모세혈관의 앞쪽(동맥 측)에 면화반(신경섬유층 경색)이 생기고, 폐쇄부 출혈이 소출혈로 관찰됩니다. 대부분 일과성이며, IFN 중단 후 소실됩니다.
MEK 억제제에 의한 장액성 망막박리
섹션 제목: “MEK 억제제에 의한 장액성 망막박리”MEK 억제제는 MAPK/ERK 경로(세포 증식·생존 신호)를 차단합니다. RPE는 ERK 신호에 의해 능동 수송(이온·수분)을 유지하므로, ERK 억제로 인해 RPE의 이온 수송·펌프 기능이 손상됩니다. 그 결과 망막하 액체 저류가 발생하여 장액성 망막박리·망막색소상피박리(PED)로 나타납니다2).
면역관문억제제(ICI)의 안구 irAE
섹션 제목: “면역관문억제제(ICI)의 안구 irAE”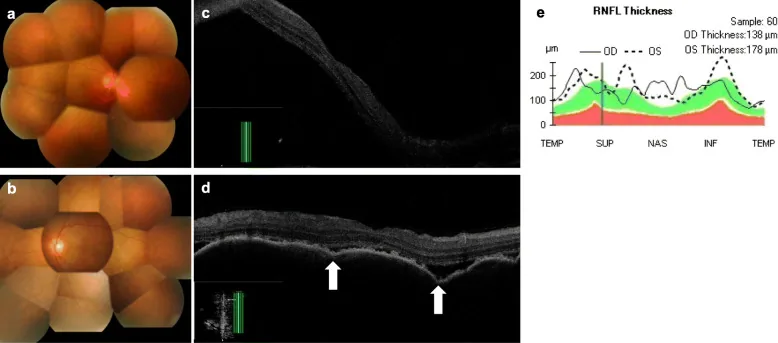
ICI(PD-1/PD-L1 억제제, CTLA-4 억제제)는 T세포의 면역관문을 해제하여 항종양 면역을 강화합니다. 그러나 이 기전은 동시에 자가면역 억제 기전을 해제하여 안구 조직(포도막, 공막, 안와, 눈물샘)에 대한 자가면역 반응을 유발합니다. VKH 유사 증후군에서는 멜라닌세포(맥락막, 섬모체, 홍채)에 대한 자가반응성 T세포가 활성화되어 범포도막염, 장액성 망막박리, 탈색소 병변이 발생합니다3).
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”ICI 관련 안구 irAE 대규모 레지스트리 연구
섹션 제목: “ICI 관련 안구 irAE 대규모 레지스트리 연구”ICI 관련 안구 irAE의 전체상을 파악하기 위해 국제 다기관 레지스트리 연구가 진행 중입니다3). 포도막염, VKH 유사 증후군, 외안근염 등 다양한 안구 irAE의 스펙트럼, 빈도, 전환을 밝힘으로써 위험 계층화와 프로토콜 확립이 기대됩니다.
항체-약물 접합체(ADC)의 각막 독성
섹션 제목: “항체-약물 접합체(ADC)의 각막 독성”트라스투주맙 데룩스테칸(T-DXd)을 비롯한 ADC는 차세대 항암 요법으로 보급되고 있지만, 각막 독성(점상 표층 각막증, 각막 실질 혼탁)이 유해 사례로 인식되고 있습니다10). 약물 감시 연구를 통한 증례 축적과 각막 보호 전략 수립이 과제입니다.
HCQ 망막증의 초극초기 검출
섹션 제목: “HCQ 망막증의 초극초기 검출”적응 광학 OCT와 다중 스펙트럼 안저 촬영을 통해 기존 방법으로는 검출할 수 없는 초기 RPE 구조 변화의 가시화가 시도되고 있습니다11). 또한 인공지능(AI)을 이용한 OCT 영상 분석을 통한 자동 선별 검사 개발도 진행 중이며, 누락 위험 감소가 기대됩니다11).
안과·종양내과 협력 프로토콜 확립
섹션 제목: “안과·종양내과 협력 프로토콜 확립”ICI 및 분자 표적 약물의 보급에 따라 안과와 종양내과의 표준화된 협력 프로토콜 확립이 요구됩니다8). CTCAE 등급에 기반한 안구 부작용 관리 알고리즘의 가이드라인화가 진행 중입니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”-
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
-
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
-
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
-
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
-
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
-
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
-
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
-
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
-
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
-
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
-
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.
