殺細胞性化学療法

抗がん剤・分子標的薬による眼の副作用(Anticancer Drug and Targeted Therapy Ocular Side Effects)
1. 抗がん剤・分子標的薬による眼の副作用とは
Section titled “1. 抗がん剤・分子標的薬による眼の副作用とは”抗がん剤・分子標的薬による眼の副作用とは、がん治療・免疫疾患治療に用いられる薬剤が眼組織に有害事象を引き起こす病態の総称である。
対象となる薬剤カテゴリは広範にわたる。
- 殺細胞性化学療法(5-FU・シスプラチン・タキサン類等):流涙・角膜上皮障害・視神経症など1)
- ホルモン療法(タモキシフェン等):クリスタリン状黄斑沈着物・CME・角膜渦状混濁
- 免疫調整薬(クロロキン・ヒドロキシクロロキン・インターフェロン):網膜症・眼底出血・綿花様白斑
- 分子標的薬(MEK阻害薬・EGFR阻害薬・BRAF阻害薬・ALK阻害薬等):各薬剤に特有の眼副作用2)
- 免疫チェックポイント阻害薬(ICI)(ニボルマブ・ペムブロリズマブ等):irAEとしてのぶどう膜炎・VKH様症候群3)
- 抗体薬物複合体(ADC)(トラスツズマブ デルクステカン等):角膜障害10)
がん治療の発展に伴い生存期間が延長し、長期治療中の眼副作用管理の重要性が増大している1)。眼副作用は軽微な不快感から不可逆的な視力障害まで幅広く、適切なスクリーニングと早期介入が視力予後に直結する。
2. 薬剤カテゴリ別の症状と臨床所見
Section titled “2. 薬剤カテゴリ別の症状と臨床所見”薬剤カテゴリごとに生じる眼副作用は異なる。以下に主な薬剤とその眼症状を示す。
ホルモン療法・免疫調整薬
分子標的薬
免疫チェックポイント阻害薬(ICI)
フィンゴリモドによる黄斑浮腫
Section titled “フィンゴリモドによる黄斑浮腫”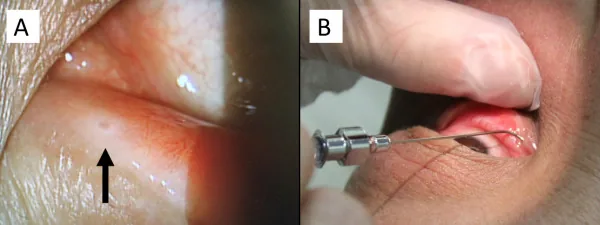
多発性硬化症の再発予防に用いるフィンゴリモド(イムセラ/ジレニア)は、黄斑浮腫を生じることが知られている。黄斑浮腫の発現率はフィンゴリモド0.5 mg/日で0.2%、1.25 mg/日で1.4%であり、多くは投与開始3〜4か月以内に認められる。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”薬剤カテゴリごとに眼副作用のリスク因子は異なる。
| 薬剤カテゴリ | 主要なリスク因子 |
|---|---|
| HCQ/クロロキン | 5年以上の投与期間、CQ >3.0 mg/kg/日 or HCQ >6.5 mg/kg/日、高齢、腎・肝機能障害、網膜疾患合併 |
| タモキシフェン | 高用量・長期使用(累積投与量増加) |
| インターフェロン | 高初期投与量、高齢、糖尿病、高血圧、貧血 |
| MEK阻害薬 | 投与量依存性(高用量で頻度増加)2) |
| ICI | 全身のirAE合併例(甲状腺炎・大腸炎等)で眼irAEも生じやすい3) |
| ADC | 薬剤固有の角膜毒性メカニズム10) |
HCQ網膜症の具体的な危険因子として以下が挙げられる。
- 投与期間: 5年以上の長期投与(累積:CQ >460 g、HCQ >1,000 g)
- 1日投与量: CQ >3.0 mg/kg/日、HCQ >6.5 mg/kg/日
- 全身リスク: 高齢、腎機能低下(HCQ排泄遅延)、肝機能障害
- 眼局所リスク: 既存の網膜疾患・黄斑症の合併
インターフェロン網膜症は糖尿病・高血圧・貧血などの全身疾患がある場合に高頻度で重症化しやすく、治療抵抗例や再発例でも発生しやすい。
4. 診断と検査方法
Section titled “4. 診断と検査方法”HCQスクリーニングプロトコル
Section titled “HCQスクリーニングプロトコル”AAO(米国眼科学会)の推奨9)に基づき、以下のスクリーニングを行う。
- 投与開始時(ベースライン): 視力・眼底・SD-OCT検査
- 投与開始後5年間: 高リスク因子がなければ年1回のスクリーニングを開始
- リスク因子あり: 5年を待たず早期からスクリーニング開始、間隔も短縮する
- 推奨投与量上限: 実体重あたり5 mg/kg/日以下9)
検査項目としては、Humphrey 10-2中心視野検査・SD-OCT・眼底自発蛍光・多局所ERG・全視野ERGが有用である。bull’s eye(輪状萎縮)は進行したHCQ網膜症に特徴的な眼底所見である。
薬剤別スクリーニング推奨
Section titled “薬剤別スクリーニング推奨”| 薬剤 | スクリーニング時期と検査 |
|---|---|
| HCQ/クロロキン | 投与開始時ベースライン + 5年以降年1回(SD-OCT・10-2視野・FAF)9) |
| タモキシフェン | 症状出現時および定期的な眼底検査・SD-OCT |
| インターフェロン | 投与開始後2〜3か月で眼底検査。症状あれば速やかに眼科受診 |
| MEK阻害薬 | 視力低下・変視症出現時にOCTで漿液性網膜剥離確認2) |
| ICI | 視力低下・充血・眼痛出現時に速やかに眼科受診3) |
| フィンゴリモド | 投与前ベースライン眼底検査 + 投与後3〜4か月でフォローアップ |
ICI使用患者で視力低下・充血・眼痛が生じた場合は、前房内炎症細胞・硝子体混濁・脈絡膜病変の評価を行い、irAEとしてのぶどう膜炎・VKH様症候群の可能性を念頭に置く3)。
投与開始時にベースラインとして視力・眼底・SD-OCTを含む眼科検査を受けることが推奨される。その後、リスク因子(5年以上の投与期間・高用量・高齢・腎機能障害等)がなければ5年以降から年1回のスクリーニングを開始する。リスク因子がある場合はより早期・頻回の検査が必要となる。SD-OCT・Humphrey 10-2視野検査・眼底自発蛍光が主な検査項目である。
5. 標準的な治療法
Section titled “5. 標準的な治療法”HCQ/クロロキン網膜症
Section titled “HCQ/クロロキン網膜症”投与中止が唯一の治療法である。体内からの排出が遅いため、投薬中止後も病変が進行・悪化することがある。このため早期発見が極めて重要であり、不可逆的な障害が生じる前の段階での薬剤中止判断が視力予後を左右する。
タモキシフェン眼副作用
Section titled “タモキシフェン眼副作用”- 基本: 可能な限り投与中止。中止により進行が停止し、時に軽快する
- CME: CMEが消失しない場合は抗VEGF薬が有効
- クリスタリン沈着: 投与中止後も残存することが多く、完全な消失は期待しにくい
- 角膜渦状混濁: 軽症例では経過観察。重症例では投与中止を検討
インターフェロン網膜症
Section titled “インターフェロン網膜症”多くの症例は予後良好であり、無症状であれば基本的にIFN療法の終了を待つ方針とする。重症例・視力低下例ではIFNの減量・中止を検討する。糖尿病・高血圧の合併例では早期の対処が必要となる。
MEK阻害薬による漿液性網膜剥離
Section titled “MEK阻害薬による漿液性網膜剥離”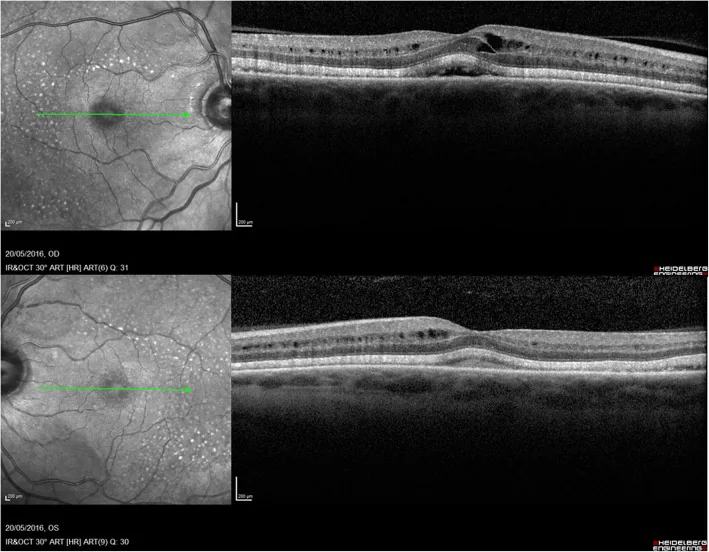
- 中等度以上の漿液性網膜剥離では薬剤中止または減量を行う2)
- 軽度の場合は経過観察しつつ投与継続も可能であり、多くは自然軽快する2)
- 中止・減量後に網膜下液の消退を確認する
EGFR阻害薬による眼副作用
Section titled “EGFR阻害薬による眼副作用”- 睫毛乱生(trichiasis): 変形した睫毛は抜去処置を行う5)
- 眼瞼炎: ステロイド軟膏・抗生物質軟膏を外用する5)
- 角膜上皮障害: 防腐剤フリー人工涙液・角膜保護点眼
ICI関連ぶどう膜炎
Section titled “ICI関連ぶどう膜炎”CTCAEグレードに基づいて管理する3)。
- Grade 1(軽度): ステロイド点眼で管理。ICI継続可能
- Grade 2(中等度): ステロイド全身投与(プレドニゾロン)。ICI一時休薬を検討
- Grade 3〜4(重症): 高用量ステロイド全身投与。ICI休薬・永久中止を検討
- VKH様症候群: メチルプレドニゾロン1 g/日 × 3日間のパルス療法後、経口ステロイド漸減8)
フィンゴリモド黄斑浮腫
Section titled “フィンゴリモド黄斑浮腫”投与中止により多くの例で改善する。必要に応じてNSAIDs点眼・ステロイド点眼を併用する。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”薬剤カテゴリごとに眼組織への障害機序は異なる。
クロロキン・HCQの網膜毒性
Section titled “クロロキン・HCQの網膜毒性”CQ・HCQはメラニン親和性が高く、網膜色素上皮(RPE)細胞のメラニン顆粒と結合して細胞内に蓄積する。蓄積したCQ/HCQはライソゾームに取り込まれてライソゾームのpH上昇を引き起こし、ライソゾーム酵素の活性を障害する。RPEの酵素代謝機能が障害されると、光受容体外節の分解・更新が障害され、光受容体変性へと進行する。体内蓄積量が多いため、投与中止後も障害が進行しうる。
タモキシフェン網膜症の機序
Section titled “タモキシフェン網膜症の機序”神経線維層・内網状層に球状病巣(神経線維の変性・軸索腫脹)が形成される。クリスタリン状沈着物はカルシウムや複合糖質を含む変性産物が神経線維内に沈着したものと考えられている。嚢胞様黄斑浮腫(CME)はMüller細胞の機能障害・液体貯留によって生じる。
インターフェロン網膜症の機序
Section titled “インターフェロン網膜症の機序”IFNは血管れん縮・白血球浸潤・血管内皮障害を誘発し、免疫複合体が毛細血管に沈着することで毛細血管閉塞を引き起こす。閉塞した毛細血管の前方(動脈側)に綿花様白斑(神経線維層梗塞)が生じ、閉塞部出血が小出血として観察される。多くは一過性であり、IFN中止後に消退する。
MEK阻害薬による漿液性網膜剥離
Section titled “MEK阻害薬による漿液性網膜剥離”MEK阻害薬はMAPK/ERK経路(細胞増殖・生存シグナル)を遮断する。RPEはERKシグナルにより能動輸送(イオン・水分)を維持しているため、ERK阻害によってRPEのイオン輸送・ポンプ機能が障害される。その結果、網膜下の液体貯留が生じ、漿液性網膜剥離・網膜色素上皮剥離(PED)として発現する2)。
免疫チェックポイント阻害薬(ICI)の眼irAE
Section titled “免疫チェックポイント阻害薬(ICI)の眼irAE”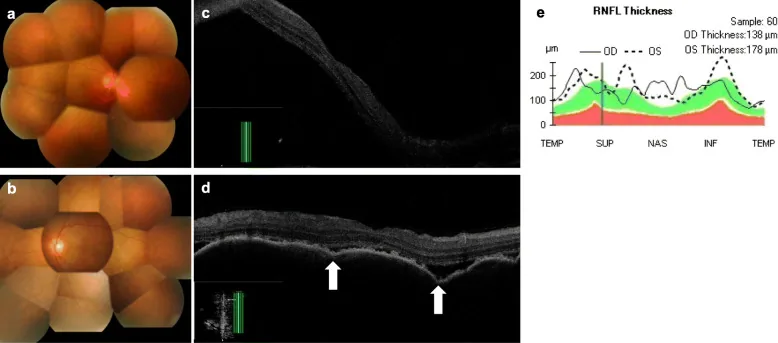
ICI(PD-1/PD-L1阻害薬・CTLA-4阻害薬)はT細胞の免疫チェックポイントを解除し、抗腫瘍免疫を増強する。しかしこの機序は同時に自己免疫抑制機構を解除し、眼組織(ぶどう膜・強膜・眼窩・涙腺)への自己免疫反応を惹起する。VKH様症候群ではメラノサイト(脈絡膜・毛様体・虹彩)に対する自己反応性T細胞が活性化し、汎ぶどう膜炎・浆液性網膜剥離・脱色素病変が生じる3)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”ICI関連眼irAEの大規模レジストリ研究
Section titled “ICI関連眼irAEの大規模レジストリ研究”ICI関連眼irAEの全体像を把握するため、国際的な多施設レジストリ研究が進められている3)。ぶどう膜炎・VKH様症候群・外眼筋炎など多彩な眼irAEのスペクトラム・頻度・転帰を明らかにすることで、リスク層別化とプロトコル確立が期待される。
抗体薬物複合体(ADC)の角膜障害
Section titled “抗体薬物複合体(ADC)の角膜障害”トラスツズマブ デルクステカン(T-DXd)をはじめとするADCは次世代の抗がん療法として普及しつつあるが、角膜障害(点状表層角膜症・角膜実質混濁)が有害事象として認識されている10)。薬剤監視研究による症例集積と角膜保護戦略の確立が課題となっている。
HCQ網膜症の超早期検出
Section titled “HCQ網膜症の超早期検出”適応光学OCT(adaptive optics OCT)やマルチスペクトラル眼底撮影により、従来法では検出できない初期RPE構造変化の可視化が試みられている11)。また人工知能(AI)を用いたOCT画像解析による自動スクリーニングの開発も進んでおり、見逃しリスクの低減が期待される11)。
眼科・腫瘍内科連携プロトコルの確立
Section titled “眼科・腫瘍内科連携プロトコルの確立”ICI・分子標的薬の普及に伴い、眼科と腫瘍内科による標準化された連携プロトコルの確立が求められている8)。CTCAEグレーディングに基づく眼副作用管理アルゴリズムのガイドライン化が進みつつある。
8. 参考文献
Section titled “8. 参考文献”-
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
-
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
-
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
-
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
-
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
-
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
-
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
-
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
-
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
-
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
-
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.
