Zytotoxische Chemotherapie
5-FU : Tränenfluss (Tränenwegsstenose), Konjunktivitis, Hornhautepithelschäden1)
Cisplatin : Optikusneuropathie, Farbsehstörungen (selten)1)
Taxane (Docetaxel, Paclitaxel) : Tränenfluss, zystoides Makulaödem4)

Augen-Nebenwirkungen von Krebsmedikamenten und zielgerichteten Therapien sind ein Sammelbegriff für pathologische Zustände, bei denen Medikamente, die in der Krebs- und Immuntherapie eingesetzt werden, unerwünschte Ereignisse im Augengewebe verursachen.
Die betroffenen Medikamentenkategorien sind breit gefächert.
Mit den Fortschritten in der Krebstherapie hat sich die Überlebenszeit verlängert, und die Bedeutung des Managements von Augen-Nebenwirkungen während der Langzeittherapie hat zugenommen1). Augen-Nebenwirkungen reichen von leichten Beschwerden bis hin zu irreversiblen Sehstörungen, und ein angemessenes Screening sowie ein frühzeitiges Eingreifen sind entscheidend für die Sehprognose.
Bei Symptomen wie Sehverschlechterung, Rötung, Augenschmerzen, Mouches volantes, Photopsie oder Metamorphopsie (verzerrtes Sehen) sollte umgehend ein Augenarzt aufgesucht werden. Auch wenn die Symptome mild sind, kann ein Ignorieren zu irreversiblen Schäden führen. Daher ist es wichtig, den behandelnden Arzt (Onkologen) zu informieren und die Zusammenarbeit mit dem Augenarzt zu koordinieren.
Die Augen-Nebenwirkungen variieren je nach Medikamentenkategorie. Nachfolgend sind die wichtigsten Medikamente und ihre Augensymptome aufgeführt.
Zytotoxische Chemotherapie
5-FU : Tränenfluss (Tränenwegsstenose), Konjunktivitis, Hornhautepithelschäden1)
Cisplatin : Optikusneuropathie, Farbsehstörungen (selten)1)
Taxane (Docetaxel, Paclitaxel) : Tränenfluss, zystoides Makulaödem4)
Hormontherapie und Immunmodulatoren
Tamoxifen : perimakuläre kristalline Ablagerungen, korneale wirbelförmige Trübungen, zystoides Makulaödem. Inzidenz: international 3–6 %, in Japan 0,2 %.
HCQ/Chloroquin : Bull’s-Eye-Makulopathie (ringförmige Atrophie), Sehverschlechterung, Nachtblindheit, Farbsehstörungen. Etwa 0,5 % nach mehr als 5-jähriger Behandlung.
Interferon: Kleine Blutungen und Cotton-Wool-Flecken am hinteren Augenpol. Treten innerhalb von 2–3 Monaten nach Verabreichung auf. Meist asymptomatisch und spontane Rückbildung.
Molekular zielgerichtete Wirkstoffe
MEK-Inhibitoren (Trametinib etc.): Seröse Netzhautablösung, PED. Inzidenz ca. 10–25 %2)
EGFR-Inhibitoren (Gefitinib etc.): Trichiasis, Blepharitis, Hornhautepithelschäden5)
BRAF-Inhibitoren (Vemurafenib etc.): Uveitis, seröse Netzhautablösung6)
ALK-Inhibitoren (Crizotinib etc.): Photopsie, verschwommenes Sehen. Etwa 60 % entwickeln Sehstörungen7)
Immun-Checkpoint-Inhibitoren (ICI)
Uveitis (vordere, hintere, Panuveitis): Inzidenz ca. 1 %3)
VKH-ähnliches Syndrom: Schwere Form, die hochdosierte Steroide erfordert3)
Trockenes Auge, Konjunktivitis, orbitale entzündliche Erkrankung, extraokuläre Myositis8)
ADC (T-DXd etc.): Hornhautschäden (oberflächliche punktförmige Keratopathie, Hornhautstromatrübung)10)
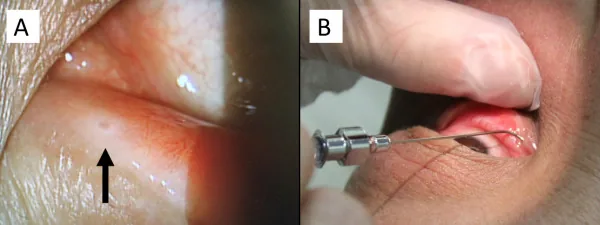
Fingolimod (Imusera/Gilenya), das zur Vorbeugung von Schüben bei Multipler Sklerose eingesetzt wird, kann ein Makulaödem verursachen. Die Inzidenz des Makulaödems beträgt 0,2 % bei 0,5 mg/Tag Fingolimod und 1,4 % bei 1,25 mg/Tag, wobei es meist innerhalb von 3–4 Monaten nach Behandlungsbeginn auftritt.
Die Risikofaktoren für Augen-Nebenwirkungen variieren je nach Medikamentenkategorie.
| Medikamentenkategorie | Hauptrisikofaktoren |
|---|---|
| HCQ/Chloroquin | Behandlungsdauer >5 Jahre, CQ >3,0 mg/kg/Tag oder HCQ >6,5 mg/kg/Tag, hohes Alter, Nieren-/Leberfunktionsstörung, begleitende Netzhauterkrankung |
| Tamoxifen | Hohe Dosis und Langzeitanwendung (erhöhte kumulative Dosis) |
| Interferon | Hohe Anfangsdosis, hohes Alter, Diabetes, Bluthochdruck, Anämie |
| MEK-Inhibitoren | Dosisabhängig (häufiger bei hoher Dosis) 2) |
| ICI | Patienten mit systemischen irAE (Thyreoiditis, Kolitis usw.) entwickeln auch leichter okuläre irAE 3) |
| ADC | Medikamentenspezifischer Mechanismus der Hornhauttoxizität 10) |
Die spezifischen Risikofaktoren für eine HCQ-Retinopathie sind:
Eine Interferon-Retinopathie tritt bei systemischen Erkrankungen wie Diabetes, Bluthochdruck oder Anämie häufiger und schwerer auf und tritt auch bei therapieresistenten oder rezidivierenden Fällen leichter auf.
Basierend auf den Empfehlungen der AAO (American Academy of Ophthalmology)9) wird das folgende Screening durchgeführt:
Zu den nützlichen Untersuchungen gehören Humphrey 10-2 Gesichtsfeldtest, SD-OCT, Fundusautofluoreszenz, multifokales ERG und Ganzfeld-ERG. Das Bull’s Eye (ringförmige Atrophie) ist ein charakteristischer Fundusbefund bei fortgeschrittener HCQ-Retinopathie.
| Medikament | Screening-Zeitpunkt und Untersuchung |
|---|---|
| HCQ/Chloroquin | Baseline bei Therapiebeginn + jährlich ab 5 Jahren (SD-OCT, 10-2 Gesichtsfeld, FAF) 9) |
| Tamoxifen | Fundusuntersuchung und SD-OCT bei Symptomen und regelmäßig |
| Interferon | Fundusuntersuchung 2–3 Monate nach Therapiebeginn. Bei Symptomen sofortige augenärztliche Vorstellung |
| MEK-Inhibitoren | Bei Sehverschlechterung oder Metamorphopsien OCT zur Bestätigung einer serösen Netzhautablösung 2) |
| ICI | Bei Sehverschlechterung, Rötung oder Augenschmerzen sofortige augenärztliche Vorstellung 3) |
| Fingolimod | Baseline-Fundusuntersuchung vor Therapie + Follow-up 3–4 Monate nach Therapiebeginn |
Bei ICI-Patienten mit Sehverschlechterung, Rötung oder Augenschmerzen sollten Entzündungszellen in der Vorderkammer, Glaskörpertrübungen und Aderhautläsionen beurteilt werden, wobei die Möglichkeit einer Uveitis oder eines VKH-ähnlichen Syndroms als irAE in Betracht gezogen werden sollte 3).
Zu Beginn der Behandlung wird eine augenärztliche Untersuchung als Basisuntersuchung empfohlen, die Sehschärfe, Fundus und SD-OCT umfasst. Danach wird, wenn keine Risikofaktoren (Behandlungsdauer >5 Jahre, hohe Dosis, hohes Alter, Nierenfunktionsstörung usw.) vorliegen, ab dem 5. Jahr ein jährliches Screening begonnen. Bei Vorliegen von Risikofaktoren sind frühere und häufigere Untersuchungen erforderlich. Die wichtigsten Untersuchungen sind SD-OCT, Humphrey 10-2 Gesichtsfeldtest und Fundus-Autofluoreszenz.
Das Absetzen des Medikaments ist die einzige Behandlung. Da die Ausscheidung aus dem Körper langsam ist, können die Läsionen auch nach Absetzen des Medikaments fortschreiten und sich verschlechtern. Daher ist eine Früherkennung äußerst wichtig, und die Entscheidung, das Medikament vor dem Auftreten irreversibler Schäden abzusetzen, bestimmt die Sehprognose.
Die meisten Fälle haben eine gute Prognose; bei asymptomatischen Fällen wird grundsätzlich das Ende der IFN-Therapie abgewartet. In schweren Fällen oder bei Sehverschlechterung wird eine Dosisreduktion oder ein Absetzen von IFN erwogen. Bei gleichzeitigem Diabetes oder Bluthochdruck ist eine frühzeitige Behandlung erforderlich.
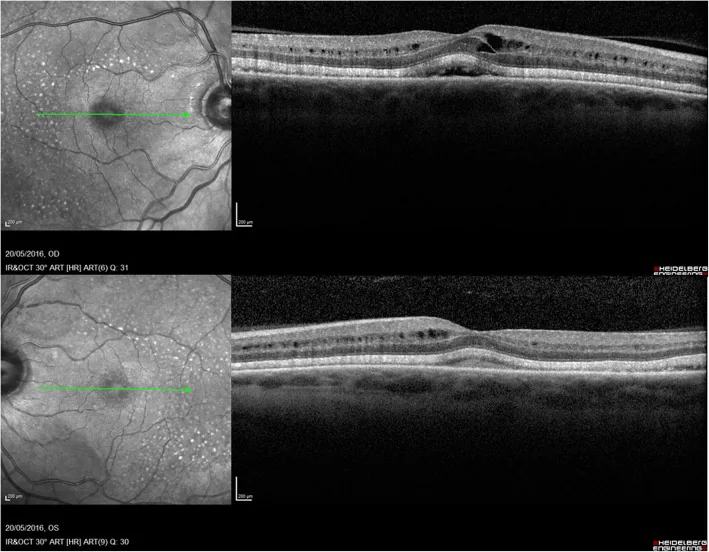
Die Behandlung erfolgt basierend auf dem CTCAE-Grad 3).
In den meisten Fällen bessert sich das Ödem nach Absetzen des Medikaments. Bei Bedarf können NSAR-Augentropfen oder Steroid-Augentropfen eingesetzt werden.
Ein Abbruch ist nicht immer erforderlich. Das Vorgehen hängt vom Schweregrad der okulären Nebenwirkungen (CTCAE-Grad) und der Art des Medikaments ab. In einigen Fällen, wie bei HCQ-Retinopathie oder Tamoxifen-Retinopathie, ist das Absetzen die Regel. Bei leichter seröser Netzhautablösung unter MEK-Inhibitoren oder Trichiasis unter EGFR-Inhibitoren kann die Behandlung unter symptomatischer Therapie fortgesetzt werden. Eine enge Zusammenarbeit zwischen Onkologe und Augenarzt ist wichtig, um individuell zu entscheiden.
Die Schädigungsmechanismen des Augengewebes unterscheiden sich je nach Medikamentenkategorie.
CQ und HCQ haben eine hohe Affinität zu Melanin und reichern sich in den Zellen des retinalen Pigmentepithels (RPE) an, indem sie an Melaningranula binden. Das akkumulierte CQ/HCQ wird in Lysosomen aufgenommen, was zu einem Anstieg des lysosomalen pH-Werts und einer Beeinträchtigung der lysosomalen Enzymaktivität führt. Wenn die enzymatische Stoffwechselfunktion des RPE gestört ist, werden Abbau und Erneuerung der Photorezeptor-Außensegmente beeinträchtigt, was zur Photorezeptordegeneration führt. Aufgrund der hohen Körperakkumulation kann die Schädigung auch nach Absetzen fortschreiten.
In der Nervenfaserschicht und der inneren plexiformen Schicht bilden sich kugelförmige Läsionen (Nervenfaserdegeneration und axonale Schwellung). Kristalline Ablagerungen werden als Degenerationsprodukte angesehen, die Kalzium und komplexe Kohlenhydrate enthalten und sich in den Nervenfasern ablagern. Das zystoide Makulaödem (CME) entsteht durch Funktionsstörung der Müller-Zellen und Flüssigkeitsansammlung.
IFN induziert Vasospasmus, Leukozyteninfiltration und vaskuläre Endothelschädigung. Immunkomplexe lagern sich in den Kapillaren ab und verursachen Kapillarverschlüsse. Stromaufwärts (arteriell) der verschlossenen Kapillaren treten Cotton-Wool-Herde (Nervenfaserschichtinfarkte) auf, und Verschlussblutungen werden als kleine Blutungen beobachtet. Meist sind diese Veränderungen vorübergehend und bilden sich nach Absetzen von IFN zurück.
MEK-Inhibitoren blockieren den MAPK/ERK-Signalweg (Zellproliferation und -überleben). Das RPE erhält den aktiven Transport (Ionen und Wasser) über das ERK-Signal aufrecht. Die ERK-Hemmung stört den Ionentransport und die Pumpfunktion des RPE. Dies führt zu Flüssigkeitsansammlung unter der Netzhaut, die sich als seröse Netzhautablösung und Pigmentepithelabhebung (PED) manifestiert2).
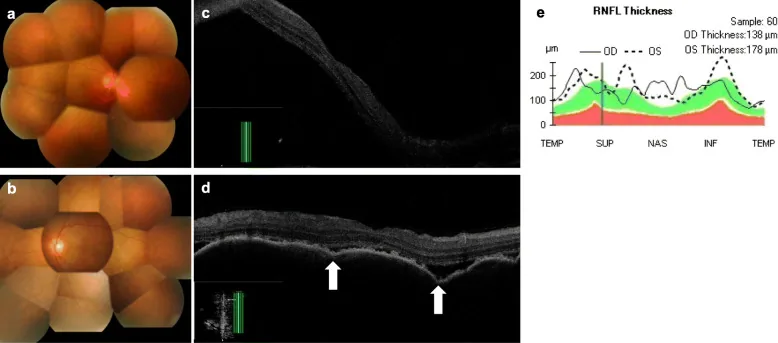
ICI (PD-1/PD-L1-Inhibitoren, CTLA-4-Inhibitoren) heben die Immun-Checkpoints der T-Zellen auf und verstärken die Antitumorimmunität. Dieser Mechanismus hebt jedoch gleichzeitig die autoimmune Suppression auf und löst autoimmune Reaktionen im Augengewebe (Uvea, Sklera, Orbita, Tränendrüse) aus. Beim VKH-ähnlichen Syndrom werden autoreaktive T-Zellen gegen Melanozyten (Aderhaut, Ziliarkörper, Iris) aktiviert, was zu Panuveitis, seröser Netzhautablösung und Depigmentierungsläsionen führt 3).
Um das Gesamtbild der ICI-assoziierten okulären irAE zu erfassen, werden internationale multizentrische Registerstudien durchgeführt 3). Durch die Klärung des Spektrums, der Häufigkeit und der Ergebnisse verschiedener okulärer irAE wie Uveitis, VKH-ähnliches Syndrom und extraokulare Myositis werden Risikostratifizierung und Protokollentwicklung erwartet.
ADCs, einschließlich Trastuzumab Deruxtecan (T-DXd), verbreiten sich als Krebstherapien der nächsten Generation, aber Hornhauttoxizität (punktförmige superfizielle Keratopathie, Hornhautstromatrübung) wird als unerwünschtes Ereignis erkannt 10). Die Sammlung von Fällen durch Arzneimittelüberwachungsstudien und die Etablierung von Hornhautschutzstrategien sind Herausforderungen.
Durch adaptive Optik-OCT und multispektrale Fundusbildgebung wird versucht, frühe RPE-Strukturveränderungen sichtbar zu machen, die mit herkömmlichen Methoden nicht nachweisbar sind 11). Darüber hinaus schreitet die Entwicklung eines automatisierten Screenings mittels KI-basierter OCT-Bildanalyse voran, was das Risiko von Übersehen verringern soll 11).
Mit der Verbreitung von ICI und zielgerichteten Therapien wird die Etablierung standardisierter Kooperationsprotokolle zwischen Augenheilkunde und Onkologie gefordert 8). Die Leitlinienentwicklung von Algorithmen zur Behandlung okulärer Nebenwirkungen basierend auf der CTCAE-Einstufung schreitet voran.
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.