
Iridoschisis
1. Qu’est-ce que l’iridoschisis ?
Section intitulée « 1. Qu’est-ce que l’iridoschisis ? »L’iridoschisis est une maladie dégénérative rare dans laquelle le stroma de l’iris se sépare en feuillets antérieur et postérieur, les fibres du stroma antérieur se désintègrent en fines fibrilles dont les extrémités libres flottent dans l’humeur aqueuse. Le nom vient du grec iris (iris) et schisis (séparation).
Schmitt a rapporté le premier cas en 19221), et Loewenstein et Foster ont nommé la maladie « iridoschisis » en 1945. Des études histologiques de l’iridoschisis bilatéral ont révélé une fissure profonde entre le stroma antérieur et postérieur1). Depuis, des rapports de cas et de petites séries se sont accumulés.
La maladie évolue de manière chronique et progressive, mais dans de nombreux cas, elle est asymptomatique et découverte lors d’examens de routine ou d’investigations pour d’autres affections. Elle est souvent bilatérale, mais le degré de progression peut être asymétrique.
2. Épidémiologie
Section intitulée « 2. Épidémiologie »- Prévalence: Plus de 100 cas ont été rapportés dans la littérature, mais il s’agit d’une maladie très rare et la prévalence exacte est inconnue.
- Âge d’apparition: Survient principalement chez les personnes âgées de 50 à 80 ans. Une revue systématique rapporte un âge moyen de 66,95 ± 17,39 ans4).
- Sexe: Légère prédominance féminine selon une revue systématique4). La différence de distribution d’âge est importante pour distinguer de l’atrophie irienne progressive (syndrome ICE).
- Caractéristiques oculaires: Survient plus fréquemment dans les yeux avec chambre antérieure peu profonde, axe court et hypermétropie1).
- Association avec le glaucome: Souvent associé au glaucome par fermeture de l’angle2). La fréquence varie selon les études.
- Association avec la cataracte: Plus fréquente que dans la cohorte du même âge4).
- Bilatéralité: Survient souvent bilatéralement, mais l’asymétrie de progression est possible.
- Localisation préférentielle: Prédominance dans le quadrant inférieur (nasal-inférieur à temporal-inférieur) de l’iris6).
L’hérédité n’est généralement pas confirmée. La dégénérescence du tissu irien liée à l’âge est considérée comme la cause principale. Quelques rares familles avec transmission autosomique dominante ont été rapportées, mais dans la pratique clinique, la majorité des cas sont sporadiques, et il n’y a actuellement pas de preuve suffisante pour expliquer aux patients qu’il s’agit d’une maladie héréditaire.
3. Pathologie (séparation du stroma irien et formation de faisceaux de fibres)
Section intitulée « 3. Pathologie (séparation du stroma irien et formation de faisceaux de fibres) »Anatomie et changements liés à l’âge de l’iris
Section intitulée « Anatomie et changements liés à l’âge de l’iris »Le stroma irien est anatomiquement composé d’un feuillet antérieur (couche limite antérieure + partie antérieure du stroma : mélanocytes, fibroblastes, collagène, vaisseaux) et d’un feuillet postérieur (partie postérieure du stroma + muscle dilatateur + deux couches d’épithélium pigmentaire irien). Avec l’âge, les microvaisseaux du stroma subissent des modifications dégénératives, entraînant une ischémie et une atrophie progressives.
Au microscope électronique, on observe une diminution marquée des fibres de collagène et un amincissement du stroma dans les zones atteintes, mais les vaisseaux et les nerfs conservent un aspect normal 1). Ces changements entraînent un affaiblissement de l’adhésion entre les feuillets antérieur et postérieur. L’angiographie fluorescéinique de l’iris montre une perfusion vasculaire préservée dans les zones de séparation, ce qui rend peu probable que l’ischémie seule soit la cause. Ce point est un élément clé de différenciation avec l’atrophie essentielle de l’iris (un type de syndrome ICE).
Progression de la séparation à la fibrose fasciculaire
Section intitulée « Progression de la séparation à la fibrose fasciculaire »- L’adhésion entre les feuillets antérieur et postérieur s’affaiblit, et la convection de l’humeur aqueuse (force qui fait osciller la surface de l’iris d’avant en arrière) favorise la séparation.
- Une théorie dominante suggère que le durcissement des vaisseaux de l’iris lié à l’âge induit un cisaillement lors de la dilatation et de la contraction pupillaire, conduisant à la séparation du stroma.
- Les fibres de collagène du feuillet antérieur séparé se détachent et se libèrent dans l’humeur aqueuse, présentant un aspect caractéristique en « céréales de blé déchiquetées » 1).
- La couche épithéliale pigmentaire postérieure est généralement intacte 6).
Hypothèses étiologiques
Section intitulée « Hypothèses étiologiques »Aucune théorie unique ne permet d’expliquer l’étiologie de l’iridoschisis 1).
- Changements liés à l’âge : La théorie du durcissement des vaisseaux de l’iris et du cisaillement est dominante.
- Traumatisme / stimulation mécanique : Des cas d’iridoschisis bilatéral et de subluxation du cristallin ont été rapportés chez des patients ayant utilisé un masseur de cou sur l’œil de manière répétée 1). Un frottement mécanique répété peut provoquer la séparation du stroma irien.
- Dermatite atopique : Un traumatisme mécanique chronique dû au frottement des yeux pourrait être une cause d’iridoschisis 3).
- Morphologie de l’iris en plateau : Des cas d’association entre iridoschisis et iris en plateau ont été rapportés, suggérant une étiologie liée à une anomalie anatomique congénitale plutôt qu’au vieillissement.
- Autres : Des cas ont été rapportés en association avec la kératite interstitielle syphilitique, l’utilisation à long terme de myotiques, et des cas familiaux (extrêmement rares).
4. Maladies associées
Section intitulée « 4. Maladies associées »Glaucome à angle fermé
Section intitulée « Glaucome à angle fermé »Les caractéristiques anatomiques telles qu’une chambre antérieure peu profonde, un axe oculaire court et une hypermétropie sont des facteurs de risque communs à l’iridoschisis et au glaucome à angle fermé. La zone de contact entre l’iris et le cristallin est large, ce qui prédispose à un bloc pupillaire (augmentation de la résistance au passage de l’humeur aqueuse au niveau du bord pupillaire). De plus, l’accumulation de fibres libres de la couche antérieure de l’iris dans l’angle accélère l’obstruction, et les deux mécanismes agissent en synergie pour augmenter la pression intraoculaire2).
Syndrome exfoliatif (PEX)
Section intitulée « Syndrome exfoliatif (PEX) »Il s’agit d’un diagnostic différentiel à envisager chez les personnes âgées présentant un glaucome secondaire avec des dépôts blancs sur la capsule antérieure du cristallin et le bord pupillaire. Il se distingue de l’iridoschisis par l’absence de libération de fibres iriennes.
Traumatismes et stimulations mécaniques
Section intitulée « Traumatismes et stimulations mécaniques »L’utilisation répétée d’appareils de massage du cou sur l’œil ou le frottement chronique des yeux dû à une dermatite atopique peuvent être associés au développement de l’iridoschisis1)3). Dans les cas de dermatite atopique, le pronostic de la greffe de cornée est extrêmement défavorable3).
Troubles endothéliaux cornéens et maladies nécessitant une greffe de cornée
Section intitulée « Troubles endothéliaux cornéens et maladies nécessitant une greffe de cornée »Les fibres iriennes flottantes peuvent endommager mécaniquement l’endothélium cornéen, conduisant à une décompensation endothéliale (kératopathie bulleuse) à un stade avancé. Cela peut nécessiter une DSAEK ou une DMEK5).
5. Tableau clinique
Section intitulée « 5. Tableau clinique »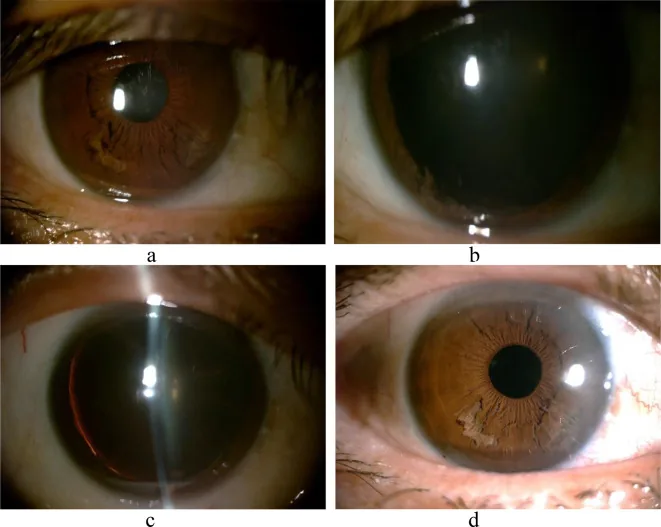
Symptômes subjectifs
Section intitulée « Symptômes subjectifs »Les symptômes subjectifs dus à l’iridoschisis lui-même sont souvent rares. Les symptômes dépendent de la progression des complications (glaucome, troubles endothéliaux cornéens).
- Souvent asymptomatique: Découvert fortuitement lors d’un examen à la lampe à fente.
- Céphalées et douleurs oculaires: En cas de glaucome associé, des céphalées et douleurs oculaires intermittentes peuvent survenir.
- Baisse de l’acuité visuelle: Due à une atteinte du champ visuel par glaucome associé ou à la progression d’une cataracte.
- Vision trouble: Apparaît lorsque les troubles endothéliaux cornéens progressent et provoquent un œdème cornéen.
- Lors d’une crise de fermeture de l’angle aiguë: Douleur oculaire intense, céphalées, nausées, baisse brutale de l’acuité visuelle. Nécessite une prise en charge urgente.
- Myodésopsie: Parfois perçue lorsque des fibres iriennes libérées flottent dans la chambre antérieure (rare).
Signes cliniques
Section intitulée « Signes cliniques »- Survient principalement dans l’iris inférieur (quadrants inféro-nasal à inféro-temporal), et dans les cas avancés, peut être circonférentiel 1)6).
- À la lampe à fente, aspect caractéristique de « fils blancs effilochés » ou de « franges » flottant dans la chambre antérieure.
- La couche postérieure de l’iris apparaît amincie en transillumination, mais le sphincter pupillaire est souvent préservé 1).
- L’épithélium pigmentaire postérieur est généralement intact 6).
- Les fibres libérées entrent en contact avec l’endothélium cornéen, provoquant des lésions endothéliales par irritation mécanique 3).
- Dépôts de fibres dans l’angle → risque d’obstruction mécanique du trabéculum 2).
- S’accompagne fréquemment de signes d’œil hypermétrope avec chambre antérieure peu profonde et axe court.
- Les fibres libres dans la chambre antérieure peuvent se déplacer avec les changements de position (debout/couché) et être observées lors de l’examen à la lampe à fente.
L’iridoschisis lui-même ne provoque presque pas de douleur ni de baisse de vision. Cependant, environ deux tiers des cas sont associés à un glaucome, ce qui peut entraîner des symptômes tels que maux de tête, douleurs oculaires et baisse de vision. De plus, si les fibres flottantes de l’iris blessent l’endothélium cornéen, un œdème cornéen peut provoquer une vision trouble. Un suivi ophtalmologique régulier est important.
6. Examens
Section intitulée « 6. Examens »Le diagnostic de l’iridoschisis repose principalement sur l’examen clinique à la lampe à fente. Il n’existe pas de critères diagnostiques standardisés indépendants, et la confirmation des signes caractéristiques à la lampe à fente est essentielle pour le diagnostic définitif.
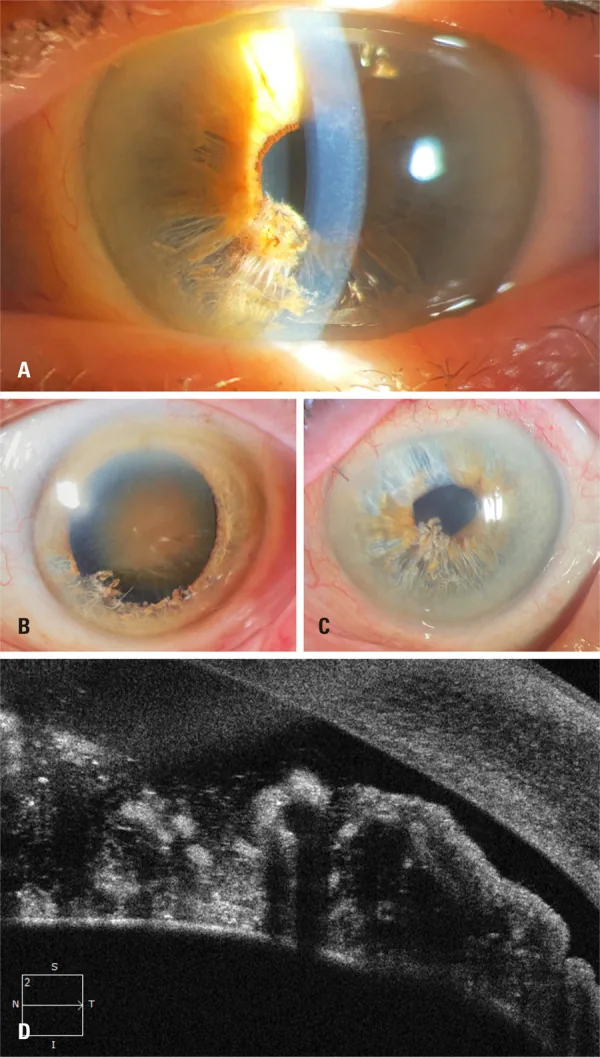
Examen à la lampe à fente
Section intitulée « Examen à la lampe à fente »On observe des fibres atrophiques ressemblant à des « céréales déchiquetées » dans l’iris inférieur et des fibres flottantes dans la chambre antérieure 1)6). C’est la première étape du diagnostic. On évalue l’étendue de la séparation (nombre de quadrants) et la quantité de fibres dans la chambre antérieure. La présence de fibres blanches filamenteuses flottant dans la chambre antérieure est le principal signe diagnostique.
Gonioscopie
Section intitulée « Gonioscopie »Évaluer en détail la présence d’un angle fermé, l’étendue des synéchies antérieures périphériques (PAS), les dépôts de fibres dans l’angle et l’état du trabéculum. Il est souhaitable de la réaliser chez tous les patients.
OCT du segment antérieur (AS-OCT)
Section intitulée « OCT du segment antérieur (AS-OCT) »Visualise en détail la séparation en deux couches du stroma irien, les fibres flottantes et l’état de l’épithélium pigmentaire postérieur 1)5)6). On observe une rupture de la couche limitante antérieure, une séparation stromale en « mites » (moth-eaten) et des ombres de fibres libres dans la chambre antérieure. Même en cas d’œdème cornéen rendant la gonioscopie difficile, l’évaluation de l’angle est possible 5).
L’indice ITC (iridotrabecular contact) est un indicateur quantitatif de la zone de contact entre l’iris périphérique et le trabéculum. Chez une femme de 76 ans présentant une iridoschisis bilatéral, l’indice ITC est passé de 23,6 % à 4,7 % après une chirurgie de la cataracte, puis à 0 % après une DSAEK5).
Microscopie ultrasonore biomicroscopique (UBM)
Section intitulée « Microscopie ultrasonore biomicroscopique (UBM) »Elle permet de visualiser la séparation de l’échogénicité interne de l’iris, l’antéposition du corps ciliaire et la dissociation des ligaments suspenseurs1). Utile pour évaluer les mécanismes de fermeture de l’angle, tels que l’iris plateau et la rotation antérieure du corps ciliaire.
Autres examens
Section intitulée « Autres examens »- Tonométrie : réalisée chez tous les patients. Dépistage du glaucome. En raison de possibles variations diurnes importantes, il est souhaitable de mesurer à plusieurs moments de la journée.
- Microscopie spéculaire de l’endothélium cornéen : évaluation quantitative de la densité cellulaire endothéliale (ECD). Permet de déterminer le degré et l’évolution des lésions endothéliales dues au contact avec les fibres libres.
- Examen du champ visuel (Humphrey 30-2, etc.) : en cas de glaucome associé, une évaluation régulière du champ visuel est indispensable. Même en l’absence de glaucome, il est recommandé de réaliser une première mesure comme valeur de référence.
- Mesure de la longueur axiale (scan A/IOL Master) : confirmation d’un œil court et hypermétrope. Utile pour l’évaluation quantitative de la prédisposition à la fermeture de l’angle.
7. Diagnostic et diagnostic différentiel
Section intitulée « 7. Diagnostic et diagnostic différentiel »Diagnostic différentiel
Section intitulée « Diagnostic différentiel »| Maladie | Âge et sexe | Unilatéral/bilatéral | Principaux signes | Points de différenciation |
|---|---|---|---|---|
| Iridoschisis | 50-80 ans, légèrement plus fréquent chez les femmes | Bilatéral | Séparation et libération des fibres du feuillet antérieur de l’iris | Angle ouvert, épithélium pigmentaire postérieur préservé |
| Syndrome ICE (atrophie progressive de l’iris) | 30-40 ans, plus fréquent chez les femmes | Unilatéral | Anomalie de l’endothélium cornéen, atrophie de l’iris, déviation pupillaire | Cellules atypiques au spéculaire |
| Syndrome d’Axenfeld-Rieger | Présent à la naissance | Bilatéral | Atrophie de l’iris, embryotoxon postérieur | Congénital, anomalie de l’angle |
| Syndrome d’exfoliation (PEX) | Personnes âgées | Unilatéral/bilatéral | Dépôts blancs sur la capsule antérieure du cristallin et le bord pupillaire | Pas de libération de fibres iriennes |
| Lésion traumatique de l’iris | Tous âges | Unilatéral | Déchirure irienne localisée, déformation pupillaire | Antécédent de traumatisme, asymétrie |
Dans le diagnostic différentiel avec le syndrome ICE, l’iridoschisis survient plus souvent chez les personnes âgées, est souvent bilatéral et peut être différencié par les résultats gonioscopiques. Le syndrome ICE se caractérise par des cellules endothéliales cornéennes atypiques, et la microscopie spéculaire est utile pour le diagnostic différentiel.
Le diagnostic clinique est posé par l’examen à la lampe à fente montrant des fibres atrophiques dans la partie inférieure de l’iris et des fibres flottantes dans la chambre antérieure. L’OCT du segment antérieur peut visualiser en détail la séparation en deux couches du stroma irien, et l’UBM permet d’évaluer le corps ciliaire et la zonule. Le diagnostic différentiel avec le syndrome ICE et le syndrome d’Axenfeld-Rieger est important, et on les distingue par l’âge d’apparition, la latéralité et le motif des modifications iriennes.
8. Traitement
Section intitulée « 8. Traitement »Il n’existe pas de traitement curatif de la maladie elle-même. La prise en charge des complications (glaucome, troubles endothéliaux cornéens) constitue l’essentiel du traitement. La stratégie thérapeutique est déterminée en fonction de la présence ou non d’un glaucome, du niveau de pression intraoculaire, du degré d’atteinte du champ visuel et de l’importance des troubles endothéliaux cornéens.
Traitement médicamenteux en cas de glaucome associé
Section intitulée « Traitement médicamenteux en cas de glaucome associé »Environ deux tiers des cas présentent un glaucome associé, il est donc recommandé de réaliser un bilan glaucomateux de base (examen du champ visuel, OCT, gonioscopie, mesure de la pression intraoculaire) chez tous les patients. La plupart des cas avec élévation de la pression intraoculaire répondent au traitement médicamenteux.
| Classe de médicament | Médicament représentatif | Posologie |
|---|---|---|
| Analogues des prostaglandines (première intention) | Latanoprost collyre 0,005 % | 1 fois par jour au coucher |
| Travoprost collyre 0,004 % | 1 fois par jour au coucher | |
| Bêta-bloquants (deuxième intention) | Timolol collyre 0,5 % | 2 fois par jour |
| Cartéolol collyre à libération prolongée 2 % | 1 fois par jour | |
| Inhibiteurs de l’anhydrase carbonique | Dorzolamide 1% collyre | 3 fois par jour |
| Brinzolamide 1% collyre | 2 fois par jour | |
| Agonistes α2 | Brimonidine 0,1% collyre | 2 fois par jour |
| Combinaisons fixes | Collyre combiné latanoprost/timolol | 1 fois par jour |
| Lors d’une crise aiguë | D-mannitol 250 mL (1,0-1,5 g/kg) perfusion intraveineuse + acétazolamide 250-500 mg IV + pilocarpine 2% collyre en instillations fréquentes | — |
Lors d’une crise aiguë de fermeture de l’angle, la priorité est d’abaisser rapidement la pression intraoculaire, et un traitement d’urgence est effectué sous hospitalisation. Après la baisse de la pression intraoculaire, une iridotomie au laser est réalisée sur l’œil atteint.
Traitement au laser
Section intitulée « Traitement au laser »- Iridotomie périphérique au laser (LPI) : Réalisée pour lever le blocage de l’angle. En raison de la fragilité du tissu irien, il faut être prudent lors de l’irradiation 2). Après la LPI, il existe un risque de reblocage dû à l’accumulation de fibres flottantes, nécessitant une évaluation régulière de l’angle postopératoire.
- Si la LPI est techniquement difficile ou insuffisamment efficace, envisager un traitement chirurgical (reconstruction du cristallin).
Chirurgie de la cataracte
Section intitulée « Chirurgie de la cataracte »La chirurgie de la cataracte dans les yeux atteints d’iridoschisis est difficile pour les raisons suivantes 4) :
- Mydriase insuffisante : En raison de l’atrophie irienne et des lésions du sphincter pupillaire, la dilatation est souvent insuffisante. L’utilisation de dispositifs pupillaires (tels que les rétracteurs d’iris) est recommandée 1)4).
- Risque d’aspiration des fibres flottantes : La sonde de phacoémulsification peut aspirer les fibres flottantes. Des techniques telles que la formation d’une barrière avec un dispositif viscoélastique (OVD) ou la résection préalable des fibres avec un vitréotome ont été rapportées 4).
- Risque élevé de déchirure irienne lors de l’utilisation de rétracteurs d’iris.
- Utiliser des réglages de bas débit et de basse aspiration pour minimiser les fluctuations de la pression intraoculaire.
- Protéger l’iris avec un dispositif viscoélastique pendant la manipulation.
Une revue systématique (21 cas, 35 yeux) a montré que la phacoémulsification était l’intervention la plus fréquemment réalisée, avec une amélioration significative de l’acuité visuelle postopératoire. Les complications rapportées comprenaient une inflammation de la chambre antérieure, un œdème cornéen et des plis de la membrane de Descemet 4).
Effet d’ouverture de l’angle
Section intitulée « Effet d’ouverture de l’angle »La chirurgie de la cataracte améliore significativement le blocage de l’angle. Chez une femme de 76 ans, l’indice ITC est passé de 23,6 % à 4,7 % après chirurgie de la cataracte 5). Une chirurgie précoce de la cataracte doit être envisagée pour prévenir la progression des lésions endothéliales cornéennes 5). Même en l’absence de cataracte, l’extraction du cristallin clair peut être envisagée pour contrôler le blocage de l’angle.
Chirurgie filtrante et goniosynechiolyse
Section intitulée « Chirurgie filtrante et goniosynechiolyse »- Trabéculectomie (avec mitomycine C) : Indiquée en cas de contrôle insuffisant de la pression intraoculaire par les médicaments et le laser.
- Goniosynéchie (goniosynechialysis) : Envisagée en cas de formation de PAS.
- MIGS (chirurgie du glaucome mini-invasive) : Pourrait être une option thérapeutique dans les cas de glaucome associé ; des données supplémentaires sont attendues.
Prise en charge des troubles endothéliaux cornéens et greffe de cornée
Section intitulée « Prise en charge des troubles endothéliaux cornéens et greffe de cornée »En cas de décompensation endothéliale cornéenne, une DSAEK (greffe endothéliale automatisée avec stripping du Descemet) ou une DMEK peut être réalisée5). Après DSAEK, une amélioration de l’indice ITC à 0 % a été rapportée5).
Surveillance (cas légers sans glaucome)
Section intitulée « Surveillance (cas légers sans glaucome) »Même les cas légers sans glaucome nécessitent un suivi régulier en raison du risque futur de développer un glaucome.
- Mesure de la pression intraoculaire : tous les 3 à 6 mois
- Gonioscopie : tous les 6 à 12 mois
- Examen du champ visuel : tous les 6 à 12 mois (plus fréquent en cas de glaucome associé)
- Mesure de la densité des cellules endothéliales cornéennes : environ une fois par an
- Conseils de positionnement : pour réduire le contact des fibres libres avec l’endothélium cornéen, il a été rapporté de recommander une position surélevée de la tête pendant le sommeil
Il n’existe pas de chirurgie pour traiter l’iridoschisis lui-même. La prise en charge du glaucome associé constitue le principal traitement. La chirurgie de la cataracte peut être réalisée pour corriger une chambre antérieure peu profonde, mais des précautions particulières sont nécessaires en raison de la fragilité de l’iris. En cas de lésions endothéliales avancées, une greffe endothéliale cornéenne peut être envisagée. Dans tous les cas, il est important de décider de la stratégie thérapeutique après une consultation approfondie avec un spécialiste.
9. Évolution et pronostic
Section intitulée « 9. Évolution et pronostic »Mécanisme de progression pathologique
Section intitulée « Mécanisme de progression pathologique »- L’adhésion entre les couches antérieure et postérieure de l’iris s’affaiblit, et la séparation progresse par convection de l’humeur aqueuse.
- Les fibres de collagène de la couche antérieure séparée se libèrent dans l’humeur aqueuse.
- Les fibres libérées atteignent l’angle iridocornéen et s’y déposent, obstruant mécaniquement le trabéculum → augmentation de la pression intraoculaire de type glaucome secondaire à angle ouvert.
- Le bombement de la racine de l’iris et l’accumulation de fibres entraînent la formation de synéchies antérieures périphériques (PAS), évoluant vers un glaucome secondaire par fermeture de l’angle 2).
- La théorie dominante est que les fibres du stroma antérieur flottant se plient vers l’avant, entrent en contact avec le trabéculum et obstruent l’écoulement de l’humeur aqueuse 6).
- Un mécanisme a également été proposé selon lequel l’épithélium pigmentaire postérieur pend sur la capsule antérieure du cristallin, induisant un bloc pupillaire.
Mécanisme des lésions endothéliales cornéennes
Section intitulée « Mécanisme des lésions endothéliales cornéennes »Les fibres d’iris flottantes entrent en contact direct avec l’endothélium cornéen, provoquant un œdème cornéen localisé et une diminution des cellules endothéliales par stimulation mécanique 1)3). À un stade avancé, cela conduit à une décompensation endothéliale cornéenne (kératopathie bulleuse).
Chez 3 patients atteints de dermatite atopique, la protéine totale dans l’humeur aqueuse était significativement augmentée à 0,80, 0,95 et 1,40 mg/mL (valeur normale 0,25-0,40 mg/mL), suggérant que la fuite de protéines du site de séparation de l’iris contribue à l’échec précoce du greffon cornéen 3).
Pronostic et perspectives
Section intitulée « Pronostic et perspectives »- En raison de la rareté de la maladie, il n’existe pratiquement pas d’essais contrôlés randomisés à grande échelle ni d’études de cohorte ; les rapports de cas et les petites séries de cas sont prédominants.
- Dans les cas compliqués de glaucome, le pronostic du champ visuel dépend du contrôle de la pression intraoculaire. La détection et le traitement précoces sont essentiels pour préserver la fonction visuelle.
- Dans les cas avancés de lésions endothéliales cornéennes, une greffe d’endothélium cornéen est nécessaire, et le pronostic est extrêmement défavorable chez les patients atteints de dermatite atopique 3).
- L’indice ITC mesuré par OCT du segment antérieur est un nouvel indicateur quantifiant la zone de contact entre l’iris et le trabéculum, permettant un suivi objectif des changements avant et après la chirurgie de la cataracte ou la DSAEK 5). À l’avenir, son utilité comme indicateur du moment de la chirurgie est attendue.
- Une revue systématique a organisé les risques et les mesures lors de la chirurgie de la cataracte 4). Le traitement des fibres flottantes par microcautère, la méthode de barrière OVD, l’utilisation de dispositifs pupillaires, etc., le choix de la technique en fonction du cas est important.
- Le rôle de la reconstruction du cristallin dans le glaucome à angle fermé est réévalué, et même dans les cas compliqués d’iridoschisis, l’accumulation de preuves sur l’efficacité d’une intervention chirurgicale précoce pour lever la chambre antérieure peu profonde est souhaitée.
10. Références
Section intitulée « 10. Références »-
Niu TT, Xin WJ. A case of iridoschisis with partial lens dislocation in both eyes. BMC Ophthalmol. 2024;24:66.
-
Pegu J, Jain K, Dubey S. Iridoschisis: Spectrum of Presentation. Middle East Afr J Ophthalmol. 2020;27(4):224-227. PMID: 33814819. PMCID: PMC7993048. doi:10.4103/meajo.MEAJO_120_19.
-
Kusano Y, Yamaguchi T, Shimazaki J, et al. Iridoschisis in patients with atopic dermatitis leads to intractable bullous keratopathy. BMC Ophthalmol. 2025;25:401.
-
Amaral DC, Rodrigues MP, Marques GN, et al. Iridoschisis associated with cataract: a systematic review of case reports. einstein (São Paulo). 2026;24:eRW1685.
-
Omoto T, Agata C, Akiyama R, et al. Iridotrabecular and Iridocorneal Contact Changes after Cataract Surgery and Endothelial Keratoplasty in Bilateral Iridoschisis. Case Rep Ophthalmol. 2021;12:198-203.
-
Bari A, Thulkar T, Tripathi M, et al. Iridoschisis: a rare ocular morbidity. BMJ Case Rep. 2023;16:e255297.
