رویکرد داخلی از طریق ملتحمه
فراوانی استفاده: 59%، بیشترین میزان.
مزایا: کوتاهترین مسیر. از نظر زیبایی عالی است.
معایب: خطر انحراف چشم و طولانی بودن زمان جراحی.

دکمپرسیون غلاف عصب بینایی (ONSD) که فنستراسیون غلاف عصب بینایی (ONSF) نیز نامیده میشود، به یک روش جراحی واحد اشاره دارد. با ایجاد یک شکاف یا پنجره (فنستر) در سختشامهای که عصب بینایی را احاطه کرده است، مایع مغزی-نخاعی از فضای زیرعنکبوتیه تخلیه شده و فشار موضعی روی عصب بینایی کاهش مییابد. کد CPT 67570 به این روش اختصاص داده شده است.
شایعترین اندیکاسیون، فشار خون بالای داخل جمجمه ایدیوپاتیک (IIH) است که حدود ۲۵٪ موارد مقاوم به درمان پزشکی نیاز به مداخله جراحی دارند. سایر موارد شامل ترومبوز سینوس وریدی مغز، مننژیت کریپتوکوکی، شبهتومور مغزی ناشی از اسید رتینوئیک تمامترانس (ATRA)1) و بیماری مویامویا4) میتواند اندیکاسیون باشد.
اپیدمیولوژی (IIH): میزان بروز سالانه IIH در ایالات متحده 1.15 در 100,000 نفر است. این میزان در زنان (1.97 در 100,000) بیشتر از مردان (0.36 در 100,000) است و بیشترین شیوع در سنین 18 تا 44 سال (2.47 در 100,000) دیده میشود. با افزایش جهانی چاقی، شیوع IIH نیز در حال افزایش است.
| سال | رویداد |
|---|---|
| ۱۸۵۳ | تورک و کوکسیوس برای اولین بار ادم پاپی را گزارش کردند |
| ۱۸۷۲ | د وکر برای اولین بار ONSD را گزارش کرد (به عنوان درمان نورورتینیت) |
| ۱۹۶۴ | Hayreh ناپدید شدن ادم پاپی پس از شکافتن غلاف عصب بینایی را نشان داد |
| ۱۹۷۳ | Galbraith و Sullivan رویکرد داخلی ترانس کنژنکتیوال را توسعه دادند |
| 1988 | Tse و همکاران رویکرد جانبی اربیت را گسترش دادند |
| 2001 | Pelton و Patel رویکرد برش پلک فوقانی داخلی را گزارش کردند |
هر دو به یک روش جراحی اشاره دارند. تنها تفاوت در نامگذاری است و عمل ایجاد شکاف یا پنجره در دورای عصب بینایی برای تخلیه مایع مغزی-نخاعی یکسان است. این سردرگمی ناشی از ترجمه انگلیسی ONSD (decompression غلاف عصب بینایی) و ONSF (fenestration غلاف عصب بینایی) به فارسی به ترتیب به «کمفشاری» و «پنجرهسازی» است.
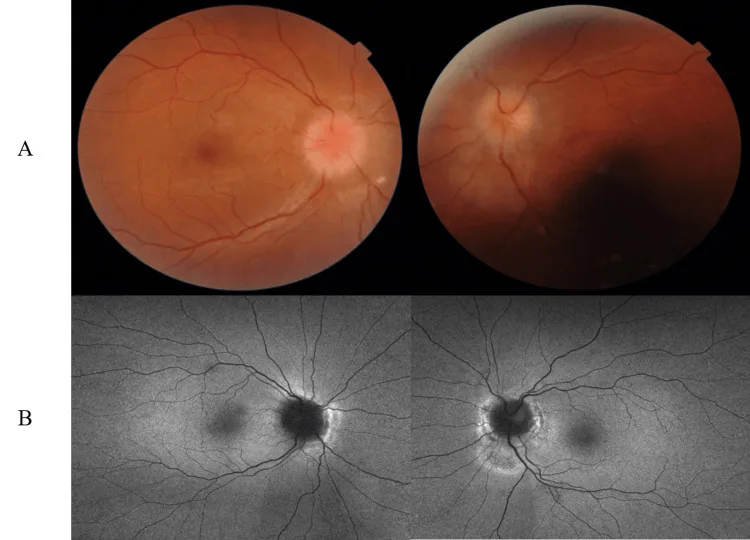
در افزایش فشار داخل جمجمهای (به ویژه IIH) که نشانهای برای ONSD است، علائم زیر ظاهر میشوند.
ویژگیهای نوع شدید (IIH برقآسا): کاهش سریع بینایی در عرض چند هفته، pRNFL بیش از 300 میکرومتر، میانگین فشار باز شدن CSF در اولین پونکسیون کمری 54.1 سانتیمتر آب (محدوده 29-70) مشخصه است. اگر میانگین انحراف میدان بینایی Humphrey کمتر از 7- دسیبل باشد، بهبود بینایی ضعیف است.
عوامل خطر IIH که ONSF بیشتر در آنها انجام میشود به شرح زیر است:
سایر علل افزایش فشار داخل جمجمه (مانند بیماری مویامویا4)، ترومبوز سینوس وریدی مغز، عفونتها و ضایعات اشغالکننده فضا) نیز میتوانند نشانهای برای ONSF باشند.
علاوه بر IIH، شرایطی مانند ترومبوز سینوس وریدی مغز، مننژیت کریپتوکوکی، افزایش فشار داخل جمجمه ناشی از بیماری مویامویا، و سندرم تومور کاذب مغزی ناشی از ATRA (رتینوئیک اسید تمام ترانس) نیز میتوانند اندیکاسیون داشته باشند. در موارد بیماری مویامویا، ONSF برای افزایش فشار داخل جمجمه مقاوم به درمان محافظهکارانه انجام شده و بهبود بینایی گزارش شده است.
لازم است تمام موارد زیر برآورده شوند.
تشخیص افتراقی: ترومبوز سینوس وریدی، کمخونی، آپنه انسدادی خواب، دارویی (تتراسایکلین، ویتامین A و غیره)، اختلالات غدد درونریز. در صورت کاهش حاد بینایی، افتراق از فشار خون بدخیم، مننژیت، نوریت اپتیک (MOG، NMOSD و غیره)، و نفوذ توموری به عصب بینایی (لوسمی، لنفوم) مهم است.
موارد استفاده: در مواردی که سردرد خفیف است، اما ادم پاپی واضح و کاهش بینایی پیشرونده یا تهدیدکننده وجود دارد. هدف اصلی حفظ بینایی است و برای درمان سردرد مؤثر نیست.
روش جراحی: عمدتاً از سه نوع رویکرد استفاده میشود.
رویکرد داخلی از طریق ملتحمه
فراوانی استفاده: 59%، بیشترین میزان.
مزایا: کوتاهترین مسیر. از نظر زیبایی عالی است.
معایب: خطر انحراف چشم و طولانی بودن زمان جراحی.
برش لبه پلک فوقانی داخلی
فراوانی استفاده: 31%.
مزایا: کوتاهترین زمان جراحی. بدون نیاز به میکروسکوپ.
معایب: مسیر طولانی و خطر افتادگی پلک.
برش جانبی مدار
فراوانی استفاده: ۱۰٪، کمترین میزان.
مزایا: تجسم خوب عصب بینایی امکانپذیر است.
معایب: خطر آسیب به گانگلیون مژگانی وجود دارد.
نتایج جراحی (متاآنالیز: 19 مطالعه، 1159 مشاهده)3):
| شاخص پیامد | نرخ بهبود | فاصله اطمینان 95% |
|---|---|---|
| بهبود بینایی | 41.09% | 29 تا 55% |
| بهبود میدان بینایی | 76.34% | 61 تا 87% |
| بهبود پاپیادم | 97% | 84-100% |
نرخ بهبود میدان بینایی در رویکرد ترانس ملتحمه (86%) به طور معنیداری بیشتر از سایر رویکردها (57%) است (0.018=p). نرخ بهبود بینایی بین رویکردها تفاوت معنیداری ندارد (0.715=p)3).
اثر دوطرفه با جراحی یکطرفه: انجام ONSF یکطرفه باعث بهبود ادم پاپیلای طرف مقابل نیز میشود. در ۹ مورد (همگی زن) از فشار خون بالای داخل جمجمهای ایدیوپاتیک، پس از ONSF یکطرفه و پیگیری ۲ ساله، بهبود بینایی دوطرفه در همه موارد تأیید شد2).
خطر عوارض: به طور کلی ۱۰ تا ۱۵٪. جدیترین عارضه از دست دادن بینایی به دلیل انسداد شریان مرکزی شبکیه یا انسداد ورید مرکزی شبکیه (۱ تا ۲٪). سایر عوارض شامل دوبینی (۲۲.۲٪)، خونریزی زیر ملتحمه (۴۴.۴٪) و سلولیت اربیت (۱۱.۱٪) گزارش شده است که اغلب موقتی هستند2).
استنتگذاری سینوس وریدی ممکن است در موارد مقاوم به دارو که تنگی سینوس و گرادیان فشار ثابت شده است، مفید باشد. درمان ضد پلاکتی به مدت ۶ ماه پس از جراحی لازم است. سطح شواهد هنوز پایین است و یک کارآزمایی بالینی تصادفیشده (شنت در مقابل استنت) در بریتانیا در حال انجام است.
در مواردی که چاقی علت اصلی باشد، حتی در موارد مقاوم به درمان معمول، نرخ موفقیت بالایی گزارش شده است. کاهش وزن ۳ تا ۱۵٪ با بهبودی همراه بوده است. در نوع حاد توصیه نمیشود.
تأیید شده است که ONSF یکطرفه باعث بهبود پاپیلادم طرف مقابل نیز میشود. در یک مطالعه دو ساله بر روی ۹ بیمار مبتلا به فشار خون بالای داخل جمجمهای ایدیوپاتیک، بهبود بینایی دوطرفه در همه موارد گزارش شده است. یکی از ویژگیهای مهم این روش، امکان محافظت از بینایی طرف مقابل پس از انجام یکطرفه است.
عود بالینی در ۳۲٪ از بیماران گزارش شده است. در صورت عود، ممکن است نیاز به درمان جراحی اضافی (جراحی مجدد، شانتگذاری، یا استنتگذاری) باشد. پیگیری منظم با معاینات چشمی اهمیت دارد.
فضای زیر عنکبوتیه عصب بینایی با فضای زیر عنکبوتیه سیستم عصبی مرکزی پیوسته است. هنگامی که افزایش فشار داخل جمجمه در طول عصب بینایی به دیسک بینایی منتقل میشود، آسیب از طریق مکانیسمهای زیر رخ میدهد.
الگوی از دست دادن بینایی ابتدا به صورت بزرگ شدن نقطه کور شروع میشود و سپس به نقص پیشرونده میدان بینایی محیطی تبدیل میشود.
مکانیسم محافظت ONSF از عصب بینایی به دو مرحله تقسیم میشود.
نکته مهم: ONSF فشار داخل جمجمه را کاهش نمیدهد. این روش تنها اثر محافظتی موضعی بر عصب بینایی دارد، بنابراین نمیتوان انتظار تأثیر بر علائم سیستمیک مانند سردرد را داشت.
مکانیسم دقیق افزایش فشار داخل جمجمه در فشار خون بالای ایدیوپاتیک داخل جمجمه به طور کامل شناخته نشده است. اختلال در تنظیم دینامیک مایع مغزی-نخاعی و دخالت عوامل متابولیک و هورمونی مطرح است. فشار خون بالای ایدیوپاتیک داخل جمجمه به عنوان یک بیماری متابولیک سیستمیک مستقل از چاقی مورد توجه قرار گرفته و نقش اختلال تنظیم آندروژن نیز پیشنهاد شده است.
ATRA یک مشتق ویتامین A است که با تحریک گیرندههای RAR در شبکه کوروئید، تولید مایع مغزی-نخاعی را افزایش میدهد. همچنین اختلال در جذب مایع مغزی-نخاعی در گرانولهای عنکبوتیه نیز محتمل است.
Prokop و همکاران (2024) یک مرور سیستماتیک و متاآنالیز روی 19 مطالعه و 1159 مشاهده انجام دادند و پیامدهای بینایی ONSF را به طور جامع ارزیابی کردند3). میزان بهبود بینایی 41.09% (95%CI: 29 تا 55%)، میزان بهبود میدان بینایی 76.34% (95%CI: 61 تا 87%)، و میزان بهبود ادم پاپی 97% (95%CI: 84 تا 100%) گزارش شد. تأخیر جراحی بیش از 6 ماه پس از تشخیص، پیامد میدان بینایی را به طور قابل توجهی بدتر کرد (OR 0.06، 95%CI 0.005 تا 0.70). در 32% موارد عود بالینی مشاهده شد.
Latif و همکاران (2023) در ۹ بیمار (همگی زن، میانگین سنی ۲۴ سال) مبتلا به فشار خون بالای داخل جمجمهای ایدیوپاتیک، عمل ONSF را از طریق رویکرد یکطرفه داخلی ملتحمهای انجام دادند و به مدت ۲ سال پیگیری کردند2). BCVA قبل از عمل (logMAR) در چشم بهتر ۰.۵±۰.۲۸ و در چشم بدتر ۱.۰±۰.۵۷ بود. بهبود در هفته اول پس از عمل (چشم بهتر ۰.۲۷±۰.۳۲، p=۰.۰۰۱) پس از ۲ سال نیز حفظ شد (چشم بهتر ۰.۳۰±۰.۳۰، p=۰.۰۰۲). در همه موارد، اثر دوطرفه پس از جراحی یکطرفه تأیید شد. در ۶۶.۶۷٪ موارد، بهبود سردرد و کاهش موفقیتآمیز داروها حاصل شد.
Hokazono و همکاران (2023) در یک زن 32 ساله مبتلا به سندرم تومور کاذب مغزی ناشی از ATRA (45 mg/m²) (فشار باز شدن کمری 42 cm H₂O)، درمان ترکیبی کاهش دوز ATRA، استازولامید 2 گرم در روز و ONSF چشم راست را انجام دادند1). پس از 6 ماه، بهبودی کامل شامل دید 20/20 در هر دو چشم، میدان بینایی طبیعی، ناپدید شدن ادم پاپی و رفع فلج عصب ابدوسنس حاصل شد.
Barh و همکاران (2021) در یک دختر 13 ساله مبتلا به بیماری مویامویا (تنگی شریان کاروتید داخلی چپ + انسداد شریان مغزی میانی چپ) با افزایش فشار داخل جمجمه (فشار باز شدن 75 سانتیمتر آب) عمل ONSF چشم راست را انجام دادند4). درمان محافظهکارانه (مانیتول، استازولامید، توپیرامات) پاسخ نداد، اما یک ماه پس از عمل، دید چشم راست به 3/60 و چشم چپ به 6/24 بهبود یافت و ادم پاپیل دو طرفه نیز برطرف شد. پس از شش ماه، دید چشم راست 6/36 و چشم چپ 6/24 حفظ شد.
این یک رویکرد جدید است که مزایای آن کمتهاجمی بودن، کاهش زمان جراحی و عدم نیاز به قطع عضله میباشد. انتظار میرود آسیب بافتی کاهش یابد، اما هنوز استاندارد نشده است3).
Hokazono K, Cunha LP, Preti RC, Zacharias LC, Monteiro MLR. Optic nerve sheath fenestration as adjuvant treatment for severe pseudotumor cerebri syndrome induced by all-trans retinoic acid. Case Rep Ophthalmol. 2023;14:326-330.
Latif S, Rizwan A, Khan AA, Zahra S. Optic nerve sheath fenestration for salvaging acutely threatened vision in Idiopathic Intracranial Hypertension - A two-year completed follow up. Pak J Med Sci. 2023;39(6):1853-1857.
Prokop K, Opchowska A, Siekiewicz A, Lisowski L, Mariak Z, Lyso T. Effectiveness of optic nerve sheath fenestration in preserving vision in idiopathic intracranial hypertension: an updated meta-analysis and systematic review. Acta Neurochir. 2024;166:476.
Barh A, Mukherjee B, Ambika S. Optic nerve sheath fenestration for visual rehabilitation in moyamoya disease. Saudi J Ophthalmol. 2020;34:223-226.