Medialer transkonjunktivaler Zugang
Häufigkeit: 59%, am häufigsten.
Vorteile: Kürzester Zugang. Kosmetisch überlegen.
Nachteile: Schielrisiko, längere Operationszeit.

Die Optikusnervenscheiden-Dekompression (ONSD), auch Optikusnervenscheiden-Fensterung (ONSF) genannt, bezeichnet dasselbe chirurgische Verfahren. Dabei wird ein Schlitz oder Fenster in die Dura, die den Sehnerv umgibt, geschnitten, um Liquor aus dem Subarachnoidalraum abfließen zu lassen und so den Druck auf den Sehnerv lokal zu reduzieren. Der CPT-Code 67570 ist zugeordnet.
Die häufigste Indikation ist die idiopathische intrakranielle Hypertension (IIH); etwa 25% der medikamentös therapierefraktären Fälle benötigen einen chirurgischen Eingriff. Weitere mögliche Indikationen sind zerebrale Sinusvenenthrombose, Kryptokokken-Meningitis, durch all-trans-Retinsäure (ATRA) induzierter Pseudotumor cerebri1) und Moyamoya-Erkrankung4).
Epidemiologie (IIH): Die jährliche Inzidenz von IIH beträgt in den USA 1,15/100.000. Frauen sind mit 1,97/100.000 häufiger betroffen als Männer (0,36/100.000), mit einem Höhepunkt im Alter von 18–44 Jahren (2,47/100.000). Mit der weltweit zunehmenden Adipositas steigt auch die Prävalenz von IIH.
| Jahr | Ereignis |
|---|---|
| 1853 | Turck und Coccius berichten erstmals über Papillenödem |
| 1872 | De Wecker berichtet erstmals über ONSD (als Behandlung der Neuroretinitis) |
| 1964 | Hayreh demonstrierte das Verschwinden des Papillenödems nach Optikusscheidenfensterung |
| 1973 | Galbraith & Sullivan entwickelten den medialen transkonjunktivalen Zugang |
| 1988 | Tse et al. erweiterten den lateralen Orbitazugang |
| 2001 | Pelton & Patel berichteten über den superomedialen Lidspaltenzugang |
Beide bezeichnen denselben chirurgischen Eingriff. Es handelt sich lediglich um einen Unterschied in der Bezeichnung; der Vorgang, einen Schlitz oder ein Fenster in die Dura des Sehnervs zu schneiden, um CSF abzuleiten, ist derselbe. Die Verwirrung entsteht dadurch, dass die englischen Begriffe ONSD (optic nerve sheath decompression) und ONSF (optic nerve sheath fenestration) im Japanischen als „Dekompressionsverfahren“ bzw. „Fensterungsverfahren“ übersetzt werden.
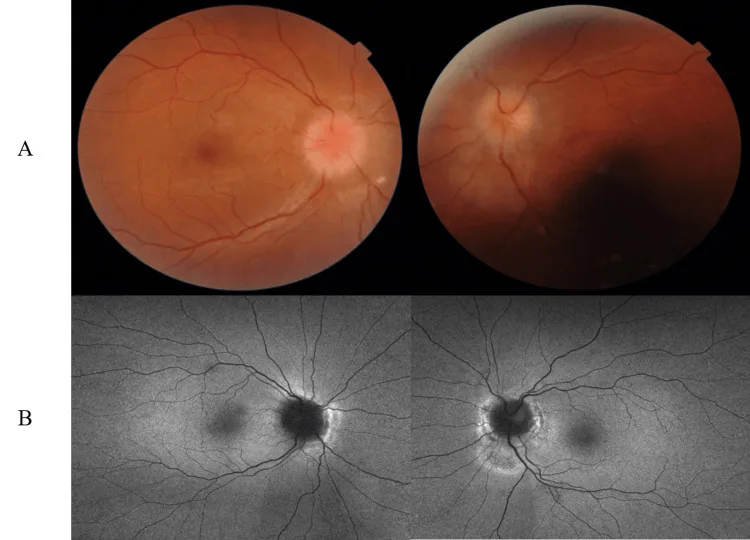
Bei erhöhtem intrakraniellem Druck (insbesondere IIH), der eine ONSD-Indikation darstellt, treten folgende Symptome auf.
Merkmale der schweren Form (fulminante IIH): Rasche Sehverschlechterung innerhalb weniger Wochen, pRNFL >300 μm, mittlerer CSF-Eröffnungsdruck bei erster Lumbalpunktion 54,1 cm H₂O (Spanne 29–70) sind charakteristisch. Bei einem mittleren Defekt im Humphrey-Gesichtsfeld < -7 dB ist die Seherholung schlecht.
Nachfolgend sind die Risikofaktoren für IIH aufgeführt, bei denen ONSF am häufigsten durchgeführt wird.
Auch bei anderen Ursachen für erhöhten intrakraniellen Druck (Moyamoya-Erkrankung 4), zerebrale Sinusvenenthrombose, Infektionen, raumfordernde Läsionen usw.) kann eine ONSF indiziert sein.
Neben IIH können auch Hirnvenenthrombose, Kryptokokken-Meningitis, erhöhter intrakranieller Druck im Zusammenhang mit Moyamoya-Erkrankung und ATRA-induziertes Pseudotumor-cerebri-Syndrom Indikationen sein. Bei Moyamoya-Patienten wurde ONSF bei konservativ therapierefraktärem erhöhtem intrakraniellen Druck durchgeführt, und es wurde über eine Verbesserung des Sehvermögens berichtet.
Es müssen alle folgenden Punkte erfüllt sein.
Differenzialdiagnose: Sinusvenenthrombose, Anämie, obstruktive Schlafapnoe, medikamentös bedingt (Tetrazykline, Vitamin A usw.), endokrine Störungen. Bei akuter Sehverschlechterung ist die Abgrenzung zu maligner Hypertonie, Meningitis, Optikusneuritis (MOG, NMOSD usw.), Optikusinfiltration (Leukämie, Lymphom) wichtig.
Indikation: Bei leichten Kopfschmerzen, ausgeprägter Papillenschwellung und fortschreitender oder drohender Sehverschlechterung. Hauptziel ist der Seherhalt, zur Behandlung von Kopfschmerzen ist sie unwirksam.
Operationszugang: Es werden hauptsächlich drei Zugänge verwendet.
Medialer transkonjunktivaler Zugang
Häufigkeit: 59%, am häufigsten.
Vorteile: Kürzester Zugang. Kosmetisch überlegen.
Nachteile: Schielrisiko, längere Operationszeit.
Obere mediale Lidrandinzision
Häufigkeit: 31%.
Vorteile: Kürzeste Operationszeit. Kein Mikroskop erforderlich.
Nachteile: Langer Zugangsweg, Risiko eines Augenlidschlags.
Laterale Orbitotomie
Häufigkeit: 10%, am seltensten.
Vorteile: Gute Visualisierung des Sehnervs möglich.
Nachteile: Risiko einer Schädigung des Ganglion ciliare.
Operationsergebnisse (Metaanalyse: 19 Studien, 1159 Beobachtungen)3):
| Ergebnisparameter | Verbesserungsrate | 95%-KI |
|---|---|---|
| Sehverbesserung | 41,09% | 29–55% |
| Gesichtsfeldverbesserung | 76,34% | 61–87% |
| Verbesserung der Papillenschwellung | 97% | 84–100% |
Die Gesichtsfeldverbesserungsrate beim transkonjunktivalen Zugang (86%) ist signifikant höher als bei anderen Zugängen (57%) (p=0,018). Die Sehschärfenverbesserungsrate unterschied sich nicht signifikant zwischen den Zugängen (p=0,715) 3).
Einseitige Operation mit beidseitigem Effekt: Eine einseitige ONSF verbessert auch die Papillenschwellung der Gegenseite. Bei 9 Patientinnen (alle weiblich) mit idiopathischer intrakranieller Hypertension wurde nach einseitiger ONSF über 2 Jahre hinweg eine beidseitige Sehverbesserung bestätigt 2).
Komplikationsrisiko: Insgesamt 10–15 %. Die schwerwiegendste Komplikation ist der Sehverlust durch Verschluss der Arteria centralis retinae oder der Vena centralis retinae (1–2 %). Weitere Komplikationen wie Doppelbilder (22,2 %), subkonjunktivale Blutungen (44,4 %) und orbitale Zellulitis (11,1 %) wurden berichtet, sind jedoch meist vorübergehend 2).
Kann bei medikamentös refraktären Fällen mit nachgewiesener Sinusstenose und Druckgradient nützlich sein. Postoperativ ist eine 6-monatige Thrombozytenaggregationshemmung erforderlich. Die Evidenz ist noch gering; eine RCT (Shunt vs. Stent) läuft in Großbritannien.
Wenn Fettleibigkeit die Hauptursache ist, wird selbst bei therapieresistenten Fällen eine hohe Erfolgsrate berichtet. Eine Gewichtsreduktion von 3–15 % kann zu einer Remission führen. Bei fulminanten Formen wird sie nicht empfohlen.
Es wurde bestätigt, dass eine einseitige ONSF auch die Papillenödem auf der Gegenseite verbessert. In einer zweijährigen Studie mit 9 Patienten mit idiopathischer intrakranieller Hypertonie wurde bei allen eine beidseitige Sehverbesserung berichtet. Die Möglichkeit, nach einseitiger Durchführung einen Sehschutz auf der Gegenseite zu erwarten, ist ein wichtiges Merkmal dieses Verfahrens.
Bei 32 % der Patienten wurde ein klinisches Rezidiv berichtet. Im Falle eines Rezidivs kann eine zusätzliche chirurgische Behandlung (erneute Operation, Shunt-Operation, Stent-Implantation) erforderlich sein. Regelmäßige augenärztliche Kontrolluntersuchungen sind wichtig.
Der Subarachnoidalraum des Sehnervs ist mit dem Subarachnoidalraum des zentralen Nervensystems verbunden. Wenn der erhöhte ICP entlang des gesamten Sehnervs auf die Papille übertragen wird, kommt es durch folgende Mechanismen zu einer Schädigung.
Das Muster des Sehverlusts beginnt früh mit einer Vergrößerung des blinden Flecks und geht in einen fortschreitenden Gesichtsfeldausfall über.
Der Mechanismus, durch den die ONSF den Sehnerv schützt, lässt sich in zwei Schritte unterteilen.
Wichtiger Punkt: ONSF senkt den ICP nicht. Es entfaltet nur eine lokale Schutzwirkung auf den Sehnerv, daher ist kein Effekt auf systemische Symptome wie Kopfschmerzen zu erwarten.
Der genaue Mechanismus der intrakraniellen Drucksteigerung bei idiopathischer intrakranieller Hypertonie ist nicht vollständig geklärt. Es wird angenommen, dass eine Störung der Liquordynamik sowie metabolische und hormonelle Faktoren eine Rolle spielen. Die idiopathische intrakranielle Hypertonie wird zunehmend als eine von Adipositas unabhängige systemische Stoffwechselerkrankung betrachtet, und es gibt Hinweise auf eine Beteiligung einer gestörten Androgenregulation.
ATRA ist ein Vitamin-A-Derivat, das die RAR-Rezeptoren im Plexus choroideus stimuliert und die Liquorproduktion erhöht. Es wird vermutet, dass auch eine gestörte Liquorresorption an den Arachnoidalzotten beteiligt ist.
Prokop et al. (2024) führten eine systematische Übersichtsarbeit und Metaanalyse von 19 Studien mit 1159 Beobachtungen durch und bewerteten umfassend die visuellen Ergebnisse der ONSF3). Sie berichteten eine Verbesserungsrate der Sehschärfe von 41,09% (95%-KI: 29–55%), eine Verbesserungsrate des Gesichtsfelds von 76,34% (95%-KI: 61–87%) und eine Verbesserungsrate des Papillenödems von 97% (95%-KI: 84–100%). Bei einer Operationsverzögerung von mehr als 6 Monaten nach der Diagnose verschlechterten sich die Gesichtsfeldergebnisse erheblich (OR 0,06; 95%-KI 0,005–0,70). Bei 32% trat ein klinisches Rezidiv auf.
Latif et al. (2023) führten bei 9 Patientinnen (alle weiblich, Durchschnittsalter 24 Jahre) mit idiopathischer intrakranieller Hypertension eine einseitige mediale transkonjunktivale ONSF durch und beobachteten sie über 2 Jahre 2). Der präoperative BCVA (logMAR) betrug 0,5±0,28 am besseren Auge und 1,0±0,57 am schlechteren Auge. Die Verbesserung eine Woche postoperativ (besseres Auge 0,27±0,32, p=0,001) blieb nach 2 Jahren erhalten (besseres Auge 0,30±0,30, p=0,002). Bei allen Fällen wurde ein bilateraler Effekt nach einseitiger Operation bestätigt. Bei 66,67% der Patientinnen besserten sich die Kopfschmerzen und die Medikation konnte erfolgreich reduziert werden.
Hokazono et al. (2023) behandelten eine 32-jährige Frau mit ATRA (45 mg/m²)-induziertem Pseudotumor cerebri (Lumbalpunktion Eröffnungsdruck 42 cm H₂O) mit einer Kombination aus ATRA-Dosisreduktion, Acetazolamid 2 g/Tag und ONSF am rechten Auge 1). Nach 6 Monaten wurde eine vollständige Erholung mit 20/20-Sehschärfe auf beiden Augen, normalem Gesichtsfeld, Abklingen des Papillenödems und Verschwinden der Abduzensparese erreicht.
Barh et al. (2021) führten eine rechtsseitige ONSF bei einem 13-jährigen Mädchen mit erhöhtem intrakraniellem Druck (Eröffnungsdruck 75 cm H₂O) infolge einer Moyamoya-Erkrankung (linke ICA-Stenose + linke MCA-Okklusion) durch 4). Die konservative Therapie (Mannitol, Acetazolamid, Topiramat) war erfolglos, aber einen Monat nach dem Eingriff besserte sich der Visus auf 3/60 rechts und 6/24 links, und das bilaterale Papillenödem bildete sich zurück. Nach sechs Monaten blieb der Visus bei 6/36 rechts und 6/24 links stabil.
Dies ist ein neuer Ansatz, der als minimalinvasiv mit kürzerer Operationszeit und ohne Muskelabtrennung gilt. Eine Reduktion der Gewebeschädigung wird erwartet, jedoch ist das Verfahren noch nicht standardisiert 3).
Hokazono K, Cunha LP, Preti RC, Zacharias LC, Monteiro MLR. Optic nerve sheath fenestration as adjuvant treatment for severe pseudotumor cerebri syndrome induced by all-trans retinoic acid. Case Rep Ophthalmol. 2023;14:326-330.
Latif S, Rizwan A, Khan AA, Zahra S. Optic nerve sheath fenestration for salvaging acutely threatened vision in Idiopathic Intracranial Hypertension - A two-year completed follow up. Pak J Med Sci. 2023;39(6):1853-1857.
Prokop K, Opchowska A, Siekiewicz A, Lisowski L, Mariak Z, Lyso T. Effectiveness of optic nerve sheath fenestration in preserving vision in idiopathic intracranial hypertension: an updated meta-analysis and systematic review. Acta Neurochir. 2024;166:476.
Barh A, Mukherjee B, Ambika S. Optic nerve sheath fenestration for visual rehabilitation in moyamoya disease. Saudi J Ophthalmol. 2020;34:223-226.