یافتههای پلکی
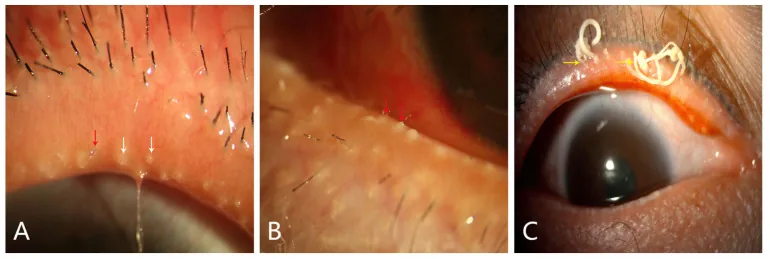
گشاد شدن مویرگهای لبه پلک: در ۵۰ تا ۹۴٪ موارد دیده میشود. همراه با قرمزی 1).
نارسایی غدد میبومین: تا ۹۲٪ موارد وجود دارد. ترشح غلیظ و کدر میبوم. انسداد دهانه غدد.
عود گل مژه و شالازیون: به دنبال نارسایی غدد میبومین رخ میدهد.

روزاسه چشمی (ocular rosacea) نوع چشمی روزاسه، یک بیماری التهابی مزمن پوستی (زیرگروه IV) است 1). با اتساع عروق مویرگی، بلفاریت، اختلال عملکرد غدد میبومین (MGD) و کراتیت مشخص میشود و التهاب مزمن سطح چشم را ایجاد میکند.
شیوع جهانی روزاسه حدود ۵.۵٪ است که از این میان علائم چشمی در ۵۸ تا ۷۲٪ بیماران دیده میشود 1). سن شایع بروز ۲۵ تا ۵۵ سال است و در زنان بیشتر تشخیص داده میشود. در انواع پوستی فیتزپاتریک I-II (پوست روشن) شایعتر است، اما در افراد با پوست تیره نیز رخ میدهد 1).
در ۵۳٪ موارد یافتههای پوستی先行، در ۲۷٪ همزمانی پوست و چشم، و در ۲۰٪ موارد یافتههای چشمی مقدم هستند 1). بنابراین باید توجه داشت که روزاسه چشمی حتی بدون علائم پوستی نیز ممکن است بروز کند. موارد کودکان (بلفاروکراتوکونژکتیویت اطفال) نیز گزارش شده است 1).
در حدود ۲۰٪ از موارد، علائم چشمی قبل از علائم پوستی ظاهر میشوند1). حتی بدون وجود علائم پوستی典型 مانند قرمزی صورت و گشاد شدن عروق، ممکن است به صورت التهاب مزمن پلک یا اختلال عملکرد غدد میبومین بروز کند. در صورت تداوم علائم سطحی چشم، باید احتمال روزاسه چشمی را در نظر گرفت.
علائم ذهنی روزاسه چشمی غیراختصاصی هستند و نیاز به افتراق از خشکی چشم دارند1).
علائم معمولاً با دورههای تشدید و بهبودی، در طول زمان پیشرونده هستند1). شدت علائم پوستی و چشمی لزوماً با هم همبستگی ندارند.
یافتههای پلکی
گشاد شدن مویرگهای لبه پلک: در ۵۰ تا ۹۴٪ موارد دیده میشود. همراه با قرمزی 1).
نارسایی غدد میبومین: تا ۹۲٪ موارد وجود دارد. ترشح غلیظ و کدر میبوم. انسداد دهانه غدد.
عود گل مژه و شالازیون: به دنبال نارسایی غدد میبومین رخ میدهد.
یافتههای ملتحمه و قرنیه
قرمزی ملتحمه: قرمزی ملتحمه کره چشم. همراه با واکنش فولیکولی و پاپیلاری 1).
ضایعات قرنیه: در ۲۵ تا ۵۰٪ موارد ظاهر میشود. میتواند از کراتیت سطحی نقطهای به نفوذ حاشیهای، عروق جدید، زخم و سوراخ شدن پیشرفت کند 1).
اسکار قرنیه: اگر التهاب مزمن به محور بینایی برسد، باعث اختلال بینایی میشود.
یافتههای نادر
سندرم مورهان: ادم نفوذی پیشانی، بینی، ناحیه بین ابروها، گونهها و اطراف چشم. همراه با لنف ادم 5).
رینوفیما (بینی غدهای): یافته پوستی در مراحل晚期. ضخیم شدن پوست، ندول و فیبروز.
برای ارزیابی مورفولوژی غدد میبومین، میبوگرافی غیرتهاجمی مفید است. میبوگرافی تنها روشی است که ساختار غدد میبومین را به صورت درونبدنی و مورفولوژیک با مشاهده پلک در نور عبوری ارزیابی میکند.
علت دقیق روزاسه چشمی ناشناخته است، اما ناهنجاریهای ایمنی، نارسایی تنظیم عروق، عوامل میکروبی و استعداد ژنتیکی به طور ترکیبی نقش دارند 1).
قرار گرفتن طولانی مدت در معرض اشعه فرابنفش، مصرف الکل و کافئین، غذاهای تند و نوشیدنیهای داغ، استرس روانی، ورزش شدید، و قرار گرفتن در معرض دما و باد شدید از عوامل تشدیدکننده معمول هستند. این عوامل باعث گشاد شدن عروق و التهاب شده و عود علائم را تحریک میکنند. از آنجایی که عوامل تشدیدکننده در افراد مختلف متفاوت است، توصیه میشود با ثبت روزانه، محرکهای شخصی خود را شناسایی کنید.
روزاسه چشمی یک تشخیص بالینی است و معیار آزمایشگاهی اختصاصی وجود ندارد1). کنسرسیوم جهانی روزاسه (ROSCO) در سال ۲۰۱۹ یک رویکرد جامع تشخیصی را توصیه کرده است1).
تشخیص افتراقی با سندرم خشکی چشم، ورم ملتحمه باکتریایی/آلرژیک، بلفاریت سبورئیک، کراتیت هرپس سیمپلکس، لوپوس اریتماتوز سیستمیک، سندرم شوگرن و غیره ضروری است1). روزاسه چشمی باید در مواردی که به درمان معمول بلفاریت پاسخ نمیدهد، مشکوک شود6).
درمان روزاسه چشمی با رویکرد مرحلهای بر اساس شدت بیماری توصیه میشود1). پانل بینالمللی ROSCO، کمیته تخصصی انجمن ملی روزاسه آمریکا و راهنمای درمان سوئیس توصیههای درمانی را ارائه کردهاند.
خفیف
بهداشت پلک: شستشوی پلک با صابون غیرتحریککننده، کمپرس گرم، ماساژ1).
اشک مصنوعی: حتی با مواد نگهدارنده قابل قبول است.
اجتناب از عوامل تشدیدکننده: محافظت در برابر اشعه UV، توصیههای غذایی.
اسیدهای چرب امگا 3: EPA 720 میلیگرم + DHA 480 میلیگرم در روز1).
متوسط
قطره چشمی آزیترومایسین 1 تا 1.5%: 2 بار در روز به مدت 2 روز، یا 1 بار در روز به مدت 5 روز1).
سیکلوسپورین قطره چشمی 0.05-0.1%: دو بار در روز. قابل استفاده طولانی مدت 1).
تاکرولیموس قطره چشمی 0.03%: دو بار در روز 1).
قطره استروئیدی: استفاده کوتاه مدت در التهاب فعال.
شدید
داکسی سایکلین خوراکی: دوز اولیه 100 میلیگرم 1-2 بار در روز → دوز نگهدارنده 40 میلیگرم در روز. به مدت 12 هفته 1).
آزیترومایسین خوراکی: 500 میلیگرم یک بار در روز به مدت 3 روز، یا یک بار در هفته به مدت 3 هفته 1).
سیکلوسپورین سیستمیک: فقط در موارد مقاوم به درمان 1).
IPL + MGX: در موارد متوسط به بالا در نظر گرفته شود.
در کودکان از اریترومایسین خوراکی یا مترونیدازول استفاده میشود 1).
| دارو | دوز | توضیحات |
|---|---|---|
| داکسی سایکلین | 40-100 میلیگرم در روز | خط اول. اثربخشی در RCT ثابت شده است 1) |
| آزیترومایسین | 500 میلیگرم/روز به مدت 3 روز | در صورت عدم تحمل تتراسایکلین |
| مینوسایکلین | 100 میلیگرم/روز به مدت 12 هفته | جایگزین داکسیسایکلین |
حذف دمودکس با استفاده از دستمالهای پلکی حاوی ترپینن-4-اول (T4O) مؤثر است.
یین و همکاران (2021) موردی از یک زن 72 ساله با بلفاریت مقاوم مرتبط با روزاسه به مدت 5 سال را گزارش کردند که با دستمال T4O درمان شد4). اریتم صورت و پلک در یک ماه به طور قابل توجهی بهبود یافت و تلانژکتازی در دو ماه ناپدید شد. نمره OSDI از 37 به 15 کاهش یافت و در پیگیری 8 ماهه، ریشهکنی کامل دمودکس و消失 علائم حفظ شد.
در مرور سیستماتیک شرگیل و همکاران (2024)، ترکیب IPL + MGX در 91٪ (89 از 98) موارد پاسخ نسبی نشان داد3). هیچ مورد بهبودی کامل وجود نداشت، اما فراوانی و شدت علائم خشکی چشم و قرمزی لبه پلک کاهش یافت. پروتکل Toyos با 3-4 جلسه در فواصل 4-6 هفته اغلب استفاده میشود.
در صورت درگیری محور بینایی توسط اسکار قرنیه، کراتوپلاستی لایهای عمیق (DALK) توصیه میشود1). کراتوپلاستی تماملایه به دلیل عروقزایی قرنیه و التهاب مزمن پیشآگهی ضعیفی دارد. برای سوراخ شدن قرنیه از فلپ ملتحمه، پیوند تکهای تونون و چسب بافتی استفاده میشود1).
درمان IPL (نور پالسی شدید) درمانی است که با استفاده از نور پالسی تولید شده توسط لامپ فلاش به صورت تابانده میشود تا بهبود خروج غدد میبومین، کاهش التهاب و از بین بردن دمودکس را به همراه داشته باشد. این درمان مستقیماً روی پلک انجام نمیشود و با استفاده از محافظ انجام میگیرد. معمولاً ۳ تا ۴ جلسه با فاصله ۴ تا ۶ هفته انجام میشود. برای جزئیات بیشتر به بخش درمان استاندارد مراجعه کنید.
روزاسه چشمی یک بیماری مزمن است و درمان کامل آن دشوار است. هدف درمان کنترل علائم و پیشگیری از عوارض است. با ادامه بهداشت پلک و اجتناب از عوامل تشدیدکننده، اغلب میتوان وضعیت پایداری را حفظ کرد، اما در صورت عود التهاب، نیاز به درمان دارویی مناسب است.
پاتوفیزیولوژی روزاسه چشمی یک التهاب مزمن است که در آن فعالسازی بیش از حد سیستم ایمنی ذاتی، اختلال تنظیم عصبی-عروقی و نارسایی غدد میبومین به طور پیچیدهای دخیل هستند1)2).
بیان بیش از حد TLR2 در کراتینوسیتها نقش اصلی را ایفا میکند1)2). TLR2 مسیر سیگنالینگ NF-κB را فعال کرده و تولید سیتوکینهای التهابی مانند IL-1β، TNF-α، IL-6 و IL-8 را القا میکند. همزمان، از طریق سرین پروتئاز KLK5، تولید کاتلیسیدین LL-37 افزایش مییابد2).
LL-37 با اثرات ترکیبی زیر التهاب مزمن را حفظ میکند:
در اشک بیماران مبتلا به روزاسه چشمی، غلظت IL-1α/β، MMP-8 و MMP-9 افزایش یافته است2). IL-1α تولید و فعالسازی MMP-9 را افزایش داده و باعث علائم تحریکی پلک و سطح چشم، نقص اپیتلیال قرنیه، زخم قرنیه و رگزایی قرنیه میشود2). هرچه کلیرانس اشک کاهش یابد، غلظت این عوامل التهابی بیشتر میشود.
MGD به عنوان «یک اختلال مزمن منتشر غدد میبومین که با انسداد انتهای مجرا و/یا تغییرات کیفی و کمی ترشحات غدد مشخص میشود» تعریف میگردد. انسداد ناشی از افزایش کراتینه شدن اپیتلیوم مجرا و افزایش ویسکوزیته میبوم منجر به تحلیل رفتن، آتروفی و کاهش ترشح غدد میشود 2). کاهش لایه لیپیدی تبخیر اشک را تسریع کرده و باعث خشکی چشم تبخیری میشود.
نارسایی غدد میبومین به دو نوع کاهش ترشح و افزایش ترشح تقسیم میشود که هر کدام به دو دسته اولیه و ثانویه تقسیم میشوند.
Demodex folliculorum و D. brevis در غدد چربی زندگی میکنند. در بیماران مبتلا به روزاسه، تراکم آنها بیشتر از پوست طبیعی است و با فعالسازی TLR2 پاسخ ایمنی ذاتی را افزایش میدهند 4). سوپرآنتیژنهای تولید شده توسط باکتری همزیست Bacillus oleronius از طریق تولید IL-8 و IL-12p70 سلولهای T CD4+ و ماکروفاژها را فعال کرده و نفوذ سلولهای لانگرهانس را افزایش میدهند 4). دمودکس همچنین تولید لیپاز و استراز را افزایش داده و تجزیه لیپیدهای میبوم را تسریع میکند و نارسایی غدد میبومین را تشدید میکند.
در مرور محمد-نوریگا و همکاران (2025) گزارش شده است که با پیشرفت درک ناهنجاریهای ایمنی و تغییرات میکروبیوم، تحقیقات در مورد درمانهای هدفمند از جمله داروهای بیولوژیک و مهارکنندههای مولکول کوچک در حال افزایش است 1). نام داروهای خاص و نتایج کارآزماییهای بالینی هنوز به اندازه کافی جمعآوری نشده است.
احتمال دارد که دیسبیوز روده (اختلال در فلور روده) در تشدید یا عود روزاسه نقش داشته باشد 1). کشف مسیرهای التهابی از طریق محور روده-چشم (gut-eye axis) ممکن است به یافتن اهداف درمانی جدید منجر شود.
مطالعات ارتباط ژنومی گسترده (GWAS) نشان دادهاند که پلیمورفیسمهای تکنوکلئوتیدی در ژنهای HLA-DRA، BTNLA2 و HLA-DRB1*03:01 با روزاسه مرتبط هستند 1). کشف استعداد ژنتیکی میتواند پایهای برای درمان شخصیسازی شده باشد.
قطرههای ضد VEGF یا تزریق زیر ملتحمه برای مدیریت عروق جدید قرنیه بررسی شدهاند1). دیاترمی با سوزن ریز برای تلانژکتازیهای موجود نیز به عنوان یک گزینه گزارش شده است.