CNA1 (نوع اتوزومال غالب)
شدت: خفیف
ژن عامل: ناشناخته (ژن کاندید در ناحیه 12q)
قدرت انکساری قرنیه: حدود 38 دیوپتر (3 تا 7 دیوپتر کمتر از نرمال)
مرکز قرنیه: شفاف
دوربینی: خفیف تا متوسط (میانگین 6.33+ دیوپتر)

قرنیهی مسطح (cornea plana) یک بیماری مادرزادی است که در آن قسمت محیطی قرنیه اسکلروتیزه شده و قرنیه صاف میشود. مرز بین قرنیه و صلبیه نامشخص شده و قطر قرنیه شفاف کاهش مییابد. معمولاً دوطرفه است و در هر دو جنس رخ میدهد.
تصور میشود که در اثر ناهنجاری در پایه لیمبوس در مرحله جنینی ایجاد میشود. به دو نوع CNA1 اتوزومال غالب و CNA2 اتوزومال مغلوب تقسیم میشود.
این بیماری بسیار نادر است. CNA2 در شمال فنلاند و عربستان سعودی به دلیل اثر بنیانگذار تجمع دارد. موارد فنلاندی حدود 80٪ از موارد جهانی CNA2 را تشکیل میدهند. خانوادههای مبتلا به CNA1 در دانمارک، آلمان، ایالات متحده، هلند و کوبا گزارش شدهاند.
CNA1 (نوع اتوزومال غالب)
شدت: خفیف
ژن عامل: ناشناخته (ژن کاندید در ناحیه 12q)
قدرت انکساری قرنیه: حدود 38 دیوپتر (3 تا 7 دیوپتر کمتر از نرمال)
مرکز قرنیه: شفاف
دوربینی: خفیف تا متوسط (میانگین 6.33+ دیوپتر)
CNA2 (نوع اتوزومال مغلوب)
شدت: شدید
ژن عامل: جهش هموزیگوت در ژن KERA (12q)
قدرت انکساری قرنیه: حدود 30 دیوپتر یا کمتر1)
مرکز قرنیه: اغلب با کدورت همراه است
دوربینی: شدید (بیش از 10+ دیوپتر)
CNA1 یک نوع خفیف با وراثت اتوزومال غالب است. مرکز قرنیه شفاف بوده، قدرت انکساری قرنیه حدود 38 دیوپتر (نزدیک به محدوده نرمال) و دوربینی خفیف است. در مقابل، CNA2 یک نوع شدید با وراثت اتوزومال مغلوب ناشی از جهش در ژن KERA است. مرکز قرنیه با کدورت همراه بوده، قدرت انکساری قرنیه تا حدود 30 دیوپتر کاهش مییابد و دوربینی شدید بیش از 10+ دیوپتر دیده میشود. در CNA2، ناهنجاریهای زاویه و عنبیه و سایر عوارض چشمی شایعتر بوده و پیشآگهی بدتر از CNA1 است.
بیماران اغلب در دوران کودکی به دلیل دید ضعیف ناشی از دوربینی شدید مراجعه میکنند. در CNA2 ممکن است تنبلی چشم همراه باشد. همچنین ممکن است کاهش بینایی ناشی از کدورت قرنیه گزارش شود.
قرنیه صاف میشود و مرز بین قرنیه و صلبیه نامشخص است. ناحیه اطراف قرنیه کدر میشود و در CNA2 ممکن است کدورت در مرکز نیز دیده شود. قوس پیری (arcus lipoides) در سنین نسبتاً پایین ظاهر میشود. اتاق قدامی کم عمق است و عمق اتاق قدامی گزارش شده 0.8 تا 2.1 میلیمتر است.
| یافته | CNA1 | CNA2 |
|---|---|---|
| قدرت انکساری قرنیه | حدود 38 D | حدود 30 D یا کمتر |
| مرکز قرنیه | شفاف | کدورت دارد |
| درجه دوربینی | حدود 6.33+ D | بیش از 10+ D |
در CNA2 ممکن است یک ضخیمشدگی دایرهای و کدر به قطر 4 تا 6 میلیمتر در مرکز قرنیه دیده شود. این ضخیمشدگی به غشای دسمه متصل است و قرنیه در اطراف آن نازکترین است. ممکن است ناهنجاریهای عنبیه (آتروفی عنبیه، گره عنبیه، ناهنجاری مردمک) نیز همراه باشد.
در یک مورد، مقادیر K به ترتیب 21.8/27.0 D و 19.4/28.7 D بسیار صاف بود، عمق اتاق قدامی 1.15 میلیمتر و 0.97 میلیمتر، و ضخامت مرکزی قرنیه 410 میکرومتر و 315 میکرومتر نازک بود1).
CNA2 در اثر جهش هموزیگوت در ژن KERA روی کروموزوم 12 ایجاد میشود. ژن KERA کدکننده کراتوکان است. کراتوکان یک پروتئوگلیکان اختصاصی قرنیه است که در تنظیم فاصله و قطر فیبریلهای کلاژن نقش دارد.
هر دو نوع جهش missense و nonsense گزارش شدهاند. به ویژه در جمعیت عربستان سعودی، 7 جهش مختلف KERA شناسایی شده است. تاکنون 15 جهش KERA گزارش شده که 7 تای آنها از نوع missense هستند1).
ژن عامل CNA1 هنوز شناسایی نشده است. دو ژن کاندید روی کروموزوم 12 در حال بررسی هستند، اما ژنهای شناخته شده مانند DCN، DSPG3، LUM، PITX2 و FOXC1 به عنوان عامل رد شدهاند.
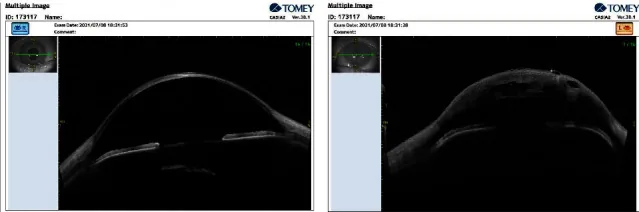
اسکلرالیزاسیون محیط قرنیه و مسطح شدن قرنیه تأیید میشود. با چرخاندن سیستم مشاهده لامپ شکاف به طرفین، مسطح شدن قرنیه به وضوح قابل مشاهده است. در CNA2، کدورت مرکزی قرنیه نیز ارزیابی میشود.
اندازهگیری قدرت انکساری قرنیه برای تمایز بین CNA1 و CNA2 مفید است. در CNA2، قدرت قرنیه حدود 30 دیوپتر و در CNA1 حدود 38 دیوپتر است. کراتومترهای قدیمی ممکن است نتوانند مقادیر زیر 30 دیوپتر را اندازهگیری کنند، بنابراین از یک لنز پلاس ضعیف برای گسترش دامنه اندازهگیری استفاده میشود.
رابطه بین قرنیه، زاویه عنبیه-قرنیه و عنبیه را به خوبی نشان میدهد و مفید است. همچنین برای ارزیابی عمق و وسعت کدورت مرکزی قرنیه استفاده میشود.
| بیماری | نکات افتراقی |
|---|---|
| اسکلرالیزاسیون قرنیه | فقط کدورت و مسطح شدن قرنیه |
| EDS نوع VI | همراه با علائم سیستمیک |
| ناهنجاری Rieger | دیسژنزیس بخش قدامی چشم |
علاوه بر این، تشخیص افتراقی از دیستروفی پلیمورف خلفی قرنیه (PPCD)، موکوپلیساکاریدوز و میکروقرنیه ضروری است. مسطح شدن قرنیه بدون ناهنجاریهای سیستمیک به احتمال زیاد قرنیه مسطح است.
تشخیص قرنیه مسطح بر اساس تأیید مسطح شدن قرنیه و اسکلرالیزاسیون محیطی با معاینه با لامپ شکاف، و اندازهگیری کاهش قدرت انکساری قرنیه با کراتومتری است. در CNA2، قدرت انکساری قرنیه تا حدود 30 D کاهش مییابد. OCT بخش قدامی برای ارزیابی دقیق قرنیه و زاویه مفید است. برای تشخیص قطعی از آزمایش ژنتیکی ژن KERA استفاده میشود. در تشخیص افتراقی باید اسکلرالیزاسیون قرنیه، سندرم اهلرز-دانلوس نوع VI و ناهنجاری Rieger را رد کرد.
اگر کدورت محدود به محیط باشد، اصلاح دوربینی اساس درمان است. در تجویز عینک، بر اساس معاینه انکساری ذهنی، توصیه میشود عدسیهایی ۳ تا ۴ دیوپتر ضعیفتر از مقادیر اندازهگیری شده عینی تجویز شود.
اگر کدورت به مرکز گسترش یابد، پیوند قرنیه در نظر گرفته میشود. با این حال، نتایج پیوند تماملایه قرنیه ضعیف است و باید به خطر گلوکوم ناشی از ناهنجاری زاویه توجه کرد.
در قرنیه مسطح، به دلیل اتاق قدامی کم عمق و مقادیر غیرطبیعی K، جراحی آب مروارید دشوار است. در محاسبه قدرت لنز داخل چشمی، ممکن است دستگاههای اندازهگیری نوری معمولی قابل استفاده نباشند و از فرمول رگرسیون SRK استفاده شود1). در یک مورد، از لنز داخل چشمی توریک ۳۴ دیوپتر استفاده شد و دید اصلاح شده پس از عمل ۶/۱۲ به دست آمد1). در حین جراحی، استفاده کافی از مواد ویسکوالاستیک و حفظ اتاق قدامی با فشار پرفیوژن بالا مهم است1).
به دلیل اتاق قدامی کم عمق، خطر گلوکوم زاویه بسته بالا است. مواردی از گلوکوم زاویه باز نیز گزارش شده است. پایش منظم فشار داخل چشم و معاینه زاویه ضروری است.
امکانپذیر است اما از نظر فنی دشوار است. به دلیل اتاق قدامی کم عمق و قرنیه غیرطبیعی مسطح، دستگاههای اندازهگیری معمولی ممکن است برای محاسبه قدرت لنز داخل چشمی مناسب نباشند. از روشهای محاسباتی جایگزین مانند فرمول رگرسیون SRK استفاده میشود. در حین جراحی، استفاده کافی از مواد ویسکوالاستیک برای حفظ اتاق قدامی و محافظت از اندوتلیوم قرنیه مهم است. استفاده از لنز داخل چشمی توریک امکان اصلاح آستیگماتیسم بالا را نیز فراهم میکند. گزارشهای اخیر نتایج انکساری خوبی را نشان دادهاند.
کراتوکان که توسط ژن KERA کد میشود، به خانواده پروتئوگلیکانهای کوچک غنی از لوسین (SLRP) تعلق دارد. کراتوکان دارای ۱۰ موتیف تکرار شونده غنی از لوسین (LRR) است و فاصله (۴۲-۴۴ نانومتر) و قطر فیبریلهای کلاژن استرومای قرنیه را کنترل میکند1). این آرایش یکنواخت فیبریلها برای حفظ شفافیت، قدرت انکساری و استحکام قرنیه ضروری است.
جهش KERA باعث بیثباتی ساختار کراتوکان و اختلال در اتصال آن به فیبریلهای کلاژن میشود. یک جهش جدید (c.659T>C, p.Leu220Ser) نشان داده است که هسته آبگریز درون موتیف LRR تخریب شده و ساختار پایدار نردبان آسپاراژین مختل میشود1).
PACD یک بیماری اتوزومال غالب است که در اثر حذف هتروزیگوت چهار ژن SLRP شامل KERA، LUM، DCN و EPYC واقع در 12q21.33 ایجاد میشود2). مانند قرنیه مسطح، با کاهش مقدار K (کمتر از 41 D) و نازک شدن قرنیه تظاهر میکند2). وجه مشترک هر دو بیماری تغییر ساختار قرنیه به دلیل ناهنجاری ژن KERA است، اما تفاوت ژنتیکی در این است که PACD ناشی از حذف چند ژن است، در حالی که CNA2 قرنیه مسطح ناشی از جهش نقطهای در ژن KERA است.
پیشرفت در آزمایشهای ژنتیکی منجر به شناسایی جهشهای جدید KERA شده است. تاکنون 15 جهش KERA گزارش شده است که به بهبود دقت مشاوره ژنتیک کمک میکند1). پیشبینی بیماریزایی واریانتهای با اهمیت نامشخص (VUS) با استفاده از مدلسازی پروتئین به عنوان یک رویکرد جدید در تشخیص ژنتیکی مورد توجه قرار گرفته است1).
در جراحی آب مروارید، استفاده از لنزهای داخل چشمی تریک و روشهای بیومتری به نتایج انکساری مطلوبی منجر شده است1). در آینده، شرکت در کارآزماییهای بالینی سلول درمانی و ژن درمانی نیز قابل تصور است1).