CNA1 (Otozomal dominant tip)
Şiddet: Hafif
Sorumlu gen: Tanımlanmamış (12q bölgesinde aday gen)
Kornea kırma gücü: Yaklaşık 38 D (normalden 3-7 D daha düşük)
Kornea merkezi: Saydam
Hipermetropi: Hafif ila orta (ortalama +6.33 D)

Kornea plana, kornea periferinin skleralize olmasıyla korneanın düzleştiği konjenital bir hastalıktır. Kornea-sklera sınırı belirsizleşir ve saydam kornea çapı küçülür. Genellikle iki taraflıdır ve her iki cinsiyette de görülür.
Embriyonik dönemde limbustaki primordiyal anormallikten kaynaklandığı düşünülmektedir. Otozomal dominant CNA1 ve otozomal resesif CNA2 olmak üzere iki tipe ayrılır.
Oldukça nadir bir hastalıktır. CNA2, kurucu etki nedeniyle kuzey Finlandiya ve Suudi Arabistan’da yoğunlaşmıştır. Finlandiya vakaları dünyadaki CNA2 vakalarının yaklaşık %80’ini oluşturur. CNA1 aileleri Danimarka, Almanya, ABD, Hollanda ve Küba’da bildirilmiştir.
CNA1 (Otozomal dominant tip)
Şiddet: Hafif
Sorumlu gen: Tanımlanmamış (12q bölgesinde aday gen)
Kornea kırma gücü: Yaklaşık 38 D (normalden 3-7 D daha düşük)
Kornea merkezi: Saydam
Hipermetropi: Hafif ila orta (ortalama +6.33 D)
CNA2 (Otozomal resesif tip)
Şiddet: Şiddetli
Sorumlu gen: KERA geninde (12q) homozigot mutasyon
Kornea kırma gücü: Yaklaşık 30 D veya daha düşük1)
Kornea merkezi: Sıklıkla bulanıklık eşlik eder
Hipermetropi: Yüksek (+10 D üzeri)
CNA1, otozomal dominant geçişli hafif tiptir. Kornea merkezi saydamdır, kornea kırma gücü yaklaşık 38 D ile normale yakındır ve hipermetropi hafiftir. Buna karşılık CNA2, KERA gen mutasyonuna bağlı otozomal resesif geçişli şiddetli tiptir. Kornea merkezinde bulanıklık eşlik eder, kornea kırma gücü yaklaşık 30 D’ye düşer ve +10 D üzerinde yüksek hipermetropi görülür. CNA2’de açı anomalileri, iris anomalileri gibi diğer oküler komplikasyonlar da sık eşlik eder ve prognoz CNA1’den daha kötüdür.
Hastalar sıklıkla çocukluk döneminde yüksek hipermetropiye bağlı görme azlığı ile başvurur. CNA2’de ambliyopi eşlik edebilir. Kornea bulanıklığına bağlı görme azlığı da bildirilebilir.
Kornea düzleşir ve kornea-sklera sınırı belirsizleşir. Periferik kornea bulanıklaşır, CNA2’de merkezde de bulanıklık görülebilir. Nispeten genç yaşta arcus lipoides (yaş halkası) ortaya çıkar. Ön kamara sığdır ve bildirilen ön kamara derinliği 0.8-2.1 mm arasındadır.
| Bulgular | CNA1 | CNA2 |
|---|---|---|
| Kornea kırma gücü | Yaklaşık 38 D | Yaklaşık 30 D veya altı |
| Kornea merkezi | Saydam | Bulanıklık var |
| Hipermetropi derecesi | Yaklaşık +6.33 D | +10 D üzeri |
CNA2’de kornea merkezinde 4-6 mm çapında yuvarlak, opak bir kalınlaşma görülebilir. Bu kalınlaşma Descemet membranına yapışıktır ve çevresinde kornea en ince halini alır. İris anomalileri (iris atrofisi, iris nodülleri, pupil anomalileri) eşlik edebilir.
Bir vakada K değerleri 21.8/27.0 D ve 19.4/28.7 D ile oldukça düzdü, ön kamara derinliği 1.15 mm ve 0.97 mm, merkezi kornea kalınlığı ise 410 μm ve 315 μm ile inceydi1).
CNA2, kromozom 12 üzerindeki KERA geninin homozigot mutasyonu sonucu oluşur. KERA geni, keratokanı kodlar. Keratokan, korneaya özgü bir proteoglikandır ve kollajen fibrillerinin aralığı ile çapının düzenlenmesinde rol oynar.
Hem missense hem de nonsense mutasyonlar rapor edilmiştir. Özellikle Suudi Arabistan popülasyonunda 7 farklı KERA mutasyonu tanımlanmıştır. Şimdiye kadar 15 KERA mutasyonu rapor edilmiş olup bunlardan 7’si missense mutasyondur1).
CNA1’in sorumlu geni henüz tanımlanmamıştır. Kromozom 12 üzerindeki iki aday genin analizi devam etmektedir, ancak DCN, DSPG3, LUM, PITX2 ve FOXC1 gibi bilinen genler neden olarak dışlanmıştır.
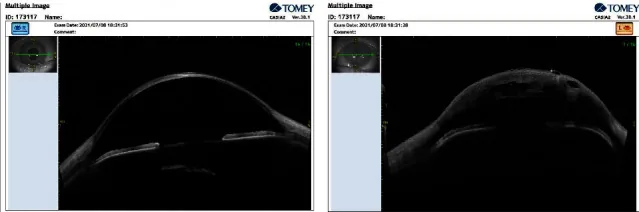
Kornea periferinde skleralizasyon ve kornea düzleşmesi doğrulanır. Yarık lambanın gözlem sistemini yana doğru genişçe çevirdiğinizde kornea düzleşmesi net bir şekilde görülür. CNA2’de santral kornea bulanıklığı da değerlendirilir.
Kornea kırma gücünün ölçümü, CNA1 ve CNA2’nin ayırt edilmesinde faydalıdır. CNA2’de yaklaşık 30 D, CNA1’de ise yaklaşık 38 D’ye kadar düzleşme olur. Eski keratometreler 30 D’nin altını ölçemeyebilir, bu nedenle zayıf bir artı lens takılarak ölçüm aralığı genişletilir.
Kornea, açı ve iris arasındaki ilişkiyi net bir şekilde gösterir ve faydalıdır. Ayrıca santral kornea opasitesinin derinliğini ve yaygınlığını değerlendirmek için kullanılır.
| Hastalık | Ayırıcı noktalar |
|---|---|
| Skleralize kornea | Sadece kornea opasitesi ve düzleşmesi |
| EDS tip VI | Sistemik bulgular eşlik eder |
| Rieger anomalisi | Ön segment disgenezisi |
Ayrıca posterior polimorföz kornea distrofisi (PPCD), mukopolisakkaridoz ve mikrokerneadan ayırt edilmesi gerekir. Sistemik anomaliler olmaksızın izole kornea düzleşmesi büyük olasılıkla düz korneadır.
Düz kornea tanısı, yarık lamba muayenesi ile kornea düzleşmesi ve periferik skleralizasyonun doğrulanmasına ve keratometri ile kornea kırma gücünde azalmanın ölçülmesine dayanır. CNA2’de kornea kırma gücü yaklaşık 30 D’ye düşer. Ön segment OCT, kornea ve açının ayrıntılı değerlendirilmesinde faydalıdır. Kesin tanı için KERA geninin genetik testi kullanılır. Ayırıcı tanıda skleralize kornea, Ehlers-Danlos sendromu tip VI ve Rieger anomalisi dışlanmalıdır.
Bulanıklık çevreyle sınırlıysa, hipermetropinin düzeltilmesi temel tedavidir. Gözlük reçetesinde, subjektif refraksiyon muayenesine dayanarak objektif ölçümlerden 3-4 D daha zayıf lenslerin reçete edilmesi önerilir.
Bulanıklık merkeze uzanıyorsa kornea nakli düşünülür. Ancak tam kat kornea naklinin sonuçları kötüdür ve açı anomalisine bağlı glokom riskine dikkat edilmelidir.
Düz korneada, sığ ön kamara ve anormal K değerleri nedeniyle katarakt cerrahisi zordur. Göz içi lens gücü hesaplamasında normal optik ölçüm cihazları kullanılamayabilir ve SRK regresyon formülü kullanılabilir1). Bir vakada 34 D torik göz içi lens kullanılmış ve ameliyat sonrası düzeltilmiş görme keskinliği 6/12 elde edilmiştir1). Cerrahi sırasında viskoelastik maddenin yeterli kullanımı ve yüksek perfüzyon basıncı ile ön kamaranın korunması önemlidir1).
Sığ ön kamara nedeniyle açı kapanması glokomu riski yüksektir. Açık açılı glokom vakaları da bildirilmiştir. Düzenli göz içi basıncı ölçümü ve açı muayenesi ile izlem zorunludur.
Mümkündür ancak teknik olarak zordur. Sığ ön kamara ve anormal derecede düz kornea nedeniyle, göz içi lens gücü hesaplaması normal ölçüm cihazlarıyla yapılamayabilir. SRK regresyon formülü gibi alternatif hesaplama yöntemleri kullanılır. Cerrahi sırasında ön kamarayı korumak ve kornea endotelini korumak için viskoelastik maddenin yeterli kullanımı önemlidir. Torik göz içi lens kullanımı yüksek astigmatizmanın düzeltilmesine de olanak tanır. Son raporlar iyi refraktif sonuçlar göstermektedir.
KERA geni tarafından kodlanan keratokan, Küçük Lösin Zengini Proteoglikan (SLRP) ailesine aittir. Keratokan, lösin açısından zengin 10 tekrar (LRR) motifine sahiptir ve kornea stromasındaki kollajen fibrillerinin aralığını (42-44 nm) ve çapını kontrol eder1). Bu homojen fibril düzeni, korneanın şeffaflığı, kırma gücü ve mukavemetinin korunması için gereklidir.
KERA mutasyonu, keratokan yapısını destabilize eder ve kollajen fibrillerine bağlanmasını bozar. Yeni bir mutasyon (c.659T>C, p.Leu220Ser) protein modellemesi ile LRR motifi içindeki hidrofobik çekirdeğin bozulduğunu ve asparajin merdiveninin stabil yapısının hasar gördüğünü göstermiştir1).
PACD, 12q21.33’te yer alan KERA, LUM, DCN ve EPYC olmak üzere dört SLRP geninin heterozigot delesyonu sonucu oluşan otozomal dominant bir hastalıktır2). Düz kornea gibi, K değerinde düşüş (41 D altı) ve kornea incelmesi ile kendini gösterir2). Her iki hastalığın ortak noktası, KERA gen anormalliğine bağlı kornea yapısındaki değişikliktir, ancak genetik mekanizma farklıdır: PACD çoklu gen delesyonu iken, düz kornea CNA2, KERA genindeki tek gen nokta mutasyonudur.
Genetik testlerdeki ilerlemeler, yeni KERA mutasyonlarının tanımlanmasını hızlandırmıştır. Şimdiye kadar 15 KERA mutasyonu rapor edilmiş ve genetik danışmanlığın doğruluğunun artmasına katkıda bulunmuştur1). Protein modellemesi kullanılarak önemi bilinmeyen varyantların (VUS) patojenite tahmini, genetik tanıda yeni bir yaklaşım olarak dikkat çekmektedir1).
Katarakt cerrahisinde, trick göz içi lensleri ve biyometri yöntemleri ile iyi refraktif sonuçlar elde edilmiştir1). Gelecekte, hücre tedavisi ve gen tedavisi klinik çalışmalarına katılım da söz konusu olabilir1).