CNA1 (النوع السائد)
الشدة: خفيفة
الجين المسبب: غير محدد (جين مرشح في المنطقة 12q)
قوة انكسار القرنية: حوالي 38 D (أقل من الطبيعي بمقدار 3-7 D)
مركز القرنية: شفاف
طول النظر: خفيف إلى متوسط (متوسط +6.33 D)

القرنية المسطحة (cornea plana) هي مرض خلقي تصبح فيه القرنية مسطحة بسبب تصلب الجزء المحيطي منها. تصبح الحدود بين القرنية والصلبة غير واضحة، ويقل قطر القرنية الشفاف. غالبًا ما تكون ثنائية الجانب وتصيب الذكور والإناث.
يُعتقد أنها تنشأ بسبب خلل في أساسيات الحوف أثناء مرحلة التطور. تُصنف إلى نوعين: CNA1 السائد وCNA2 المتنحي.
مرض نادر جدًا. يتركز CNA2 في شمال فنلندا والمملكة العربية السعودية بسبب تأثير المؤسس. تمثل الحالات الفنلندية حوالي 80% من حالات CNA2 في العالم. تم الإبلاغ عن عائلات مصابة بـ CNA1 في الدنمارك وألمانيا والولايات المتحدة وهولندا وكوبا.
CNA1 (النوع السائد)
الشدة: خفيفة
الجين المسبب: غير محدد (جين مرشح في المنطقة 12q)
قوة انكسار القرنية: حوالي 38 D (أقل من الطبيعي بمقدار 3-7 D)
مركز القرنية: شفاف
طول النظر: خفيف إلى متوسط (متوسط +6.33 D)
CNA2 (النوع المتنحي الجسدي)
شدة المرض: شديد
الجين المسبب: طفرة متماثلة في جين KERA (12q)
قوة انكسار القرنية: حوالي 30 D أو أقل1)
مركز القرنية: غالبًا ما يكون مصحوبًا بعتامة
طول النظر: شديد (أكثر من +10 D)
CNA1 هو نوع وراثي سائد جسدي خفيف. مركز القرنية شفاف، وقوة انكسار القرنية حوالي 38 D قريبة من الطبيعي، وطول النظر خفيف. بينما CNA2 هو نوع وراثي متنحي جسدي ناتج عن طفرة في جين KERA، وهو شديد. يصاحبه عتامة في مركز القرنية، وتنخفض قوة انكسار القرنية إلى حوالي 30 D، ويحدث طول نظر شديد يتجاوز +10 D. غالبًا ما يصاحب CNA2 مضاعفات عينية أخرى مثل شذوذ الزاوية والقزحية، ويكون التشخيص أسوأ من CNA1.
غالبًا ما يتم التشخيص في مرحلة الطفولة بسبب ضعف البصر الناتج عن طول النظر الشديد. قد يصاحب CNA2 الحول. قد يشكو المريض أيضًا من انخفاض الرؤية بسبب عتامة القرنية.
تصبح القرنية مسطحة وتكون الحدود بين القرنية والصلبة غير واضحة. تظهر عتامة في محيط القرنية، وفي CNA2 قد تظهر عتامة أيضًا في المركز. يظهر قوس الشيخوخة (arcus lipoides) في سن مبكرة نسبيًا. تُلاحظ غرفة أمامية ضحلة، ويتراوح عمق الغرفة الأمامية المُبلغ عنه بين 0.8 و 2.1 مم.
| العلامة | CNA1 | CNA2 |
|---|---|---|
| قوة انكسار القرنية | حوالي 38 D | حوالي 30 D أو أقل |
| مركز القرنية | شفاف | يوجد عتامة |
| درجة طول النظر | حوالي +6.33 D | أكثر من +10 D |
في CNA2، قد يُلاحظ وجود سُمك دائري غير شفاف بقطر 4-6 مم في مركز القرنية. يلتصق هذا السُمك بغشاء ديسيميه، وتكون القرنية في أقصى درجات الرقة حوله. قد يصاحبه تشوهات في القزحية (ضمور القزحية، عقيدات القزحية، تشوهات الحدقة).
في إحدى الحالات، كانت قيم K مسطحة جدًا عند 21.8/27.0 D و 19.4/28.7 D، وكان عمق الغرفة الأمامية 1.15 مم و 0.97 مم، وسُمك القرنية المركزي 410 ميكرومتر و 315 ميكرومتر (رفيعة)1).
يحدث CNA2 بسبب طفرة متماثلة اللواقح في جين KERA على الكروموسوم 12. يرمز جين KERA للبروتيوغليكان كيراتوكان، وهو بروتيوغليكان خاص بالقرنية يشارك في تنظيم تباعد وقطر ألياف الكولاجين.
تم الإبلاغ عن كل من الطفرات المغيرة للمعنى والطفرات غير المنطقية. في المجموعات السكانية السعودية على وجه الخصوص، تم تحديد 7 طفرات مختلفة في جين KERA. حتى الآن، تم الإبلاغ عن 15 طفرة في جين KERA، 7 منها طفرات مغيرة للمعنى1).
لم يتم تحديد الجين المسبب لـ CNA1 بعد. يجري تحليل جينين مرشحين على الكروموسوم 12، ولكن تم استبعاد الجينات المعروفة مثل DCN وDSPG3 وLUM وPITX2 وFOXC1 كأسباب.
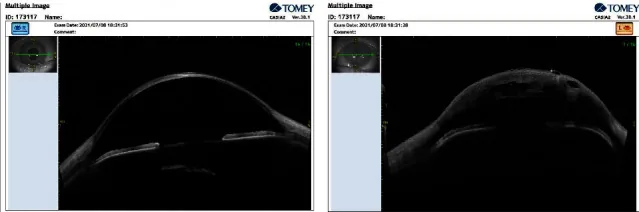
تأكيد تصلب محيط القرنية وتسطيح القرنية. عند إمالة نظام المراقبة للمصباح الشقي جانبًا بشكل كبير، يصبح تسطيح القرنية واضحًا. في CNA2، يتم أيضًا تقييم عتامة القرنية المركزية.
قياس قوة انكسار القرنية مفيد في التمييز بين CNA1 وCNA2. في CNA2، يصبح التسطيح حوالي 30 D، وفي CNA1 حوالي 38 D. نظرًا لأن أجهزة قياس القرنية القديمة لا تستطيع قياس أقل من 30 D، فهناك تقنية لتركيب عدسة زائدة ضعيفة لتوسيع نطاق القياس.
يوضح العلاقة بين القرنية والزاوية والقزحية بشكل مفيد. ويستخدم أيضًا لتقييم عمق ومدى عتامة القرنية المركزية.
| المرض | نقاط التمييز |
|---|---|
| تصلب القرنية | عتامة القرنية وتسطيحها فقط |
| متلازمة إهلرز-دانلوس من النوع السادس | مصحوب بأعراض جهازية |
| شذوذ ريجر | خلل تنسج الجزء الأمامي |
بالإضافة إلى ذلك، يجب التفريق بين حثل القرنية متعدد الأشكال الخلفي (PPCD)، وداء عديد السكاريد المخاطي، وصغر القرنية. إن تسطيح القرنية المعزول دون تشوهات جهازية يشير غالبًا إلى القرنية المسطحة.
يعتمد تشخيص القرنية المسطحة على تأكيد تسطيح القرنية وتصلب الأطراف المحيطية باستخدام المصباح الشقي، وقياس انخفاض قوة انكسار القرنية باستخدام قياس القرنية. في CNA2، تنخفض قوة انكسار القرنية إلى حوالي 30 ديوبتر. يُعد التصوير المقطعي للجزء الأمامي مفيدًا للتقييم التفصيلي للقرنية والزاوية. يستخدم الاختبار الجيني لجين KERA للتشخيص النهائي. يجب استبعاد التشخيصات التفريقية مثل تصلب القرنية، ومتلازمة إهلرز-دانلوس من النوع السادس، وشذوذ ريجر.
إذا كان العتامة محدودة في المحيط، فإن أساس العلاج هو تصحيح طول النظر. يُوصى عند وصف النظارات بإجراء فحص انكسار ذاتي ووصف عدسات أضعف بمقدار 3-4 ديوبتر من القياسات الموضوعية.
إذا كانت العتامة تمتد إلى المركز، فيجب النظر في زرع القرنية. ومع ذلك، فإن نتائج زرع القرنية كامل السماء ضعيفة، ويجب الانتباه إلى خطر الجلوكوما المرتبط بشذوذ الزاوية.
في القرنية المسطحة، تكون جراحة الساد صعبة بسبب ضيق الغرفة الأمامية وقيم K غير الطبيعية. في حساب قوة العدسة داخل العين، قد لا يمكن استخدام أجهزة القياس البصرية العادية، وقد تُستخدم معادلة SRK الانحدارية 1). في إحدى الحالات، استُخدمت عدسة داخل العين تريك بقوة 34 D، وتم الحصول على حدة بصرية مصححة 6/12 بعد الجراحة 1). أثناء الجراحة، من المهم استخدام كمية كافية من المواد اللزجة المرنة والحفاظ على الغرفة الأمامية بضغط تروية مرتفع 1).
بسبب ضيق الغرفة الأمامية، يكون خطر الجلوكوما مغلقة الزاوية مرتفعًا. هناك أيضًا تقارير عن الجلوكوما مفتوحة الزاوية. المراقبة المنتظمة لضغط العين وفحص الزاوية أمر ضروري.
نعم ممكن، لكنه صعب تقنيًا. بسبب ضيق الغرفة الأمامية والقرنية المسطحة بشكل غير طبيعي، قد لا يمكن حساب قوة العدسة داخل العين باستخدام أجهزة القياس العادية. تُستخدم طرق حساب بديلة مثل معادلة SRK الانحدارية. أثناء الجراحة، من المهم استخدام كمية كافية من المواد اللزجة المرنة للحفاظ على الغرفة الأمامية وحماية بطانة القرنية. يمكن استخدام عدسة داخل العين تريك لتصحيح اللابؤرية العالية. أظهرت التقارير الحديثة نتائج انكسارية جيدة.
ينتمي الكيراتوكان، الذي يرمز له جين KERA، إلى عائلة البروتيوغليكان الصغيرة الغنية بالليوسين (SLRP). يحتوي الكيراتوكان على 10 تكرارات غنية بالليوسين (LRR) ويتحكم في التباعد (42-44 نانومتر) وقطر ألياف الكولاجين في سدى القرنية 1). هذا الترتيب المنتظم للألياف ضروري للحفاظ على شفافية القرنية وقوتها الانكسارية وقوتها.
تؤدي طفرة KERA إلى زعزعة استقرار بنية الكيراتوكان، مما يضعف ارتباطه بألياف الكولاجين. أظهرت إحدى الطفرات الجديدة (c.659T>C, p.Leu220Ser) من خلال النمذجة البروتينية أنها تدمر النواة الكارهة للماء داخل نمط LRR وتخل بالبنية المستقرة لسلم الأسباراجين1).
PACD هو مرض جسمي سائد ينتج عن حذف متغاير الزيجوت لأربعة جينات SLRP: KERA وLUM وDCN وEPYC، الواقعة على 12q21.332). كما هو الحال في القرنية المسطحة، يظهر بانخفاض قيمة K (أقل من 41 D) وترقق القرنية2). القاسم المشترك بين المرضين هو تغير بنية القرنية بسبب خلل في جين KERA، لكن الفرق في الآلية الجينية هو أن PACD ينتج عن حذف جينات متعددة، بينما القرنية المسطحة CNA2 تنتج عن طفرة نقطية في جين KERA وحده.
أدى التقدم في الفحوصات الجينية إلى تسريع تحديد طفرات KERA الجديدة. تم الإبلاغ عن 15 طفرة في KERA حتى الآن، مما يساهم في تحسين دقة الاستشارة الوراثية1). يُعتبر التنبؤ بالإمراضية للمتغيرات غير المؤكدة الأهمية (VUS) باستخدام النمذجة البروتينية نهجًا جديدًا في التشخيص الجيني1).
في جراحة الساد، أدى استخدام العدسات داخل العين الذكية والتحسينات في القياسات الحيوية إلى تحقيق نتائج انكسارية جيدة1). في المستقبل، قد يكون من الممكن المشاركة في التجارب السريرية للعلاج الخلوي والعلاج الجيني1).