眼前节和外眼

全身性毛细血管渗漏综合征的眼科特征
一目了然的要点
Section titled “一目了然的要点”1. 全身性毛细血管渗漏综合征的眼科特征
Section titled “1. 全身性毛细血管渗漏综合征的眼科特征”全身性毛细血管渗漏综合征(Systemic Capillary Leak Syndrome; SCLS)是一种罕见的疾病,其特征是毛细血管向组织一过性且重度地渗漏水分和大分子物质。1960年Clarkson首次报道,因此也称为Clarkson病。自1960年以来,全球报告病例不足500例2),诊断时患者中位年龄为48岁,多见于老年男性。
特发性SCLS中高达80%合并MGUS(意义未明的单克隆丙种球蛋白病,主要为IgG型),但进展为骨髓瘤的风险并未增加。
由于水分渗漏可发生于任何组织,眼部并发症也多种多样。主要眼部表现包括结膜水肿、脉络膜渗出和眼压升高。也有合并急性闭角型青光眼和非动脉炎性前部缺血性视神经病变(NAION)的严重病例报道1)。
自1960年以来,全球报告病例不足500例,是一种极为罕见的疾病2)。诊断时中位年龄为48岁,多见于老年男性。由于其罕见性,诊断容易延迟,需注意。
2. 主要症状和临床发现
Section titled “2. 主要症状和临床发现”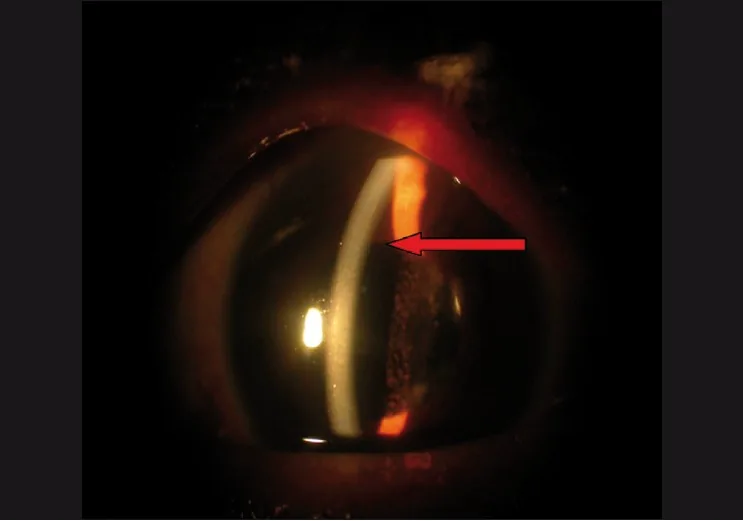
全身症状(常先于眼部症状出现)
Section titled “全身症状(常先于眼部症状出现)”- 前驱症状:非特异性轻度症状(类似呼吸道感染)在渗漏期前1-4天出现2)。
- 气短、乏力:因肺水肿和胸腔积液导致的呼吸困难及全身虚弱。
- 全身性水肿:以四肢为主的快速水肿。
- 流泪、畏光、异物感、瘙痒:由结膜水肿引起。视力通常保持正常。
- 视力下降、眼痛:在伴有脉络膜渗出和急性闭角型青光眼的病例中有报道。
- 上方视野缺损:在合并非动脉炎性前部缺血性视神经病变的病例中,SCLS恢复期可出现双侧对称性上方弓形视野缺损1)。
临床所见(医生检查时确认的发现)
Section titled “临床所见(医生检查时确认的发现)”后段和视神经
脉络膜渗出:由于血清白蛋白急剧下降导致胶体渗透压降低引起。常为双侧性。
睫状体渗出:从后段到睫状体的广泛渗出。
视盘苍白(非动脉炎性前部缺血性视神经病变):双侧下方视盘苍白1)。
RNFL变薄(非动脉炎性前部缺血性视神经病变):OCT显示双眼下方RNFL变薄1)。
在合并非动脉炎性前部缺血性视神经病变的病例中,可能会留下永久性视野缺损。报告病例显示,虽然出现双侧对称性上方弓形视野缺损,但双眼中心视力仍保持在6/7.5(约0.8)1)。另一方面,由结膜水肿、脉络膜渗出和闭角引起的视力下降通常随着全身状况的改善而恢复。
3. 原因与风险因素
Section titled “3. 原因与风险因素”SCLS的原因大部分是特发性(原因不明)。除特发性外,还报告了以下诱因。
- 药物诱发:吉西他滨、克拉屈滨等抗癌药,单克隆抗体,治疗用生长因子。地尼白介素-白喉毒素(CTCL治疗药)的临床试验中,36%的患者出现SCLS9)。
- 病毒感染:甲型和乙型流感、带状疱疹、登革热。在合并非动脉炎性前部缺血性视神经病变的病例报告中,确认了乙型流感1)。
- COVID-19相关:除COVID-19感染本身外,阿斯利康、强生-杨森、辉瑞-BioNTech疫苗也有发病报告7)8)。欧洲药品管理局(EMA)建议有SCLS病史者禁用阿斯利康疫苗7)。
- 减压病:已有报道潜水后减压病继发的SCLS6)。
- 恶性肿瘤:弥漫性大B细胞淋巴瘤(DLBCL)等引起的副肿瘤综合征性SCLS3)。
- 遗传背景:家族性SCLS中已发现TLN1基因的剪接位点突变(c.7188+2T>C)。呈常染色体显性遗传,不完全外显4)。
易合并非动脉炎性前部缺血性视神经病变的危险因素包括SCLS引起的低血压、血液浓缩、高凝状态,以及糖尿病、高血压、动脉硬化、小视盘拥挤1)。
已有腺病毒载体型和mRNA疫苗两种接种后发病的报道7)8)。因果关系尚未确定,但EMA建议有SCLS病史者禁用阿斯利康疫苗。有SCLS病史者应在接种前咨询主治医生。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”SCLS是一种排除性诊断,基于全身性水肿、难治性低血压等毛细血管渗漏征象的存在,并排除其他疾病。
全身检查所见
Section titled “全身检查所见”急性期可见以下特征性实验室检查异常。
- 低白蛋白血症(无蛋白尿):平均约1.7 g/dL2)。重症病例有报告白蛋白16 g/L5)、18 g/L8)。
- 血液浓缩:血细胞比容升高(平均约60%)。重症病例Ht可达69%5)、72.3%8)。
- MGUS:血清蛋白电泳(SPEP)检出率高达80%。以IgG-κ2)5)和IgG-λ1)多见。
- 血栓栓塞风险:血液浓缩导致高凝状态。有合并深静脉血栓、下腔静脉血栓8)、肺栓塞2)的病例。
- 急性肾损伤(AKI):部分病例发生9)。
99mTc-HSA闪烁显像可通过24小时后四肢皮下HSA积聚直接证明血管通透性增高9)。
- 裂隙灯显微镜检查:评估结膜水肿程度、浅前房及房角关闭的有无。
- B型超声:确认脉络膜渗出的有无及程度。
- Humphrey视野检查:检测上方弓形视野缺损(非动脉炎性前部缺血性视神经病变合并病例)1)。
- 光学相干断层扫描(OCT):定量评估下方视网膜神经纤维层变薄(合并非动脉炎性前部缺血性视神经病变的病例)1)。
- 头部和眼眶MRI:用于排除局部梗死或占位性病变1)。
主要鉴别疾病如下。
- 败血症、过敏反应、血管性水肿:最重要的鉴别。
- 肾病综合征:SCLS无重度蛋白尿,可与之鉴别。
- 卵巢过度刺激综合征(OHSS):女性患者需进行鉴别诊断。
- 噬血细胞性淋巴组织细胞增多症(HLH):还需考虑病毒性出血热和蛇毒。
- 遗传性血管性水肿:若C1酯酶抑制剂正常则可排除6)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”全身治疗(内科治疗)
Section titled “全身治疗(内科治疗)”急性期支持治疗
Section titled “急性期支持治疗”- 液体管理:晶体液为首选。过量输液会增加肺水肿和筋膜室综合征的风险。仅在收缩压低于70 mmHg时考虑使用高分子胶体液作为“允许性低血压”策略的一部分6)。
- 升压药:使用去甲肾上腺素等。
- 全身性类固醇/IVIG(急性期):IVIG以1–2 g/kg/天给药2–3天。
- 血栓栓塞预防:针对血液浓缩导致的高凝状态进行预防性治疗。
发作预防(维持治疗)
Section titled “发作预防(维持治疗)”发作预防的主要选择如下所示。
- IVIG(静脉注射免疫球蛋白):定期给药,最大剂量2 g/kg/月。合并MGUS的SCLS患者中,IVIG组的5年生存率为91%,10年生存率为77%,而非IVIG组分别为47%和37%,差异显著。IVIG治疗下年发作频率中位数为0(范围0–3.3)8)。
- β2受体激动剂(特布他林)+ 茶碱:通过升高cAMP抑制内皮通透性。特布他林5 mg每日3次,茶碱400–1600 mg/日6)。但治疗下年发作频率中位数为2.25(范围0–20),效果不如IVIG8)。
- 甲泼尼龙冲击 + IVIG联合治疗:已报道使用mPSL 1000 mg/日×3天 + IVIG 1 g/kg的方案8)。
每月静脉注射IVIG(静脉注射免疫球蛋白)被认为最有效。IVIG组的5年生存率为91%,而非IVIG组为47%,差异显著。IVIG组的年发作频率中位数为0,显示出优异的抑制效果8)。
- 脉络膜/睫状体渗出:使用全身和局部(滴眼液、眼周)类固醇,部分报告有效。一些病例系列显示反应不佳。
- 眼压管理:使用局部降眼压药物。
- 结膜水肿/暴露性角膜病变:使用人工泪液润滑。严重病例可考虑临时睑板缝合术,但有压迫眼眶导致眼眶间隔综合征的风险。
- 房角关闭:可考虑激光虹膜周切术(LPI)或白内障手术,但需注意即使人工晶体眼,睫状体渗出也可能导致房角持续关闭。
- 脉络膜渗出的手术/激光:通常耐药。SCLS尚无确立的外科治疗方法。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”SCLS的最终共同通路是血管内皮功能障碍。内皮细胞间的间隙增大,导致大分子渗漏和水分外渗。
细胞因子与分子机制
Section titled “细胞因子与分子机制”发作期间观察到以下变化:
- 单核细胞IL-2受体表达增加,CXCL10、CCL2、IL-1β、IL-8、IL-12产生增加
- CD8+/CD25+ T细胞浓度增加,TNF-α表达增加
- VEGF-D增加5)
- 发作期间VEGF和血管生成素-2升高5)
在体外模型中,血管生成素-2抑制剂和IVIG显著降低了内皮通透性,而贝伐珠单抗(VEGF抑制剂)的效果微乎其微5)。
TLN1基因突变与内皮屏障破坏
Section titled “TLN1基因突变与内皮屏障破坏”Elefant等人(JCI Insight, 2024)在3例家族性SCLS患者中发现了TLN1基因的杂合剪接突变(c.7188+2T>C)4)。该突变导致外显子54框内跳跃,使talin1 R13结构域不稳定。C端肌动蛋白结合位点(ABS3)功能障碍导致VE-钙黏蛋白的连接定位显著减少,黏附连接(AJ)和紧密连接(TJ)碎片化,内皮屏障通透性增加。在凝血酶刺激下,SCLS突变内皮细胞对FITC-葡聚糖的通透性约为对照组的4倍。
IL-2受体介导的机制
Section titled “IL-2受体介导的机制”地尼白介素-白喉毒素融合蛋白与表达IL-2受体的细胞结合,通过内化白喉毒素片段抑制蛋白质合成。SCLS被认为是由血管通透性增加(IL-2R作用)和蛋白质合成抑制(白喉毒素作用)共同引起的9)。
眼部症状的发生机制
Section titled “眼部症状的发生机制”- 脉络膜渗出:由血清白蛋白急剧下降导致的胶体渗透压降低引起。
- 睫状体渗出和房角关闭:睫状体渗出 → 睫状体前旋 → 浅前房和房角关闭。由于不是瞳孔阻滞机制,即使在人工晶状体眼中也可能发生。
- 眼压升高:除房角关闭外,巩膜上静脉压升高也起作用。
- 非动脉炎性前部缺血性视神经病变:低血压加高凝状态 → 后睫状动脉导致的视盘区域性梗死。由于后睫状动脉形成终末动脉和分水岭区,休克时容易发生视盘梗死 1)。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”靶向TLN1的基因治疗策略
Section titled “靶向TLN1的基因治疗策略”Elefant等人(2024)表明,在表达SCLS突变talin1的内皮细胞中,通过剪接转换反义寡核苷酸恢复正常剪接可作为治疗策略提出4)。如果VE-钙黏蛋白的连接部定位和黏附连接完整性得以恢复,则可能有助于修复内皮屏障功能。
靶向VEGF-D和血管生成素2的治疗
Section titled “靶向VEGF-D和血管生成素2的治疗”SCLS患者中记录到VEGF-D水平升高,VEGFR3介导的通路被认为是未来的治疗靶点候选。抗VEGF治疗(静脉注射贝伐珠单抗)曾在一例病例中尝试,但未获得临床反应。另一方面,血管生成素2抑制剂在体外模型中与IVIG一起显著降低了内皮通透性,但临床报告有限5)。
COVID-19疫苗相关SCLS的因果关系研究
Section titled “COVID-19疫苗相关SCLS的因果关系研究”mRNA疫苗和腺病毒载体疫苗均有发病报道7)8),但因果关系尚未确定,需要进一步研究。
8. 参考文献
Section titled “8. 参考文献”- Neo YN, Sobti M, Zambarakji H. Bilateral simultaneous non-arteritic ischaemic optic neuropathy: a rare complication of idiopathic systemic capillary leak syndrome (SCLS). BMJ Case Rep. 2021;14:e242847.
- Correia R, Santos D, Delgado M. Idiopathic Systemic Capillary Leak Syndrome: A Clinical Case. Cureus. 2023;15(12):e50301.
- Silva B, Gaspar V, Alves C, et al. Systemic Capillary Leak Syndrome as a Paraneoplastic Syndrome. Cureus. 2024;16(5):e60923.
- Elefant N, Rouni G, Arapatzi C, et al. Talin1 dysfunction is genetically linked to systemic capillary leak syndrome. JCI Insight. 2024;9(24):e173664.
- Bouchlarhem A, Lamzouri O, El aidouni G, et al. Consider systemic capillary leak syndrome in monoclonal gammopathy with shock. Ann Med Surg. 2021;72:103013.
- Mathavan A, Mathavan A, Jones K, et al. Systemic capillary leak syndrome secondary to decompression sickness. BMJ Case Rep. 2023;16:e253045.
- Yang C, Tsang MYC, Zypchen LN, et al. Pericardial effusion and systemic capillary leak syndrome late post-SARS-CoV-2 vaccination. BMJ Case Rep. 2023;16:e256527.
- Inoue M, Yasue Y, Kobayashi Y, et al. Systemic capillary leak syndrome (SCLS) after receiving BNT162b2 mRNA COVID-19 (Pfizer-BioNTech) vaccine. BMJ Case Rep. 2022;15:e248927.
- Horino T, Okada D, Inotani S, et al. Denileukin diftitox-induced systemic capillary leak syndrome with acute kidney injury. CEN Case Reports. 2023;12:63-67.
