전안부 및 외안부

전신성 모세혈관 누출 증후군의 안과적 특징
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 전신성 모세혈관 누출 증후군의 안과적 특징
섹션 제목: “1. 전신성 모세혈관 누출 증후군의 안과적 특징”전신성 모세혈관 누출 증후군(Systemic Capillary Leak Syndrome; SCLS)은 모세혈관에서 조직으로 일시적이고 심각한 수분 및 거대분자 누출을 특징으로 하는 희귀 질환입니다. 1960년 Clarkson이 처음 보고하여 ‘클락슨병’이라고도 불립니다. 1960년 이후 보고된 사례는 500건 미만이며2), 진단 시 환자의 중앙 연령은 48세이고 고령 남성에서 흔합니다.
특발성 SCLS의 최대 80%에서 MGUS(의의 불명의 단클론 감마글로불린병증, 주로 IgG형)가 동반되지만, 골수종으로의 진행 위험은 증가하지 않는 것으로 알려져 있습니다.
수분 누출은 모든 조직에서 발생할 수 있으므로 안과적 합병증도 다양합니다. 주요 안 소견으로 결막 부종, 맥락막 삼출, 안압 상승이 있습니다. 급성 폐쇄각이나 비동맥염성 허혈성 시신경병증(NAION)이 동반된 중증 사례도 보고되었습니다1).
1960년 이후 전 세계 보고 사례가 500건 미만으로 매우 희귀한 질환입니다2). 진단 시 중앙 연령은 48세이며 고령 남성에서 많습니다. 희귀성으로 인해 진단이 지연되기 쉬우므로 주의가 필요합니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”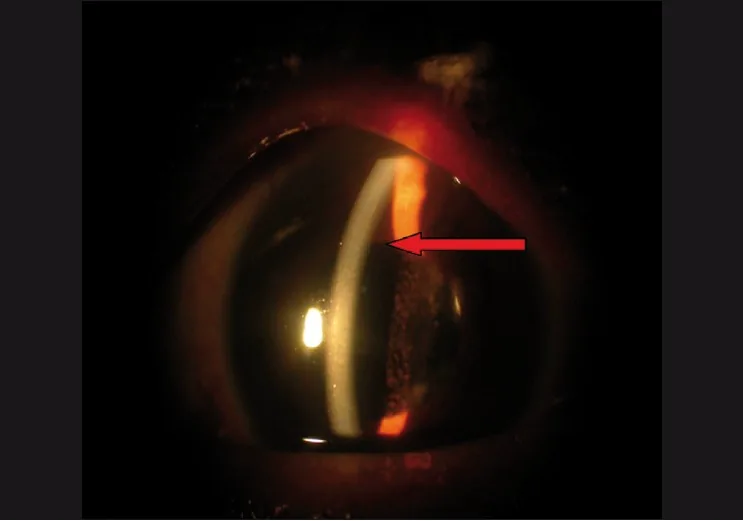
자각 증상
섹션 제목: “자각 증상”전신 증상 (안구 증상에 선행하는 경우가 많음)
섹션 제목: “전신 증상 (안구 증상에 선행하는 경우가 많음)”- 전구 증상: 비특이적 경미한 증상(호흡기 감염 유사)이 누출기 1~4일 전에 나타남2).
- 호흡곤란·권태감: 폐부종·흉수로 인한 호흡곤란과 전신 쇠약.
- 전신성 부종: 말초를 중심으로 한 급격한 부종.
안구 증상
섹션 제목: “안구 증상”- 눈물흘림·눈부심·이물감·가려움증: 결막 부종(케모시스)으로 인함. 시력은 대개 유지됨.
- 시력 저하·안통: 맥락막 삼출 및 급성 폐쇄각을 보인 증례에서 보고됨.
- 상부 시야 결손: 비동맥염성 전방 허혈성 시신경병증이 동반된 경우, SCLS 회복기에 양측 대칭성 상부 아치형 시야 결손이 명확해짐1).
임상 소견 (의사가 진찰 시 확인하는 소견)
섹션 제목: “임상 소견 (의사가 진찰 시 확인하는 소견)”후안부 및 시신경
맥락막 삼출: 혈청 알부민의 급격한 감소로 인한 교질 삼투압 저하가 원인. 종종 양측성.
섬모체 삼출: 후안부에서 섬모체로의 광범위한 삼출.
시신경 유두 창백(비동맥염성 전방 허혈성 시신경병증): 양측 하방 시신경 유두 창백1).
RNFL 얇아짐(비동맥염성 전방 허혈성 시신경병증): OCT에서 하방 RNFL 얇아짐이 양안에서 관찰됨1).
비동맥염성 전방허혈시신경병증이 합병된 증례에서는 영구적인 시야결손이 남을 수 있습니다. 보고된 증례에서는 양측 대칭성 상방궁상시야결손을 보이면서도 중심시력은 양안 모두 6/7.5(약 0.8)로 유지되었습니다1). 한편, 결막부종, 맥락막삼출, 폐쇄각으로 인한 시력저하는 전신상태의 호전과 함께 회복되는 경우가 많습니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”SCLS의 원인은 대부분 특발성(원인 불명)입니다. 특발성 외에 다음과 같은 유발 요인이 보고되었습니다.
- 약물 유발: 젬시타빈, 클로파라빈 등의 항암제, 단일클론항체, 치료용 성장인자. 데닐류킨 디프티톡스(CTCL 치료제)의 임상시험에서 36%에서 SCLS가 발생했습니다9).
- 바이러스 감염: 인플루엔자 A 및 B, 대상포진, 뎅기열. 비동맥염성 전방허혈시신경병증이 합병된 증례 보고에서는 인플루엔자 B가 확인되었습니다1).
- COVID-19 관련: COVID-19 감염 자체 외에도 아스트라제네카, 존슨앤드존슨-얀센, 화이자-바이오엔테크 백신에서 발병이 보고되었습니다7)8). 유럽의약품청(EMA)은 아스트라제네카 백신을 SCLS 병력자에게 금기로 권고하고 있습니다7).
- 감압병: 잠수 후 감압병에 이차적으로 발생한 SCLS가 보고되었습니다6).
- 악성 종양: 미만성 거대 B세포 림프종(DLBCL) 등에 의한 부종양 증후군으로서의 SCLS3).
- 유전적 배경: 가족성 SCLS에서 TLN1 유전자의 스플라이스 부위 돌연변이(c.7188+2T>C)가 확인되었습니다. 상염색체 우성, 불완전 침투의 형태를 보입니다4).
비동맥염성 전방 허혈성 시신경병증이 합병되기 쉬운 위험 인자로는 SCLS로 인한 저혈압, 혈액 농축, 응고 항진 상태에 더해 당뇨병, 고혈압, 동맥경화, 작은 crowded disc가 있습니다1).
아데노바이러스 벡터형과 mRNA 백신 모두에서 발병 사례가 보고되었습니다7)8). 인과관계는 확립되지 않았지만, EMA는 아스트라제네카 백신을 SCLS 병력자에게 금기로 권고하고 있습니다. SCLS 병력자는 백신 접종 전 주치의와 상담이 필요합니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”SCLS는 제외 진단이며, 전신성 부종, 불응성 저혈압 등 모세혈관 누출 징후의 존재와 다른 질환의 배제에 기반하여 진단합니다.
전신 검사 소견
섹션 제목: “전신 검사 소견”급성기에 특징적인 검사치 이상으로 다음이 관찰됩니다.
- 저알부민혈증(단백뇨 동반 없음): 평균 약 1.7 g/dL2). 중증 예에서는 알부민 16 g/L5), 18 g/L8) 보고도 있습니다.
- 혈액 농축: 헤마토크리트 상승(평균 약 60%). 중증 예에서는 Ht 69%5), Ht 72.3%8)에 달할 수 있습니다.
- MGUS: 혈청 단백 전기영동(SPEP)에서 최대 80% 검출됩니다. IgG-κ2)5) 및 IgG-λ1)가 많습니다.
- 혈전색전증 위험: 혈액 농축으로 인한 응고 항진 상태. 심부정맥 혈전·하대정맥 혈전8), 폐색전증2) 합병 예가 있습니다.
- 급성 신손상(AKI): 일부 증례에서 발생9).
99mTc-HSA 신티그라피는 24시간 후 사지 피하 조직 내 HSA 축적을 통해 혈관 투과성 증가를 직접 증명할 수 있습니다9).
안과 검사
섹션 제목: “안과 검사”- 세극등 현미경 검사: 결막 부종 정도, 전방 천공 및 전방각 폐쇄 유무를 평가합니다.
- B-모드 초음파: 맥락막 삼출의 유무와 정도를 확인합니다.
- Humphrey 시야 검사: 상방 아치형 시야 결손(비동맥염성 전방 허혈성 시신경병증 동반 증례) 검출1).
- 광간섭단층촬영(OCT): 하측 망막신경섬유층의 얇아짐(비동맥염성 전방허혈시신경병증 동반 예)의 정량적 평가1).
- 두부 및 안와 MRI: 국소 경색 또는 종괴 병변 배제에 사용1).
감별 진단
섹션 제목: “감별 진단”주요 감별 질환은 다음과 같습니다.
- 패혈증, 아나필락시스, 혈관부종: 가장 중요한 감별 질환.
- 신증후군: SCLS에서는 심한 단백뇨가 나타나지 않아 감별 가능.
- 난소과자극증후군(OHSS): 여성 환자에서 감별 진단이 필요합니다.
- 혈구탐식성림프조직구증(HLH): 바이러스성 출혈열, 뱀독도 고려합니다.
- 유전성 혈관부종: C1 에스테라제 억제제가 정상이면 배제할 수 있습니다6).
5. 표준 치료법
섹션 제목: “5. 표준 치료법”전신 치료(내과적 치료)
섹션 제목: “전신 치료(내과적 치료)”급성기 지지 요법
섹션 제목: “급성기 지지 요법”- 수액 관리: 결정질액이 일차 선택입니다. 과도한 수액 투여는 폐부종 및 구획증후군의 위험을 증가시킵니다. “허용적 저혈압” 전략의 일환으로 수축기 혈압이 70 mmHg 미만인 경우에만 고분자 콜로이드 사용을 고려합니다6).
- 승압제: 노르에피네프린 등을 사용합니다.
- 전신 스테로이드/IVIG(급성기): IVIG를 1–2 g/kg/일로 2–3일간 투여합니다.
- 혈전색전증 예방: 혈액 농축으로 인한 과응고 상태에 대해 예방적으로 시행합니다.
발작 예방(유지 요법)
섹션 제목: “발작 예방(유지 요법)”발작 예방의 주요 선택지는 다음과 같습니다.
- IVIG(정맥 면역글로불린) : 최대 2 g/kg/월 정기 투여. MGUS를 동반한 SCLS 환자에서 IVIG군의 5년 생존율은 91%, 10년 생존율은 77%인 반면, 비IVIG군은 각각 47%와 37%로 유의한 차이가 있습니다. IVIG 치료 하에서 연간 발작 빈도 중앙값은 0(범위 0~3.3)입니다8).
- β2 작용제(테르부탈린) + 테오필린 : cAMP 상승을 통한 내피 투과성 억제를 기대하여 사용됩니다. 테르부탈린 5 mg 1일 3회, 테오필린 400
1600 mg/일6). 그러나 치료 하에서 연간 발작 빈도 중앙값은 2.25(범위 020)로 IVIG보다 열등합니다8). - 메틸프레드니솔론 펄스 + IVIG 병용 : mPSL 1000 mg/일×3일 + IVIG 1 g/kg 투여가 보고되었습니다8).
IVIG(정맥 면역글로불린)의 월간 투여가 가장 효과적인 것으로 간주됩니다. IVIG군의 5년 생존율은 91%인 반면, 비IVIG군은 47%로 큰 차이가 있습니다. 연간 발작 빈도도 IVIG군에서 중앙값 0으로 우수한 억제 효과를 보입니다8).
안과적 치료
섹션 제목: “안과적 치료”- 맥락막/모양체 삼출: 전신 및 국소(점안, 안와주위) 스테로이드가 사용되며 일부 보고에서 효과가 있습니다. 일부 증례 시리즈에서는 반응이 좋지 않습니다.
- 안압 관리: 국소 안압하강제를 사용합니다.
- 결막 부종/노출성 각막병증: 인공눈물로 윤활합니다. 중증의 경우 일시적 안검봉합술이 고려될 수 있으나, 안와를 압박하여 안와구획증후군을 유발할 위험이 있습니다.
- 전방각 폐쇄: 레이저 홍채절개술(LPI) 또는 백내장 수술이 고려될 수 있으나, 인공수정체안에서도 모양체 삼출로 인해 전방각 폐쇄가 지속될 수 있으므로 주의가 필요합니다.
- 맥락막 삼출에 대한 수술/레이저: 일반적으로 저항성을 보입니다. SCLS에 대한 확립된 외과적 치료법은 없습니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”SCLS의 최종 공통 경로는 혈관 내피 기능 장애입니다. 내피 세포 간 간격이 확대되어 거대 분자의 누출과 수분의 혈관 외 유출이 발생합니다.
사이토카인 및 분자 기전
섹션 제목: “사이토카인 및 분자 기전”발작 중에는 다음과 같은 변화가 관찰됩니다.
- 단핵세포의 IL-2 수용체 발현 증가, CXCL10, CCL2, IL-1β, IL-8, IL-12 생성 증가
- CD8+/CD25+ T 세포 농도 증가, TNF-α 발현 증가
- VEGF-D 증가5)
- 발작 중 VEGF 및 안지오포이에틴-2 상승5)
시험관 모델에서 안지오포이에틴-2 억제제와 IVIG는 내피 투과성을 유의하게 감소시킨 반면, 베바시주맙(VEGF 억제제)의 효과는 미미했습니다5).
TLN1 유전자 돌연변이와 내피 장벽 파괴
섹션 제목: “TLN1 유전자 돌연변이와 내피 장벽 파괴”Elefant 등(JCI Insight, 2024)은 가족성 SCLS 환자 3명에서 TLN1 유전자의 이형접합 스플라이스 돌연변이(c.7188+2T>C)를 확인했습니다4). 이 돌연변이는 엑손 54의 인프레임 스킵을 유발하여 talin1 R13 도메인을 불안정하게 만듭니다. C-말단 액틴 결합 부위(ABS3)의 기능 장애로 인해 VE-카드헤린의 접합부 국소화가 현저히 감소하고, 부착 연접(AJ)과 밀착 연접(TJ)이 단편화되어 내피 장벽 투과성이 증가합니다. 트롬빈 자극 시 SCLS 돌연변이 내피는 대조군에 비해 약 4배 더 많은 FITC-덱스트란 투과성을 보였습니다.
IL-2 수용체를 통한 기전
섹션 제목: “IL-2 수용체를 통한 기전”데닐류킨 디프티톡스는 IL-2 수용체를 발현하는 세포에 결합하여 디프테리아 독소 단편의 내재화를 통해 단백질 합성을 억제합니다. SCLS는 혈관 투과성 증가(IL-2R 작용)와 단백질 합성 억제(디프테리아 독소 작용) 모두에 의해 유발되는 것으로 생각됩니다9).
안구 증상의 발생 기전
섹션 제목: “안구 증상의 발생 기전”- 맥락막 삼출: 혈청 알부민의 급격한 감소로 인한 교질 삼투압 저하가 원인입니다.
- 섬모체 삼출 및 폐쇄각: 섬모체 삼출 → 섬모체 전방 회전 → 얕은 전방 및 폐쇄각. 동공 차단 기전이 아니므로 인공수정체안에서도 발생할 수 있습니다.
- 안압 상승: 폐쇄각 외에도 공막상정맥압 상승이 기여합니다.
- 비동맥염성 전방 허혈성 시신경병증: 저혈압 및 혈액 응고 항진 → 후섬모체동맥에 의한 시신경유두의 분절성 경색. 후섬모체동맥은 종말동맥과 분수계 영역을 형성하므로 쇼크 시 시신경유두 경색이 발생하기 쉽습니다 1).
7. 최신 연구 및 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구 및 향후 전망 (연구 단계 보고)”TLN1을 표적으로 한 유전자 치료 전략
섹션 제목: “TLN1을 표적으로 한 유전자 치료 전략”Elefant 등(2024)은 SCLS 돌연변이 talin1을 발현하는 내피 세포에서 스플라이스 전환 안티센스 올리고뉴클레오타이드에 의한 정상 스플라이싱 회복이 치료 전략으로 제안될 수 있음을 보여주었습니다4). VE-카드헤린의 접합부 국소화와 AJ 완전성이 회복되면 내피 장벽 기능 복구로 이어질 수 있습니다.
VEGF-D 및 안지오포이에틴2를 표적으로 한 치료
섹션 제목: “VEGF-D 및 안지오포이에틴2를 표적으로 한 치료”SCLS 환자에서 VEGF-D 농도 상승이 기록되었으며, VEGFR3을 매개한 경로가 향후 치료 표적 후보로 제시되고 있습니다. 항VEGF 요법(베바시주맙 정맥내 투여)은 1예에서 시도되었으나 임상 반응을 얻지 못했습니다. 한편, 안지오포이에틴2 억제제는 시험관 내 모델에서 IVIG와 함께 내피 투과성을 유의하게 감소시켰지만, 임상 보고는 제한적입니다5).
COVID-19 백신 관련 SCLS 인과관계 연구
섹션 제목: “COVID-19 백신 관련 SCLS 인과관계 연구”mRNA 백신과 아데노바이러스 벡터 백신 모두에서 발병이 보고되었지만7)8), 인과관계는 확립되지 않았으며 추가 연구가 필요합니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Neo YN, Sobti M, Zambarakji H. Bilateral simultaneous non-arteritic ischaemic optic neuropathy: a rare complication of idiopathic systemic capillary leak syndrome (SCLS). BMJ Case Rep. 2021;14:e242847.
- Correia R, Santos D, Delgado M. Idiopathic Systemic Capillary Leak Syndrome: A Clinical Case. Cureus. 2023;15(12):e50301.
- Silva B, Gaspar V, Alves C, et al. Systemic Capillary Leak Syndrome as a Paraneoplastic Syndrome. Cureus. 2024;16(5):e60923.
- Elefant N, Rouni G, Arapatzi C, et al. Talin1 dysfunction is genetically linked to systemic capillary leak syndrome. JCI Insight. 2024;9(24):e173664.
- Bouchlarhem A, Lamzouri O, El aidouni G, et al. Consider systemic capillary leak syndrome in monoclonal gammopathy with shock. Ann Med Surg. 2021;72:103013.
- Mathavan A, Mathavan A, Jones K, et al. Systemic capillary leak syndrome secondary to decompression sickness. BMJ Case Rep. 2023;16:e253045.
- Yang C, Tsang MYC, Zypchen LN, et al. Pericardial effusion and systemic capillary leak syndrome late post-SARS-CoV-2 vaccination. BMJ Case Rep. 2023;16:e256527.
- Inoue M, Yasue Y, Kobayashi Y, et al. Systemic capillary leak syndrome (SCLS) after receiving BNT162b2 mRNA COVID-19 (Pfizer-BioNTech) vaccine. BMJ Case Rep. 2022;15:e248927.
- Horino T, Okada D, Inotani S, et al. Denileukin diftitox-induced systemic capillary leak syndrome with acute kidney injury. CEN Case Reports. 2023;12:63-67.
