กลุ่มอาการรั่วของหลอดเลือดฝอยทั่วร่างกาย (SCLS, โรคคลาร์กสัน) เป็นโรคหายากที่มีรายงานน้อยกว่า 500 รายตั้งแต่ปี ค.ศ. 1960
มีลักษณะสามประการคือ ความดันโลหิตต่ำ ภาวะอัลบูมินในเลือดต่ำ และภาวะเลือดเข้มข้น และพบร่วมกับ MGUS (ภาวะแกมมาโกลบูลินชนิดเดียวที่ไม่ทราบความสำคัญ) ได้ถึง 80%
อาการทางตาที่สำคัญคือ เยื่อบุตา บวม น้ำในคอรอยด์ รั่ว และความดันลูกตา สูง เยื่อบุตา บวมรุนแรงเป็นความเสี่ยงต่อโรคกระจกตา จากการเปิดเผย
ภาวะต้อหินมุมปิดเฉียบพลัน จากน้ำในซิลิอารีรั่วสามารถเกิดขึ้นได้แม้ในตาที่ใส่เลนส์แก้วตาเทียม ในกรณีที่มี NAION (โรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่อาร์เทอริติก) ร่วมด้วย อาจมีข้อบกพร่องของลานสายตาถาวรหลงเหลืออยู่
การให้ IVI G รายเดือนมีประสิทธิภาพในการป้องกันการกำเริบ และอัตราการรอดชีวิต 5 ปีในกลุ่มที่ได้รับ IVI G สูงถึง 91%
การทำลายผนังเซลล์เยื่อบุหลอดเลือดจากการกลายพันธุ์ของยีน TLN1 เพิ่งถูกระบุว่าเป็นกลไกการเกิดโรค SCLS ชนิดครอบครัว
กลุ่มอาการรั่วของหลอดเลือดฝอยทั่วร่างกาย (Systemic Capillary Leak Syndrome; SCLS) เป็นโรคหายากที่มีลักษณะเฉพาะคือการรั่วของของเหลวและโมเลกุลขนาดใหญ่จากหลอดเลือดฝอยไปยังเนื้อเยื่ออย่างรุนแรงและชั่วคราว เรียกอีกชื่อว่า “โรคคลาร์กสัน” ตามชื่อของคลาร์กสันที่รายงานครั้งแรกในปี ค.ศ. 1960 มีรายงานน้อยกว่า 500 รายตั้งแต่ปี ค.ศ. 1960 2) โดยอายุเฉลี่ยของผู้ป่วยเมื่อวินิจฉัยคือ 48 ปี และพบมากในผู้ชายสูงอายุ
มากถึง 80% ของผู้ป่วย SCLS ที่ไม่ทราบสาเหตุมีภาวะ MGUS (ภาวะแกมมาโกลบูลินชนิดโมโนโคลนอลที่ไม่ทราบความสำคัญ ส่วนใหญ่เป็นชนิด IgG) ร่วมด้วย แต่ความเสี่ยงในการ发展为มะเร็งไขกระดูกไม่เพิ่มขึ้น
เนื่องจากการรั่วของของเหลวสามารถเกิดขึ้นได้ในเนื้อเยื่อใดๆ ภาวะแทรกซ้อนทางจักษุวิทยาจึงมีความหลากหลายเช่นกัน อาการทางตาที่สำคัญ ได้แก่ อาการบวมน้ำของเยื่อบุตา การไหลออกของคอรอยด์ และความดันลูกตา สูง มีรายงานกรณีรุนแรงที่มีภาวะมุมปิดเฉียบพลันหรือภาวะประสาทตาขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ (NAION ) ร่วมด้วย 1)
Q
SCLS หายากแค่ไหน?
A
มีรายงานน้อยกว่า 500 รายทั่วโลกตั้งแต่ปี ค.ศ. 1960 ทำให้เป็นโรคที่หายากมาก 2) อายุเฉลี่ยเมื่อวินิจฉัยคือ 48 ปี และพบมากในผู้ชายสูงอายุ เนื่องจากความหายาก จึงควรสังเกตว่าการวินิจฉัยอาจล่าช้า
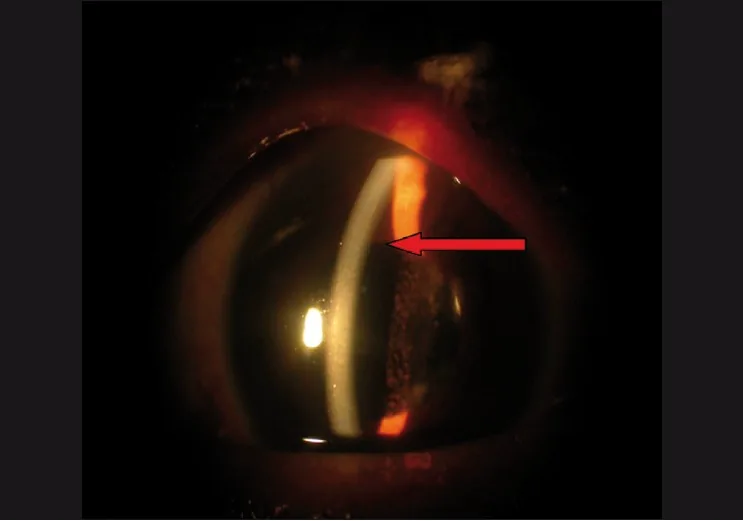
กลุ่มอาการรั่วของหลอดเลือดฝอยทั่วร่างกายที่มีช่องหน้าลึก Management of complications in glaucoma surgery. Indian J Ophthalmol. 2011 Jan; 59(Suppl1):S131-S140. Figure 4. PM
CI D: PMC3038515. License: CC BY.
ตอบสนองต่อการรักษาทางการแพทย์ สังเกตช่องหน้าที่ลึก
อาการนำ : อาการเล็กน้อยที่ไม่จำเพาะ (คล้ายการติดเชื้อทางเดินหายใจ) ปรากฏ 1-4 วันก่อนระยะรั่ว2) .หายใจลำบากและอ่อนเพลีย : หายใจลำบากจากปอดบวมน้ำและน้ำในช่องเยื่อหุ้มปอด ร่วมกับอ่อนแรงทั่วร่างกายบวมทั่วตัว : บวมเฉียบพลัน โดยเฉพาะบริเวณปลายมือปลายเท้า
น้ำตาไหล กลัวแสง รู้สึกมีสิ่งแปลกปลอม คันตา : เนื่องจากเยื่อบุตา บวม (chemosis) การมองเห็น มักยังคงปกติการมองเห็น ลดลงและปวดตา คอรอยด์ และมุมปิดเฉียบพลันความบกพร่องของลานสายตา ส่วนบนเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ ความบกพร่องของลานสายตา รูปโค้งส่วนบนทั้งสองข้างแบบสมมาตรจะชัดเจนในช่วงฟื้นตัวของ SCLS1) .
ส่วนหน้าของลูกตาและบริเวณรอบเบ้าตา
อาการบวมของเปลือกตาและรอบเบ้าตา : ร่วมกับใบหน้าบวม อาจทำให้เกิดตาโปน (เนื่องจากเลือดคั่งในเบ้าตา )
อาการบวมของเยื่อบุตา (chemosis) : อาจรุนแรงมาก ทำให้เสี่ยงต่อภาวะตาปิดไม่สนิทและกระจกตา อักเสบจากการสัมผัส ร่วมกับหลอดเลือดเยื่อบุตา ขยายและคดเคี้ยว
ช่องหน้าม่านตาตื้น และมุมปิดรูม่านตา และสามารถเกิดขึ้นได้แม้ในตาที่ใส่เลนส์แก้วตาเทียม
ความดันลูกตา สูงตาขาว ที่เพิ่มขึ้นก็มีส่วนร่วมด้วย
ส่วนหลังของลูกตาและเส้นประสาทตา
การรั่วของคอรอยด์ : เกิดจากความดันออนโคติกลดลงเนื่องจากการลดลงของอัลบูมินในซีรัมอย่างรวดเร็ว มักเป็นทั้งสองข้าง
การรั่วของซิลิอารีบอดี : การรั่วอย่างกว้างขวางจากส่วนหลังของลูกตาไปยังซิลิอารีบอดี
จานประสาทตา ซีด (ในกรณีของภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ)จานประสาทตา ซีดด้านล่างทั้งสองข้าง1)
RNFL บางลง (ในกรณีของภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ)RNFL บางลงด้านล่างทั้งสองข้างจากการตรวจ OCT 1)
Q
การมองเห็นสามารถลดลงอย่างถาวรใน SCLS ได้หรือไม่?
A
ในกรณีที่มีภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบร่วมด้วย อาจเกิดความบกพร่องของลานสายตา อย่างถาวรได้ ในรายงานผู้ป่วยพบว่ามีความบกพร่องของลานสายตา แบบโค้งด้านบนทั้งสองข้างแบบสมมาตร ในขณะที่การมองเห็น ส่วนกลางยังคงอยู่ที่ 6/7.5 (ประมาณ 0.8) ในทั้งสองตา1) ในทางกลับกัน การมองเห็น ลดลงจากเยื่อบุตา บวม น้ำในคอรอยด์ และมุมปิด มักจะดีขึ้นเมื่ออาการทางระบบดีขึ้น
สาเหตุของ SCLS ส่วนใหญ่เป็นแบบไม่ทราบสาเหตุ (ไม่ทราบสาเหตุแน่ชัด) นอกเหนือจากแบบไม่ทราบสาเหตุแล้ว ยังมีรายงานปัจจัยกระตุ้นดังต่อไปนี้
เกิดจากยา : ยาเคมีบำบัด เช่น gemcitabine, clofarabine, แอนติบอดีโมโนโคลนอล, ปัจจัยการเจริญเติบโตเพื่อการรักษา ในยา denileukin diftitox (ยารักษา CTCL ) พบ SCLS ใน 36% ในการทดลองทางคลินิก9) .การติดเชื้อไวรัส : ไข้หวัดใหญ่ A และ B, งูสวัด, ไข้เลือดออกเดงกี ในรายงานผู้ป่วยที่มีภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบ พบว่ามีการยืนยันการติดเชื้อไข้หวัดใหญ่ B1) .ที่เกี่ยวข้องกับโควิด-19 : นอกจากการติดเชื้อโควิด-19 เองแล้ว ยังมีรายงานการเกิดร่วมกับวัคซีนแอสตราเซเนกา จอห์นสันแอนด์จอห์นสัน-แจนเซน และไฟเซอร์-ไบโอเอ็นเทค7) 8) สำนักงานยาแห่งยุโรป (EMA) แนะนำให้วัคซีนแอสตราเซเนกาเป็นข้อห้ามใช้ในผู้ที่มีประวัติ SCLS7) .โรค decompression sickness : มีรายงาน SCLS ที่เกิดตามหลังโรค decompression sickness หลังการดำน้ำ6) .เนื้องอกมะเร็ง : SCLS เป็นกลุ่มอาการพารานีโอพลาสติก จากมะเร็งต่อมน้ำเหลืองชนิดดิฟฟิวส์ลาร์จบีเซลล์ (DLBCL) และอื่นๆ3) .ภูมิหลังทางพันธุกรรม : พบการกลายพันธุ์ที่ตำแหน่งต่อประกบของยีน TLN1 (c.7188+2T>C) ใน SCLS ชนิด familial รูปแบบการถ่ายทอดเป็นแบบ autosomal dominant โดยมีการแสดงออกไม่สมบูรณ์ 4) .
ปัจจัยเสี่ยงที่ทำให้เกิดภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่อักเสบจากหลอดเลือดแดงได้ง่าย นอกเหนือจากภาวะความดันโลหิตต่ำ ภาวะเลือดเข้มข้น และภาวะเลือดแข็งตัวง่ายจาก SCLS แล้ว ยังรวมถึงเบาหวาน ความดันโลหิตสูง หลอดเลือดแดงแข็ง และจานประสาทตา ที่มีขนาดเล็กและแออัด 1) .
การให้ IVI G (อิมมูโนโกลบูลินทางหลอดเลือดดำ) ทุกเดือนมีประสิทธิภาพสูงสุดในการป้องกันการเกิด SCLS
วัคซีนโควิด-19 (โดยเฉพาะชนิดอะดีโนไวรัสเวกเตอร์) ต้องใช้ความระมัดระวังในผู้ที่มีประวัติ SCLS ควรปรึกษาแพทย์ผู้รักษาก่อนฉีดวัคซีน
การติดเชื้อไวรัส เช่น ไข้หวัดใหญ่ อาจกระตุ้นให้เกิดอาการชักได้ ดังนั้นควรป้องกันการติดเชื้อ
Q
วัคซีนโควิด-19 ทำให้เกิด SCLS หรือไม่?
A
มีรายงานผู้ป่วยที่เกิดจากวัคซีนทั้งชนิดอะดีโนไวรัสเวกเตอร์และ mRNA 7) 8) ยังไม่มีการกำหนดความสัมพันธ์เชิงสาเหตุ แต่ EMA แนะนำให้วัคซีนแอสตราเซเนกาเป็นข้อห้ามใช้ในผู้ที่มีประวัติ SCLS ผู้ที่มีประวัติ SCLS ควรปรึกษาแพทย์ก่อนฉีดวัคซีน
SCLS วินิจฉัยโดยการแยกโรคออก โดยอาศัยการมีสัญญาณของการรั่วของเส้นเลือดฝอย เช่น อาการบวมน้ำทั่วร่างกายและความดันโลหิตต่ำที่ดื้อต่อการรักษา และการแยกโรคอื่นออก
ในระยะเฉียบพลัน จะพบความผิดปกติของค่าห้องปฏิบัติการที่มีลักษณะเฉพาะดังต่อไปนี้:
ภาวะอัลบูมินในเลือดต่ำ (ไม่มีโปรตีนในปัสสาวะ): ค่าเฉลี่ยประมาณ 1.7 กรัม/เดซิลิตร2) ในรายที่รุนแรง มีรายงานอัลบูมิน 16 กรัม/ลิตร5) และ 18 กรัม/ลิตร8) ภาวะเลือดเข้มข้น : ฮีมาโตคริตสูงขึ้น (ค่าเฉลี่ยประมาณ 60%) ในรายที่รุนแรง Ht อาจสูงถึง 69%5) และ 72.3%8) MGUS : ตรวจพบได้สูงถึง 80% ของผู้ป่วยโดยการตรวจอิเล็กโตรโฟรีซิสโปรตีนในซีรัม (SPEP) ที่พบบ่อยคือ IgG-κ2) 5) และ IgG-λ1) ความเสี่ยงต่อการเกิดลิ่มเลือดอุดตัน : ภาวะเลือดแข็งตัวง่ายเนื่องจากเลือดเข้มข้น มีรายงานผู้ป่วยร่วมกับลิ่มเลือดอุดตันในหลอดเลือดดำลึก ลิ่มเลือดอุดตันในหลอดเลือดดำใหญ่ inferior vena cava8) และลิ่มเลือดอุดตันในปอด2) ภาวะไตบาดเจ็บเฉียบพลัน (AKI) : เกิดขึ้นในบางกรณี9) .
การตรวจ scintigraphy ด้วย 99mTc-HS A สามารถพิสูจน์การเพิ่มขึ้นของการซึมผ่านของหลอดเลือดโดยตรงผ่านการสะสมของ HS A ใต้ผิวหนังบริเวณแขนขาหลังจาก 24 ชั่วโมง9) .
การตรวจด้วยกล้อง slit-lamp : ประเมินระดับของอาการบวมน้ำที่เยื่อบุตา , การมีช่องหน้าม่านตาตื้น หรือมุมปิด.อัลตราซาวนด์โหมด B : ตรวจสอบการมีอยู่และระดับของน้ำในคอรอยด์ .การตรวจลานสายตา Humphrey โรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบ)1) .เครื่องตรวจการเชื่อมโยงแสง (OCT ) : การประเมินเชิงปริมาณของการบางลงของชั้นใยประสาทจอประสาทตา ส่วนล่าง (ในกรณีที่มีภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบ) 1) .MRI ศีรษะและเบ้าตา : ใช้เพื่อแยกภาวะกล้ามเนื้อตายเฉพาะที่และรอยโรคที่เป็นก้อน 1) .
โรคที่ต้องวินิจฉัยแยกโรคหลักมีดังนี้:
ภาวะติดเชื้อในกระแสเลือด, ภาวะแพ้รุนแรง, ภาวะบวมน้ำจากหลอดเลือด : การวินิจฉัยแยกโรคที่สำคัญที่สุด.กลุ่มอาการเนฟโฟรติก : สามารถแยกจาก SCLS ได้โดยไม่มีโปรตีนในปัสสาวะระดับรุนแรง.กลุ่มอาการรังไข่ถูกกระตุ้นมากเกิน (OHS S) : จำเป็นต้องแยกวินิจฉัยในผู้ป่วยหญิงโรคเม็ดเลือดขาวและเนื้อเยื่อลิมฟอยด์กินเซลล์เม็ดเลือด (HLH) : ควรพิจารณาไข้เลือดออกจากไวรัสและพิษงูด้วยภาวะหลอดเลือดบวมน้ำจากพันธุกรรม : สามารถแยกออกได้หากสารยับยั้ง C1 เอสเทอเรสปกติ6)
การจัดการสารน้ำ : สารละลายคริสตัลลอยด์เป็นทางเลือกแรก การให้สารน้ำมากเกินไปเพิ่มความเสี่ยงของปอดบวมน้ำและกลุ่มอาการ compartment syndrome พิจารณาใช้สารขยายปริมาตรโมเลกุลใหญ่เฉพาะเมื่อความดันโลหิตซิสโตลิกต่ำกว่า 70 มิลลิเมตรปรอท เป็นกลยุทธ์ “การยอมให้ความดันโลหิตต่ำ” 6) .ยาขยายหลอดเลือด : ใช้ norepinephrine และอื่นๆสเตียรอยด์ ทั่วร่างกายและ IVI G (ระยะเฉียบพลัน)IVI G ขนาด 1-2 กรัม/กิโลกรัม/วัน นาน 2-3 วันการป้องกันลิ่มเลือดอุดตัน : ดำเนินการเพื่อป้องกันภาวะเลือดแข็งตัวมากเกินจากเลือดข้น
ทางเลือกหลักในการป้องกันการกำเริบมีดังนี้
IVI G (อิมมูโนโกลบูลินทางหลอดเลือดดำ)IVI G มีอัตรารอดชีวิต 5 ปี 91% และ 10 ปี 77% เทียบกับกลุ่มที่ไม่ได้รับ IVI G ที่ 47% และ 37% แตกต่างอย่างมีนัยสำคัญ ความถี่ของการเกิดอาการกำเริบเฉลี่ยต่อปีภายใต้การรักษาด้วย IVI G คือ 0 (ช่วง 0–3.3)8) .ยาตัวรับ β2 (terbutaline) + theophylline : ใช้เพื่อยับยั้งการซึมผ่านของเยื่อบุผนังหลอดเลือดโดยเพิ่ม cAMP Terbutaline 5 มก. 3 ครั้ง/วัน, theophylline 400–1600 มก./วัน6) อย่างไรก็ตาม ความถี่ของการเกิดอาการกำเริบเฉลี่ยต่อปีภายใต้การรักษาคือ 2.25 (ช่วง 0–20) ซึ่งด้อยกว่า IVI G8) .Methylprednisolone ขนาดสูงแบบ pulse ร่วมกับ IVIg : มีรายงานการให้ mPSL 1,000 มก./วัน นาน 3 วัน + IVIg 1 กรัม/กก.8) .
Q
การรักษาใดมีประสิทธิภาพสูงสุดในการป้องกันการกำเริบของ SCLS?
A
การให้ IVI G (อิมมูโนโกลบูลินทางหลอดเลือดดำ) รายเดือนถือว่ามีประสิทธิภาพสูงสุด อัตรารอดชีวิต 5 ปีในกลุ่ม IVI G คือ 91% เทียบกับ 47% ในกลุ่มที่ไม่ได้รับ IVI G ซึ่งแตกต่างกันมาก ความถี่ของการเกิดอาการกำเริบเฉลี่ยต่อปีในกลุ่ม IVI G คือ 0 แสดงให้เห็นถึงฤทธิ์ยับยั้งที่ดีเยี่ยม8) .
การรั่วของคอรอยด์ และซิลิอารีบอดี ้ : ใช้สเตียรอยด์ ทั้งระบบและเฉพาะที่ (ยาหยอดตาและรอบดวงตา) และมีรายงานบางฉบับที่แสดงถึงการตอบสนองที่ดี อย่างไรก็ตาม มีชุดผู้ป่วยบางรายที่ไม่ตอบสนองดีนัก.การจัดการความดันลูกตา : ใช้ยาหยอดตาลดความดันลูกตา เฉพาะที่.เยื่อบุตา บวมและกระจกตา อักเสบจากการเปิดรับตาเทียม ในกรณีรุนแรง อาจพิจารณาเย็บเปลือกตาชั่วคราว แต่มีความเสี่ยงที่จะทำให้เกิดภาวะกลุ่มอาการช่องเบ้าตา โดยการกดเบ้าตา การปิดมุม : อาจพิจารณาการตัดม่านตาด้วยเลเซอร์ (LPI ) หรือการผ่าตัดต้อกระจก แต่ต้องระวังเนื่องจากการปิดมุมอาจคงอยู่ได้จากการไหลซึมของเลนส์ปรับเลนส์แม้ในตาที่มีเลนส์แก้วตาเทียม การผ่าตัดและเลเซอร์สำหรับน้ำในคอรอยด์ : โดยปกติแล้วจะดื้อต่อการรักษา ไม่มีการรักษาทางศัลยกรรมที่กำหนดไว้สำหรับ SCLS.
เส้นทางร่วมสุดท้ายของ SCLS คือความผิดปกติของเยื่อบุผนังหลอดเลือด ช่องว่างระหว่างเซลล์เยื่อบุผนังหลอดเลือดขยายกว้างขึ้น ทำให้เกิดการรั่วของโมเลกุลขนาดใหญ่และน้ำออกนอกหลอดเลือด
ในระหว่างการกำเริบ จะพบการเปลี่ยนแปลงดังต่อไปนี้
การแสดงออกของตัวรับ IL-2 บนเซลล์โมโนนิวเคลียร์เพิ่มขึ้น การผลิต CXCL10, CCL2, IL-1β, IL-8, IL-12 เพิ่มขึ้น
ความเข้มข้นของเซลล์ T CD8+/CD25+ เพิ่มขึ้น การแสดงออกของ TNF -α เพิ่มขึ้น
VEGF-D เพิ่มขึ้น5)
VEGF และ Angiopoietin-2 เพิ่มขึ้นในระหว่างการกำเริบ5)
ในแบบจำลองในหลอดทดลอง สารยับยั้งแองจิโอพอยอิติน-2 และ IVI G ลดการซึมผ่านของเยื่อบุผนังหลอดเลือดได้อย่างมีนัยสำคัญ ในขณะที่ผลของเบวาซิซูแมบ (สารยับยั้ง VEGF) มีเพียงเล็กน้อย 5) .
Elefant และคณะ (JCI Insight, 2024) ระบุการกลายพันธุ์แบบเฮเทอโรไซกัสที่ตำแหน่ง splicing (c.7188+2T>C) ในยีน TLN1 ในผู้ป่วย SCLS ในครอบครัว 3 ราย 4) การกลายพันธุ์นี้ทำให้เกิดการข้าม exon 54 แบบ in-frame ซึ่งทำให้โดเมน talin1 R13 ไม่เสถียร เมื่อตำแหน่งจับแอคตินปลาย C (ABS3) ทำงานผิดปกติ การกระจายตัวของ VE-cadherin ที่รอยต่อจะลดลงอย่างมีนัยสำคัญ และรอยต่อยึดติด (AJ) และรอยต่อแน่น (TJ) แตกเป็นชิ้น ส่งผลให้การซึมผ่านของสิ่งกีดขวางเยื่อบุผนังหลอดเลือดเพิ่มขึ้น เมื่อกระตุ้นด้วย thrombin เซลล์เยื่อบุผนังหลอดเลือดกลายพันธุ์ SCLS แสดงการซึมผ่านของ FITC-dextran สูงกว่ากลุ่มควบคุมประมาณ 4 เท่า
เดนิลิวคิน ดิฟติทอกซ์จับกับเซลล์ที่แสดงตัวรับ IL-2 และยับยั้งการสังเคราะห์โปรตีนผ่านการนำชิ้นส่วนทอกซินคอตีบเข้าสู่เซลล์ เชื่อว่า SCLS เกิดจากทั้งการเพิ่มการซึมผ่านของหลอดเลือด (ฤทธิ์ของ IL-2R) และการยับยั้งการสังเคราะห์โปรตีน (ฤทธิ์ของทอกซินคอตีบ)9) .
การรั่วของคอรอยด์ : เกิดจากความดันออสโมติกคอลลอยด์ลดลงเนื่องจากการลดลงอย่างรวดเร็วของอัลบูมินในซีรัมการรั่วของซิลิอารีบอดี และการปิดมุม : การรั่วของซิลิอารีบอดี → การหมุนของซิลิอารีบอดี ไปข้างหน้า → ช่องหน้าม่านตาตื้น และการปิดมุม ไม่เกิดผ่านกลไกการอุดตันของรูม่านตา จึงสามารถเกิดขึ้นได้ในตาที่มีเลนส์แก้วตาเทียม ความดันลูกตา สูงโรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบจานประสาทตา เนื่องจากหลอดเลือดแดงซิลิอารีส่วนหลัง เนื่องจากหลอดเลือดแดงซิลิอารีส่วนหลังก่อตัวเป็นหลอดเลือดแดงปลายทางและบริเวณ watershed กล้ามเนื้อตายของจานประสาทตา จึงเกิดขึ้นได้ง่ายในภาวะช็อก1)
Elefant และคณะ (2024) แสดงให้เห็นว่าในเซลล์บุผนังหลอดเลือดที่แสดงออก talin1 กลายพันธุ์แบบ SCLS การฟื้นฟูการต่อประกบปกติด้วยโอลิโกนิวคลีโอไทด์แอนติเซนส์แบบสลับการต่อประกบสามารถเสนอเป็นกลยุทธ์การรักษาได้ 4) หากการแปลตำแหน่งรอยต่อของ VE-cadherin และความสมบูรณ์ของ AJ ได้รับการฟื้นฟู อาจนำไปสู่การซ่อมแซมการทำงานของสิ่งกีดขวางบุผนังหลอดเลือด
มีการบันทึกความเข้มข้นของ VEGF-D ที่เพิ่มขึ้นในผู้ป่วย SCLS และเส้นทางผ่าน VEGFR3 ถูกกล่าวถึงว่าเป็นเป้าหมายการรักษาที่มีศักยภาพในอนาคต การรักษาด้วยการต้าน VEGF (bevacizumab ทางหลอดเลือดดำ) ได้รับการทดลองในผู้ป่วย 1 ราย แต่ไม่มีการตอบสนองทางคลินิก ในทางกลับกัน ยายับยั้ง angiopoietin-2 ช่วยลดการซึมผ่านของเยื่อบุผนังหลอดเลือดร่วมกับ IVI G ในแบบจำลองในหลอดทดลองอย่างมีนัยสำคัญ แต่รายงานทางคลินิกยังมีจำกัด5) .
มีรายงานการเกิดโรคในทั้งวัคซีน mRNA และวัคซีนอะดีโนไวรัสเวกเตอร์7) 8) แต่ยังไม่มีการพิสูจน์ความสัมพันธ์เชิงสาเหตุ และจำเป็นต้องมีการวิจัยเพิ่มเติม
Neo YN, Sobti M, Zambarakji H. Bilateral simultaneous non-arteritic ischaemic optic neuropathy: a rare complication of idiopathic systemic capillary leak syndrome (SCLS). BMJ Case Rep. 2021;14:e242847.
Correia R, Santos D, Delgado M. Idiopathic Systemic Capillary Leak Syndrome: A Clinical Case. Cureus. 2023;15(12):e50301.
Silva B, Gaspar V, Alves C, et al. Systemic Capillary Leak Syndrome as a Paraneoplastic Syndrome. Cureus. 2024;16(5):e60923.
Elefant N, Rouni G, Arapatzi C, et al. Talin1 dysfunction is genetically linked to systemic capillary leak syndrome. JCI Insight. 2024;9(24):e173664.
Bouchlarhem A, Lamzouri O, El aidouni G, et al. Consider systemic capillary leak syndrome in monoclonal gammopathy with shock. Ann Med Surg. 2021;72:103013.
Mathavan A, Mathavan A, Jones K, et al. Systemic capillary leak syndrome secondary to decompression sickness. BMJ Case Rep. 2023;16:e253045.
Yang C, Tsang MYC, Zypchen LN, et al. Pericardial effusion and systemic capillary leak syndrome late post-SARS-CoV-2 vaccination. BMJ Case Rep. 2023;16:e256527.
Inoue M, Yasue Y, Kobayashi Y, et al. Systemic capillary leak syndrome (SCLS) after receiving BNT162b2 mRNA COVID-19 (Pfizer-BioNTech) vaccine. BMJ Case Rep. 2022;15:e248927.
Horino T, Okada D, Inotani S, et al. Denileukin diftitox-induced systemic capillary leak syndrome with acute kidney injury. CEN Case Reports. 2023;12:63-67.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต