视神经病变

胶质母细胞瘤的神经眼科征象
一目了然的要点
Section titled “一目了然的要点”1. 胶质母细胞瘤的神经眼科征象
Section titled “1. 胶质母细胞瘤的神经眼科征象”胶质母细胞瘤(GBM)是一种WHO 4级星形细胞瘤,是成人最常见的原发性恶性脑肿瘤。美国发病率约为每10万人3例,每年诊断超过10,000例。占所有脑肿瘤的12%~15%,占恶性中枢神经系统肿瘤的45.2%3)。诊断时平均年龄为64岁,男女比例为1.5:1。
神经眼科体征由以下三种机制中的一种或多种组合引起。
- 直接发生/浸润:肿瘤直接发生或浸润视神经、视交叉、视束
- 压迫:周围结构占位效应导致视路受压
- 颅内压增高:肿瘤引起脑压升高伴发的视乳头水肿
视神经原发GBM极为罕见,占所有脑肿瘤的0.6%~1.2%,文献报道仅约70例1)。成人型视神经胶质瘤恶性程度高,好发于中年男性。预后约6个月,与儿童型病程完全不同。
累及视路时的平均生存期约为8个月,短于非视路GBM的14.6个月。
原发性视神经胶质母细胞瘤占所有脑肿瘤的0.6%至1.2%,全球文献报告仅约70例1)。这是一种非常罕见的疾病,需注意诊断容易延迟。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”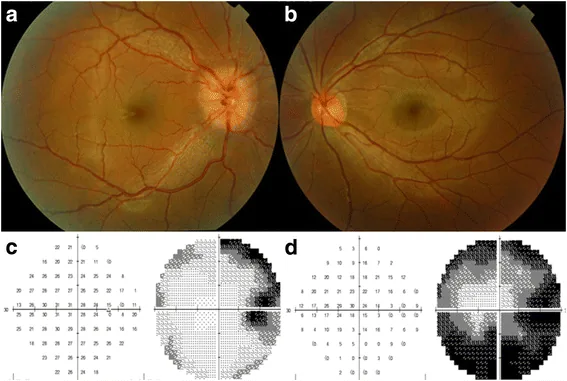
- 视力下降:单侧或双侧。由视神经或视交叉受累引起。成人型视神经胶质瘤可表现为单眼视力障碍,数周内浸润视交叉导致双眼失明。
- 视野缺损:模式与肿瘤部位相对应(见下文)。
- 眼球突出:肿瘤发生于视神经时出现。Brokāns报告的病例以左眼球突出、视力下降和向上注视受限6个月为主诉1)。
- 头痛:由颅内压增高或肿瘤直接效应引起。
- 复视:由动眼神经麻痹或外展神经麻痹引起的眼球运动障碍所致。
根据视路受累的部位,可获得特征性的神经眼科表现。
视交叉及视交叉后
因颅内压增高导致的视乳头水肿,初期仅表现为视物模糊和Mariotte盲点扩大。若长期持续,则会出现视神经萎缩,视野狭窄和视力下降逐渐加重。
MRI的成像方向因病变部位而异。视交叉前方的病变必须进行眼眶冠状位扫描,后方病变则脑水平位扫描更有用。
视野缺损的模式因肿瘤位置而异。视神经受累时出现同侧中心暗点和周边视野缺损,视交叉受累时出现双颞侧偏盲,视交叉后方(视束或视放射)受累时出现对侧同向偏盲。
3. 病因与危险因素
Section titled “3. 病因与危险因素”约95%的GBM为散发性,仅约5%与遗传性综合征相关。发生可分为原发性和继发性,两者分子特征不同。
原发性和继发性的主要分子变化如下所示。
| 类型 | 主要分子变化 |
|---|---|
| 原发性 | EGFR扩增、MDM2扩增、PTEN突变、CDKN2A缺失 |
| 继发性 | IDH1突变、p53突变、MET扩增 |
| 共同 | RAS/PI3K通路激活 |
与颅外转移风险相关的因素包括TP53、TERT、PTEN突变、染色体+7/−10和肉瘤样组织学类型6)。软脑膜播散的风险因素包括脑室开放、反复手术、男性和室管膜浸润3)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”- MRI(首选):T1增强和T2/FLAIR高信号的组合具有特征性。对于视交叉前方病变,需加做眼眶冠状位扫描1)。
- CT:用于筛查及检测骨骼或钙化1)。
- OCT:检测视网膜神经纤维层和神经节细胞层变薄。对轻微视神经萎缩的检出能力高,有助于早期病变的识别。
- 视野检查:评估与肿瘤部位对应的视野缺损模式。有助于推断病变部位,如双颞侧偏盲或同向偏盲。
- RAPD评估:强烈提示视神经病变,是一项简便且重要的发现。
确诊必须进行活检。评估项目包括IDH1/2突变、GFAP和Ki-671)。
按部位列出需要鉴别的疾病。
| 部位 | 主要鉴别诊断 |
|---|---|
| 视神经 | 视神经鞘瘤、视神经鞘脑膜瘤、视神经淋巴瘤 |
| 视交叉 | 垂体腺瘤、颅咽管瘤、脑膜瘤 |
5. 标准治疗方法
Section titled “5. 标准治疗方法”目标是最大安全范围的切除。视神经原发性GBM因邻近视觉结构,常难以完全切除1)。在日本,根据肿瘤的位置和进展选择观察、手术、化疗和放疗。
解除视交叉压迫可能改善视力。然而,在视神经萎缩进展的病例中,即使解除压迫,视力恢复也难以预期,预后不良。
标准照射方案为60 Gy/30次/6周1)。
化疗(替莫唑胺;TMZ)
Section titled “化疗(替莫唑胺;TMZ)”- 同步放疗期:75 mg/m²/日,与放疗同时给药3)。
- 辅助治疗期:200 mg/m²/天,连续给药5天,每28天为一个周期3)。
手术+放疗+TMZ的Stupp方案使中位生存期约为14.6个月。
软脑膜播散(LMS)的处理
Section titled “软脑膜播散(LMS)的处理”GBM患者中2%~4%(最高15%25%)发生软脑膜播散,生存期极短,为0.29.7个月2)。原发性LMS极为罕见。尚无标准治疗方案,鞘内化疗和额外放疗效果有限。
由于视神经原发性GBM毗邻视觉结构,优先考虑功能保留时,完全切除往往困难1)。通常进行最大安全切除后辅以放疗和化疗。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”GBM增殖、侵袭和血管生成的核心通路是通过EGFR扩增激活RAS/PI3K通路。此外,肿瘤微环境的免疫抑制是其特点,T细胞浸润缺乏、调节性T细胞(Treg)和髓源性抑制细胞(MDSC)增加促进了免疫逃逸4)。
播散的主要途径是通过蛛网膜下腔3)。尸检发现25%的病例有脊髓播散。
对视路的影响源于以下三种机制。
- 直接发生/浸润:肿瘤直接发生或浸润扩散至视神经、视交叉、视束、视放射
- 压迫:邻近肿瘤团块对视路的压迫和变形
- 颅内压增高:肿瘤导致脑压升高→视乳头水肿→视神经萎缩
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”激光间质热疗法(LITT)与免疫激活
Section titled “激光间质热疗法(LITT)与免疫激活”LITT在46°C以上引起凝固性坏死,而在33–43°C时则开放血脑屏障(BBB)并诱导免疫原性细胞死亡4)。
Chandar等人(2023)对新诊断的GBM患者进行了LITT治疗,治疗后观察到CD8+ T细胞和PD-L1显著增加4)。该患者实现了9年无复发生存。
术前三联免疫检查点抑制剂治疗(新辅助ICI)
Section titled “术前三联免疫检查点抑制剂治疗(新辅助ICI)”Long等人(2025)在新诊断的GBM患者中,术前给予纳武利尤单抗、伊匹木单抗和瑞拉利单抗的三药ICI方案5)。治疗后,肿瘤浸润CD3+T细胞从9.8%增加到32.7%,活化T细胞增加了8.5倍。一例患者实现了17个月的无复发生存,目前GIANT试验正在计划中。
目前,免疫疗法尚未确立为标准治疗。然而,术前三种ICI联合给药已被证实能显著增加肿瘤内T细胞浸润5),未来临床试验的验证值得期待。
颅外转移的分子标志物
Section titled “颅外转移的分子标志物”颅外转移发生在0.4%–2.0%的GBM病例中,转移后中位生存期极短,仅为1.5个月6)。转移病例的分子特征包括TP53、TERT和PTEN突变,这些突变正作为转移风险的生物标志物被研究6)。
8. 参考文献
Section titled “8. 参考文献”- Brokāns A, Dolgopolova J, Saulītis A, et al. Optic Nerve Glioblastoma with Optic Chiasm Involvement: A Case Report and a Brief Literature Review. Medicina. 2024;60(10):1687.
- Mondia MWL, Hooks RE, Maragkos GA, et al. Primary diffuse leptomeningeal glioblastoma: a case report and literature review. J Neuro-Oncol. 2025;172:265-272.
- Zhang K, Yang Y, Zhuang J, et al. Intracranial dissemination of glioblastoma multiforme: a case report and literature review. J Int Med Res. 2022;50(7):03000605221112047.
- Chandar JS, Bhatia S, Ingle S, et al. Laser Interstitial Thermal Therapy Induces Robust Local Immune Response for Newly Diagnosed Glioblastoma with Long Term Survival and Disease Control. J Immunother. 2023;46(9):351-354.
- Long GV, et al. Neoadjuvant triplet immune checkpoint blockade in newly diagnosed glioblastoma. Nat Med. 2025;31:1557-1566.
- Yuen CA, Pekmezci M, Bao S, Kong XT. Metastatic glioblastoma to the lungs: a case report and literature review. CNS Oncol. 2024;13(1):2351789.
