視神經病變

膠質母細胞瘤的神經眼科徵象
一目瞭然的要點
Section titled “一目瞭然的要點”1. 膠質母細胞瘤的神經眼科徵象
Section titled “1. 膠質母細胞瘤的神經眼科徵象”膠質母細胞瘤(GBM)是一種WHO第4級星狀細胞瘤,是成人最常見的原發性惡性腦腫瘤。美國發生率約為每10萬人3例,每年診斷超過10,000例。佔所有腦腫瘤的12%~15%,佔惡性中樞神經系統腫瘤的45.2%3)。診斷時平均年齡為64歲,男女比為1.5:1。
神經眼科徵候由以下三種機制的單一或組合引起。
- 直接發生/浸潤:腫瘤直接發生或浸潤視神經、視交叉、視束
- 壓迫:周圍結構的腫塊效應導致視路受壓
- 顱內壓升高:腫瘤引起腦壓升高伴隨的視乳頭水腫
視神經原發GBM極為罕見,佔所有腦腫瘤的0.6%~1.2%,文獻報告僅約70例1)。成人型視神經膠質瘤惡性度高,好發於中年男性。預後約6個月,與兒童型病程完全不同。
侵犯視路時的平均存活期約8個月,短於非視路GBM的14.6個月。
原發性視神經膠質母細胞瘤佔所有腦腫瘤的0.6%至1.2%,全球文獻報告僅約70例1)。這是一種非常罕見的疾病,需注意診斷容易延遲。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”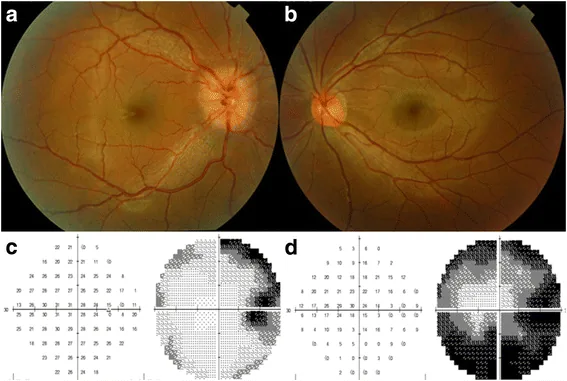
- 視力下降:單側或雙側。由視神經或視交叉受累引起。成人型視神經膠質瘤可表現為單眼視力障礙,數週內浸潤視交叉導致雙眼失明。
- 視野缺損:模式與腫瘤部位相對應(見下文)。
- 眼球突出:腫瘤發生於視神經時出現。Brokāns報告的病例以左眼球突出、視力下降和向上注視受限6個月為主訴1)。
- 頭痛:由顱內壓增高或腫瘤直接效應引起。
- 複視:由動眼神經麻痺或外展神經麻痺引起的眼球運動障礙所致。
根據視路受影響的部位,可獲得特徵性的神經眼科表現。
視交叉及視交叉後
因顱內壓增高導致的視乳頭水腫,初期僅表現為視物模糊和Mariotte盲點擴大。若長期持續,則會出現視神經萎縮,視野狹窄和視力下降逐漸加重。
MRI的成像方向因病變部位而異。視交叉前方的病變必須進行眼眶冠狀位掃描,後方病變則腦水平位掃描更有用。
視野缺損的模式因腫瘤位置而異。視神經受累時出現同側中心暗點和周邊視野缺損,視交叉受累時出現雙顳側偏盲,視交叉後方(視束或視放射)受累時出現對側同向偏盲。
3. 病因與危險因素
Section titled “3. 病因與危險因素”約95%的GBM為散發性,僅約5%與遺傳性症候群相關。發生可分為原發性和繼發性,兩者分子特徵不同。
原發性與繼發性的主要分子變化如下所示。
| 類型 | 主要分子變化 |
|---|---|
| 原發性 | EGFR擴增、MDM2擴增、PTEN突變、CDKN2A缺失 |
| 繼發性 | IDH1突變、p53突變、MET擴增 |
| 共同 | RAS/PI3K路徑活化 |
與顱外轉移風險相關的因素包括TP53、TERT、PTEN突變、染色體+7/−10和肉瘤樣組織型態6)。軟腦膜播散的風險因素包括腦室開放、反覆手術、男性和室管膜浸潤3)。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”- MRI(首選):T1顯影增強與T2/FLAIR高信號的組合具有特徵性。對於視交叉前方病變,需加做眼眶冠狀斷層掃描1)。
- CT:用於篩檢及偵測骨骼或鈣化1)。
- OCT:偵測視網膜神經纖維層及神經節細胞層變薄。對輕微視神經萎縮的偵測能力高,有助於早期病變的掌握。
- 視野檢查:評估對應腫瘤部位的視野缺損模式。有助於推斷病變位置,如雙顳側偏盲或同側偏盲。
- RAPD評估:強烈提示視神經病變,是一項簡便且重要的發現。
確診必須進行切片檢查。評估項目包括IDH1/2突變、GFAP和Ki-671)。
按部位列出需要鑑別的疾病。
| 部位 | 主要鑑別診斷 |
|---|---|
| 視神經 | 視神經鞘瘤、視神經鞘腦膜瘤、視神經淋巴瘤 |
| 視交叉 | 垂體腺瘤、顱咽管瘤、腦膜瘤 |
5. 標準治療方法
Section titled “5. 標準治療方法”目標是最大安全範圍的切除。視神經原發性GBM因鄰近視覺結構,常難以完全切除1)。在日本,根據腫瘤的位置和進展選擇觀察、手術、化療和放療。
解除視交叉壓迫可能改善視力。然而,在視神經萎縮進展的病例中,即使解除壓迫,視力恢復也難以預期,預後不良。
標準照射方案為60 Gy/30次/6週1)。
化學治療(替莫唑胺;TMZ)
Section titled “化學治療(替莫唑胺;TMZ)”- 同步放療期:75 mg/m²/日,與放療同時給藥3)。
- 輔助治療期:200 mg/m²/天,連續給藥5天,每28天為一個週期3)。
手術+放射線+TMZ的Stupp方案使中位存活期約為14.6個月。
軟腦膜播種(LMS)的處理
Section titled “軟腦膜播種(LMS)的處理”GBM患者中2%~4%(最高15%25%)發生軟腦膜播種,存活期極短,為0.29.7個月2)。原發性LMS極為罕見。尚無標準治療方案,鞘內化療和額外放射線效果有限。
由於視神經原發性GBM鄰近視覺結構,優先考慮功能保留時,完全切除往往困難1)。通常進行最大安全切除後輔以放射治療和化學治療。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”GBM增殖、侵襲和血管新生的核心通路是通過EGFR擴增激活RAS/PI3K通路。此外,腫瘤微環境的免疫抑制是其特點,T細胞浸潤缺乏、調節性T細胞(Treg)和髓源性抑制細胞(MDSC)增加促進了免疫逃逸4)。
播散的主要途徑是通過蛛網膜下腔3)。屍檢發現25%的病例有脊髓播散。
對視路的影響源於以下三種機制。
- 直接發生/浸潤:腫瘤直接發生或浸潤擴散至視神經、視交叉、視束、視放射
- 壓迫:鄰近腫瘤團塊對視路的壓迫和變形
- 顱內壓升高:腫瘤導致腦壓升高→視乳頭水腫→視神經萎縮
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”雷射間質熱療法(LITT)與免疫活化
Section titled “雷射間質熱療法(LITT)與免疫活化”LITT在46°C以上引起凝固性壞死,而在33–43°C時則開放血腦屏障(BBB)並誘導免疫原性細胞死亡4)。
Chandar等人(2023)對新診斷的GBM患者進行了LITT治療,治療後確認CD8+ T細胞和PD-L1顯著增加4)。該患者達成了9年無復發生存。
術前三聯免疫檢查點抑制劑治療(新輔助ICI)
Section titled “術前三聯免疫檢查點抑制劑治療(新輔助ICI)”Long等人(2025)在新診斷的GBM患者中,術前給予nivolumab、ipilimumab和relatlimab的三藥ICI方案5)。治療後,腫瘤浸潤CD3+T細胞從9.8%增加到32.7%,活化T細胞增加了8.5倍。一例患者實現了17個月的無復發生存,目前GIANT試驗正在計劃中。
目前免疫療法尚未確立為標準治療。然而,術前三種ICI聯合給藥已被證實能顯著增加腫瘤內T細胞浸潤5),未來臨床試驗的驗證值得期待。
顱外轉移的分子標記
Section titled “顱外轉移的分子標記”顱外轉移發生於0.4%–2.0%的GBM病例,轉移後中位存活期極短,僅1.5個月6)。轉移病例的分子特徵包括TP53、TERT和PTEN突變,這些突變正作為轉移風險的生物標記被研究6)。
8. 參考文獻
Section titled “8. 參考文獻”- Brokāns A, Dolgopolova J, Saulītis A, et al. Optic Nerve Glioblastoma with Optic Chiasm Involvement: A Case Report and a Brief Literature Review. Medicina. 2024;60(10):1687.
- Mondia MWL, Hooks RE, Maragkos GA, et al. Primary diffuse leptomeningeal glioblastoma: a case report and literature review. J Neuro-Oncol. 2025;172:265-272.
- Zhang K, Yang Y, Zhuang J, et al. Intracranial dissemination of glioblastoma multiforme: a case report and literature review. J Int Med Res. 2022;50(7):03000605221112047.
- Chandar JS, Bhatia S, Ingle S, et al. Laser Interstitial Thermal Therapy Induces Robust Local Immune Response for Newly Diagnosed Glioblastoma with Long Term Survival and Disease Control. J Immunother. 2023;46(9):351-354.
- Long GV, et al. Neoadjuvant triplet immune checkpoint blockade in newly diagnosed glioblastoma. Nat Med. 2025;31:1557-1566.
- Yuen CA, Pekmezci M, Bao S, Kong XT. Metastatic glioblastoma to the lungs: a case report and literature review. CNS Oncol. 2024;13(1):2351789.
