ไกลโอบลาสโตมา (GBM) เป็นแอสโตรไซโตมา WHO เกรด 4 ซึ่งเป็นเนื้องอกสมองชนิดร้ายแรงปฐมภูมิที่พบบ่อยที่สุดในผู้ใหญ่
อาการทางประสาทจักษุวิทยาเกิดจาก 3 กลไก ได้แก่ การเกิดโดยตรง การแทรกซึม และการกดทับของทางเดินประสาทตา รวมถึงความดันในกะโหลกศีรษะสูง
ขึ้นอยู่กับตำแหน่ง อาจพบอาการต่างๆ เช่น ตาบอดครึ่งซีกทั้งสองข้าง ตาบอดครึ่งซีก同名 ตามัว และ RAPD
GBM ปฐมภูมิของเส้นประสาทตา พบได้น้อยมาก คิดเป็น 0.6–1.2% ของเนื้องอกสมองทั้งหมด มีรายงานใน文献เพียงประมาณ 70 ราย
การรักษามาตรฐานคือ Stupp protocol (ผ่าตัด + ฉายรังสี 60 Gy + temozolomide) อายุร median survival ประมาณ 14.6 เดือน
การวินิจฉัย首选 MRI with contrast และการวินิจฉัยยืนยันต้องอาศัยการตรวจชิ้นเนื้อทางพยาธิวิทยา
การคลายการกดทับ optic chiasm อาจช่วยให้การมองเห็น ดีขึ้น แต่ในกรณีที่เส้นประสาทตา ฝ่อมากแล้วพยากรณ์โรคไม่ดี
ไกลโอบลาสโตมา มัลติฟอร์ม (Glioblastoma multiforme; GBM) เป็นแอสโตรไซโตมาที่จัดอยู่ในระดับ 4 ตามเกณฑ์ของ WHO ซึ่งเป็นมะเร็งสมองชนิดปฐมภูมิที่พบบ่อยที่สุดในผู้ใหญ่ อุบัติการณ์ในสหรัฐอเมริกาอยู่ที่ประมาณ 3 รายต่อประชากร 100,000 คน โดยมีการวินิจฉัยมากกว่า 10,000 รายต่อปี คิดเป็นร้อยละ 12–15 ของเนื้องอกสมองทั้งหมด และร้อยละ 45.2 ของเนื้องอกระบบประสาทส่วนกลางชนิดร้ายแรง3) อายุเฉลี่ยเมื่อวินิจฉัยคือ 64 ปี และอัตราส่วนเพศชายต่อหญิงคือ 1.5:1
อาการทางประสาทจักษุวิทยาเกิดจากกลไกอย่างใดอย่างหนึ่งหรือหลายอย่างร่วมกันดังต่อไปนี้
การเกิดหรือการแทรกซึมโดยตรง : การเกิดหรือการแทรกซึมของเนื้องอกโดยตรงที่เส้นประสาทตา ออปติกไคแอสมา หรือออปติกแทรกต์การกดทับ : การกดทับทางเดินประสาทตาจากผลของก้อนเนื้องอกต่อโครงสร้างโดยรอบความดันในกะโหลกศีรษะสูง : ภาวะ papilledema ที่เกิดจากความดันในสมองสูงขึ้นเนื่องจากเนื้องอก
GBM ปฐมภูมิของเส้นประสาทตา พบได้น้อยมาก คิดเป็น 0.6–1.2% ของเนื้องอกสมองทั้งหมด และมีรายงานในเอกสารเพียงประมาณ 70 ราย1) เนื้องอกเส้นประสาทตา ชนิดผู้ใหญ่มีระดับความร้ายแรงสูง พบได้บ่อยในชายวัยกลางคน การพยากรณ์โรคด้านอายุขัยประมาณ 6 เดือน ซึ่งแตกต่างอย่างสิ้นเชิงจากชนิดในเด็ก
กรณีที่ลุกลามไปยังทางเดินประสาทตา อายุขัยเฉลี่ยประมาณ 8 เดือน ซึ่งสั้นกว่า GBM ที่ไม่เกี่ยวข้องกับทางเดินประสาทตาที่มีอายุขัยเฉลี่ย 14.6 เดือน
Q
การเกิดของไกลโอบลาสโตมาในทางเดินประสาทตาพบได้น้อยเพียงใด?
A
GBM ชนิดปฐมภูมิของเส้นประสาทตา คิดเป็น 0.6–1.2% ของเนื้องอกในสมองทั้งหมด โดยมีรายงานในเอกสารทั่วโลกเพียงประมาณ 70 ราย1) เป็นภาวะที่พบได้ยากมาก และต้องระวังว่าการวินิจฉัยอาจล่าช้าได้ง่าย
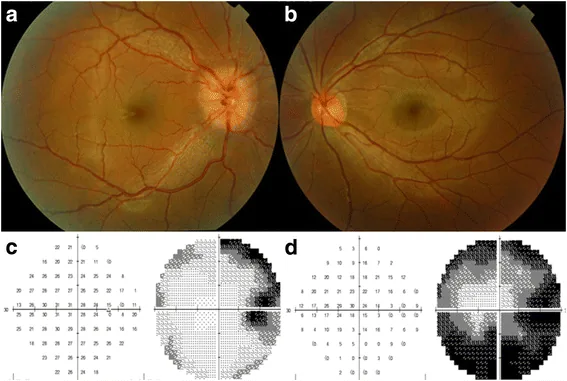
??????????????????? Chia-Ying Lin, Hsiu-Mei Huang. Unilateral malignant optic glioma following glioblastoma multiforme in the young: a case report and literature review. BMC Ophthalmology. 2017 Mar 11; 17:21. Figure 1. PM
CI D: PMC5346192. License: CC BY.
???????????????????????????????????????????????????????????????
การมองเห็น ลดลงเส้นประสาทตา และออปติกไคแอสมาของเส้นประสาทตา ในกรณีของออปติกไกลโอมาในผู้ใหญ่ มักเริ่มต้นด้วยการมองเห็น ลดลงในตาข้างเดียว และอาจลุกลามไปยังออปติกไคแอสมาของเส้นประสาทตา ภายในไม่กี่สัปดาห์ ส่งผลให้ตาบอดทั้งสองข้างการสูญเสียลานสายตา : มีรูปแบบที่สอดคล้องกับตำแหน่งของเนื้องอก (ดูด้านล่าง)ตาโปน : เกิดขึ้นเมื่อเนื้องอกเกิดขึ้นที่เส้นประสาทตา ในกรณีของ Brokāns ผู้ป่วยมีอาการหลักคือตาโปนซ้าย การมองเห็น ลดลง และการจำกัดการมองขึ้นด้านบนเป็นเวลา 6 เดือนก่อนมาโรงพยาบาล1) ปวดศีรษะ : เกิดจากความดันในกะโหลกศีรษะสูงหรือผลโดยตรงของเนื้องอกเห็นภาพซ้อน
ลักษณะทางจักษุประสาทวิทยาที่จำเพาะจะพบได้ขึ้นอยู่กับตำแหน่งของรอยโรคในวิถีการเห็น
รอยโรคของเส้นประสาทตา
การมองเห็น ลดลงข้างเดียวการมองเห็น ในตาข้างที่ได้รับผลกระทบ
ข้อบกพร่องของลานสายตา : จุดบอดกลาง ข้อบกพร่องของลานสายตาส่วนปลาย เป็นต้น
ความผิดปกติของการมองเห็นสี
RAPD (Relative Afferent Pupillary Defect)เส้นประสาทตา
การเปลี่ยนแปลงใน Optical Coherence Tomography (OCT ) : ตรวจพบได้จากการบางลงของชั้นเส้นใยประสาทจอตาและความเสียหายของ GCL 1)
ออปติกไคแอสมาและบริเวณหลังออปติกไคแอสมา
ตาบอดครึ่งซีกข้างขมับทั้งสองข้าง (Bitemporal hemianopia) : เกี่ยวข้องกับออปติกไคแอสมาอาจมีจังก์ชันสโกโตมาร่วมด้วย
ตาบอดครึ่งซีกข้างเดียวกันฝั่งตรงข้าม (Homonymous hemianopia) : เกี่ยวข้องกับส่วนหลังของออปติกไคแอสมา (optic tract และ optic radiation)
ฝ่อของเส้นประสาทตา แบบแถบ (Band optic atrophy)RAPD ฝั่งตรงข้ามเมื่อเกี่ยวข้องกับ optic tract ลักษณะเด่นคือหัวประสาทตาซีดบริเวณขมับและจมูกส่วนกลาง
RAPD แบบเทคตัล (Tectal RAPD )RAPD โดยไม่มีความบกพร่องทางการมองเห็น
ภาวะ papilledema จากความดันในกะโหลกศีรษะสูง ในระยะแรกจะมีเพียงตามัวและตรวจพบการขยายของจุดบอด Mariotte หากเป็นต่อเนื่องนานจะทำให้เกิดการฝ่อของเส้นประสาทตา ส่งผลให้ลานตาแคบลงและการมองเห็น ลดลง
ทิศทางการถ่ายภาพ MRI ขึ้นอยู่กับตำแหน่งของรอยโรค สำหรับรอยโรคด้านหน้าของ optic chiasm จำเป็นต้องใช้ภาพ冠状断面ของเบ้าตา ส่วนรอยโรคด้านหลัง การใช้ภาพตัดขวางของสมองจะมีประโยชน์
Q
Glioblastoma ทำให้เกิดรูปแบบการสูญเสียลานตาแบบใด?
A
รูปแบบการสูญเสียลานตาขึ้นอยู่กับตำแหน่งของเนื้องอก หากเกี่ยวข้องกับเส้นประสาทตา จะเกิด central scotoma และการสูญเสียลานตาส่วนปลายข้างเดียวกัน หากเกี่ยวข้องกับ optic chiasm จะเกิด hemianopsia แบบ両耳側 (bitemporal) หากเกี่ยวข้องกับส่วนหลังของ optic chiasm (optic tract หรือ optic radiation) จะเกิด homonymous hemianopsia ฝั่งตรงข้าม
ประมาณ 95% ของ GBM เกิดขึ้นแบบประปราย และมีเพียงประมาณ 5% เท่านั้นที่เกี่ยวข้องกับกลุ่มอาการทางพันธุกรรม การเกิดแบ่งออกเป็นชนิดปฐมภูมิและทุติยภูมิ ซึ่งมีโปรไฟล์โมเลกุลที่แตกต่างกัน
การเปลี่ยนแปลงโมเลกุลหลักของชนิดปฐมภูมิและทุติยภูมิแสดงดังนี้
ประเภท การเปลี่ยนแปลงโมเลกุลหลัก ปฐมภูมิ EGFR amplification, MDM2 amplification, PTEN mutation, CDKN2A deletion ทุติยภูมิ IDH1 mutation, p53 mutation, MET amplification ทั่วไป การกระตุ้นวิถี RAS/PI3K
ปัจจัยที่เกี่ยวข้องกับความเสี่ยงของการแพร่กระจายนอกกะโหลกศีรษะ ได้แก่ การกลายพันธุ์ของ TP53, TERT, PTEN, โครโมโซม +7/−10 และชนิดเนื้อเยื่อซาร์โคมาทอยด์6) ปัจจัยเสี่ยงของการแพร่กระจายเยื่อหุ้มสมองอ่อน ได้แก่ การเปิดโพรงสมอง การผ่าตัดซ้ำ เพศชาย และการบุกรุกของเยื่อบุโพรงสมอง3)
ผลการตรวจทางอิมมูโนฮิสโตเคมีที่พบได้ทั่วไปใน GBM ของเส้นประสาทตา ได้แก่ IDH ชนิดป่า (IDH-WT), GFA P บวก, ATRX ลบ, Ki-67 20–25% 1) ซึ่งมีประโยชน์ในการยืนยันการวินิจฉัยและพยากรณ์โรค
MRI (ทางเลือกแรก) : การเพิ่มความเข้มของ T1 และสัญญาณสูงใน T2/FLAIR ร่วมกันเป็นลักษณะเฉพาะ สำหรับรอยโรคด้านหน้าของออปติกไคแอสม ควรเพิ่มการสแกนแนวโคโรนาของเบ้าตา 1) CT : ใช้สำหรับการคัดกรองและการตรวจหาการเปลี่ยนแปลงของกระดูกและการกลายเป็นปูน 1)
OCT ฝ่อของเส้นประสาทตา เล็กน้อย ซึ่งมีประโยชน์ในการประเมินรอยโรคระยะเริ่มต้นการตรวจลานสายตา การประเมิน RAPD : เป็นการตรวจที่สำคัญและง่าย ซึ่งบ่งชี้ถึงรอยโรคของเส้นประสาทตา ได้อย่างชัดเจน
การวินิจฉัยที่แน่นอนจำเป็นต้องตัดชิ้นเนื้อเพื่อตรวจทางพยาธิวิทยา รายการที่ประเมิน ได้แก่ การกลายพันธุ์ของ IDH1/2, GFA P และ Ki-67 1)
โรคที่ควรแยกวินิจฉัยจำแนกตามตำแหน่งของรอยโรคมีดังนี้
เป้าหมายคือการตัดเนื้องอกออกให้มากที่สุดเท่าที่จะทำได้อย่างปลอดภัย ใน GBM ต้นกำเนิดจากเส้นประสาทตา การตัดออกทั้งหมดมักทำได้ยากเนื่องจากอยู่ติดกับโครงสร้างการมองเห็น 1) ในญี่ปุ่น การเลือกวิธีการรักษา เช่น การสังเกต การผ่าตัด เคมีบำบัด และการฉายรังสี ขึ้นอยู่กับตำแหน่งและการแพร่กระจายของเนื้องอก
การคลายการกดทับของออปติกไคแอสมาอาจช่วยให้การมองเห็น ดีขึ้นได้ ในทางกลับกัน ในกรณีที่เส้นประสาทตา ฝ่ออย่างรุนแรง การมองเห็น มักไม่ฟื้นตัวแม้หลังคลายการกดทับ และการพยากรณ์โรคไม่ดี
โปรโตคอลการฉายรังสีมาตรฐานคือ 60 Gy แบ่งเป็น 30 ครั้ง ใน 6 สัปดาห์ 1)
ระยะฉายรังสีร่วม : ให้ 75 มก./ตร.ม./วัน พร้อมกับการฉายรังสี3) ระยะเสริม : ให้ 200 มก./ตร.ม./วัน เป็นเวลา 5 วัน ในรอบ 28 วัน3)
ตามแนวทาง Stupp protocol (การผ่าตัด + การฉายรังสี + TMZ) ค่ามัธยฐานการรอดชีวิตอยู่ที่ประมาณ 14.6 เดือน
การแพร่กระจายของเยื่อหุ้มสมองอ่อน (LMS ) เกิดขึ้นใน 2–4% (สูงสุด 15–25%) ของผู้ป่วย GBM และระยะเวลาการรอดชีวิตสั้นมากคือ 0.2–9.7 เดือน2) LMS ชนิดปฐมภูมินั้นพบได้น้อยมาก ยังไม่มีการรักษามาตรฐานที่ชัดเจน และการให้เคมีบำบัดในช่องไขสันหลังหรือการฉายรังสีเพิ่มเติมมีประสิทธิภาพจำกัด
Q
สามารถผ่าตัดเนื้องอกไกลโอบลาสโตมาของเส้นประสาทตาให้หมดได้หรือไม่?
A
เนื่องจาก GBM ปฐมภูมิของเส้นประสาทตา อยู่ติดกับโครงสร้างการมองเห็น การผ่าตัดให้หมดจึงมักทำได้ยากหากต้องรักษาการทำงานของตาไว้1) โดยทั่วไปจะทำการผ่าตัดเอาออกอย่างปลอดภัยที่สุดแล้วตามด้วยการฉายรังสีและเคมีบำบัด
เส้นทางหลักของการเจริญเติบโต การแทรกซึม และการสร้างเส้นเลือดใหม่ของ GBM คือการกระตุ้นวิถี RAS/PI3K ผ่านการเพิ่มจำนวน EGFR นอกจากนี้ สภาพแวดล้อมจุลภาคของเนื้องอกมีลักษณะเด่นคือการกดภูมิคุ้มกัน โดยการขาดการแทรกซึมของทีเซลล์ การเพิ่มขึ้นของทีเซลล์ควบคุม (Treg) และเซลล์กดภูมิคุ้มกันที่มาจากไขกระดูก (MDSC) ส่งเสริมการหลบหลีกภูมิคุ้มกัน4)
เส้นทางหลักของการแพร่กระจายคือผ่านช่องว่างใต้เยื่อหุ้มสมองชั้นอแร็กนอยด์ 3) ในการชันสูตรพลิกศพพบการแพร่กระจายไปยังไขสันหลังใน 25%
ผลกระทบต่อทางเดินสายตานั้นเกิดจาก 3 กลไกดังนี้
การเกิดโดยตรงและการแทรกซึม : การเกิดโดยตรงหรือการแทรกซึมของเนื้องอกไปยังเส้นประสาทตา ออปติกไคแอสซึม ออปติกแทรกต์ และออปติกเรดิเอชันการกดทับ : การกดทับและการเปลี่ยนรูปของทางเดินสายตาจากก้อนเนื้องอกที่อยู่ติดกันความดันในกะโหลกศีรษะสูง : เนื้องอกทำให้ความดันในสมองเพิ่มขึ้น → ภาวะคั่งเลือดในจอประสาทตา → เส้นประสาทตา ฝ่อ
以下の内容は現在研究段階、あるいは治験中のものであり、一般的な病院で受けられる標準治療ではありません。今後の医療発展に関する専門家向けの参考情報です。
LITTは46°C以上で凝固壊死を引き起こす一方、33〜43°CではBBB(血液脳関門)開放と免疫原性細胞死を誘導する4) 。
Chandarら(2023)は新規診断GBMの1例にLITTを施行し、治療後にCD8+T細胞とPD-L1の著明な増加を確認した4) 。同症例は9年間の無再発生存を達成した。
Long และคณะ (2025) ได้ให้การบำบัดด้วย ICI สามชนิด ได้แก่ nivolumab, ipilimumab และ relatlimab ก่อนผ่าตัดในผู้ป่วย GBM ที่เพิ่งได้รับการวินิจฉัย5) หลังการรักษา เซลล์ CD3+ T ที่แทรกซึมในเนื้องอกเพิ่มขึ้นจาก 9.8% เป็น 32.7% และเซลล์ T ที่ถูกกระตุ้นเพิ่มขึ้น 8.5 เท่า ผู้ป่วยหนึ่งรายไม่มีการกลับเป็นซ้ำนาน 17 เดือน และปัจจุบันมีการวางแผนการทดลอง GIANT
Q
การบำบัดด้วยภูมิคุ้มกันมีประสิทธิภาพต่อ glioblastoma หรือไม่?
A
ปัจจุบันการบำบัดด้วยภูมิคุ้มกันยังไม่ได้รับการยอมรับให้เป็นการรักษามาตรฐาน อย่างไรก็ตาม การให้ ICI สามชนิดก่อนผ่าตัดแสดงให้เห็นถึงการเพิ่มขึ้นอย่างมีนัยสำคัญของเซลล์ T ที่แทรกซึมในเนื้องอก5) ซึ่งคาดว่าจะได้รับการตรวจสอบในการทดลองทางคลินิกในอนาคต
การแพร่กระจายนอกกะโหลกศีรษะเกิดขึ้นใน 0.4–2.0% ของ GBM และระยะเวลาการรอดชีวิตหลังการแพร่กระจายมีค่ามัธยฐานเพียง 1.5 เดือน6) ลักษณะทางโมเลกุลของกรณีที่มีการแพร่กระจาย ได้แก่ การกลายพันธุ์ของ TP53, TERT และ PTEN ซึ่งกำลังถูกศึกษาในฐานะตัวบ่งชี้ทางชีวภาพ ของความเสี่ยงในการแพร่กระจาย6)
Brokāns A, Dolgopolova J, Saulītis A, et al. Optic Nerve Glioblastoma with Optic Chiasm Involvement: A Case Report and a Brief Literature Review. Medicina. 2024;60(10):1687.
Mondia MWL, Hooks RE, Maragkos GA, et al. Primary diffuse leptomeningeal glioblastoma: a case report and literature review. J Neuro-Oncol. 2025;172:265-272.
Zhang K, Yang Y, Zhuang J, et al. Intracranial dissemination of glioblastoma multiforme: a case report and literature review. J Int Med Res. 2022;50(7):03000605221112047.
Chandar JS, Bhatia S, Ingle S, et al. Laser Interstitial Thermal Therapy Induces Robust Local Immune Response for Newly Diagnosed Glioblastoma with Long Term Survival and Disease Control. J Immunother. 2023;46(9):351-354.
Long GV, et al. Neoadjuvant triplet immune checkpoint blockade in newly diagnosed glioblastoma. Nat Med. 2025;31:1557-1566.
Yuen CA, Pekmezci M, Bao S, Kong XT. Metastatic glioblastoma to the lungs: a case report and literature review. CNS Oncol. 2024;13(1):2351789.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต