İndüksiyon Tedavisi
Steroid pulsu: Metilprednizolon 1 g/gün × 3-5 gün.
Oral steroid: Prednizolon 1 mg/kg/gün’e geçildikten sonra kademeli olarak azaltılır.
Siklofosfamid: 500 mg/ay × 6 ay (NIH protokolü). Steroidlerle birlikte kullanımı standarttır.

Primer santral sinir sistemi vasküliti (PACNS), beyin, omurilik ve meninkslerin arter ve venlerinde sınırlı inflamasyonla seyreden bir vaskülittir ve sekonder CNS vaskülitinden (sistemik hastalıklarla ilişkili) açıkça ayrılır.
İlk kez 1922’de Harbitz tarafından bildirilmiş ve 1988’de Calabrese tanı kriterlerini önermiştir5).
Epidemiyolojik olarak yıllık insidansı yaklaşık 2,4/1.000.000 olan nadir bir hastalıktır1, 2). Tanı anında medyan yaş yaklaşık 50 olmakla birlikte, çocuklar dahil her yaşta görülebilir. Cinsiyet dağılımı daha önce erkeklerde 2:1 oranında fazla bildirilmiş olsa da, son yıllardaki vaka serilerinde cinsiyet farkı olmadığını bildiren çalışmalar da vardır.
Vaskülit sendromları, etkilenen damarların boyutuna göre sınıflandırılan bir kavramlar bütünüdür ve PACNS, bu grupta CNS damarlarıyla sınırlı bir alt tip olarak yer alır.
Etiyolojisi bilinmemektedir; VZV, mikoplazma gibi enfeksiyöz ajanların inflamatuar yanıtı tetiklediği öne sürülmüş ancak kesin kanıt yoktur.
PACNS, CNS ile sınırlı bir vaskülittir ve sistemik hastalıkların eşlik etmemesi ile karakterizedir. Sekonder CNS vasküliti, SLE, Sjögren sendromu, enfeksiyonlar, maligniteler gibi sistemik hastalıklarla ilişkili olarak ortaya çıkar ve çok daha sıktır. Ateş veya belirgin ESR yüksekliği varsa sekonder nedenler öncelikle düşünülmelidir.
PACNS belirtileri genellikle nonspesifiktir ve tanıda gecikmeye yol açabilir.
Çocuklarda hemiparezi (%80’e kadar), duyu kaybı (%79), ince motor bozukluk (%73) sık görülür; baş ağrısı ve bilişsel bozukluk erişkinlere göre daha azdır (%56, %37).
Zhuo ve ark. (2022) tarafından bildirilen tümör benzeri PACNS’li 5 yaşındaki kız çocuğunda sol homonim hemianopsi mevcuttu ve görüntülemede sol oksipital ve temporal loblarda kitle benzeri lezyonlar saptandı2).
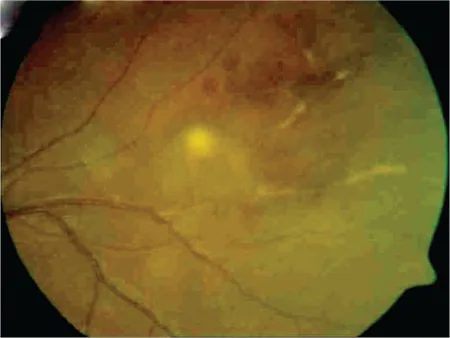
Görme yolu (optik sinir, kiazma, oksipital lob) veya okülomotor sinirler etkilendiğinde görme azalması, görme alanı defekti ve diplopi oluşur. Üveit ve retinal vaskülit PACNS’de tipik değildir; mevcutsa sistemik vaskülit gibi sekonder nedenlerin dışlanması gerekir.
PACNS’nin kesin etiyolojisi bilinmemektedir ve belirli risk faktörleri kanıtlanmamıştır.
Aşağıda sekonder CNS vaskülitinin nedenleri yer almaktadır ve PACNS tanısı konulurken dışlanması gereken hastalık gruplarıdır.
| Neden Kategorisi | Temsili Hastalıklar/Faktörler |
|---|---|
| Enfeksiyonlar | VZV, HIV, HCV, CMV, sifiliz, tüberküloz, aspergilloz |
| Bağ Dokusu Hastalıkları | SLE, RA, Sjögren sendromu, dermatomiyozit |
| Diğer Sistemik Hastalıklar | Antifosfolipid antikor sendromu, malign lenfoma, nörosarkoidoz |
| İlaç | Kokain, amfetamin, efedrin |
PACNS dışlama tanısıdır ve tek bir kesin biyobelirteç yoktur.
Calabrese & Mallek (1988) kriterleri yaygın olarak kullanılır1).
Ayrıca Rice & Scolding sınıflandırmasında “kesin” (histolojik kanıt) ve “büyük olasılık” (klinik, görüntüleme ve BOS bulgularına dayalı) olarak ikiye ayrılır5).
En önemli ayırıcı tanı RCVS’dir (Geridönüşümlü Serebral Vazokonstriksiyon Sendromu). RCVS genç erişkinlerde daha sık görülür, şiddetli tekrarlayan yıldırım baş ağrısı ile ortaya çıkar ve BOS genellikle normaldir. PACNS’den farklı olarak, RCVS’de immünosupresif tedavi kontrendikedir.
Dev hücreli arterit genellikle 60’lı yaşların sonundan itibaren baş ağrısı ile başlar ve arter biyopsisi ile doğrulanır. %25-50 oranında anterior iskemik optik nöropati eşlik ettiğinden, oftalmolojik bulguların değerlendirilmesi önemlidir.
Altın standart, beyin biyopsisi ile histolojik doğrulamadır, ancak duyarlılığı yaklaşık %75 ile yüksek değildir3). MRI, serebral anjiyografi ve BOS analizi birleştirilerek sekonder nedenler dışlandıktan sonra kapsamlı bir şekilde tanı konur. Duyarlılığın tamamlayıcı olması için birden fazla testin paralel olarak yapılması önerilir.
PACNS tedavisinde immünosupresif tedavi temel oluşturur. Nörolog ve romatolog ile multidisipliner iş birliği içinde yönetilir.
İndüksiyon Tedavisi
Steroid pulsu: Metilprednizolon 1 g/gün × 3-5 gün.
Oral steroid: Prednizolon 1 mg/kg/gün’e geçildikten sonra kademeli olarak azaltılır.
Siklofosfamid: 500 mg/ay × 6 ay (NIH protokolü). Steroidlerle birlikte kullanımı standarttır.
İdame Tedavisi
Başlangıç zamanı: İndüksiyon tedavisinden 4-6 ay sonra geçiş yapılır.
İlaç seçimi: Mikofenolat mofetil (MMF), metotreksat veya azatioprin kullanılır.
MMF doz örneği: Günde 2 kez 500 mg ile başlanır, günde 2 kez 1000 mg’a yükseltilir4).
İndüksiyon tedavisinden 4-6 ay sonra geçilir. MMF, metotreksat, azatioprin kullanılır6).
Kuruvilaa ve ark. (2022) 35 yaşında bir erkek hastada steroid + MMF (500 mg×2→1000 mg×2) ile tedaviye başlanmış ve iyi sonuç alınmıştır4).
Datyner ve ark. (2023) tarafından bildirilen 8 yaşındaki SV-cPACNS’li (GFAP antikoru pozitif) bir çocukta, Brainworks protokolüne göre deksametazon → 5 gün metilprednizolon puls → 12 ay azaltma + 7 kez CYC → MMF idame tedavisi uygulanmıştır8).
İndüksiyon tedavisi (steroid + CYC) yaklaşık 6 ay sürer, ardından MMF gibi idame tedavisine geçilir. Nüks riski nedeniyle uzun süreli takip gereklidir ve tedavi süresi vakaya göre değişir. Düzenli görüntüleme ve klinik değerlendirme ile tedavi yanıtı izlenirken doz azaltılır.
PACNS’nin üç ana histopatolojik alt tipi vardır.
Granülomatöz
Sıklık: En yaygın alt tip.
Patolojik bulgular: Damar duvarının tüm katmanlarını tutan, sınırları belirgin granülom.
Beta-amiloid ile ilişki: Vakaların %50’sine kadar beta-amiloid birikimi eşlik eder ve inflamatuar serebral amiloid anjiyopati ile örtüşme olduğu düşünülür.
Lenfositik
Patolojik bulgular: Lenfositler ve plazma hücreleri tarafından damar duvarı infiltrasyonu.
Çocuklarda özellikler: Çocukluk çağı PACNS’de lenfositik patern daha sıktır 5).
Nekrotizan
Patolojik bulgular: Damar duvarında fibrinoid nekroz.
Nadir alt tip: Eozinofilik infiltrasyon gösteren olgular da bildirilmiştir; EGPA’nın patolojik bulgularını sergiler ancak sistemik EGPA tanı kriterlerini karşılamaz 7).
Damar duvarındaki enflamasyonda, immün hücre infiltrasyonu ve sitokin-kemokin ağı merkezi rol oynar5).
Genellikle PACNS iki taraflıdır (Mayo Clinic kohort F’nin %95,6’sı iki taraflı), ancak nadiren sadece bir tarafta tekrarlayan bir alt tip bildirilmiştir. Bunun nedeninin serebral hemisferler arasındaki bağışıklık yanıtı asimetrisi olduğu düşünülmektedir ve şimdiye kadar 7 vaka bildirilmiştir10).
Vibha ve ark. (2023), yalnızca tekrarlayan fokal bilinç koruyucu nöbetler gösteren 35 yaşında bir erkekte PACNS vakası bildirdi10). Sadece fokal konvülsiyonlarla başlayan ve biyopside granülomatöz vaskülit saptanan hastada steroid + MMF ile nöbetler kayboldu.
Vasküler duvar MRG, PACNS ve RCVS’nin ayırıcı tanısında umut verici bir yöntemdir. PACNS’de vasküler duvarda kontrastlanma (inflamatuar değişiklikler) görülürken, RCVS’de genellikle görülmez. Serebral MRA’nın duyarlılığının %90-100 olduğu bildirilmiştir 1).
Tümör benzeri PACNS, tüm PACNS vakalarının yaklaşık %5’ini oluşturur ve tümörlerle görüntüleme ayrımı zordur 2). SWI (manyetik duyarlılık ağırlıklı görüntüleme) ve ASL (arteriyel spin etiketleme) kombinasyonunun ayırıcı tanıda yararlı olduğu bildirilmiştir. PACNS’de düşük perfüzyon, tümörlerde ise hiperperfüzyon eğilimi görülür.
CNS vaskülitinin %1.8’inde hidrosefali bildirilmiştir ve hastane içi ölümlerin ana nedenidir 3). PACNS ile sınırlandırıldığında son derece nadirdir ve sadece 2 vaka rapor edilmiştir. Meninkslerin fibrotik skarlaşmasına bağlı BOS akış bozukluğunun mekanizma olduğu düşünülmektedir.
Levit ve ark. (2023), kompleman faktör I (CFI) eksikliğine bağlı kompleman aracılı CNS vasküliti olan bir olgu bildirdi9). CFI, C3b ve C4b’yi inaktive ederek C3 dönüştürücü enzim oluşumunu baskılar; ancak eksikliğinde alternatif yolak anormal şekilde aktive olur ve nötrofilik vaskülit gelişir. IL-1 inhibitörü anakinra uygulamasından sonra 20 ay boyunca nüks gözlenmemiştir.