BALAD คือการแยกชั้นในจอตาที่เกิดขึ้นในไมออยด์ของส่วนในเซลล์รับแสง (ระหว่าง ELM และ EZ ) ซึ่งเป็นตัวบ่งชี้ทางชีวภาพ ที่วินิจฉัยด้วย OCT พบได้ในโรคต่างๆ เช่น ม่านตาอักเสบ (โรคโวกท์-โคยานางิ-ฮาราดา, จอประสาทตา อักเสบชนิด acute posterior multifocal placoid pigment epitheliopathy), จอประสาทตา เสื่อมชนิดเปียกที่สัมพันธ์กับอายุ, CSC R, จอประสาทตาลอก เป็นต้น
อัตราการเกิดในโรคโวกท์-โคยานางิ-ฮาราดาสูงถึง 47% เป็นตัวบ่งชี้ระยะเฉียบพลันของการอักเสบและการขับสาร
อาการที่ผู้ป่วยรับรู้ขึ้นอยู่กับโรคพื้นฐาน และมักพบครั้งแรกจากการตรวจ OCT
หลักการรักษาคือจัดการกับโรคพื้นฐาน และมักหายไปเมื่อรักษาอย่างเหมาะสม
BALAD ที่สัมพันธ์กับ nAMD ทำให้เกิดพังผืดใต้จอประสาทตา ใน 77% ของกรณีภายใน 4 ปี จึงเป็นเครื่องหมายพยากรณ์โรคที่ไม่ดี ภาวะชั้นเซลล์รูปแท่ง และรูปกรวยหลุดลอก (Bacillary Layer Detachment; BALAD ) คือการแยกตัวภายในจอประสาทตา ที่เกิดขึ้นระหว่างเยื่อจำกัดชั้นนอก (ELM) และบริเวณอิลลิปซอยด์ (EZ ) ซึ่งก็คือบริเวณไมออยด์ของส่วนในของเซลล์รับแสง (myoid zone; MZ) เป็นการตรวจพบจากการทำ OCT 5)
คำว่า “bacillary” มาจากคำจำกัดความของนักประสาทกายวิภาคศาสตร์ Polyak ในปี 1941 ที่เรียกส่วนในและส่วนนอกของเซลล์รับแสง (IS-OS) ว่า “ชั้นเซลล์รูปแท่ง ” BALAD ได้รับการตั้งชื่ออย่างเป็นทางการในปี 2018 เมื่อ Mehta และคณะรายงานการตรวจพบ OCT นี้ในผู้ป่วยโรคทอกโซพลาสมาและโรคพาคิคอรอยด์ 1),3),5),9)
อุบัติการณ์พบได้น้อย แต่รายงานเพิ่มขึ้นทุกปี ในกลุ่มผู้ป่วย nAMD อุบัติการณ์ 4.5% (20 จาก 442 ตา) และในการศึกษา HAWK รายงาน 7.2%4) ในโรคโวกท์-โคยานางิ-ฮาราดา อัตราการเกิดสูงถึง 47%9) และความถี่แตกต่างกันมากตามประเภทโรค ความถี่จำแนกตามโรคที่รายงานคือ VKH 47%, APMPPE 11%, จักษุอักเสบจากภูมิคุ้มกันร่วม 7.3%, หลอดเลือดใหม่คอรอยด์ 6.2%, ทอกโซพลาสมา 5.5%, AIm 5.5%9)
ทั้งนี้ รายงานแรกเกี่ยวกับ “การสะสมของเหลวในจอประสาทตา ชั้นนอก” คือการศึกษาของ Maruyama & Kishi ในปี 2009 ในผู้ป่วยโรคโวกท์-โคยานางิ-ฮาราดา9)
Q
BALAD พบได้บ่อยแค่ไหนในการตรวจ OCT?
A
ใน nAMD พบ 4.5–7.2% ในโรคโวกท์-โคยานางิ-ฮาราดาพบสูงถึง 47% เป็นการตรวจพบที่พบได้น้อยแต่สำคัญ และมักปรากฏในระยะเฉียบพลัน/ระยะขับสารของโรค
อาการที่ผู้ป่วยรับรู้ขึ้นอยู่กับโรคพื้นฐาน ตัวอย่างทั่วไปแสดงไว้ด้านล่าง
สายตาลดลง : อาการหลักที่พบบ่อยที่สุด ใน BALAD ที่สัมพันธ์กับ nAMD ค่าเฉลี่ยของสายตาที่ดีที่สุดที่แก้ไขแล้วคือ 20/138 ช่วงตั้งแต่ CF ถึง 20/400 1),4),5) ภาพบิดเบี้ยว BALAD เกิดขึ้นใกล้รอยบุ๋มจอตา จุดบอดกลาง รอยบุ๋มจอตา จุดลอย : ในโรคอักเสบ เกิดขึ้นเมื่อมีขุ่นในวุ้นตา
โรคอักเสบ (เช่น ทอกโซพลาสมา โรคโวกต์-โคยานางิ-ฮาราดะ ) มักมีอาการเริ่มต้นเฉียบพลัน 3),6) ในขณะที่โรคเสื่อมหรือโรคที่มีพื้นฐานจากเส้นเลือดใหม่ในคอรอยด์ (CNV ) จะมีอาการดำเนินไปอย่างช้าๆ
การวินิจฉัย BALAD ทำโดย OCT ผลการตรวจที่มีลักษณะเฉพาะแสดงดังต่อไปนี้
โครงสร้างของ BALAD
ตำแหน่งของโพรงสะท้อนต่ำ : โพรงแยกที่เกิดขึ้นระหว่าง ELM และ EZ (ไมออยด์ของส่วนในเซลล์รับแสง ) 5)
ลักษณะการสะท้อนภายในโพรง : ประกอบด้วยสารสะท้อนสูงลอยตัวที่มีการสะท้อนปานกลาง 1),4)
รูปร่าง : รูปร่างคล้ายลูกแพร์ที่มีฐานเป็นมุมแหลม (รูปร่าง piriform) เป็นลักษณะเฉพาะ
การเกิดร่วมกับ SRF : มักมีของเหลวใต้จอตา (SRF) ร่วมด้วย 5)
ภาพถ่ายหลายรูปแบบ
FAF 1)
OCTA AMD สามารถตรวจพบเส้นเลือดใหม่ใต้จอประสาทตา ได้ 4)
ตำแหน่งที่พบบ่อย : โฟเวีย > พาราโฟเวีย > รอบหัวประสาทตา
ตัวอย่าง CRT : ในผู้ป่วย nAMD 3 ราย พบ 929 μm, 598 μm และ 543 μm ตามลำดับ 4)
พบคอรอยด์หนา ตัวใน 93.8% ของผู้ป่วย BALAD 8)
มีสองชนิดย่อยของ BALAD ที่เกิดร่วมกับจอประสาทตาลอก ชนิดมีรอยฉีกขาด (RRD) 2)
ชนิดหลังคาโฟเวียสมบูรณ์ : ชนิดที่รักษาหลังคาโฟเวียไว้ได้ คาดว่าฟื้นตัวได้ดีด้วยการอัดลูกตาชนิดแผ่นบาง (ชนิดสูญเสียหลังคาโฟเวีย) : ชนิดที่สูญเสียหลังคาโฟเวีย มีความเสี่ยงที่จะ发展为รอยยุบจอประสาทตา ทะลุตลอดความหนา (FTMH)
Q
จะแยก BALAD ออกจากจอประสาทตาลอกชนิดน้ำใส (SRF) ทั่วไปใน OCT ได้อย่างไร?
A
SRF คือช่องว่างของเหลวสะท้อนต่ำที่เกิดขึ้นระหว่าง RPE และจอประสาทตา ชั้นประสาท ส่วน BALAD คือการแยกตัวที่เกิดขึ้นระหว่าง ELM และ EZ (ไมออยด์) และยังแตกต่างตรงที่มีสารสะท้อนปานกลางถึงสูงภายในช่องว่าง การประเมินต้องพิจารณาทั้งตำแหน่งและลักษณะการสะท้อนร่วมกัน
BALAD ไม่ใช่โรคเดียว แต่พบในกลุ่มโรคที่ต่างกันซึ่งมีลักษณะ OCT ร่วมกัน
โรคอักเสบ
ติดเชื้อ (ชนิดไม่เป็นเม็ด) : จอประสาทตา อักเสบจากทอกโซพลาสมา 3) , เยื่อบุตาอักเสบจากเชื้อรา ภายในร่างกาย 9)
ติดเชื้อ (ชนิดเป็นเม็ด) : คอรอยด์ อักเสบแบบคดเคี้ยวจากวัณโรค (SLC) 6)
ไม่ติดเชื้อ : โรคโวกต์-โคยานางิ-ฮาราดา, โรคตาอักเสบซิมพาเทติก, โรคอีพิทีลิโอพาธีรงควัตถุแบบแผ่นหลายจุดเฉียบพลันหลัง, AIm. ที่เกี่ยวข้องกับโควิด-19 (การใช้สเตียรอยด์ + ภาวะอักเสบทั่วร่างกาย) 8)
โรคเสื่อมและโรคหลอดเลือด
จอประสาทตา เสื่อมตามอายุชนิดเปียก (nAMD )1),4),5)
ที่เกี่ยวข้องกับพาคิคอรอยด์ : CSC R (จอประสาทตา อักเสบจากซีรั่มส่วนกลาง) 7),8) . ในสายตายาว สูง แกนสั้น → คอรอยด์ คั่งเลือด → CSC R อาจนำไปสู่ BALAD 7)
โรคหลอดเลือดอื่นๆ : จอประสาทตา จากความดันโลหิตสูง, ครรภ์เป็นพิษ, จอประสาทตา จากเบาหวาน, เส้นเลือดดำจอประสาทตา อุดตัน 5)
เนื้องอก การบาดเจ็บ และยา
เนื้องอก : กระดูกคอรอยด์ , มะเร็งต่อมน้ำเหลืองคอรอยด์ , การแพร่กระจายไปยังคอรอยด์
การบาดเจ็บ : การบาดเจ็บแบบทื่อ, คอรอยด์ แตก, จอประสาทตาลอก แบบมีรอยฉีกขาด 2)
ที่เกิดจากยา : ดาบราเฟนิบ, ทราเมทินิบ (ยายับยั้ง MEK/BRAF)
การจัดการโรคพื้นฐานช่วยป้องกัน BALAD ผู้ป่วยจอประสาทตา เสื่อมตามอายุชนิดเปียกควรรับการรักษาด้วยยาต้าน VEGF อย่างสม่ำเสมอ หากเกิดการมองเห็น ลดลงหรือภาพบิดเบี้ยว ขณะใช้สเตียรอยด์ (ทั่วร่างกายหรือในลูกตา) ให้ไปพบจักษุแพทย์ทันที
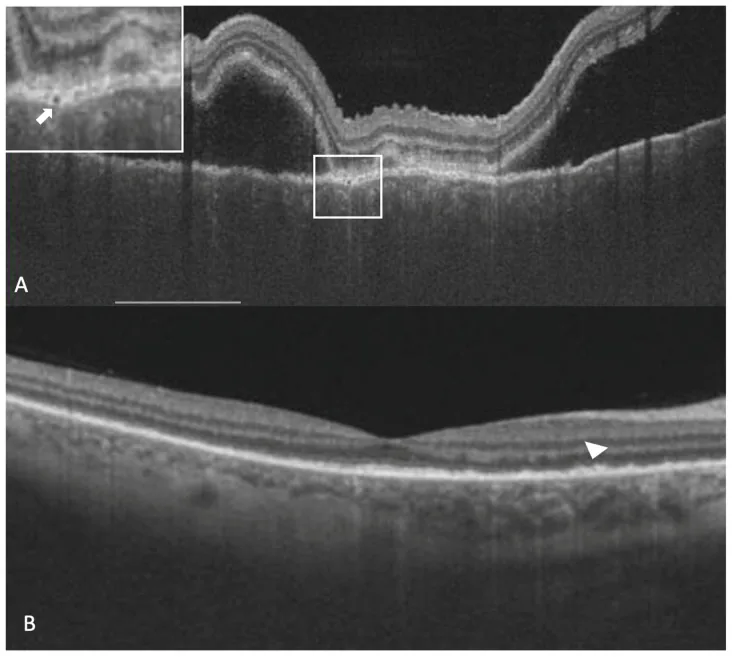
ภาพการหลุดลอกของชั้นเซลล์รูปแท่ง Ninan Jacob; Mudit Tyagi; Jay Chhablani; Raja Narayanan; Anup Kelgaonkar; Mukesh Jain. Retinal Pigment Epithelial Characteristics in Acute and Resolved Vogt-Koyanagi-Harada Disease. J Clin Med. 2023 Mar 19; 12(6):2368 Figure 3. PM
CI D: PMC10054856. License: CC BY.
หญิงอายุ 26 ปี ได้รับการวินิจฉัยว่าเป็นโรคโวกต์-โคยานางิ-ฮาราดาเฉียบพลัน ตาขวาแสดงของเหลวใต้จอประสาทตา คอรอยด์หนา เยื่อบุผิวรงควัตถุจอประสาทตา (RPE ) หนา และช่องว่างใน RPE (ลูกศรสีขาวในกรอบสีขาวที่มุมซ้ายบน) ในการตรวจเอกซเรย์เชื่อมโยงแสงแนวตั้ง (A) หลังจากของเหลวใต้จอประสาทตา หายไป จะเห็นคราบสะสมถาวรบน RPE (หัวลูกศร) (B)
OCT (SD-OCT , SS-OCT )BALAD ระบุโพรงสะท้อนต่ำระหว่าง ELM และ EZ 5) .การตรวจและถ่ายภาพจอประสาทตา : พบรอยนูนขอบเขตชัดเจนที่รอยบุ๋มจอประสาทตา คล้าย SRFFAF 1) .FFA : การเรืองแสงสูงเนื่องจากการสะสมของสีในโพรง BALAD ICGA คอรอยด์ ไม่เพียงพอ มีประโยชน์ในการประเมินโรค Vogt-Koyanagi-Harada และโรคแกรนูโลมาOCTA AMD ตรวจหาเส้นเลือดใหม่ในคอรอยด์ 4),5) .
ด้านล่างคือการแยก BALAD ออกจากโรคที่มีผล OCT คล้ายกัน
โรค ตำแหน่งโพรง การสะท้อนภายในโพรง BALAD ระหว่าง ELM และ EZ การสะท้อนปานกลาง SRF/SRD ระหว่าง RPE และจอประสาทตา ชั้นประสาท การสะท้อนต่ำ (ไม่มีเสียงสะท้อน) จอประสาทตาฉีกขาด ภายในชั้นจอประสาทตา ส่วนประสาท มีเส้นใยเชื่อมต่อ
ไม่มีการรักษาเฉพาะสำหรับ BALAD โดยตรง การรักษาโรคพื้นฐานจะทำให้ BALAD หายไป .
แสดงระยะเวลาการหายไปของ BALAD สำหรับแต่ละโรค.
โรคพื้นฐาน การรักษา ระยะเวลาที่ BALAD หายไป nAMD การฉีดยา anti-VEGF หายไปอย่างรวดเร็ว โรค VKH Methylprednisolone ทางหลอดเลือดดำ 2-5 วัน ทอกโซพลาสมา TMP-SMX + สเตียรอยด์ ภายใน 1 สัปดาห์ SLC วัณโรค ATT + เพรดนิโซน ประมาณ 2 เดือน CSC Rการจี้ด้วยเลเซอร์ ประมาณ 16 วัน
การรักษาทางเลือกแรกสำหรับ nAMD คือการฉีดยา anti-VEGF เข้าแก้วตา และ BALAD จะหายไปอย่างรวดเร็วหลังการรักษา1),4),5) ยาและขนาดยาหลักมีดังนี้5)
bevacizumab : 1.25 มก./0.05 มล.ranibizumab : 0.5 มก./0.05 มล.aflibercept : 2.0 มก./0.05 มล.
Jung JJ และคณะ (2021) รายงานผู้ป่วย 2 รายที่ BALAD หายไปอย่างสมบูรณ์หลังการฉีด bevacizumab เพียงครั้งเดียว5) รายแรกดีขึ้นจาก 20/80 เป็น 20/25 รายที่สองจาก 20/160 เป็น 20/50 นอกจากนี้ยังมีรายงานผู้ป่วยที่ CRT ลดลงจาก 929 μm เหลือ 310 μm หลังการให้ aflibercept 6 ครั้ง และสายตาที่ดีที่สุดดีขึ้นจาก CF เป็น 20/504)
Desai & Tyagi (2023) รายงานว่าในจอประสาทตา อักเสบจากทอกโซพลาสมา การใช้ TMP-SMX (160/800 มก. วันละสองครั้ง 2 เดือน) เพียงอย่างเดียวทำให้การอักเสบยังคงอยู่และ BALAD ขยายใหญ่ขึ้น แต่การเพิ่ม prednisolone 50 มก./วัน ทำให้ BALAD หายไปภายใน 1 สัปดาห์ 3)
สำหรับ SLC จากวัณโรค มีรายงานว่า BALAD หายไปภายใน 2 เดือนด้วย ATT (rifampicin + isoniazid + pyrazinamide + ethambutol) + prednisone 60 มก./วัน 6)
มีรายงาน BALAD ที่เกี่ยวข้องกับ CSC R จากสายตายาว สูงได้รับการรักษาด้วยเลเซอร์ จับตัว (532 nm, 250 μm, 50 mW, 200 ms) และ BALAD หายไปภายใน 16 วัน 7) ใน CSC R ที่ใช้สเตียรอยด์ ควรพิจารณาหยุดสเตียรอยด์ 8)
การเลือกวิธีการผ่าตัดสำหรับ BALAD ที่เกี่ยวข้องกับจอประสาทตาลอก แบบมีรอยฉีกขาดขึ้นอยู่กับชนิดย่อย 2)
ชนิดหลังคาฟอฟเวียสมบูรณ์ : การฟื้นฟูการมองเห็น ที่ดีด้วยการอัดลูกตา (สายตาที่ดีที่สุดที่แก้ไขแล้ว 20/200→20/25, ความหนาฟอฟเวีย 80→166 μm)ชนิดชั้นบาง : เนื่องจากเสี่ยงต่อการ发展为 FTMH หลังการอัดลูกตา แนะนำให้ทำ vitrectomy + ลอก ILM + วิธี inverted flap
มีรายงาน BALAD หายไปภายใน 3 สัปดาห์ด้วยการฉีด voriconazole เข้าแก้วตา 100 μg/0.05 mL ร่วมกับยาต้านเชื้อราทั่วร่างกาย 9)
แม้ BALAD จะหายไป แต่สามารถกลับมาได้อีกหากโรคพื้นเดิมกำเริบ ควรติดตาม OCT อย่างสม่ำเสมอ
ในกรณี BALAD ที่เกี่ยวข้องกับ nAMD มีรายงานว่า 77% เกิดพังผืดใต้จอประสาทตา ภายใน 4 ปี 4) จึงต้องระวังพยากรณ์การมองเห็น ระยะยาว
หากใช้สเตียรอยด์ ใน CSC R BALAD อาจขยายใหญ่ขึ้น ควรตรวจสอบประวัติการใช้สเตียรอยด์
Q
BALAD รักษาหายได้หรือไม่?
A
BALAD มักหายไปเมื่อรักษาโรคพื้นฐาน ใน nAMD BALAD หายไปด้วยการฉีด anti-VEGF ในโรคอักเสบด้วยสเตียรอยด์ หรือยาปฏิชีวนะ อย่างไรก็ตาม แม้ BALAD จะหายไป อาจยังคงมีความบกพร่องทางการมองเห็น ระยะยาว เช่น 77% ของผู้ป่วย nAMD เกิดพังผืดใต้จอประสาทตา ภายใน 4 ปี 4)
ส่วนใน (IS) แบ่งตามหน้าที่ออกเป็นสองโซน
โซนไมออยด์ (MZ) : ประกอบด้วยกอลจิ บอดี ไรโบโซม และเอนโดพลาสมิกเรติคูลัม (ER) มีโครงสร้างไม่แข็งแรงเท่า ELM และ EZ และมีแนวโน้มเกิดการแยกตัวเทียมในชิ้นเนื้อ 5),9) โซนเอลลิปซอยด์ (EZ ) : ประกอบด้วยไมโตคอนเดรียหนาแน่น ก่อให้เกิดเส้นสะท้อนสูงใน OCT
ความอ่อนแอทางโครงสร้างของ MZ เป็นพื้นฐานทางกายวิภาคของการเกิด BALAD
Mehta และคณะเสนอปัจจัยสองประการในการเกิด BALAD 5)
แรงดันน้ำที่เพียงพอจากคอรอยด์ : แรงดันน้ำที่สูงจากคอรอยด์ ส่งเสริมการสะสมของเหลวในจอประสาทตา จุดอ่อนโครงสร้างของ MZ : MZ ระหว่าง ELM และ EZ เป็นระนาบการแยกตัวที่เปราะบางที่สุด
การไหลเข้าของของเหลวที่มีโปรตีนสูงอย่างรวดเร็วผ่านความบกพร่องของ RPE /เยื่อบรูค ทำให้ ELM ยกตัวขึ้น เลือดออกใต้จอประสาทตา ทำให้เกิดการยึดเกาะของไฟบรินระหว่าง EZ และ RPE ทำให้เกิดการแยกตัวใน MZ 5)
พบความหนาของคอรอยด์ ใน 93.8% ของผู้ป่วย BALAD 8) ในโรค Vogt-Koyanagi-Harada และ acute posterior multifocal placoid pigment epitheliopathy ภาวะขาดเลือดของคอรอยด์ 被认为กระตุ้นให้เกิด BALAD
เชื่อว่าแรงในแนวสัมผัสที่จุดรับภาพทำให้ Müller cell cone แตก ส่งผลให้เยื่อจำกัดชั้นนอกหลุดออกและเกิดการแยกตัวในชั้น myoid 2)
Govetto และคณะ (2023) เสนอความเป็นไปได้ของ “กลไกการสร้างรอยบุ๋ม” ซึ่งเซลล์รูปกรวย ที่แข็งแรงในพาราฟอเวียเคลื่อนที่เข้าสู่ศูนย์กลางเพื่อสร้างรอยบุ๋มขึ้นใหม่ในระหว่างการซ่อมแซม BALAD หลังจอประสาทตาลอก ชนิดมีรอยฉีกขาด 2) เนื่องจากเซลล์รูปกรวย หลังการแบ่งตัวไม่สามารถเพิ่มจำนวนได้ สมมติฐานนี้จึงเสนอว่าการสร้างรอยบุ๋มใหม่เกิดจากการเคลื่อนที่ ไม่ใช่การสร้างใหม่
Q
เหตุใดการแยกตัวจึงเกิดขึ้นที่ myoid ของส่วนในเซลล์รับแสง?
A
ชั้น myoid (MZ) ไม่แข็งแรงทางโครงสร้างเท่ากับเยื่อจำกัดชั้นนอกหรือชั้น ellipsoid และเป็นจุดอ่อนทางกายวิภาค เป็นที่ทราบกันดีว่าการแยกตัวเทียมเกิดขึ้นได้ง่ายที่ตำแหน่งนี้ในชิ้นเนื้อทางจุลกายวิภาค 5),9) เมื่อมีความดันน้ำจากคอรอยด์ เพิ่มขึ้น จะเกิดการแยกตัวที่จุดอ่อนนี้ ทำให้เกิด BALAD
Flindris และคณะ (2025) รายงานว่า BALAD ที่เกี่ยวข้องกับ nAMD เป็นตัวบ่งชี้ทางชีวภาพ ที่แสดงฟีโนไทป์ของโรคที่รุนแรง 4) ดวงตาที่มี nAMD และ BALAD แสดงให้เห็นว่า 77% เกิดพังผืดใต้จอประสาทตา ภายใน 4 ปี สิ่งนี้ชี้ให้เห็นว่า BALAD ไม่ใช่เพียงแค่การตรวจพบจาก OCT แต่สามารถใช้เป็นตัวบ่งชี้พยากรณ์โรคได้
พบการฟื้นตัวแบบค่อยเป็นค่อยไปของชั้น ellipsoid และชั้น interdigitation ในมากกว่าครึ่งหนึ่งของกรณี BALAD 9) เนื่องจากเซลล์รูปกรวย หลังการแบ่งตัวไม่สามารถเพิ่มจำนวนได้ กลไกการสร้างรอยบุ๋มที่กล่าวถึงข้างต้น (การสร้างรอยบุ๋มใหม่โดยการเคลื่อนที่เข้าสู่ศูนย์กลาง) อาจเป็นกุญแจสำคัญในการฟื้นตัว 2)
มีรายงานการเกิดเส้นเลือดใหม่ในคอรอยด์ หลังจากการหายไปของ BALAD ที่เกี่ยวข้องกับเยื่อบุตาอักเสบจากเชื้อรา ภายในตา 9) ซึ่งบ่งชี้ว่า BALAD อาจสร้างพื้นฐานสำหรับเส้นเลือดใหม่ในคอรอยด์ ผ่านการทำลายชั้นนอกของจอประสาทตา
ความสัมพันธ์ทางจุลพยาธิวิทยาที่แน่นอนของ BALAD ยังไม่ได้รับการยืนยัน 1),4),5) ปัจจุบันส่วนใหญ่เป็นรายงานผู้ป่วยหรือชุดผู้ป่วยขนาดเล็ก และจำเป็นต้องมีการศึกษาไปข้างหน้าขนาดใหญ่เพื่ออธิบายประวัติธรรมชาติและปัจจัยพยากรณ์โรคของ BALAD
Palmieri F, Younis S, Raslan W, Fabozzi L. Bacillary layer detachment in neovascular age-related macular degeneration: case series. Biomedicines. 2023;11(3):988.
Govetto A, Radice P, Lucchini S, et al. Recovery of bacillary layer detachment associated with macula-off rhegmatogenous retinal detachment: evidence of foveation mechanisms? Am J Ophthalmol Case Rep. 2023;32:101923.
Desai A, Tyagi M. Bacillary layer detachment as an inflammatory biomarker in toxoplasmosis retinochoroiditis: serial evolution on optical coherence tomography. BMJ Case Rep. 2023;16:e256629.
Flindris K, Gorgoli K, Koumpoulis I. A case series of bacillary layer detachment (BALAD ) in neovascular age-related macular degeneration (nAMD ): a novel optical coherence tomography (OCT ) biomarker. Cureus. 2025;17(11):e96819.
Jung JJ, Soh YQ, Yu DJG, et al. Bacillary layer detachment due to macular neovascularization. Retina. 2021;41(10):2106-2114.
Socci da Costa D, Gomes e Silva A, Melichar A, et al. Bacillary layer detachment in serpiginous-like choroiditis of presumed intraocular tuberculosis: report of two cases. Am J Ophthalmol Case Rep. 2022;27:101653.
Murillo SA, Medina SP, Romero RM, Murillo FH. Bacillary layer detachment in an atypical case of central serous chorioretinopathy associated with high hyperopia. Case Rep Ophthalmol. 2022;13:504-510.
Fuganti RM, Casella AM, Roisman L, et al. Case series bacillary layer detachment associated with acute central serous chorioretinopathy in patients with COVID-19. Am J Ophthalmol Case Rep. 2022;28:101690.
Cox JT, Wu F, Rossin EJ, Tang WM, Eliott D. Bacillary layer detachment associated with endogenous fungal endophthalmitis. J VitreoRetinal Diseases. 2022;6(4):316-319.