Aniridia fibrosis syndrome (AFS) เป็นภาวะแทรกซ้อนที่พบได้ยากในผู้ป่วย aniridia แต่กำเนิดหลังการผ่าตัดตา
เยื่อพังผืดก่อตัวจากรากม่านตา ที่หลงเหลือ ทำให้เลนส์แก้วตาเทียม เคลื่อนที่ เยื่อบุกระจกตา ล้มเหลว และความดันลูกตาต่ำ
การมองเห็น ลดลงแบบไม่เจ็บปวดและค่อยเป็นค่อยไป มักทำให้การวินิจฉัยล่าช้าการวินิจฉัยใช้กล้องจุลทรรศน์ชีวภาพแบบร่องกราดเป็นหลัก หากกระจกตา ขุ่น จำเป็นต้องใช้กล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (UBM )
การรักษาหลักคือการตัดเยื่อพังผืดออกโดยการผ่าตัดตั้งแต่เนิ่นๆ และการถอดเลนส์แก้วตาเทียม (IOL ) พร้อมกันช่วยป้องกันการกลับเป็นซ้ำ
การเกิดพังผืดสามารถดำเนินไปโดยไม่มีการอักเสบที่ตรวจพบได้ทางคลินิก ดังนั้นการติดตามผลหลังผ่าตัดอย่างสม่ำเสมอจึงสำคัญ
กลุ่มอาการพังผืดในตาที่ไม่มีม่านตา (aniridic fibrosis syndrome, AFS) เป็นภาวะแทรกซ้อนที่พบได้ยากซึ่งเกิดขึ้นหลังการผ่าตัดตาในผู้ป่วยที่ไม่มีม่านตา แต่กำเนิด (congenital aniridia) 1)
เยื่อพังผืดจะก่อตัวจากรากม่านตา ที่เหลืออยู่ (rudimentary iris root) และสามารถลุกลามไปยังเลนส์แก้วตาเทียม ซิลิอารีบอดี และจอประสาทตา ส่วนหน้า Tsai และคณะรายงานผู้ป่วย 7 ตาใน 6 รายเป็นครั้งแรกในปี 2005 ภายใต้ชื่อ “กลุ่มอาการพังผืดส่วนหน้าลุกลามหลังผ่าตัดในผู้ป่วยที่ไม่มีม่านตา แต่กำเนิด” 1) ณ เวลาที่มีรายงานผู้ป่วยที่เป็นพื้นฐานของบทความนี้ (Banifatemi et al. 2024) มีรายงานทั่วโลกเพียง 19 ราย 1)
การไม่มีม่านตา แต่กำเนิดเป็นโรคตาทั่วลูกตาที่มีลักษณะเฉพาะคือการขาดหายไปของเนื้อเยื่อม่านตา บางส่วนหรือทั้งหมด 1)
อุบัติการณ์อยู่ที่ 1:64,000 ถึง 1:96,000 1) 90% ของผู้ป่วยเกิดจากการกลายพันธุ์ของยีน PAX6 (11p13) โดยมีรูปแบบการถ่ายทอดทางพันธุกรรมแบบออโตโซมัลเด่น (penetrance สูง) 1) สองในสามของทั้งหมดเป็นแบบครอบครัว และหนึ่งในสามเป็นแบบประปราย 1)
การไม่มีม่านตา แต่กำเนิดนอกจากการขาดหายไปของม่านตา แล้ว ยังมีภาวะแทรกซ้อนทางตาอื่นๆ อีกมากมาย
ภาวะแทรกซ้อนทางตา อุบัติการณ์ ภาวะพร่องเซลล์ต้นกำเนิดกระจกตา และกระจกตา ขุ่น 78–96% ตาแห้ง 56–95% อาตา 64–95% จอประสาทตา พัฒนาน้อย79–86% ต้อกระจก 50–85% ต้อหิน 46–70% เลนส์เคลื่อน 42% เส้นประสาทตา พัฒนาน้อย11–29%
การมองเห็น มักถูกจำกัดอยู่ที่ประมาณ 20/100 ถึง 20/200 1) เนื่องจากความเปราะบางของโซนูลของ Zinn การใส่เลนส์แก้วตาเทียม จึงต้องพิจารณาอย่างรอบคอบ
ผลิตภัณฑ์ของยีน PAX6 อยู่ติดกับยีนต้านเนื้องอก WT1 บนโครโมโซม 11p13 และอาจทำให้เกิด WAGR syndrome (เนื้องอก Wilms, aniridia, ความผิดปกติของระบบสืบพันธุ์และทางเดินปัสสาวะ, และความบกพร่องทางสติปัญญา) ในฐานะ contiguous gene syndrome
Q
ผู้ป่วย aniridia แต่กำเนิดที่ได้รับการผ่าตัดภายในตาจะเกิด aniridia fibrosis syndrome ทุกรายหรือไม่?
A
Aniridia fibrosis syndrome เกิดขึ้นหลังการผ่าตัดภายในตา แต่เป็นภาวะแทรกซ้อนที่พบได้ยากและไม่เกิดในทุกราย การทบทวนอย่างเป็นระบบเกี่ยวกับการฝังม่านตาเทียม รายงานอัตราการเกิด 3.1% 1) และกลไกการเกิดยังไม่เป็นที่เข้าใจอย่างสมบูรณ์
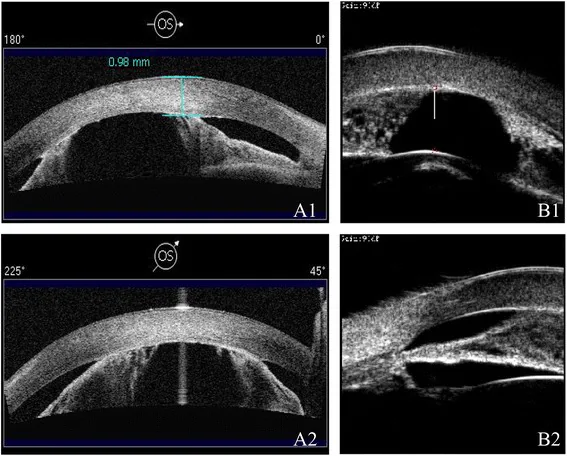
ภาพ AS-OCT และ UBM ใน aniridia Ni W, et al. A novel histopathologic finding in the Descemet’s membrane of a patient with Peters Anomaly: a case-report and literature review. BMC Ophthalmol. 2015. Figure 2. PM
CI D: PMC4619091. License: CC BY.
AS-OCT (a) และ
UBM (b) ของตาซ้ายแสดงให้เห็น
ช่องหน้าม่านตาตื้น และการยึดเกาะของ
ม่านตา ส่วนปลาย ซึ่งสอดคล้องกับ anterior synechia ที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
ข้อร้องเรียนหลักของกลุ่มอาการ aniridia fibrosis syndrome คือ การมองเห็น ลดลงอย่างค่อยเป็นค่อยไปโดยไม่เจ็บปวด1) เนื่องจากไม่เจ็บปวด ผู้ป่วยจึงมักมาพบแพทย์ช้า ในระยะลุกลาม ผู้ป่วยที่สังเกตเก่งอาจสังเกตเห็นเยื่อบางๆ
อาการระยะแรก
เยื่อเส้นใยที่เกิดจากรากม่านตา : สามารถตรวจพบเยื่อที่เกิดจากรากม่านตา ที่เหลืออยู่ได้ด้วยกล้องจุลทรรศน์ชีวภาพ มักส่งผลต่อเลนส์แก้วตาเทียม
การเคลื่อนของเลนส์แก้วตาเทียม ไปข้างหน้าเลนส์แก้วตาเทียม เคลื่อนไปข้างหน้าเนื่องจากการดึงรั้งของเยื่อ และเมื่อลุกลามจะสัมผัสกับกระจกตา
อาการระยะลุกลาม
ความดันลูกตาต่ำ IOP ตาขวา = 0 mmHg1)
ความล้มเหลวของเยื่อบุผนังกระจกตา : ในที่สุดนำไปสู่การบวมและความเสียหายของเยื่อบุผนังกระจกตา ทั้งหมด ในผู้ป่วยรายนี้พบกระจกตา บวมทั้งแผ่น1)
จอประสาทตาลอก จอประสาทตา ส่วนหน้า
ในรายงานผู้ป่วยของ Banifatemi et al. (เด็กหญิงอายุ 3 ปี หลังการผ่าตัด Ahmed glaucoma valve ทั้งสองข้าง 2 ปี) พบอาการต่อไปนี้ในตาขวา1)
ตาความดันต่ำ (IOP 0 mmHg) ร่วมกับกระจกตา บวมทั่วทั้งแผ่น
ต้อกระจก แก่ที่เคลื่อนหลุดขึ้นด้านบนและโซนูลหลุดลอกด้านล่างเยื่อสีขาวมีเส้นเลือดจากม่านตา ที่เหลืออยู่ไปจนถึงส่วนล่างของเลนส์ที่เคลื่อนหลุด
กล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ: เยื่อเส้นใยหนาที่เกิดจากโคนม่านตา แผ่ไปถึงด้านหลังของเลนส์ต้อกระจก
B-scan: ความยาวแกนตา 21 มม., จานประสาทตา บวม, จอประสาทตาลอก แบบตื้นใน 2 ใน 3 ส่วนหน้า (ไม่มีจอประสาทตาลอก )
Q
เหตุใดจึงเกิดความดันต่ำและกระจกตาบวม?
A
ความดันลูกตาต่ำ เกิดจากการที่เยื่อเส้นใยปกคลุมเลนส์ปรับตา ทำให้การทำงานของเลนส์ปรับตาถูกรบกวน ส่งผลให้การผลิตอารมณ์ขันในลูกตาลดลง1) อาการบวมน้ำที่กระจกตา เกิดจากการสัมผัสของเลนส์แก้วตาเทียม กับกระจกตา หรือความเสียหายของเซลล์บุผนังกระจกตา ที่เกิดจากความดันลูกตาต่ำ
ไม่ทราบสาเหตุที่แน่ชัดของกลุ่มอาการพังผืดในตาที่ไม่มีม่านตา อย่างไรก็ตาม ผู้ป่วยทุกรายที่รายงานมีประวัติการผ่าตัดภายในลูกตามาก่อน
ปัจจัยเสี่ยงได้แก่:
ประวัติการผ่าตัดภายในลูกตา : การผ่าตัดต้อกระจก ร่วมกับการใส่เลนส์แก้วตาเทียม เป็นสาเหตุที่พบบ่อยที่สุดการใส่อุปกรณ์ภายในลูกตา : อุปกรณ์ภายในลูกตาหลายชนิด เช่น อุปกรณ์ระบายน้ำสำหรับโรคต้อหิน (ท่อชันต์) มีความเกี่ยวข้องเพศหญิง : ร้อยละ 88 ของผู้ป่วยที่รายงานเป็นเพศหญิงการผ่าตัดภายในลูกตาหลายครั้ง : ในรายงานแรกของ Tsai et al ผู้ป่วยทุกรายมีประวัติการผ่าตัดภายในลูกตาหลายครั้ง1)
Tsai et al รายงานผู้ป่วย 6 ราย 7 ตา ที่มีประวัติการผ่าตัด1) : ผ่าตัดต้อกระจก ร่วมกับการใส่เลนส์แก้วตาเทียม 7 ตา, การผ่าตัดท่อระบายน้ำ 6 ตา, การปลูกถ่ายกระจกตา 4 ตา Bakhtiari et al รายงาน 9 ราย1) : ผู้ป่วยทุกรายได้รับการผ่าตัดต้อกระจก ร่วมกับการใส่เลนส์แก้วตาเทียม , การผ่าตัดท่อระบายน้ำ 7 ราย, การปลูกถ่ายกระจกตา /การปลูกถ่ายเนื้อเยื่อขอบกระจกตา 7 ราย
มีสองทฤษฎีที่เสนอเกี่ยวกับกลไกการเกิดโรค
ทฤษฎีการกระตุ้นเชิงกล : อุปกรณ์ภายในตาสัมผัสกับเนื้อเยื่อม่านตา ที่เหลืออยู่หรือหลอดเลือดม่านตา ที่ยังไม่เจริญเต็มที่ ทำให้เกิดโครงสร้างสำหรับการสร้างเยื่อ1) ทฤษฎีความโน้มเอียงต่อการเกิดพังผืดที่เกี่ยวข้องกับการกลายพันธุ์ของ PAX6 : PAX6 ควบคุมสัญญาณ Wnt ในทางลบ การกลายพันธุ์ของ PAX6 ทำให้สัญญาณ Wnt เรื้อรังเพิ่มขึ้น ซึ่งส่งเสริมการเกิดพังผืด การศึกษาในแบบจำลองหนูของ Wang et al พบว่าภาวะ PAX6 haploinsufficiency ทำให้เกิดภาวะก่อนพังผืดก่อนการผ่าตัด1)
ที่น่าสังเกตคือ มีรายงานการเกิดพังผืดที่ลุกลามซ้ำในทารกอายุ 8 เดือนหลังการผ่าตัด Descemet membrane stripping automated endothelial keratoplasty (DSAEK )1) ซึ่งบ่งชี้ว่าอาจเกิดได้โดยไม่มีอุปกรณ์ภายในตา
หากผู้ป่วยโรคอนิริเดียแต่กำเนิดต้องเข้ารับการผ่าตัดตา ควรได้รับการตรวจด้วยกล้องจุลทรรศน์ชนิดร่องกราดเป็นประจำหลังผ่าตัด แม้ไม่มีอาการปวด หากมีการเปลี่ยนแปลงของการมองเห็น ควรปรึกษาแพทย์โดยเร็ว การจำกัดการใช้อุปกรณ์ภายในตาให้น้อยที่สุดอาจช่วยป้องกันโรคพังผืดในอนิริเดียได้
การวินิจฉัย Aniridia Fibrosis Syndrome อาศัยการสังเกตทางคลินิกในผู้ป่วย aniridia แต่กำเนิดที่มีประวัติการผ่าตัดภายในตา
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด เป็นประจำเป็นพื้นฐานของการวินิจฉัย1) สามารถตรวจพบเยื่อพังผืดที่เกิดจากรากม่านตา และหุ้มเลนส์แก้วตาเทียม ในระยะแรกที่กระจกตา ยังใส สามารถประเมินส่วนหน้าของตาได้อย่างละเอียด
การตรวจนี้จำเป็นเมื่อมีสื่อของส่วนหน้าขุ่น เช่น กระจกตา ขุ่น1)
การประเมินสภาพของซิลิอารีบอดี
การประเมินขอบเขตของเยื่อพังผืด
การยืนยันการเกิดเยื่อพังผืดรูปวงแหวน (cyclitic membrane)
ในผู้ป่วยรายนี้ ได้ทำการตรวจด้วยกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (UBM ) ภายใต้การดมยาสลบด้วยคลอรัลไฮเดรต และพบเยื่อเส้นใยหนาตั้งแต่โคนม่านตา ไปจนถึงด้านหลังของเลนส์ต้อกระจก 1)
จำเป็นต้องแยกโรคจากภาวะต่อไปนี้
เยื่อในตาจากสาเหตุอื่น : เยื่อหลังการอักเสบจากการผ่าตัด, เยื่อรอบเลนส์แก้วตาเทียม (peripseudophakic membrane)ปฏิกิริยาการอักเสบหลังผ่าตัด : การแยกจากปฏิกิริยาการอักเสบหลังผ่าตัดธรรมดา (กลุ่มอาการพังผืดในตาที่ไม่มีม่านตา มีลักษณะเด่นคือมีสัญญาณการอักเสบน้อย)ภาวะแทรกซ้อนจากโรคพื้นฐาน (ภาวะไม่มีม่านตา ) : ต้อหิน , ภาวะพร่องเซลล์ต้นกำเนิดลิมบัส ของกระจกตา
การรักษาโรคอนิริเดียไฟโบรซิสซินโดรมเน้นที่การผ่าตัด การวินิจฉัยและการแทรกแซงตั้งแต่เนิ่นๆ ช่วยให้พยากรณ์การมองเห็น ดีขึ้น1)
เพื่อป้องกันการเจริญเติบโตของเยื่อพังผืดและการทำลายเนื้อเยื่อเพิ่มเติม แนะนำให้ผ่าตัดเยื่อพังผืดออกตั้งแต่เนิ่นๆ ผ่านการปลูกถ่ายกระจกตา แบบทะลุทะลวง (penetrating keratoplasty, PKP )
ในรายงานของ Tsai et al. ในผู้ป่วย 6 ราย 7 ตา ที่ได้รับการผ่าตัด 5 ราย1) :
ได้รับการปลูกถ่ายกระจกตา แบบทะลุทะลวงร่วมกับการตัดเยื่อพังผืด
ในรายที่มีความดันลูกตาต่ำ ความดันลูกตา กลับมาเป็นปกติหลังตัดเยื่อพังผืด (คงที่ 5-10 มิลลิเมตรปรอท)
ผู้ป่วยทั้ง 5 รายมีการมองเห็น ดีขึ้น ไม่มีการกลับเป็นซ้ำหลังผ่าตัด
Tsai et al (รายงานครั้งแรก)
เทคนิคการผ่าตัด : การปลูกถ่ายกระจกตา ทุกชั้นร่วมกับการตัดเยื่อหุ้ม บางรายทำการถอด/เปลี่ยนเลนส์แก้วตาเทียม ร่วม
การกลับเป็นซ้ำ : พบการกลับเป็นซ้ำเฉพาะในรายที่ได้รับการถอด/เปลี่ยนเลนส์แก้วตาเทียม สรุปว่าการถอดเลนส์แก้วตาเทียม พร้อมกันมีประสิทธิภาพในการป้องกันการกลับเป็นซ้ำ
ผลการมองเห็น : ผู้ป่วยทั้ง 5 รายที่ได้รับการผ่าตัดมีการมองเห็น ดีขึ้น1)
Bakhtiari et al (9 ราย)
เทคนิคการผ่าตัด : ทุกรายใส่ Boston KPro type 1 (ครั้งแรกหรือครั้งที่สอง) ใน 9 ราย มี 7 รายที่ถอดเลนส์แก้วตาเทียม และ 8 รายที่ทำการตัดน้ำวุ้นตา
ภาวะแทรกซ้อนหลังผ่าตัด : เยื่อหุ้มหลัง KPro 5 ตา, เลือดออกใต้คอรอยด์ 1 ตา, จอประสาทตาลอก ชนิด tractional 1 ตา
ผลการมองเห็น : ดีขึ้นในทุกรายจากระดับ hand motion ถึง light perception ก่อนผ่าตัด เป็น 20/200 ถึง 2/500 หลังผ่าตัด1)
กระจกตาเทียมแบบบอสตัน ชนิดที่ 1 เป็นทางเลือกการรักษาที่เป็นไปได้ โดยไม่พบความสัมพันธ์กับการกลับเป็นซ้ำของกลุ่มอาการพังผืดในตาที่ไม่มีม่านตา 1) เนื่องจาก KPro ถูกวางตำแหน่งให้ห่างจากรากม่านตา (จุดเริ่มต้นของรอยโรค) จึงเชื่อว่ากระตุ้นม่านตา น้อยกว่า
อย่างไรก็ตาม ควรระวังว่าการเกิดเยื่อหลัง KPro ในตาที่ไม่มีม่านตา มีอัตราสูง (61–66%) ซึ่งสูงกว่าตาที่มีม่านตา ปกติอย่างมีนัยสำคัญ (26.7–39%)1) และเยื่อหลัง KPro นี้อาจเป็นฟีโนไทป์หนึ่งของกลุ่มอาการพังผืดในตาที่ไม่มีม่านตา 1)
Dyer และคณะรายงานอัตราการคงอยู่ของ Boston KPro type 1 ในตาที่ไม่มีม่านตา เท่ากับ 83.3% (ติดตามเฉลี่ย 58.7 เดือน) ส่วน Shah และคณะรายงาน 87% (ติดตาม 54 เดือน)1)
Bakhtiari และคณะแนะนำให้ทำ การตัดแก้วตาแบบสมบูรณ์ ไม่ใช่แค่การตัดแก้วตาส่วนหน้า เพื่อป้องกันการกลับเป็นซ้ำ1)
ในกลุ่มอาการอนิริเดีย-ไฟโบรซิส การติดตามผลหลังผ่าตัดเป็นสิ่งจำเป็น ต้องมีการตรวจด้วยกล้องจุลทรรศน์แบบร่องกรีดเป็นระยะเพื่อยืนยันการกลับเป็นซ้ำ1)
มีรายงานการกลับเป็นซ้ำเฉพาะในกรณีที่เปลี่ยนเลนส์แก้วตาเทียม เพียงอย่างเดียว (โดยไม่ถอดออก) ดังนั้นเมื่อทำการตัดเยื่อพังผืด ควรพิจารณาถอดเลนส์แก้วตาเทียม พร้อมกัน1)
ในกรณีนี้ (เด็กหญิงอายุ 3 ปี) ผู้ปกครองปฏิเสธการผ่าตัด จึงไม่ได้ทำการผ่าตัด1) ในเด็ก การอธิบายและการยินยอมจากผู้ปกครองมีความสำคัญเป็นพิเศษ
Q
หากไม่ได้รับการผ่าตัด การมองเห็นจะเป็นอย่างไร?
A
ข้อมูลผลลัพธ์ในกรณีที่ได้รับการวินิจฉัยแน่ชัดว่าเป็น AFS แต่ไม่ได้รับการผ่าตัดนั้นมีจำกัด ในรายงานผู้ป่วยนี้ (Banifatemi et al. 2024) ไม่ได้ทำการผ่าตัดเนื่องจากผู้ปกครองปฏิเสธ1) โดยทั่วไป หากไม่รักษา อาจมีความเสี่ยงต่อการลุกลามของภาวะเยื่อบุผนังกระจกตา ล้มเหลว ความดันลูกตาต่ำ และจอประสาทตาลอก รายงานของ Tsai et al พบว่าผู้ป่วยทุกรายที่ได้รับการผ่าตัดมีการมองเห็น ดีขึ้น ซึ่งเน้นย้ำถึงความสำคัญของการแทรกแซงตั้งแต่เนิ่นๆ1)
กลไกการเกิดโรคที่แน่ชัดของกลุ่มอาการอนิริเดีย-ไฟโบรซิสยังไม่เป็นที่ทราบแน่ชัด แต่หลักฐานหลายประการสนับสนุนว่ารากม่านตา เป็นจุดเริ่มต้นของการเกิดพังผืด
การวิเคราะห์ทางพยาธิวิทยาโดย Tsai et al พบสิ่งต่อไปนี้1)
ต้นกำเนิดของเนื้อเยื่อเส้นใย : เนื้อเยื่อเส้นใยจากรากม่านตา ที่เป็นร่องรอยลักษณะของเยื่อ : เยื่อเส้นใยที่มีเซลล์น้อยและหนาแน่น มีหลอดเลือดน้อยอิมมูโนฮิสโตเคมี : พบทีเซลล์และมาโครฟาจจำนวนน้อยใน 2 ราย → บ่งชี้ว่าการอักเสบไม่ใช่สาเหตุหลัก (ใน 1 รายพบเซลล์อักเสบ)กล้องจุลทรรศน์อิเล็กตรอน : พบการปะปนของมัดคอลลาเจนที่ยังไม่เจริญเต็มที่และเส้นใยที่เจริญเต็มที่ ไม่พบเซลล์เกลีย, เซลล์บุผนังกระจกตา และเซลล์เยื่อบุเลนส์ตา
Banifatemi et al. (2024) กล่าวว่า “เยื่อเส้นใยมีลักษณะคล้ายกับเยื่อรอบเลนส์แก้วตาเทียม หลังการผ่าตัดในผู้ป่วยม่านตาอักเสบ เรื้อรัง แต่แตกต่างตรงที่ไม่มีการอักเสบ” 1)
มีกลไกที่ถูกเสนอไว้ 2 กลไก
สมมติฐานการกระตุ้นเชิงกล
ทฤษฎีที่ว่าอุปกรณ์ภายในตาสัมผัสกับเนื้อเยื่อม่านตา ที่เหลืออยู่หรือหลอดเลือดม่านตา ที่ยังไม่เจริญเต็มที่ ทำให้เกิดโครงสร้างสำหรับการสร้างเยื่อพังผืด1) ซึ่งสอดคล้องกับข้อเท็จจริงทางคลินิกที่ว่ากลุ่มอาการพังผืดในตาไม่มีม่านตา เกิดขึ้นสัมพันธ์กับอุปกรณ์ภายในตาต่างๆ เช่น เลนส์แก้วตาเทียม ท่อระบายน้ำ และม่านตาเทียม
สมมติฐานการเพิ่มขึ้นของสัญญาณ Wnt ที่เกี่ยวข้องกับการกลายพันธุ์ของ PAX6
PAX6 เป็นปัจจัยถอดรหัสที่ควบคุมสัญญาณ Wnt ในทางลบ ทฤษฎีที่ว่าการเพิ่มขึ้นของสัญญาณ Wnt เรื้อรังจากการกลายพันธุ์ของ PAX6 ทำให้เกิดภาวะพร่องต่อการเกิดพังผืดในตา1) Wang และคณะในการศึกษาในแบบจำลองหนูพบว่า PAX6 haploinsufficiency (haploPAX6) ทำให้เกิดภาวะก่อนพังผืดในตาที่ยังไม่ได้รับการผ่าตัดเมื่อเทียบกับหนูปกติ1)
ความผิดปกติของส่วนหน้าตาแต่กำเนิดอื่นๆ เช่น Peters anomaly ก็มีรายงานการเกิดพังผืดแบบก้าวหน้าที่คล้ายกัน ซึ่งบ่งชี้ว่าการกลายพันธุ์ของ PAX6 มีความสัมพันธ์อย่างกว้างขวางกับภาวะพร่องต่อการเกิดพังผืด1)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
อัตราการเกิดเยื่อหลัง KPro หลังการปลูกถ่าย Boston KPro type 1 ในตาที่มีภาวะไม่มีม่านตา อยู่ที่ 61–66% ซึ่งสูงกว่าตาที่ไม่มีภาวะไม่มีม่านตา อย่างมีนัยสำคัญ (26.7–39%) 1)
Yang et al ชี้ให้เห็นว่าการเกิดเยื่อหลัง KPro ในอัตราสูงนี้อาจเป็นฟีโนไทป์หนึ่งของกลุ่มอาการพังผืดในตาไม่มีม่านตา 1) ในขณะที่ Muzychuk et al รายงานว่าการไม่มีม่านตา เป็นปัจจัยเสี่ยงสำคัญต่อการสูญเสียการมองเห็น หลังการผ่าตัด Boston KPro 1)
ในการทบทวนวรรณกรรมอย่างเป็นระบบเกี่ยวกับการปลูกถ่ายม่านตาเทียม โดย Romano et al รายงานว่าอุบัติการณ์ของกลุ่มอาการพังผืดจากภาวะไม่มีม่านตา อยู่ที่ 3.1% ในการศึกษาเกี่ยวกับภาวะไม่มีม่านตา จำนวน 96 ตาโดย Figueredo และ Snyder 1) เนื่องจากการปลูกถ่ายม่านตาเทียม ทำหน้าที่เป็นอุปกรณ์ภายในตาเช่นเดียวกับเลนส์แก้วตาเทียม และท่อระบายน้ำ การปลูกถ่ายม่านตาเทียม จึงมีความเสี่ยงที่อาจเกิดขึ้นต่อการเกิดกลุ่มอาการพังผืดจากภาวะไม่มีม่านตา
การศึกษาในแบบจำลองหนูของ Wang และคณะเป็นหนึ่งในการศึกษาอย่างเป็นระบบครั้งแรกที่มุ่งอธิบายกลไกระดับโมเลกุลของกลุ่มอาการไร้ม่านตา ร่วมกับพังผืด1) มีการเสนอว่าการยับยั้งวิถีสัญญาณ Wnt แบบเลือกสรรอาจเป็นเป้าหมายการรักษาในอนาคต แต่ยังไม่ถึงขั้นนำไปใช้ทางคลินิก
Banifatemi M, Razeghinejad R, Salouti R, Abolfathzadeh N. Aniridic fibrosis syndrome in a child with Ahmed glaucoma valve: Report of a case and review of the literature. J Curr Ophthalmol. 2024;36:453-6.
Bakhtiari P, Chan C, Welder JD, de la Cruz J, Holland EJ, Djalilian AR. Surgical and visual outcomes of the type I Boston Keratoprosthesis for the management of aniridic fibrosis syndrome in congenital aniridia. Am J Ophthalmol. 2012;153(5):967-971.e2. PMID: 22265154.
Adam MP, Bick S, Mirzaa GM, Pagon RA, Wallace SE, Amemiya A, et al. PAX6-Related Aniridia. . 1993. PMID: 20301534.