عوامل خطر مستقل
دوز دوپیلوماب: دوز بالاتر خطر را افزایش میدهد
شدت AD: بروز در AD متوسط تا شدید بیشتر است
سابقه ورم ملتحمه قبل از درمان: بیماری سطحی چشم موجود به شدت بروز DIOSD را پیشبینی میکند

دوپیلوماب (dupilumab، نام تجاری: دوپیکسنت®) یک آنتیبادی مونوکلونال IgG4 انسانی است که به زیرواحد آلفای گیرنده IL-4 (IL-4Rα) متصل شده و انتقال سیگنال IL-4 و IL-13 را مهار میکند. این دارو برای درماتیت آتوپیک (AD)، آسم برونشیال و سینوزیت مزمن با پولیپ بینی تأیید شده است.
در کارآزماییهای بالینی فاز ۳، میزان بروز ورم ملتحمه در گروه دوپیلوماب + کورتیکواستروئید موضعی ۱۴-۱۹٪ بود که به طور معنیداری بیشتر از گروه دارونما (۸٪) بود1). پس از عرضه به بازار، گزارشهایی از فراوانی DIOSD (بیماری سطح چشم ناشی از دوپیلوماب) تا ۵۰٪ وجود دارد1). ۸۰٪ عوارض چشمی در ۴ ماه اول پس از شروع درمان رخ میدهد، اما موارد دیررس پس از ۵۲ هفته نیز گزارش شده است1).
DIOSD مختص درمان با دوپیلوماب برای AD است و در استفاده برای آسم یا سینوزیت گزارش نشده است. این اختصاصی بودن نشان میدهد که سطح چشم بیماران AD از قبل آسیبپذیر است1).
در حال حاضر، DIOSD مختص درمان با دوپیلوماب برای درماتیت آتوپیک (AD) در نظر گرفته میشود1). در استفاده برای آسم یا سینوزیت مزمن با پولیپ بینی، افزایش فراوانی ورم ملتحمه گزارش نشده است. تصور میشود که سطح چشم بیماران AD که از قبل توسط التهاب آلرژیک آسیب دیده است، آسیبپذیری بیشتری در برابر تغییر تعادل سیتوکینی ناشی از دوپیلوماب ایجاد میکند.
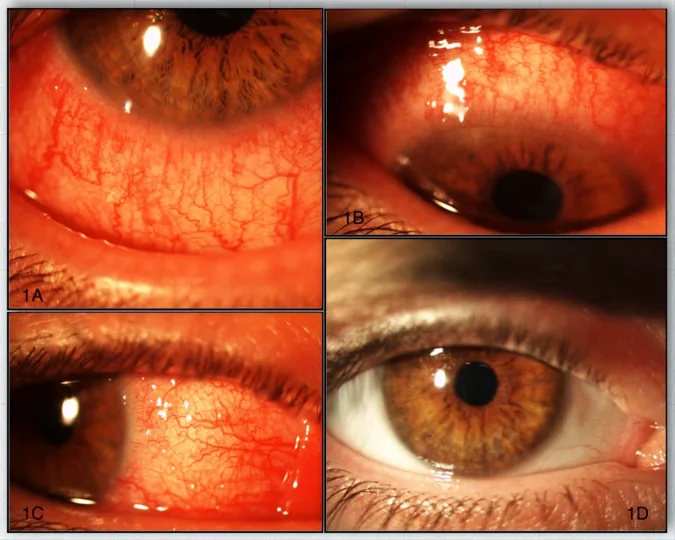
قرمزی، خارش، احساس تحریک، احساس جسم خارجی، حساسیت به نور، اشکریزش، ترشحات چشمی و کاهش بینایی دیده میشود. احساس سوزش و «شنمانند» مداوم نیز مشخصه است 1). دوبینی تکچشمی متناوب نیز گزارش شده است.
در درمان تکدارویی با دوپیلوماب، به طور متوسط حدود ۲ هفته پس از شروع بروز میکند. در موارد مصرف همزمان کورتیکواستروئیدهای موضعی، بروز کمی دیرتر و حدود ۴ تا ۸ هفته پس از شروع رخ میدهد.
DIOSD به سه مرحله زیر پیشرفت میکند. معمولاً دوطرفه اما نامتقارن است.
| مرحله | یافته |
|---|---|
| اولیه | بیماری غدد میبومین (MGD)، قرمزی ملتحمه، ورم ملتحمه پاپیلری، کراتوپاتی نقطهای سطحی |
| میانی | چسبندگی پلک به کره چشم (سیمبلفارون)، ریزش مژه، کوتاه شدن فورنیکس، التهاب لیمبوس |
| پیشرفته | چسبندگی پلکها (آنکیلوبلفارون)، از بین رفتن فورنیکس، کراتینه شدن سطح چشم |
تصویر بالینی DIOSD به 5 نوع زیر طبقهبندی میشود1).
1. ورم ملتحمه مرتبط با دوپیلوماب (DAC): شایعترین (36-50%)، شامل انواع غیراختصاصی، پاپیلاری، فولیکولی و کراتوکونژنکتیویت است1). ممکن است ندول لیمبال (شبیه لکههای ترانتاس) نیز وجود داشته باشد.
2. اختلال قرنیه: به صورت کراتوپاتی اپیتلیال نقطهای، فرسایش قرنیه و زخم قرنیه ظاهر میشود1). اغلب با کاهش BUT همراه است.
3. عوارض فیبروتیک: ورم ملتحمه اسکاردهنده، اکتروپیون اسکاردهنده و تنگی پونکتوم اشکی گزارش شده است1).
4. خشکی چشم: ناشی از کاهش سلولهای جامی و نارسایی غده اشکی است1). باعث بیثباتی لایه اشکی و التهاب مخاطی میشود.
5. بلفاریت و بلفاروکونژنکتیویت: با تورم پلک، قرمزی و درماتیت اطراف چشم تظاهر میکند1). بلفاروکونژنکتیویت اسکاردهنده یک عارضه شدید است.
عوامل خطر مستقل
دوز دوپیلوماب: دوز بالاتر خطر را افزایش میدهد
شدت AD: بروز در AD متوسط تا شدید بیشتر است
سابقه ورم ملتحمه قبل از درمان: بیماری سطحی چشم موجود به شدت بروز DIOSD را پیشبینی میکند
ماهیت پاتوفیزیولوژیک
مهار IL-13: IL-13 غالبترین سیتوکین در سطح چشم است و برای تمایز سلولهای جامی و ترشح موسین ضروری است1). مهار IL-13 توسط دوپیلوماب باعث هیپوپلازی سلولهای جامی و کاهش ترشح موسین میشود
عدم تعادل Th1/Th2: مهار IL-4/IL-13 پاسخ ایمنی غالب Th1 (IFN-γ اضافی) را القا میکند که تراکم سلولهای جامی را بیشتر کاهش میدهد1)
یافتههای بیوپسی: بیوپسی ملتحمه کاهش قابل توجه تراکم سلولهای جامی (میانگین 3.3 سلول در میلیمتر، در مقابل 32.3 در گروه کنترل) و نفوذ سلولهای CD3+/CD4+ T و ائوزینوفیلها به داخل اپیتلیوم را نشان میدهد1)
تشخیص DIOSD یک تشخیص بالینی بر اساس سابقه و یافتههای بالینی است. آزمایشهای آزمایشگاهی و بیوپسی معمولاً اندیکاسیون ندارند.
سابقه لازم: استفاده از دوپیلوماب برای AD متوسط تا شدید. زمان شروع علائم پس از شروع دوپیلوماب (معمولاً 2 تا 8 هفته).
آزمایشهای زیر برای ارزیابی مرحله و پیشآگهی انجام میشود.
رنگآمیزی قرنیه و ملتحمه: با فلورسئین و لیسامین گرین برای ارزیابی یکپارچگی ملتحمه.
تست شیرمر: حجم اشک کمتر از 10 میلیمتر نشاندهنده آسیب غده اشکی در موارد پیشرفته است.
زمان شکست لایه اشکی (TBUT): کوتاه شدن نشاندهنده کمبود موسین است.
تست حس قرنیه: با سواب پنبهای یا حسسنج قرنیه Cochet-Bonnet ارزیابی میشود.
مهمترین تشخیص افتراقی، کراتوکونژنکتیویت آتوپیک (AKC) است که قبل از شروع دوپیلوماب وجود داشته است. در AKC تراکم سلولهای جامی افزایش مییابد، در حالی که در DIOSD کاهش مییابد1). ورم ملتحمه آلرژیک، ورم ملتحمه ویروسی، پمفیگوئید چشمی و GVHD چشمی نیز در تشخیص افتراقی مطرح هستند.
هدف درمان DIOSD کنترل التهاب و بازگرداندن عملکرد سلولهای جامی است. معمولاً نیازی به قطع دوپیلوماب نیست و میتوان آن را همزمان با درمان چشمی ادامه داد1).
خط اول درمان
قطره چشمی استروئیدی با قدرت کم: فلورومتولون 0.1% در 2 مورد از 5 مورد بهبود کامل و در 3 مورد بهبود قابل توجه ایجاد کرد1). باید مراقب افزایش فشار چشم بود.
پماد چشمی تاکرولیموس: پماد چشمی تاکرولیموس 0.03% در 2 مورد از 4 مورد بهبود کامل و در 2 مورد بهبود قابل توجه ایجاد کرد1). مهارکنندههای کلسینورین ممکن است سلولهای جامی را افزایش داده و از مرگ سلولهای اپیتلیال جلوگیری کنند.
قطره چشمی سیکلوسپورین: قطره چشمی CsA 0.05% به عنوان درمان نگهدارنده استفاده میشود. گزارش شده است که همراه با پردنیزولون استات 1% بدون عود مدیریت شده است.
درمان کمکی
اشک مصنوعی: برای حفظ رطوبت سطح چشم استفاده میشود. اغلب به تنهایی کافی نیست.
کمپرس گرم و ماساژ پلک: در موارد همراه با MGD مؤثر است1).
قطره چشمی آنتیهیستامین: به تنهایی اثر کمی دارد1).
تست پچ: در صورت مشکوک بودن به آلرژی تماسی انجام میشود. گزارش شده است که با اجتناب از امولسیفایرها، سورفکتانتها و عطرها، DIOSD بهبود مییابد1).
در بیشتر موارد، نیازی به قطع نیست1). تقریباً تمام موارد DIOSD با درمان چشمی (قطرههای استروئیدی یا مهارکنندههای کلسینورین) بهبود مییابند. از آنجایی که دوپیلوماب در درمان AD و آسم مؤثر است، قطع آن ممکن است باعث تشدید بیماریهای سیستمیک شود؛ بنابراین معمولاً درمان چشمی همزمان با ادامه دوپیلوماب انجام میشود. با این حال، در صورت عوارض شدید اسکار (کانژنکتیویت اسکار پلک، زخم قرنیه) یا مقاوم به درمان، تیم چندتخصصی قطع دارو را بررسی میکند.
مکانیسم DIOSD پیچیده است و پنج فرضیه زیر مطرح شدهاند1).
مهار IL-4/IL-13 توسط دوپیلومب پاسخ Th2 را سرکوب میکند، در حالی که سیتوکینهای Th1 (IFN-γ) غالب میشوند1). IFN-γ تراکم سلولهای جامی را کاهش داده و ترشح موسین را کم میکند.
مهار IL-4/IL-13 ممکن است منجر به تکثیر دمودکس و القای التهاب روزاسهای وابسته به IL-17 شود1).
احتمال داده میشود که سیگنالدهی غیرطبیعی با واسطه OX40L فعال شده و وضعیتی شبیه به کاتار بهاری ایجاد کند1).
در طول درمان با دوپیلومب، تعداد ائوزینوفیلهای خون محیطی ممکن است افزایش یابد و نفوذ ائوزینوفیلها به سطح چشم در التهاب نقش داشته باشد1).
این قویترین فرضیه است1). IL-13 غالبترین سیتوکین در سطح چشم است و برای تمایز سلولهای جامی و ترشح موسین ضروری است1). مهار IL-13 توسط دوپیلومب باعث هیپوپلازی سلولهای جامی شده و زنجیرهای از کاهش ترشح موسین، بیثباتی لایه اشکی و التهاب مخاطی را القا میکند1). این وضعیت DAMD (کمبود موسین مرتبط با دوپیلومب) نامیده میشود1).
در بیوپسی ملتحمه توسط Bakker و همکاران، کاهش شدید سلولهای جامی (3.3 سلول/mm در مقابل 32.3 سلول/mm در گروه کنترل) و نفوذ ائوزینوفیلها و سلولهای T در بیماران DIOSD تأیید شد1). این در تضاد با افزایش سلولهای جامی (بیان بالای IL-13) در ورم ملتحمه آلرژیک و AKC است و تأیید میکند که DIOSD یک واحد بیماری مستقل است1).
در ورم ملتحمه آلرژیک و کراتوکونژونکتیویت آتوپیک (AKC)، IL-13 به میزان بالایی بیان میشود و تراکم سلولهای جامی افزایش یافته و ترشح موسین نیز افزایش مییابد. در مقابل، در DIOSD، دوپیلومب IL-13 را مهار میکند و در نتیجه تراکم سلولهای جامی کاهش مییابد1). یافتههای بیوپسی نیز کاهش تراکم سلولهای جامی به حدود یک دهم گروه کنترل را نشان میدهد1). بنابراین، هر دو بیماری التهابی سطح چشم هستند، اما تغییرات سلولهای جامی کاملاً متضاد بوده و مکانیسم پاتولوژیک آنها اساساً متفاوت است.
DIOSD و DAMD مفاهیم نسبتاً جدیدی از بیماری هستند که پس از عرضه دوپیلوماب به بازار، آگاهی از آنها به سرعت گسترش یافت 1). تأیید کاهش سلولهای جامی از طریق بیوپسی ملتحمه، درک این وضعیت را به طور قابل توجهی پیش برد 1).
احتمال دارد درماتیت تماسی یک عامل تعدیلکننده DIOSD باشد. گزارش شده است که با اجتناب از آلرژنهای شناساییشده در تست پچ (امولسیفایرها، سورفکتانتها، عطرها)، DIOSD در برخی بیماران بهبود یافته است 1).
الزامات عبارتند از: روشن شدن مکانیسمی که توسط آن مهارکنندههای کلسینورین تراکم سلولهای جامی را بازیابی میکنند، پیشبینی بروز DIOSD با استفاده از بیومارکرها، و جمعآوری دادههای بلندمدت پیشآگهی. همچنین اشاره شده است که ناهنجاری در متابولیسم رتینوئیک اسید ممکن است در DIOSD نقش داشته باشد 1) و نقش درمان مکمل ویتامین A ممکن است در آینده بررسی شود.
- Reji MA, Haque A, Goyal S, Krishnaswamy G. Dupilumab-induced ocular surface disease: a primer. BMJ Case Rep. 2022;15:e249019.