독립적 위험 인자

두필루맙 유발 결막염
1. 두필루맙 유발 결막염이란?
섹션 제목: “1. 두필루맙 유발 결막염이란?”두필루맙(상품명: 듀피젠트®)은 IL-4 수용체 알파 서브유닛(IL-4Rα)에 결합하여 IL-4 및 IL-13의 신호 전달을 억제하는 인간 단클론 IgG4 항체입니다. 아토피 피부염(AD), 기관지 천식, 비용종을 동반한 만성 부비동염에 승인되었습니다.
3상 임상시험에서 두필루맙 + 국소 스테로이드군의 결막염 발생률은 14~19%로 위약군의 8%보다 유의하게 높았습니다1). 시판 후 보고에 따르면 DIOSD(두필루맙 유발 안구표면질환)의 빈도는 최대 50%에 달할 수 있습니다1). 안구 합병증의 80%는 치료 시작 후 4개월 이내에 발생하지만, 52주 후 지연 발병 사례도 보고되었습니다1).
DIOSD는 AD에 대한 두필루맙 치료에 특이적이며, 천식이나 부비동염 사용에서는 보고되지 않았습니다. 이러한 선택성은 AD 환자의 안구표면이 이미 취약함을 시사합니다1).
현재로서 DIOSD는 아토피 피부염(AD)에 대한 두필루맙 치료에 특이적인 것으로 간주됩니다1). 천식이나 비용종을 동반한 만성 부비동염 사용에서는 결막염 빈도 증가가 보고되지 않았습니다. AD 환자의 안구표면은 원래 알레르기 염증으로 손상되어 있어 두필루맙에 의한 사이토카인 균형 변화에 더 취약한 것으로 추정됩니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”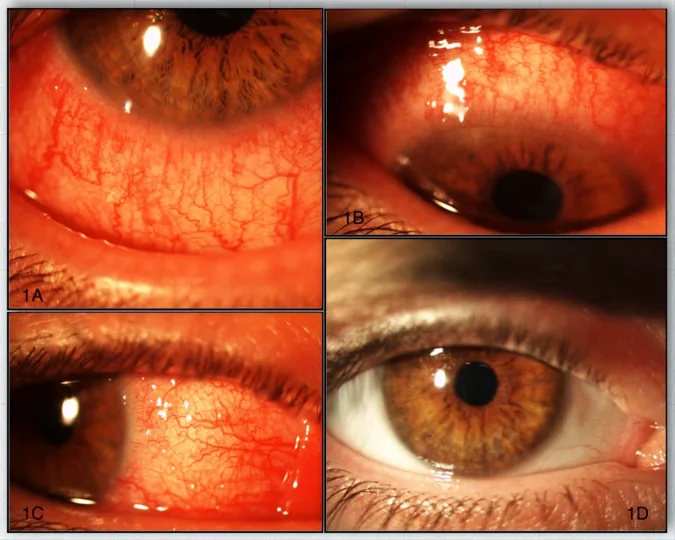
자각 증상
섹션 제목: “자각 증상”충혈, 가려움, 자극감, 이물감, 눈부심, 눈물, 눈곱, 시력 저하가 나타납니다. 작열감과 지속적인 ‘모래 알갱이 같은 느낌’도 특징적입니다1). 간헐적인 단안 복시가 보고되기도 합니다.
두필루맙 단독 요법에서는 평균 약 2주 후에 발병합니다. 국소 스테로이드 병용 시에는 4~8주 후로 발병이 다소 지연됩니다.
임상 소견
섹션 제목: “임상 소견”DIOSD는 다음 3단계로 진행됩니다. 일반적으로 양측성이지만 비대칭적입니다.
| 단계 | 소견 |
|---|---|
| 초기 | 마이봄샘 기능 장애, 결막 충혈, 유두상 결막염, 점상 표층 각막병증 |
| 중간기 | 안구 유착, 속눈썹 탈락, 원개부 단축, 각막 윤부염 |
| 진행기 | 눈꺼풀 유착, 원개부 소실, 안구 표면 각화 |
DIOSD의 5형 분류
섹션 제목: “DIOSD의 5형 분류”DIOSD의 임상 양상은 다음 5가지 유형으로 분류됩니다1).
1. 두필루맙 관련 결막염(DAC): 가장 흔하며(36~50%), 비특이형, 유두형, 여포형, 각결막염형이 있습니다1). 윤부 결절(Trantas 반점 유사)을 나타낼 수도 있습니다.
2. 각막 장애: 점상 표층 각막염, 각막 미란, 각막 궤양으로 나타납니다1). 눈물막 파괴 시간 단축을 동반하는 경우가 많습니다.
3. 섬유화 합병증: 반흔성 결막염, 반흔성 안검외반, 눈물점 협착이 보고되었습니다1).
4. 안구건조증: 술잔세포 감소와 눈물샘 기능 부전으로 인해 발생합니다1). 눈물막 불안정화와 점막 염증을 유발합니다.
5. 안검염 및 안검결막염: 안검 부종, 발적, 안와주위 피부염을 나타냅니다1). 반흔성 안검결막염은 중증 합병증입니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”병태의 본질
IL-13 억제: IL-13은 안표면에서 가장 우세한 사이토카인이며, 술잔세포 분화와 뮤신 분비에 필수적입니다1). 두필루맙에 의한 IL-13 억제는 술잔세포 저형성과 뮤신 분비 감소를 유발합니다.
Th1/Th2 균형 변화: IL-4/IL-13 억제로 Th1 우세 면역 반응(IFN-γ 과잉)이 유도되어 술잔세포 밀도가 더욱 감소합니다1).
생검 소견: 결막 생검에서 술잔세포 밀도의 현저한 감소(중앙값 3.3개/mm, 대조군 32.3개/mm)와 CD3+/CD4+ T세포 및 호산구의 상피내 침윤이 관찰됨1)
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”DIOSD의 진단은 병력과 임상 소견에 기반한 임상 진단입니다. 일반적으로 검사실 검사나 생검은 적응되지 않습니다.
필요한 병력: 중등도중증 아토피 피부염에 대해 듀필루맙을 사용 중이어야 합니다. 증상 발생 시점이 듀필루맙 시작 후(보통 28주)여야 합니다.
안과 검사
섹션 제목: “안과 검사”다음 검사로 병기와 예후를 평가합니다.
각결막 염색: 플루오레세인과 리사민 그린으로 결막의 완전성을 평가합니다.
쉬르머 검사: 눈물량이 10mm 미만이면 진행된 경우의 눈물샘 기능 장애를 시사합니다.
눈물막 파괴 시간(TBUT): 단축은 뮤신 결핍을 반영합니다.
각막 감각 검사: 면봉 또는 Cochet-Bonnet 각막 감각계로 평가합니다.
감별 진단
섹션 제목: “감별 진단”가장 중요한 감별은 듀필루맙 시작 전부터 존재했던 아토피 각결막염(AKC)과의 감별입니다. AKC에서는 술잔세포 밀도가 증가하는 반면, DIOSD에서는 감소합니다1). 알레르기 결막염, 바이러스 결막염, 안구 유천포창, 안구 이식편대숙주병도 감별에 포함됩니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”DIOSD의 치료 목표는 염증 조절과 술잔세포 기능 회복입니다. 두필루맙 중단은 일반적으로 불필요하며, 안과 치료를 받으면서 지속할 수 있습니다 1).
1차 선택
보조 요법
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”DIOSD의 기전은 복잡하며, 다음과 같은 5가지 가설이 제시되었습니다1).
1. Th1/Th2 균형 편향
섹션 제목: “1. Th1/Th2 균형 편향”두필루맙에 의한 IL-4/IL-13 억제는 Th2 반응을 억제하는 반면, Th1 사이토카인(IFN-γ)이 우세해집니다1). IFN-γ는 술잔세포 밀도를 감소시키고 뮤신 분비를 줄입니다.
2. 모낭충(Demodex) 증식
섹션 제목: “2. 모낭충(Demodex) 증식”IL-4/IL-13 억제로 모낭충이 증식하여 IL-17 매개 주사비 유사 염증이 유도될 가능성이 있습니다1).
3. OX40 리간드 매개 이상 신호
섹션 제목: “3. OX40 리간드 매개 이상 신호”비정상적인 OX40L 매개 신호가 활성화되어 봄철각결막염 유사 병태가 발생할 가능성이 지적되었습니다1).
4. 호산구 증가증
섹션 제목: “4. 호산구 증가증”두필루맙 치료 중 말초 호산구 수가 증가할 수 있으며, 안구 표면으로의 호산구 침윤이 염증에 관여할 가능성이 있습니다1).
5. IL-13 억제에 의한 술잔세포 감소(DAMD)
섹션 제목: “5. IL-13 억제에 의한 술잔세포 감소(DAMD)”가장 유력한 가설입니다1). IL-13은 안구 표면에서 가장 우세한 사이토카인이며, 술잔세포 분화와 뮤신 분비에 필수적입니다1). 두필루맙에 의한 IL-13 억제는 술잔세포 저형성을 유발하여 뮤신 분비 감소, 눈물막 불안정화, 점막 염증의 연쇄를 유도합니다1). 이 병태는 **DAMD(두필루맙 관련 뮤신 결핍)**라고 불립니다1).
Bakker 등의 결막 생검에서 DIOSD 환자는 술잔세포의 현저한 감소(3.3개/mm vs 대조군 32.3개/mm)와 호산구 및 T세포 침윤이 확인되었습니다1). 이는 알레르기 결막염이나 AKC에서의 술잔세포 증가(높은 IL-13 발현)와 대조적이며, DIOSD가 독립적인 질환 단위임을 뒷받침합니다1).
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”DIOSD/DAMD 개념 확립
섹션 제목: “DIOSD/DAMD 개념 확립”DIOSD와 DAMD는 비교적 새로운 질환 개념이며, 두필루맙 시판 후 인식이 급속히 확대되었습니다1). 결막 생검을 통한 술잔세포 감소 확인이 이 병태의 이해를 크게 진전시켰습니다1).
첩포검사를 통한 알레르겐 동정
섹션 제목: “첩포검사를 통한 알레르겐 동정”접촉피부염이 DIOSD의 수정 인자일 가능성이 제시되었습니다. 첩포검사로 동정된 알레르겐(유화제, 계면활성제, 향료)을 회피함으로써 일부 환자에서 DIOSD가 개선되었다는 보고가 있습니다1).
향후 과제
섹션 제목: “향후 과제”칼시뉴린 억제제가 술잔세포 밀도를 회복시키는 메커니즘 규명, 바이오마커를 통한 DIOSD 발병 예측, 장기 예후 데이터 축적이 필요합니다. 레티노산 대사 이상이 DIOSD에 관여할 가능성도 지적되고 있으며1), 비타민 A 보충 요법의 역할이 향후 검토될 수 있습니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”
- Reji MA, Haque A, Goyal S, Krishnaswamy G. Dupilumab-induced ocular surface disease: a primer. BMJ Case Rep. 2022;15:e249019.
- Neagu N, Dianzani C, Avallone G, Dell’Aquila C, Morariu SH, Zalaudek I, et al. Dupilumab ocular side effects in patients with atopic dermatitis: a systematic review. J Eur Acad Dermatol Venereol. 2022;36(6):820-835. PMID: 35122335.
- Shen E, Xie K, Jwo K, Smith J, Mosaed S. Dupilumab-Induced Follicular Conjunctivitis. Ocul Immunol Inflamm. 2019;27(8):1339-1341. PMID: 30335586.
