عوامل الخطر المستقلة
جرعة دوبيلوماب: تزداد المخاطر مع الجرعات العالية
شدة التهاب الجلد التأتبي (AD): معدل حدوث أعلى في AD المتوسط إلى الشديد
تاريخ التهاب الملتحمة قبل العلاج: أمراض سطح العين الموجودة مسبقًا تتنبأ بقوة بحدوث DIOSD

دوبيلوماب (الاسم التجاري: دوبيكسنت®) هو جسم مضاد بشري أحادي النسيلة IgG4 يرتبط بالوحدة الفرعية ألفا لمستقبل IL-4 (IL-4Rα) ويمنع نقل الإشارات لكل من IL-4 وIL-13. وهو معتمد لعلاج التهاب الجلد التأتبي (AD) والربو القصبي والتهاب الجيوب الأنفية المزمن مع الزوائد الأنفية.
في التجارب السريرية من المرحلة الثالثة، كان معدل حدوث التهاب الملتحمة في مجموعة دوبيلوماب + الستيرويد الموضعي 14-19%، وهو أعلى بشكل ملحوظ من 8% في مجموعة الدواء الوهمي1). بعد التسويق، تشير بعض التقارير إلى أن تواتر DIOSD (مرض سطح العين الناجم عن دوبيلوماب) قد يصل إلى 50%1). 80% من مضاعفات العين تحدث في غضون 4 أشهر من بدء العلاج، ولكن تم الإبلاغ عن حالات متأخرة بعد 52 أسبوعًا1).
DIOSD خاص بعلاج دوبيلوماب لالتهاب الجلد التأتبي (AD) ولم يتم الإبلاغ عنه عند استخدامه للربو أو التهاب الجيوب الأنفية. تشير هذه الانتقائية إلى أن سطح العين لدى مرضى AD ضعيف بالفعل1).
حاليًا، يُعتقد أن DIOSD خاص بعلاج دوبيلوماب لالتهاب الجلد التأتبي (AD)1). لم يتم الإبلاغ عن زيادة في تواتر التهاب الملتحمة عند استخدامه للربو أو التهاب الجيوب الأنفية المزمن مع الزوائد الأنفية. يُفترض أن سطح العين لدى مرضى AD، المتضرر بالفعل من الالتهاب التحسسي، يزيد من قابلية التأثر بالتغيرات في توازن السيتوكينات الناجمة عن دوبيلوماب.
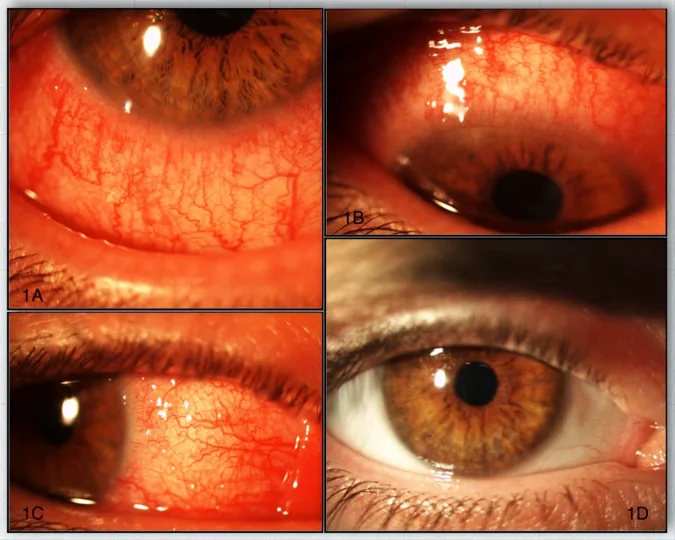
احتقان، حكة، تهيج، إحساس بجسم غريب، رهاب الضوء، دمعان، إفرازات عينية، وانخفاض الرؤية. كما أن الإحساس بالحرقة والشعور المستمر بـ”الرمال” في العين مميزان أيضًا 1). وقد يُبلغ أحيانًا عن ازدواج الرؤية الأحادي المتقطع.
في العلاج الأحادي بدوبيلوماب، يبدأ المرض بعد حوالي أسبوعين في المتوسط. في حالة الاستخدام المشترك مع الستيرويدات الموضعية، يتأخر ظهور الأعراض إلى 4-8 أسابيع.
يتطور DIOSD عبر المراحل الثلاث التالية. عادة ما يكون ثنائي الجانب ولكن غير متماثل.
| المرحلة | العلامات |
|---|---|
| مبكرة | خلل وظيفة غدة ميبوميوس، احتقان ملتحمي، التهاب ملتحمة حليمي، التهاب القرنية النقطي السطحي |
| متوسطة | التصاق الجفن بالملتحمة، فقدان الرموش، تقصير القبو، التهاب حوف القرنية |
| متقدمة | التصاق الجفنين، اختفاء القبو، تكنس سطح العين |
تصنف الصورة السريرية لـ DIOSD إلى الأنواع الخمسة التالية1).
1. التهاب الملتحمة المرتبط بدوبيلوماب (DAC): الأكثر شيوعًا (36-50%)، ويشمل أنواعًا غير محددة، حليمية، جريبية، والتهاب القرنية والملتحمة1). قد يظهر مع عقيدات ليمبية (تشبه بقع ترانتاس).
2. اضطرابات القرنية: تظهر على شكل التهاب القرنية النقطي السطحي، تآكل القرنية، أو قرحة القرنية1). غالبًا ما تكون مصحوبة بقصر زمن تمزق الدمع (BUT).
3. المضاعفات الليفية: تم الإبلاغ عن التهاب الملتحمة الندبي، الشتر الندبي، وتضيق النقاط الدمعية1).
4. جفاف العين: ناتج عن نقص الخلايا الكأسية وخلل وظيفة الغدة الدمعية1). يؤدي إلى عدم استقرار الطبقة الدمعية والتهاب الغشاء المخاطي.
5. التهاب الجفن والتهاب الملتحمة الجفني: يظهر مع تورم الجفن، احمرار، والتهاب الجلد حول الحجاج1). التهاب الملتحمة الجفني الندبي هو مضاعفة خطيرة.
عوامل الخطر المستقلة
جرعة دوبيلوماب: تزداد المخاطر مع الجرعات العالية
شدة التهاب الجلد التأتبي (AD): معدل حدوث أعلى في AD المتوسط إلى الشديد
تاريخ التهاب الملتحمة قبل العلاج: أمراض سطح العين الموجودة مسبقًا تتنبأ بقوة بحدوث DIOSD
جوهر المرض
تثبيط IL-13: IL-13 هو السيتوكين الأكثر هيمنة على سطح العين، وهو ضروري لتمايز الخلايا الكأسية وإفراز الميوسين1). يؤدي تثبيط IL-13 بواسطة دوبيلوماب إلى نقص تنسج الخلايا الكأسية وانخفاض إفراز الميوسين
اختلال توازن Th1/Th2: يؤدي تثبيط IL-4/IL-13 إلى تحفيز استجابة مناعية سائدة Th1 (زيادة IFN-γ)، مما يقلل كثافة الخلايا الكأسية أكثر1)
نتائج الخزعة: تظهر خزعة الملتحمة انخفاضًا ملحوظًا في كثافة الخلايا الكأسية (الوسيط 3.3 خلية/مم، مقابل 32.3 خلية/مم في المجموعة الضابطة) وارتشاحًا داخل الظهارة للخلايا التائية CD3+/CD4+ والحمضات1)
تشخيص DIOSD هو تشخيص سريري يعتمد على التاريخ المرضي والنتائج السريرية. لا يُستخدم الفحص المخبري أو الخزعة عادةً.
التاريخ المرضي المطلوب: استخدام دوبيلوماب لعلاج التهاب الجلد التأتبي المتوسط إلى الشديد. أن يكون وقت ظهور الأعراض بعد بدء دوبيلوماب (عادةً 2-8 أسابيع).
يتم تقييم مرحلة المرض والتشخيص باستخدام الفحوصات التالية.
صبغ القرنية والملتحمة: استخدام الفلوريسئين واللون الأخضر الليساساميني لتقييم سلامة الملتحمة.
اختبار شيرمر: تشير كمية الدموع الأقل من 10 مم إلى تلف الغدة الدمعية في الحالات المتقدمة.
زمن تكسر طبقة الدموع (TBUT): يشير التقصير إلى نقص الميوسين.
اختبار حساسية القرنية: يتم تقييمه باستخدام قطعة قطن أو مقياس حساسية القرنية Cochet-Bonnet.
أهم تشخيص تفريقي هو التهاب القرنية والملتحمة التأتبي (AKC) الموجود قبل بدء دوبيلوماب. في AKC، تزداد كثافة الخلايا الكأسية، بينما في DIOSD تنخفض1). تشمل التشخيصات التفريقية الأخرى التهاب الملتحمة التحسسي، التهاب الملتحمة الفيروسي، الفقاع العيني، ومرض الطعم ضد الثوي العيني.
هدف علاج DIOSD هو السيطرة على الالتهاب واستعادة وظيفة الخلايا الكأسية. عادة لا يكون إيقاف دوبيلوماب ضروريًا، ويمكن الاستمرار فيه مع العلاج العيني 1).
الخط الأول
قطرات الستيرويد منخفضة الفعالية: مع فلوروميثولون 0.1%، اختفت الأعراض تمامًا في 2 من 5 حالات وتحسنت بشكل ملحوظ في 3 حالات 1). يجب مراقبة ارتفاع ضغط العين.
مرهم تاكروليمس العيني: مع مرهم تاكروليمس 0.03%، اختفت الأعراض تمامًا في 2 من 4 حالات وتحسنت بشكل ملحوظ في حالتين 1). قد تزيد مثبطات الكالسينيورين من الخلايا الكأسية وتمنع موت الخلايا الظهارية.
قطرات السيكلوسبورين: يستخدم محلول سيكلوسبورين 0.05% كعلاج صيانة. تم الإبلاغ عن السيطرة دون انتكاس عند استخدامه مع بريدنيزولون أسيتات 1%.
العلاج المساعد
الدموع الاصطناعية: تستخدم للحفاظ على رطوبة سطح العين. غالبًا ما تكون غير كافية بمفردها.
الكمادات الدافئة وتدليك الجفن: فعالة في حالات MGD المصاحبة 1).
قطرات مضادات الهيستامين: غير فعالة بمفردها 1).
اختبار البقعة: يُجرى عند الاشتباه في وجود حساسية تلامسية. تم الإبلاغ عن تحسن DIOSD بتجنب المستحلبات والمواد الخافضة للتوتر السطحي والعطور 1).
في معظم الحالات، لا يكون الإيقاف ضروريًا 1). تتحسن جميع حالات DIOSD تقريبًا بالعلاج العيني (قطرات الستيرويد أو مثبطات الكالسينيورين). نظرًا لأن دوبيلوماب فعال جدًا في علاج التهاب الجلد التأتبي والربو، فإن إيقافه قد يؤدي إلى تفاقم الأمراض الجهازية، لذا من الشائع الاستمرار فيه مع العلاج العيني. ومع ذلك، في حالات المضاعفات الندبية الشديدة (التهاب الملتحمة الندبي أو قرحة القرنية) أو المقاومة للعلاج، يناقش الفريق متعدد التخصصات إمكانية الإيقاف.
آلية DIOSD معقدة، وقد تم اقتراح الفرضيات الخمس التالية 1).
تثبيط IL-4/IL-13 بواسطة دوبيلوماب يثبط استجابة Th2 بينما تصبح السيتوكينات Th1 (IFN-γ) هي السائدة 1). يقلل IFN-γ من كثافة الخلايا الكأسية ويقلل إفراز الميوسين.
قد يؤدي تثبيط IL-4/IL-13 إلى تكاثر الديموديكس وتحفيز التهاب شبيه بالوردية بوساطة IL-17 1).
يُشار إلى احتمال تنشيط إشارات غير طبيعية بوساطة OX40L مما يؤدي إلى حالة شبيهة بالتهاب الملتحمة الربيعي 1).
قد يزداد عدد الحمضات في الدم المحيطي أثناء العلاج بدوبيلوماب، وقد يشارك تسلل الحمضات إلى سطح العين في الالتهاب 1).
هذه هي الفرضية الأكثر قوة 1). IL-13 هو السيتوكين الأكثر هيمنة على سطح العين، وهو ضروري لتمايز الخلايا الكأسية وإفراز الميوسين 1). يؤدي تثبيط IL-13 بواسطة دوبيلوماب إلى نقص تنسج الخلايا الكأسية، مما يؤدي إلى سلسلة من انخفاض إفراز الميوسين، وعدم استقرار الغشاء الدمعي، والتهاب الغشاء المخاطي 1). تُسمى هذه الحالة DAMD (نقص الميوسين المرتبط بدوبيلوماب) 1).
في خزعة الملتحمة التي أجراها Bakker وآخرون، تم تأكيد انخفاض كبير في الخلايا الكأسية (3.3 خلية/مم مقابل 32.3 خلية/مم في المجموعة الضابطة) وتسلل الحمضات والخلايا التائية لدى مرضى DIOSD 1). هذا يتناقض مع زيادة الخلايا الكأسية (ارتفاع تعبير IL-13) في التهاب الملتحمة التحسسي وAKC، مما يؤكد أن DIOSD هي كيان مرضي مستقل 1).
في التهاب الملتحمة التحسسي والتهاب القرنية والملتحمة التأتبي (AKC)، يكون تعبير IL-13 مرتفعًا وتكون كثافة الخلايا الكأسية متزايدة وإفراز الميوسين مرتفعًا أيضًا. بينما في DIOSD، يثبط دوبيلوماب IL-13، وبالتالي تنخفض كثافة الخلايا الكأسية 1). تظهر نتائج الخزعة أن كثافة الخلايا الكأسية تنخفض إلى حوالي عُشر المجموعة الضابطة 1). باختصار، كلاهما من أمراض سطح العين الالتهابية، لكن التغيرات في الخلايا الكأسية متعاكسة تمامًا، وآليات المرض مختلفة جوهريًا.
DIOSD وDAMD هما مفهومان مرضيان جديدان نسبيًا، وقد انتشر الوعي بهما بسرعة بعد تسويق دواء دوبيلوماب 1). تأكيد انخفاض الخلايا الكأسية عبر خزعة الملتحمة دفع فهم هذه الحالة المرضية قدمًا بشكل كبير 1).
يُقترح أن التهاب الجلد التماسي قد يكون عاملًا معدلًا لـ DIOSD. هناك تقارير تفيد بأن تجنب المواد المسببة للحساسية المحددة عبر اختبار الرقعة (المستحلبات، المواد الخافضة للتوتر السطحي، العطور) أدى إلى تحسن DIOSD لدى بعض المرضى 1).
هناك حاجة إلى توضيح الآلية التي تستعيد بها مثبطات الكالسينيورين كثافة الخلايا الكأسية، والتنبؤ بحدوث DIOSD باستخدام المؤشرات الحيوية، وتجميع بيانات النتائج طويلة المدى. كما يُشار إلى أن خلل استقلاب حمض الريتينويك قد يشارك في DIOSD 1)، وقد يتم دراسة دور العلاج بفيتامين أ في المستقبل.
- Reji MA, Haque A, Goyal S, Krishnaswamy G. Dupilumab-induced ocular surface disease: a primer. BMJ Case Rep. 2022;15:e249019.