स्वतंत्र जोखिम कारक
डुपिलुमैब की खुराक : उच्च खुराक से जोखिम बढ़ता है
AD की गंभीरता : मध्यम से गंभीर AD में घटना दर अधिक होती है
उपचार से पहले नेत्रश्लेष्मलाशोथ का इतिहास : पूर्व-मौजूद नेत्र सतह रोग DIOSD के विकास की दृढ़ता से भविष्यवाणी करता है

डुपिलुमैब (व्यापारिक नाम: डुपिक्सेंट®) एक मानव मोनोक्लोनल IgG4 एंटीबॉडी है जो IL-4 रिसेप्टर अल्फा सबयूनिट (IL-4Rα) से जुड़ता है और IL-4 तथा IL-13 के सिग्नल ट्रांसमिशन को रोकता है। यह एटोपिक जिल्द की सूजन (AD), ब्रोन्कियल अस्थमा और नाक के जंतु के साथ क्रोनिक साइनसाइटिस के लिए अनुमोदित है।
चरण 3 नैदानिक परीक्षणों में, डुपिलुमैब + सामयिक स्टेरॉयड समूह में नेत्रश्लेष्मलाशोथ की घटना 14-19% थी, जो प्लेसीबो समूह के 8% से काफी अधिक थी1)। बाजार में आने के बाद, DIOSD (डुपिलुमैब-प्रेरित नेत्र सतह रोग) की आवृत्ति 50% तक पहुँचने की रिपोर्टें हैं1)। 80% नेत्र जटिलताएँ उपचार शुरू होने के 4 महीने के भीतर होती हैं, लेकिन 52 सप्ताह के बाद देर से होने वाले मामले भी रिपोर्ट किए गए हैं1)।
DIOSD, AD के लिए डुपिलुमैब उपचार के लिए विशिष्ट है और अस्थमा या साइनसाइटिस में इसके उपयोग में रिपोर्ट नहीं किया गया है। यह चयनात्मकता बताती है कि AD रोगियों की नेत्र सतह पहले से ही कमजोर होती है1)।
वर्तमान में, DIOSD को एटोपिक जिल्द की सूजन (AD) के लिए डुपिलुमैब उपचार के लिए विशिष्ट माना जाता है1)। अस्थमा या नाक के जंतु के साथ क्रोनिक साइनसाइटिस में उपयोग में नेत्रश्लेष्मलाशोथ की आवृत्ति में वृद्धि की रिपोर्ट नहीं है। यह अनुमान लगाया जाता है कि AD रोगियों की नेत्र सतह, जो पहले से एलर्जी सूजन से क्षतिग्रस्त है, डुपिलुमैब द्वारा साइटोकाइन संतुलन में परिवर्तन के प्रति अधिक संवेदनशील होती है।
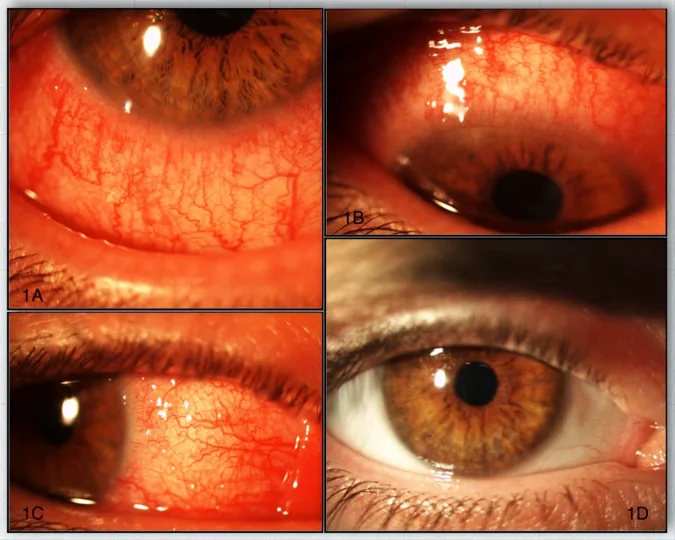
लालिमा, खुजली, जलन, विदेशी शरीर की अनुभूति, प्रकाश के प्रति संवेदनशीलता, आंसू आना, आंख से स्राव, दृष्टि में कमी। जलन और लगातार ‘रेत जैसा’ महसूस होना भी विशेषता है1)। कभी-कभी रुक-रुक कर एककोशिकीय दोहरी दृष्टि की भी सूचना मिली है।
डुपिलुमैब मोनोथेरेपी में, औसतन लगभग 2 सप्ताह बाद लक्षण शुरू होते हैं। सामयिक स्टेरॉयड के साथ संयोजन में, शुरुआत थोड़ी देर से होती है, 4-8 सप्ताह बाद।
DIOSD निम्नलिखित तीन चरणों में बढ़ता है। यह आमतौर पर द्विपक्षीय लेकिन असममित होता है।
| चरण | निष्कर्ष |
|---|---|
| प्रारंभिक | MGD, कंजंक्टिवल लालिमा, पैपिलरी कंजंक्टिवाइटिस, सतही बिंदु केराटोपैथी |
| मध्यवर्ती | सिम्बलिफेरॉन, मैडारोसिस, फोर्निक्स का छोटा होना, लिंबल केराटाइटिस |
| उन्नत | एंकिलोब्लेफेरॉन, फोर्निक्स का गायब होना, नेत्र सतह का केराटिनाइजेशन |
DIOSD के नैदानिक चित्र को निम्नलिखित 5 प्रकारों में वर्गीकृत किया गया है1)।
1. डुपिलुमैब-संबंधित नेत्रश्लेष्मलाशोथ (DAC) : सबसे आम (36-50%), इसमें गैर-विशिष्ट, पैपिलरी, कूपिक और केराटोकोनजंक्टिवाइटिस प्रकार शामिल हैं1)। कभी-कभी लिंबल नोड्यूल (ट्रांटास स्पॉट जैसे) भी हो सकते हैं।
2. कॉर्नियल विकार : सतही पंक्टेट केराटाइटिस, कॉर्नियल क्षरण या कॉर्नियल अल्सर के रूप में प्रकट होता है1)। अक्सर BUT में कमी के साथ जुड़ा होता है।
3. फाइब्रोटिक जटिलताएँ : सिकाट्रिकियल नेत्रश्लेष्मलाशोथ, सिकाट्रिकियल एक्ट्रोपियन और लैक्रिमल पंक्टल स्टेनोसिस की सूचना मिली है1)।
4. ड्राई आई : गॉब्लेट कोशिकाओं में कमी और लैक्रिमल ग्रंथि की शिथिलता के कारण1)। अश्रु फिल्म की अस्थिरता और म्यूकोसल सूजन का कारण बनता है।
5. ब्लेफेराइटिस और ब्लेफेरोकोनजंक्टिवाइटिस : पलकों की सूजन, लालिमा और पेरीऑर्बिटल त्वचाशोथ के साथ प्रस्तुत होता है1)। सिकाट्रिकियल ब्लेफेरोकोनजंक्टिवाइटिस एक गंभीर जटिलता है।
स्वतंत्र जोखिम कारक
डुपिलुमैब की खुराक : उच्च खुराक से जोखिम बढ़ता है
AD की गंभीरता : मध्यम से गंभीर AD में घटना दर अधिक होती है
उपचार से पहले नेत्रश्लेष्मलाशोथ का इतिहास : पूर्व-मौजूद नेत्र सतह रोग DIOSD के विकास की दृढ़ता से भविष्यवाणी करता है
रोगजनन का सार
IL-13 अवरोध : IL-13 नेत्र सतह पर सबसे प्रमुख साइटोकाइन है, जो गॉब्लेट कोशिका विभेदन और म्यूसिन स्राव के लिए आवश्यक है1)। डुपिलुमैब द्वारा IL-13 अवरोध गॉब्लेट कोशिका हाइपोप्लासिया और म्यूसिन स्राव में कमी का कारण बनता है।
Th1/Th2 संतुलन का विचलन : IL-4/IL-13 अवरोध Th1-प्रधान प्रतिरक्षा प्रतिक्रिया (IFN-γ अतिरिक्त) को प्रेरित करता है, जिससे गॉब्लेट कोशिका घनत्व और कम हो जाता है1)।
बायोप्सी निष्कर्ष : कंजंक्टिवा बायोप्सी में गॉब्लेट कोशिका घनत्व में उल्लेखनीय कमी (माध्यिका 3.3 कोशिकाएं/मिमी, नियंत्रण में 32.3 कोशिकाएं/मिमी) और CD3+/CD4+ T कोशिकाओं तथा इओसिनोफिल्स की अंतरउपकला घुसपैठ पाई जाती है1)
DIOSD का निदान इतिहास और नैदानिक निष्कर्षों पर आधारित एक नैदानिक निदान है। प्रयोगशाला जांच या बायोप्सी आमतौर पर संकेतित नहीं होती हैं।
आवश्यक इतिहास : मध्यम से गंभीर एटोपिक जिल्द की सूजन के लिए डुपिलुमैब का वर्तमान उपयोग। लक्षणों की शुरुआत डुपिलुमैब शुरू करने के बाद (आमतौर पर 2-8 सप्ताह) होती है।
निम्नलिखित परीक्षण चरण और पूर्वानुमान का मूल्यांकन करते हैं।
कॉर्नियल और कंजंक्टिवल धुंधलापन : फ्लोरेसिन और लिसामाइन ग्रीन से कंजंक्टिवा की अखंडता का मूल्यांकन करें।
शिमर परीक्षण : 10 मिमी से कम आंसू मात्रा उन्नत मामलों में लैक्रिमल ग्रंथि क्षति का सुझाव देती है।
आंसू फिल्म टूटने का समय (TBUT) : कम होना म्यूसिन की कमी को दर्शाता है।
कॉर्नियल संवेदनशीलता परीक्षण : कपास झाड़ू या कोशे-बोनट कॉर्नियल एस्थेसियोमीटर से मूल्यांकन करें।
सबसे महत्वपूर्ण विभेदक निदान डुपिलुमैब शुरू करने से पहले मौजूद एटोपिक केराटोकंजंक्टिवाइटिस (AKC) है। AKC में गॉब्लेट कोशिका घनत्व बढ़ा होता है, जबकि DIOSD में घटा होता है1)। एलर्जिक कंजंक्टिवाइटिस, वायरल कंजंक्टिवाइटिस, ओकुलर सिकाट्रिशियल पेम्फिगॉइड और ओकुलर GVHD भी विभेदक निदान में शामिल हैं।
DIOSD के उपचार का लक्ष्य सूजन को नियंत्रित करना और गॉब्लेट कोशिका कार्य को बहाल करना है। डुपिलुमैब को बंद करना आमतौर पर आवश्यक नहीं है और इसे नेत्र उपचार के साथ जारी रखा जा सकता है 1)।
प्रथम पंक्ति
कम शक्ति वाली स्टेरॉयड आई ड्रॉप : फ्लुओरोमेथोलोन 0.1% से 5 में से 2 मामले पूरी तरह से ठीक हुए, 3 में उल्लेखनीय सुधार हुआ 1)। आंखों के दबाव बढ़ने पर ध्यान दें।
टैक्रोलिमस आई ऑइंटमेंट : 0.03% टैक्रोलिमस आई ऑइंटमेंट से 4 में से 2 मामले पूरी तरह से ठीक हुए, 2 में उल्लेखनीय सुधार हुआ 1)। कैल्सीन्यूरिन अवरोधक गॉब्लेट कोशिकाओं को बढ़ा सकते हैं और उपकला कोशिका मृत्यु को रोक सकते हैं।
साइक्लोस्पोरिन आई ड्रॉप : 0.05% CsA आई ड्रॉप का उपयोग रखरखाव चिकित्सा के रूप में करें। 1% प्रेडनिसोलोन एसीटेट के साथ संयोजन में पुनरावृत्ति के बिना प्रबंधन की रिपोर्ट है।
सहायक चिकित्सा
कृत्रिम आंसू : आंख की सतह को नम रखने के लिए उपयोग किया जाता है। अकेले अक्सर अपर्याप्त होते हैं।
गर्म सेक और पलक मालिश : MGD के साथ मामलों में प्रभावी 1)।
एंटीहिस्टामाइन आई ड्रॉप : अकेले प्रभावहीन 1)।
पैच टेस्ट : संपर्क एलर्जी के संदेह पर किया जाता है। इमल्सीफायर, सर्फेक्टेंट और सुगंध से परहेज से DIOSD में सुधार की रिपोर्ट है 1)।
अधिकांश मामलों में, बंद करना आवश्यक नहीं है 1)। DIOSD के लगभग सभी मामले नेत्र उपचार (स्टेरॉयड आई ड्रॉप या कैल्सीन्यूरिन अवरोधक) से ठीक हो जाते हैं। एडी और अस्थमा पर डुपिलुमैब की प्रभावशीलता को देखते हुए, प्रणालीगत रोग के बिगड़ने से बचने के लिए इसे आमतौर पर नेत्र उपचार के साथ जारी रखा जाता है। हालांकि, गंभीर निशान जटिलताओं (निशानयुक्त पलक नेत्रश्लेष्मलाशोथ, कॉर्नियल अल्सर) या उपचार प्रतिरोध के मामले में, बहुविषयक टीम द्वारा बंद करने पर चर्चा की जाती है।
DIOSD का तंत्र जटिल है; पाँच परिकल्पनाएँ प्रस्तावित की गई हैं 1)।
डुपिलुमैब द्वारा IL-4/IL-13 का अवरोध Th2 प्रतिक्रिया को दबाता है, जबकि Th1 साइटोकाइन (IFN-γ) प्रमुख हो जाते हैं 1)। IFN-γ गॉब्लेट कोशिका घनत्व को कम करता है और म्यूसिन स्राव को घटाता है।
IL-4/IL-13 के दमन से डेमोडेक्स का प्रसार हो सकता है और IL-17-मध्यस्थता वाली रोसैसिया-जैसी सूजन उत्पन्न हो सकती है 1)।
यह संकेत दिया गया है कि असामान्य OX40L-मध्यस्थ संकेतन सक्रिय हो सकता है, जिससे वसंतजन्य कैटरार जैसी स्थिति उत्पन्न होती है 1)।
डुपिलुमैब उपचार के दौरान परिधीय इओसिनोफिल गिनती बढ़ सकती है, और नेत्र सतह पर इओसिनोफिल घुसपैठ सूजन में योगदान कर सकती है 1)।
यह सबसे प्रबल परिकल्पना है 1)। IL-13 नेत्र सतह पर सबसे प्रमुख साइटोकाइन है और गॉब्लेट कोशिका विभेदन और म्यूसिन स्राव के लिए आवश्यक है 1)। डुपिलुमैब द्वारा IL-13 का अवरोध गॉब्लेट कोशिका हाइपोप्लासिया का कारण बनता है, जिससे म्यूसिन स्राव में कमी, अश्रु फिल्म अस्थिरता और श्लेष्मा सूजन की श्रृंखला उत्पन्न होती है 1)। इस स्थिति को DAMD (डुपिलुमैब-संबद्ध म्यूसिन की कमी) कहा जाता है 1)।
बक्कर एट अल. के कंजंक्टिवल बायोप्सी में, DIOSD रोगियों में गॉब्लेट कोशिकाओं में उल्लेखनीय कमी (3.3 कोशिकाएं/मिमी बनाम नियंत्रण 32.3 कोशिकाएं/मिमी) और इओसिनोफिल और टी कोशिका घुसपैठ की पुष्टि हुई 1)। यह एलर्जिक कंजंक्टिवाइटिस और AKC में गॉब्लेट कोशिका वृद्धि (उच्च IL-13 अभिव्यक्ति) के विपरीत है, जो DIOSD को एक स्वतंत्र रोग इकाई के रूप में स्थापित करता है 1)।
एलर्जिक कंजंक्टिवाइटिस और एटोपिक केराटोकंजंक्टिवाइटिस (AKC) में, IL-13 उच्च रूप से व्यक्त होता है और गॉब्लेट कोशिका घनत्व बढ़ा होता है, साथ ही म्यूसिन स्राव भी बढ़ा होता है। इसके विपरीत, DIOSD में, डुपिलुमैब IL-13 को अवरुद्ध करता है, जिससे गॉब्लेट कोशिका घनत्व कम हो जाता है 1)। बायोप्सी में गॉब्लेट कोशिका घनत्व नियंत्रण के लगभग दसवें हिस्से तक कम हो जाता है 1)। इस प्रकार, दोनों सूजन संबंधी नेत्र सतह रोग हैं, लेकिन गॉब्लेट कोशिकाओं में परिवर्तन विपरीत हैं, और रोगजनन तंत्र मौलिक रूप से भिन्न हैं।
DIOSD और DAMD अपेक्षाकृत नई रोग अवधारणाएँ हैं, जिनकी पहचान डुपिलुमाब के बाजार में आने के बाद तेजी से फैली है 1)। कंजंक्टिवल बायोप्सी द्वारा गॉब्लेट कोशिकाओं में कमी की पुष्टि ने इस रोग स्थिति की समझ को काफी आगे बढ़ाया है 1)।
संपर्क जिल्द की सूजन DIOSD का एक संशोधक कारक हो सकता है। पैच टेस्ट में पहचाने गए एलर्जेन (इमल्सीफायर, सर्फेक्टेंट, सुगंध) से परहेज करने से कुछ रोगियों में DIOSD में सुधार की रिपोर्टें हैं 1)।
कैल्सीन्यूरिन अवरोधकों द्वारा गॉब्लेट कोशिका घनत्व को बहाल करने के तंत्र को स्पष्ट करना, बायोमार्कर द्वारा DIOSD की शुरुआत का पूर्वानुमान लगाना, और दीर्घकालिक पूर्वानुमान डेटा का संचय आवश्यक है। रेटिनोइक एसिड चयापचय की असामान्यता DIOSD में शामिल हो सकती है 1), और विटामिन ए पूरक चिकित्सा की भूमिका पर भविष्य में विचार किया जा सकता है।
- Reji MA, Haque A, Goyal S, Krishnaswamy G. Dupilumab-induced ocular surface disease: a primer. BMJ Case Rep. 2022;15:e249019.