
Catarata Congénita
Puntos clave de un vistazo
Sección titulada «Puntos clave de un vistazo»1. ¿Qué es la catarata congénita?
Sección titulada «1. ¿Qué es la catarata congénita?»La catarata congénita, en sentido estricto, se refiere a la opacidad del cristalino presente al nacer. Por el contrario, las opacidades que se desarrollan después del nacimiento sin estar presentes al nacer se denominan cataratas del desarrollo. Las cataratas en la infancia sin causas como traumatismos a menudo se denominan colectivamente cataratas congénitas.
En cuanto a tener una predisposición congénita, las cataratas del desarrollo que aparecen temprano después del nacimiento y progresan pertenecen a la misma categoría. Clínicamente, deben manejarse de manera similar como “cataratas de inicio temprano”. “Catarata infantil” es un término integral que incluye todas las cataratas durante la infancia, incluidos los casos traumáticos, y abarca cataratas congénitas (en sentido estricto), del desarrollo y adquiridas.
Epidemiología
Sección titulada «Epidemiología»Es una enfermedad rara que ocurre en 1 de cada 1,000 a 10,000 nacimientos. El pronóstico visual y las estrategias de tratamiento difieren mucho entre los casos bilaterales y unilaterales, siendo los unilaterales de peor pronóstico visual (debido a que es más fácil que se establezca la ambliopía por privación de forma).
El vaso fetal persistente (PFV) es una causa importante de catarata congénita, a menudo asociada con afectación unilateral y microftalmia. Se encuentra PFV en aproximadamente el 20% de las cataratas infantiles 1).
En sentido estricto, la catarata congénita es la opacidad del cristalino ya presente al nacer, mientras que la catarata del desarrollo aparece después del nacimiento pero comparte una predisposición congénita. Clínicamente, ambas se manejan de manera similar como “cataratas de inicio temprano”, requiriendo diagnóstico temprano y cirugía para prevenir la ambliopía por privación de forma.
2. Síntomas principales y hallazgos clínicos
Sección titulada «2. Síntomas principales y hallazgos clínicos»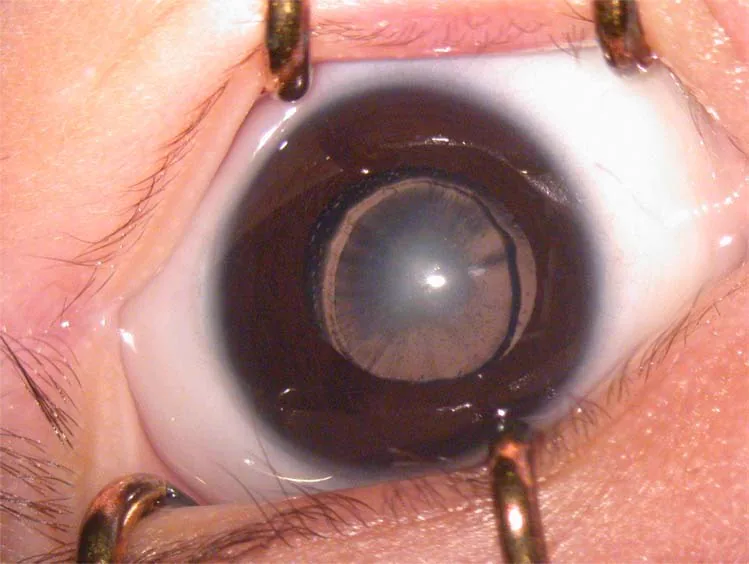
Síntomas subjetivos y pistas para la detección
Sección titulada «Síntomas subjetivos y pistas para la detección»Dado que los lactantes no pueden quejarse de síntomas, la observación por parte de los padres y la detección durante los exámenes de salud infantil son importantes.
- Leucocoria (pupila blanca): Cuando la opacidad es severa, los padres pueden notar que el ojo parece blanco. Esta es una de las pistas más comunes para la detección.
- Estrabismo: En casos unilaterales, la ambliopía puede causar desalineación ocular.
- Nistagmo: Un signo de ambliopía avanzada en casos bilaterales. Cuando aparece, se requiere cirugía urgente.
- Mala agudeza visual / mala fijación: Sugiere el desarrollo de ambliopía por deprivación visual.
Hallazgos clínicos
Sección titulada «Hallazgos clínicos»A continuación se muestran indicadores que sugieren ambliopía por deprivación visual.
| Indicador | Descripción |
|---|---|
| Disminución de la agudeza visual | Reducción de la agudeza visual desproporcionada al grado de catarata |
| Mala fijación | Retraso en el desarrollo de las respuestas de fijación y seguimiento |
| Estrabismo | Desviación ocular debida a ambliopía unilateral |
| Nistagmo | Signo de ambliopía bilateral progresiva |
| Diferencia de longitud axial entre ojos | Asimetría de 0.5 mm o más |
Como criterio para determinar si la opacidad afecta la función visual, en casos unilaterales se considera que una opacidad de 3 mm o más afecta la función visual. Generalmente, las opacidades del cápsula posterior afectan más la función visual que las del cápsula anterior, las centrales más que las periféricas, y las densas más que las tenues.
A menudo se descubre cuando un padre nota una pupila blanca o durante el examen de fondo de ojo en los controles de salud infantil. También hay casos diagnosticados tras una visita al oftalmólogo motivada por estrabismo o mala fijación. En casos unilaterales, el ojo sano se usa predominantemente, lo que hace que la disminución de la visión sea menos notoria, por lo que el cribado activo durante los controles es importante.
3. Causas y factores de riesgo
Sección titulada «3. Causas y factores de riesgo»La etiología de la catarata congénita es diversa; la idiopática (causa desconocida) representa el 30–50%.
| Etiología | Frecuencia / Enfermedades representativas |
|---|---|
| Idiopática (causa desconocida) | 30–50%. La más frecuente |
| Hereditaria | Autosómica dominante es la más común. También autosómica recesiva y recesiva ligada al cromosoma X |
| Infección intrauterina | Rubéola (síndrome de rubéola congénita), herpes, CMV, toxoplasmosis, etc. |
| Trastornos metabólicos | Galactosemia, hipocalcemia, homocistinuria, síndrome de Lowe, síndrome de Alport, etc. |
| Anomalías cromosómicas | Síndrome de Down, etc. |
| Enfermedades oculares asociadas | Microftalmía, aniridia congénita, PFV (vasculatura fetal persistente), etc. |
| Enfermedades/síndromes sistémicos | Síndrome de Hallermann-Streiff, síndrome de Pierre Robin, etc. |
La PFV (vasculatura fetal persistente) es una causa importante de catarata congénita, resultante de la falta de regresión de los vasos del vítreo primario durante el período fetal. A menudo es unilateral y se asocia con microftalmía, y se encuentra en aproximadamente el 20% de las cataratas infantiles1). Cuando se extiende posteriormente (PFV tipo posterior), el pronóstico visual es malo.
Las cataratas congénitas hereditarias son más frecuentemente autosómicas dominantes. Si hay antecedentes familiares, se recomienda asesoramiento genético y cribado familiar. Cabe señalar que el 30–50% de las cataratas congénitas son idiopáticas, por lo que pueden ocurrir incluso sin antecedentes familiares.
4. Diagnóstico y métodos de exploración
Sección titulada «4. Diagnóstico y métodos de exploración»Clasificación morfológica
Sección titulada «Clasificación morfológica»Dado que las indicaciones de tratamiento difieren según la ubicación y morfología de la opacidad del cristalino, la clasificación morfológica es fundamental para el diagnóstico.
| Nombre de la clasificación | Nombre en inglés | Características |
|---|---|---|
| Catarata nuclear | nuclear cataract | Opacidad dentro de la sutura en Y. Congénita. Mal pronóstico visual. |
| Catarata laminar | lamellar (zonular) cataract | Opacidad laminar periférica a la sutura en Y. Común en cataratas del desarrollo. |
| Lenticono posterior | posterior lenticonus | Protrusión de la cápsula posterior con opacidad. Unilateral. Puede progresar a catarata total. |
| Catarata total | total cataract | Opacidad completa del cristalino |
| Catarata capsular | capsular cataract | Opacidad de la cápsula anterior, posterior o subcapsular |
| Catarata sutural | sutural cataract | Opacidad en la sutura en Y. Poco efecto sobre la función visual. |
| Catarata punctata | punctate cataract | Opacidades puntiformes. Raramente causan deterioro visual. |
| Catarata cerúlea | cerulean cataract | Opacidades puntiformes azules en la corteza. Sin deterioro de la función visual. |
Pruebas necesarias
Sección titulada «Pruebas necesarias»- Examen con lámpara de hendidura: Prueba básica para evaluar la morfología, ubicación, gravedad y extensión de la opacidad.
- Examen de fondo de ojo: Determina el grado de opacidad de la catarata según la visibilidad del fondo. Si la visibilidad es difícil, agregue ecografía en modo B.
- Medición de la longitud axial: Esencial para el cálculo de la potencia del LIO, la predicción del tamaño del cristalino y la detección temprana del glaucoma postoperatorio (alargamiento axial anormal).
- Prueba de refracción: Utilice un autorrefractómetro portátil o retinoscopio.
- Evaluación de la agudeza visual: Utilice el método PL (mirada preferencial: evaluación de la respuesta visual preferencial mediante agudeza de rejilla) y VEP (potencial evocado visual). Los valores de VEP por debajo del 40% de lo normal indican función visual reducida.
- Examen sistémico: El cribado de enfermedades sistémicas por un pediatra es obligatorio.
La indicación de cirugía se determina generalmente en función de la agudeza visual (agudeza de rejilla) y el estado de desarrollo de las respuestas visuales como la fijación y el seguimiento.
Momento de la indicación quirúrgica
Sección titulada «Momento de la indicación quirúrgica»A continuación se presentan las pautas para considerar una indicación quirúrgica activa.
| Tipo de ojo | Criterios de indicación | Pauta de momento quirúrgico real |
|---|---|---|
| Unilateral (catarata total) | Tratar como emergencia. | Preferiblemente dentro de los primeros días después del nacimiento. |
| Unilateral (opacidad severa) | Opacidad severa antes de las 6 semanas de vida | Alrededor de 1 mes de edad |
| Bilateral (opacidad severa) | Opacidad severa antes de las 12 semanas (3 meses) de vida | Alrededor de 2 meses de edad |
| Formas que pueden ser observadas | Catarata punctata, sutural, capsular anterior; catarata nuclear laminar o pulverulenta simétrica | Seguimiento regular |
La catarata total unilateral es una emergencia; se recomienda la cirugía dentro de los primeros días de vida, a menos que haya complicaciones graves.
La catarata total unilateral es una emergencia; se recomienda la cirugía dentro de los primeros días de vida para prevenir la ambliopía por deprivación visual. En casos bilaterales, se realiza cirugía temprana alrededor de los 2-3 meses de edad. La indicación quirúrgica se determina evaluando integralmente la agudeza visual y el desarrollo de respuestas visuales como fijación y seguimiento. En formas que no afectan la función visual, como catarata punctata o sutural, se prioriza la observación.
5. Tratamiento estándar
Sección titulada «5. Tratamiento estándar»Métodos quirúrgicos
Sección titulada «Métodos quirúrgicos»El procedimiento básico en niños menores de 6 años es la aspiración (facoemulsificación) del cristalino + capsulotomía posterior + vitrectomía anterior (± implante de LIO). En niños, para prevenir la opacificación capsular posterior (opacificación del eje visual), a diferencia de la técnica estándar en adultos, la capsulotomía posterior y la vitrectomía anterior son fundamentales. Tras la capsulotomía anterior con CCC, se aspira la corteza y el núcleo del cristalino, luego se realiza una CCC posterior y se practica una vitrectomía anterior con un cutter de vítreo.
A continuación se describen los tres procedimientos quirúrgicos principales.
| Procedimiento | Indicaciones principales | Puntos clave |
|---|---|---|
| Aspiración del cristalino + capsulotomía posterior + vitrectomía anterior | Procedimiento básico para niños menores de 6 años | La capsulotomía posterior y la vitrectomía anterior se realizan juntas para prevenir la opacificación de la cápsula posterior. |
| Aspiración del cristalino + capsulotomía posterior + vitrectomía anterior + implantación de LIO | Cuando se realiza la implantación de LIO | La abertura de capsulotomía ideal es de aproximadamente 5 mm. |
| Aspiración del cristalino + implantación de LIO (igual que en adultos) | 6 años o más | La capsulotomía posterior y la vitrectomía anterior pueden omitirse. |
Consideraciones sobre las indicaciones de LIO
Sección titulada «Consideraciones sobre las indicaciones de LIO»En cuanto a la conveniencia de la implantación de LIO en lactantes, el Estudio de Tratamiento de Afaquia Infantil (IATS) proporciona criterios. La implantación de LIO dentro de los primeros 6 meses de vida no mostró diferencias en la agudeza visual a los 4.5 años en comparación con el manejo con lentes de contacto (LC), y la tasa de reoperación por opacificación del eje visual fue significativamente mayor en el grupo de LIO. Por lo tanto, la implantación de LIO dentro de los primeros 6 meses se limita a casos seleccionados. Para niños de 2 años o más, generalmente se elige la implantación primaria de LIO.
Potencia objetivo del LIO
Sección titulada «Potencia objetivo del LIO»En niños, el globo ocular se desarrolla y se vuelve más miope con el crecimiento, por lo que la sobrecorrección anticipando el crecimiento ocular futuro es el enfoque básico.
| Edad en el momento de la implantación | Refracción objetivo postoperatoria | Propósito |
|---|---|---|
| 1 año de edad | Sobrecorrección de aproximadamente +5 D | Enfocar en visión cercana para promover el desarrollo visual |
| 2 años de edad | Sobrecorrección de aproximadamente +4 D | Igual que arriba |
| Después del crecimiento (alrededor de 20 años) | Miopía leve (aproximadamente -1 a 0 D) | Buscar estabilidad refractiva a largo plazo |
El material acrílico es deseable tanto para la parte háptica como para la óptica del LIO. Se recomienda un diámetro óptico de 6 mm o menos.
Precisión del cálculo del poder del LIO
Sección titulada «Precisión del cálculo del poder del LIO»En la implantación primaria de LIO en niños, la precisión predictiva de las fórmulas de cálculo actuales es significativamente menor que en adultos. En un estudio de 108 ojos de 83 pacientes, la precisión predictiva dentro de ±1.00 D de ocho fórmulas (Holladay 1, SRK/T, Hoffer Q, Haigis, Barrett Universal II, Kane, EVO 2.0, Ladas Super Formula) fue solo del 35.2–43.5% (en adultos, 93.5–100%) 2). Las fórmulas SRK/T y Kane mostraron un rendimiento relativamente bueno, y la edad temprana y la longitud axial corta fueron los principales predictores de sorpresa refractiva (error de predicción ≥ ±2.00 D) 2). No hubo diferencias significativas en la precisión predictiva según la técnica quirúrgica o el tipo de LIO 2).
Corrección refractiva postoperatoria
Sección titulada «Corrección refractiva postoperatoria»- Postoperatorio unilateral: La corrección con lentes de contacto (LC) es el estándar. Las LC blandas suelen tener una potencia limitada a aproximadamente +25 D; por encima de eso, se usan LC rígidas.
- Postoperatorio bilateral: Es posible el manejo con gafas. En la infancia, se utilizan monturas especiales.
- Incluso en ojos con LIO, se necesitan gafas si persiste hipermetropía residual.
- Después de la edad escolar, se pueden considerar gafas bifocales.
Tratamiento de la ambliopía
Sección titulada «Tratamiento de la ambliopía»En casos unilaterales y bilaterales con diferencia interocular, es necesario ocluir el ojo sano. Según el protocolo de oclusión del IATS, hasta los 8 meses de edad, el tiempo de oclusión es igual a la edad en meses (ej., bebé de 4 meses → 4 horas); después de los 8 meses, la oclusión se dirige a la mitad de las horas de vigilia.
Resultados quirúrgicos de la catarata congénita con PFV
Sección titulada «Resultados quirúrgicos de la catarata congénita con PFV»En un estudio de registro multicéntrico del Pediatric Eye Disease Investigator Group (PEDIG), se informaron los resultados a 5 años de 64 ojos con PFV (48 afáquicos, 16 pseudofáquicos) 1). La mediana de edad en la cirugía para los ojos afáquicos fue de 2 meses, y el 96% se sometió a vitrectomía anterior. Solo el 10% (4/42 ojos, IC 95% 3–23%) logró una agudeza visual apropiada para la edad a los 5 años. Una agudeza visual mejor de 20/200 se logró en el 59% (17/29 ojos) de los ojos afáquicos con PFV, en comparación con solo el 23% (3/13 ojos) de los ojos pseudofáquicos con PFV 1). La PFV posterior (con anomalías vítreas, retinianas o del nervio óptico) tendió a tener peor pronóstico visual que la PFV anterior (mediana de agudeza visual 20/800 vs. 20/100) 1).
Según los resultados del IATS, la implantación de LIO dentro de los 6 meses de edad no muestra diferencias en la agudeza visual en comparación con el manejo con lentes de contacto, pero tiene una mayor tasa de opacificación del eje visual que requiere reintervención. Por lo tanto, la implantación de LIO durante este período se limita a casos seleccionados. En niños de 2 años o más, generalmente se elige la implantación primaria de LIO. La potencia de la LIO se selecciona con el objetivo de una sobrecorrección en previsión del cambio miópico con el crecimiento.
6. Fisiopatología y mecanismos detallados
Sección titulada «6. Fisiopatología y mecanismos detallados»Mecanismo de la ambliopía por privación de forma
Sección titulada «Mecanismo de la ambliopía por privación de forma»Las opacidades del cristalino causan ambliopía por privación de forma al bloquear la luz a lo largo del eje visual. Cuando se bloquea la estimulación visual adecuada durante el período crítico del desarrollo visual, se altera el desarrollo de la corteza visual.
El período crítico se extiende hasta las 6 semanas después del nacimiento para casos monoculares y hasta las 10–12 semanas para casos binoculares. Si existe una catarata que afecta la función visual antes del período crítico, la ambliopía se desarrolla particularmente rápido en casos monoculares. La adquisición de la función visual comienza durante el período crítico y se completa alrededor de los 10 años de edad.
La ambliopía por privación de forma es más grave y más resistente al tratamiento que la ambliopía refractiva ordinaria. Esta es la razón por la cual la cirugía temprana es indispensable.
Mecanismo de la catarata secundaria (opacificación de la cápsula posterior)
Sección titulada «Mecanismo de la catarata secundaria (opacificación de la cápsula posterior)»En niños, las células epiteliales del cristalino son altamente activas, y la opacificación de la cápsula posterior (catarata secundaria) ocurre con mayor frecuencia y más temprano después de la cirugía en comparación con los adultos. Las células epiteliales del cristalino residuales proliferan después de la cirugía, migran sobre la cápsula posterior y bloquean el eje visual. Por lo tanto, en niños menores de 6 años, la técnica quirúrgica estándar incluye capsulotomía posterior y vitrectomía anterior intraoperatorias para prevenir el desarrollo de catarata secundaria.
Diferencias en la morfología de la opacidad y el impacto en la función visual
Sección titulada «Diferencias en la morfología de la opacidad y el impacto en la función visual»El impacto en la función visual y la indicación de cirugía difieren según la ubicación y la morfología de la opacidad del cristalino. Las cataratas nucleares producen opacidades densas directamente en el eje visual, lo que conduce a un mal pronóstico visual y requiere cirugía temprana. Las cataratas suturales y punctiformes tienen menos probabilidades de afectar el desarrollo visual y a menudo pueden ser observadas. El lenticono posterior es a menudo unilateral, con protrusión de la cápsula posterior y opacificación progresiva que puede eventualmente conducir a una catarata total.
Desarrollo del cristalino y causas de opacificación
Sección titulada «Desarrollo del cristalino y causas de opacificación»La aparición de cataratas congénitas se basa en anomalías en el desarrollo embrionario del cristalino. El cristalino se forma a partir de la vesícula del cristalino derivada del ectodermo; el núcleo está compuesto por fibras primarias del cristalino (la base de las cataratas nucleares) y la corteza por fibras secundarias del cristalino (la base de las cataratas laminares y suturales). Las infecciones intrauterinas como el virus de la rubéola dañan directamente la formación de fibras del cristalino fetal. En trastornos metabólicos (p. ej., galactosemia), el galactitol acumulado aumenta la presión osmótica dentro del cristalino, causando sobrehidratación y opacificación del cristalino. En cataratas hereditarias, las anomalías funcionales de las proteínas cristalinas o de membrana (p. ej., conexinas) alteran el mantenimiento de la transparencia del cristalino.
7. Complicaciones postoperatorias y pronóstico a largo plazo
Sección titulada «7. Complicaciones postoperatorias y pronóstico a largo plazo»Catarata secundaria (opacificación del eje visual)
Sección titulada «Catarata secundaria (opacificación del eje visual)»En casos operados durante la infancia, la contracción del borde de la capsulotomía anterior y las opacidades tipo perlas de Elschnig ocurren en casi el 100% de los casos. El tratamiento es el siguiente.
- 1 año o más: es posible la capsulotomía posterior con láser Nd:YAG
- Si el láser es difícil en menores de 6 años: realizar capsulotomía posterior quirúrgica y vitrectomía anterior
La incidencia acumulada a 5 años de opacificación del eje visual en ojos pseudofáquicos con PFV fue del 45% (IC 95% 13–66%) 1). La incidencia de opacificación del eje visual cuando se realizó vitrectomía anterior en la cirugía primaria fue del 18% (IC 95% 8–28%), significativamente menor que el 60% (IC 95% 0–84%) cuando no se realizó 1).
Glaucoma secundario
Sección titulada «Glaucoma secundario»Esta es la complicación tardía más importante después de la cirugía de catarata congénita.
- Incidencia: ocurre en el 18–26% de los casos postoperatorios
- Factores de riesgo: edad más joven en el momento de la cirugía, microftalmos
- Momento de aparición: puede ocurrir más de 10 años después de la cirugía. El seguimiento a largo plazo es esencial.
La incidencia acumulada a 5 años de eventos adversos relacionados con glaucoma en ojos afáquicos con PFV fue del 24% (IC 95% 9–37%), y en ojos pseudofáquicos fue del 7% (IC 95% 0–20%) 1). No hubo diferencia significativa en el riesgo de glaucoma entre ojos con PFV y sin PFV (HR ajustado por edad=1.20, IC 95% 0.54–2.64, P=0.66), y el PFV en sí mismo no fue un factor de riesgo independiente para glaucoma 1).
Incidencia acumulada a 5 años de complicaciones en catarata congénita con PFV
Sección titulada «Incidencia acumulada a 5 años de complicaciones en catarata congénita con PFV»| Complicación | Ojo afáquico con PFV | Ojo pseudofáquico con PFV |
|---|---|---|
| Eventos adversos relacionados con glaucoma | 24% (IC 95% 9–37%) | 7% (IC 95% 0–20%) |
| Opacificación del eje visual (con vitrectomía anterior) | 18% (IC 95%: 8–28%) | — |
| Opacificación del eje visual (sin vitrectomía anterior) | 60% (IC 95%: 0–84%) | 45% (IC 95%: 13–66%) |
| Desprendimiento de retina | 4% (IC 95%: 0–10%) | 7% (IC 95%: 0–19%) |
Otras complicaciones
Sección titulada «Otras complicaciones»- Contracción capsular anterior: El borde de la capsulotomía anterior se contrae, reduciendo la abertura capsular. La progresión puede causar deterioro visual.
- Desprendimiento de retina: El riesgo es particularmente alto en casos con PFV.
Factores que afectan el pronóstico visual
Sección titulada «Factores que afectan el pronóstico visual»- Grado de ambliopía por deprivación de forma (la presencia de cirugía temprana es lo más importante)
- Presencia de comorbilidades oculares (microcórnea y microftalmos indican mal pronóstico)
- Corrección refractiva adecuada y continuación del tratamiento de la ambliopía después de la cirugía
- Comprensión y cooperación de los padres/tutores
El glaucoma secundario es la complicación más importante. Ocurre en el 18–26% de los casos después de la cirugía y puede desarrollarse incluso 10 años o más después de la operación, por lo que se requieren controles regulares de la presión intraocular incluso en la edad adulta. La opacificación de la cápsula posterior (opacificación del eje visual) ocurre en casi todos los casos de cirugía infantil, pero el tratamiento con láser YAG es posible para niños de 1 año o más, y pueden ser necesarios procedimientos invasivos para menores de 6 años.
8. Investigación más reciente y perspectivas futuras
Sección titulada «8. Investigación más reciente y perspectivas futuras»Mejora de la precisión de las fórmulas de cálculo de potencia del LIO pediátrico
Sección titulada «Mejora de la precisión de las fórmulas de cálculo de potencia del LIO pediátrico»La precisión predictiva de las fórmulas actuales de cálculo de potencia del LIO pediátrico es insuficiente en comparación con los adultos, y las fórmulas de nueva generación (Kane, Barrett Universal II, etc.) no han mostrado una clara superioridad sobre las fórmulas convencionales (SRK/T, etc.) 2). La precisión predictiva dentro de ±1.00D es solo del 35.2–43.5% para las ocho fórmulas actuales, una brecha significativa con el 93.5–100% en adultos 2).
Se requiere el desarrollo de algoritmos dedicados que tengan en cuenta la longitud axial corta, la curvatura corneal pronunciada, la profundidad de la cámara anterior superficial y el crecimiento ocular específicos de los niños 2). No hay diferencias significativas en la precisión predictiva según la técnica quirúrgica o el tipo de LIO, y en la actualidad, la corrección refractiva postoperatoria activa y el seguimiento son medidas complementarias importantes.
9. Referencias
Sección titulada «9. Referencias»- Haider KM, Repka MX, Sutherland DR, et al. Outcomes and Complications 5 Years After Surgery for Pediatric Cataract Associated With Persistent Fetal Vasculature. Am J Ophthalmol. 2024;261:156-165.
- Jin J, Shen Y, Qu Y, et al. Accuracy of new-generation and traditional intraocular lens power calculation formulas in pediatric primary implantation. J Cataract Refract Surg. 2024.
- Kaur S, Yangzes S, Ram J. Unilateral Congenital Cataract. J Pediatr Ophthalmol Strabismus. 2019;56(1):60-61. PMID: 30673102.
