
Cataracte congénitale
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que la cataracte congénitale ?
Section intitulée « 1. Qu’est-ce que la cataracte congénitale ? »La cataracte congénitale (congenital cataract) désigne, au sens strict, une opacité du cristallin présente à la naissance. En revanche, une opacité qui se développe après la naissance sans être présente à la naissance est appelée cataracte développementale. Les cataractes survenant chez le nourrisson et le jeune enfant sans cause traumatique sont souvent regroupées sous le terme de cataracte congénitale.
Du point de vue de la prédisposition congénitale, la cataracte développementale, qui apparaît tôt après la naissance et dont l’opacité progresse, appartient à la même catégorie. Cliniquement, elle doit être traitée comme une « cataracte précoce ». La « cataracte pédiatrique » est un terme global incluant toutes les cataractes de l’enfance, y compris les cas traumatiques, et englobe la cataracte congénitale (au sens strict), la cataracte développementale et la cataracte acquise.
Épidémiologie
Section intitulée « Épidémiologie »C’est une maladie rare survenant chez 1 naissance sur 1 000 à 10 000. Le pronostic visuel et la stratégie thérapeutique diffèrent considérablement entre les formes bilatérales et unilatérales, le pronostic étant moins bon pour les formes unilatérales (en raison du risque plus élevé d’amblyopie par privation de forme).
La persistance du vitré primitif (persistent fetal vasculature, PFV) est une cause importante de cataracte congénitale, souvent associée à une cataracte unilatérale et à une microphtalmie. Environ 20 % des cataractes du nourrisson sont associées à une PFV1).
La cataracte congénitale au sens strict est une opacité du cristallin déjà présente à la naissance, tandis que la cataracte développementale apparaît après la naissance mais partage une prédisposition congénitale. Cliniquement, les deux sont traitées comme une « cataracte précoce », nécessitant un diagnostic et une chirurgie précoces pour prévenir l’amblyopie par privation de forme.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »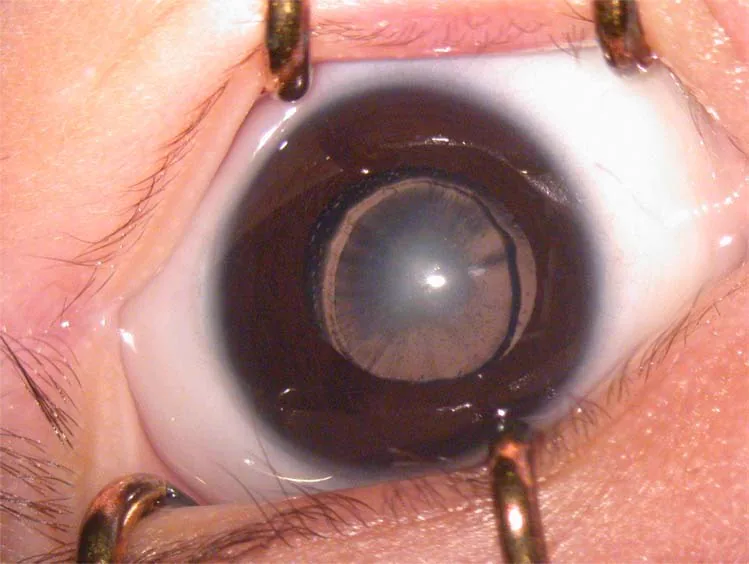
Symptômes subjectifs / Circonstances de découverte
Section intitulée « Symptômes subjectifs / Circonstances de découverte »Les nourrissons et les jeunes enfants ne pouvant pas exprimer leurs symptômes, l’observation par les parents et la détection lors des examens de santé infantile sont essentielles.
- Leucocorie (pupille blanche) : En cas d’opacité importante, les parents remarquent que « l’œil est blanc ». C’est l’un des signes de découverte les plus fréquents.
- Strabisme : En cas de cataracte unilatérale avec amblyopie, un décalage de l’axe oculaire peut apparaître.
- Nystagmus (oscillations oculaires) : Signe d’une amblyopie bilatérale avancée. Son apparition nécessite une intervention chirurgicale urgente.
- Mauvaise acuité visuelle / fixation instable : Suggère la formation d’une amblyopie par privation de forme.
Signes cliniques
Section intitulée « Signes cliniques »Les indicateurs suggérant une amblyopie par privation de forme sont présentés ci-dessous.
| Indicateur | Contenu |
|---|---|
| Baisse de l’acuité visuelle | Baisse de l’acuité visuelle disproportionnée par rapport au degré de la cataracte |
| Mauvaise fixation | Retard de développement des réactions de fixation et de poursuite |
| Strabisme | Déviation oculaire due à une amblyopie monoculaire |
| Nystagmus | Signe d’amblyopie bilatérale avancée |
| Différence de longueur axiale entre les yeux | Asymétrie ≥ 0,5 mm |
Comme critère de jugement d’une opacité affectant la fonction visuelle, une opacité de 3 mm ou plus dans un œil unilatéral est considérée comme ayant un impact sur la fonction visuelle. En général, les opacités du côté capsulaire postérieur par rapport au côté antérieur, de la région centrale par rapport à la périphérie, et les opacités denses par rapport aux légères, ont tendance à affecter davantage la fonction visuelle.
Elle est souvent découverte par les parents qui remarquent une pupille blanche, ou lors d’un examen du fond d’œil dans le cadre d’un bilan de santé du nourrisson. Il existe également des cas où le diagnostic est posé lors d’une consultation ophtalmologique pour strabisme ou mauvaise fixation. Dans les cas unilatéraux, l’œil sain étant dominant, la baisse de vision est difficile à détecter, d’où l’importance d’un dépistage actif lors des bilans de santé.
3. Causes et facteurs de risque
Section intitulée « 3. Causes et facteurs de risque »L’étiologie de la cataracte congénitale est variée, et 30 à 50 % des cas sont idiopathiques (cause inconnue).
| Étiologie | Fréquence / Maladies représentatives |
|---|---|
| Idiopathique (cause inconnue) | 30 à 50 %. Le plus fréquent |
| Héréditaire | Autosomique dominant le plus fréquent. Autosomique récessif et récessif lié à l’X possibles |
| Infection intra-utérine | Rubéole (syndrome de rubéole congénitale), herpès, CMV, toxoplasmose, etc. |
| Trouble métabolique | Galactosémie, hypocalcémie, homocystinurie, syndrome de Lowe, syndrome d’Alport, etc. |
| Anomalie chromosomique | Syndrome de Down, etc. |
| Maladie oculaire associée | Microphtalmie, aniridie congénitale, PFV (persistance du système vasculaire fœtal), etc. |
| Maladie systémique/syndrome | Syndrome de Hallermann-Streiff, syndrome de Pierre Robin, etc. |
La PFV (persistance du système vasculaire fœtal) est une cause importante de cataracte congénitale, correspondant à la persistance du système vasculaire vitréen primitif qui n’a pas régressé. Elle est souvent unilatérale et associée à une microphtalmie, et se retrouve dans environ 20 % des cataractes du nourrisson1). Lorsqu’elle s’étend à la partie postérieure (PFV de type postérieur), le pronostic visuel est défavorable.
La cataracte congénitale héréditaire est le plus souvent autosomique dominante. En cas d’antécédents familiaux, un conseil génétique et un dépistage familial sont recommandés. Il est important de noter que 30 à 50 % des cataractes congénitales sont idiopathiques, donc elles peuvent survenir même sans antécédents familiaux.
4. Diagnostic et méthodes d’examen
Section intitulée « 4. Diagnostic et méthodes d’examen »Classification morphologique
Section intitulée « Classification morphologique »Étant donné que les indications thérapeutiques diffèrent selon le site et la morphologie de l’opacité du cristallin, la classification morphologique est fondamentale pour le diagnostic.
| Nom de la classification | Nom anglais | Caractéristiques |
|---|---|---|
| Cataracte nucléaire | nuclear cataract | Opacité à l’intérieur de la suture en Y. Congénitale. Mauvais pronostic visuel |
| Cataracte lamellaire | lamellar (zonular) cataract | Opacité lamellaire autour de la suture en Y. Fréquente dans la cataracte développementale |
| Lenticône postérieur | posterior lenticonus | Saillie de la capsule postérieure avec opacité. Unilatéral. Peut évoluer vers une cataracte totale |
| Cataracte totale | total cataract | Opacification complète du cristallin |
| Cataracte capsulaire | capsular cataract | Opacité de la capsule antérieure, postérieure ou sous-capsulaire |
| Cataracte suturale | sutural cataract | Opacité au niveau des sutures en Y. Peu d’impact sur la fonction visuelle |
| Cataracte ponctuée | punctate cataract | Opacités ponctuées. Rarement cause de troubles visuels |
| Cataracte céruléenne | cerulean cataract | Opacités ponctuées bleues dans le cortex. Aucun trouble visuel |
Examens nécessaires
Section intitulée « Examens nécessaires »- Examen à la lampe à fente : évaluation de la forme, du site, du degré et de l’étendue de l’opacité, examen de base
- Examen du fond d’œil : détermination du degré d’opacité de la cataracte par la transparence du fond d’œil. En cas de difficulté de transparence, ajouter une échographie en mode B
- Mesure de la longueur axiale : indispensable pour déterminer la puissance de l’IOL, prédire la taille du cristallin et détecter précocement le glaucome postopératoire (allongement anormal de la longueur axiale)
- Examen de la réfraction : utiliser un autoréfractomètre portable ou un rétinoscope
- Évaluation de l’acuité visuelle : utiliser la méthode PL (preferential looking : évaluation de la réponse de préférence visuelle par des bandes) et la VEP (potentiel évoqué visuel). En VEP, une valeur inférieure à 40 % de la normale indique une diminution de la fonction visuelle
- Examen général : un dépistage des maladies systémiques par un pédiatre est obligatoire
L’indication chirurgicale est en principe déterminée en fonction de l’acuité visuelle (acuité des bandes) et de l’état de développement des réponses visuelles telles que la fixation et la poursuite.
Période d’indication chirurgicale
Section intitulée « Période d’indication chirurgicale »Les critères pour une indication chirurgicale active sont présentés ci-dessous.
| Œil | Critères d’indication | Calendrier chirurgical réel |
|---|---|---|
| Unilatéral (cataracte totale) | Traiter comme une urgence | De préférence dans les premiers jours après la naissance |
| Unilatéral (opacité sévère) | Opacité sévère avant 6 semaines de vie | Environ 1 mois après la naissance |
| Bilatéral (opacité sévère) | Opacité sévère avant 12 semaines (3 mois) de vie | Environ 2 mois après la naissance |
| Forme nécessitant une simple surveillance | Cataracte ponctuée, suturale, capsulaire antérieure, cataracte lamellaire ou poudreuse sans asymétrie | Surveillance régulière |
La cataracte totale unilatérale est une urgence ; une intervention chirurgicale dans les premiers jours de vie est souhaitable en l’absence de complications graves.
La cataracte totale unilatérale est une urgence ; une chirurgie précoce dans les premiers jours de vie est souhaitable pour prévenir l’amblyopie par privation de forme. Même en cas de cataracte bilatérale, une chirurgie précoce est réalisée vers l’âge de 2 à 3 mois. L’indication chirurgicale est déterminée en évaluant globalement l’acuité visuelle et le développement des réactions visuelles (fixation, poursuite). Pour les formes n’affectant pas la fonction visuelle (cataracte ponctuée, suturale), la surveillance est privilégiée.
5. Traitement standard
Section intitulée « 5. Traitement standard »Méthode chirurgicale
Section intitulée « Méthode chirurgicale »La technique de base pour les enfants de moins de 6 ans est l’aspiration du cristallin (émulsification) + capsulotomie postérieure + vitrectomie antérieure (± implantation de LIO). Chez l’enfant, pour prévenir l’opacification de l’axe visuel (cataracte secondaire), la capsulotomie postérieure et la vitrectomie antérieure sont systématiques, contrairement à la technique standard chez l’adulte. Après une capsulotomie antérieure par CCC, le cortex et le noyau du cristallin sont aspirés, puis une capsulotomie postérieure par CCC est réalisée, suivie d’une vitrectomie antérieure au vitréotome.
Les trois principales techniques chirurgicales sont présentées ci-dessous.
| Technique chirurgicale | Principales indications | Points clés |
|---|---|---|
| Aspiration du cristallin + capsulotomie postérieure + vitrectomie antérieure | Technique de base pour les moins de 6 ans | Capsulotomie postérieure et vitrectomie antérieure réalisées en une seule fois pour prévenir l’opacification capsulaire secondaire |
| Aspiration du cristallin + capsulotomie postérieure + vitrectomie antérieure + implantation de LIO | Lorsqu’une implantation de LIO est réalisée | L’ouverture capsulaire antérieure et postérieure idéale est d’environ 5 mm |
| Aspiration du cristallin + implantation de LIO (comme chez l’adulte) | 6 ans et plus | La capsulotomie postérieure et la vitrectomie antérieure peuvent être omises |
Réflexions sur les indications de la LIO
Section intitulée « Réflexions sur les indications de la LIO »Concernant l’opportunité de l’implantation de LIO chez les nourrissons, l’Infant Aphakia Treatment Study (IATS) a fourni des critères. L’implantation de LIO avant l’âge de 6 mois ne montre pas de différence d’acuité visuelle à 4,5 ans par rapport à la gestion par lentilles de contact (LC), et les yeux implantés de LIO ont présenté significativement plus de réinterventions pour opacification de l’axe visuel. Par conséquent, l’implantation de LIO avant 6 mois est limitée à des cas sélectionnés. À partir de 2 ans, l’implantation primaire de LIO est généralement choisie.
Valeur cible de la puissance de l’IOL
Section intitulée « Valeur cible de la puissance de l’IOL »Chez l’enfant, l’œil se développe et devient plus myope avec la croissance. Par conséquent, une hypercorrection est généralement pratiquée pour tenir compte de la croissance future de l’œil.
| Âge à l’implantation | Réfraction cible postopératoire | Objectif |
|---|---|---|
| À 1 an | Hypercorrection d’environ +5 D | Mettre au point sur la vision de près et favoriser le développement de la fonction visuelle |
| À 2 ans | Hypercorrection d’environ +4 D | Idem |
| Après la croissance (vers 20 ans) | Myopie légère (environ -1 à 0 D) | Visant une stabilité réfractive à long terme |
Le matériau de l’IOL doit être en acrylique pour la partie de support et la partie optique. Un diamètre de la partie optique de 6 mm ou moins est recommandé.
Précision du calcul de la puissance de l’IOL
Section intitulée « Précision du calcul de la puissance de l’IOL »Lors de l’implantation primaire d’IOL chez l’enfant, la précision prédictive des formules de calcul actuelles est nettement inférieure à celle chez l’adulte. Dans une étude portant sur 108 yeux de 83 patients, le taux de prédiction à ±1,00 D de huit formules (Holladay 1, SRK/T, Hoffer Q, Haigis, Barrett Universal II, Kane, EVO 2.0, Ladas Super Formula) n’était que de 35,2 à 43,5 % (contre 93,5 à 100 % chez l’adulte)2). Les formules SRK/T et Kane ont montré des résultats relativement bons, et un jeune âge ainsi qu’une longueur axiale courte étaient les principaux facteurs prédictifs de surprise réfractive (erreur de prédiction ≥ ±2,00 D)2). Il n’y avait pas de différence significative de précision prédictive selon la technique chirurgicale ou le type d’IOL2).
Correction réfractive postopératoire
Section intitulée « Correction réfractive postopératoire »- Unilatéral postopératoire : La correction par lentilles de contact (LC) est la base. Les LC souples ont souvent une puissance maximale d’environ +25 D ; au-delà, on utilise des LC rigides.
- Bilatéral postopératoire : La gestion par lunettes est possible. Pendant la petite enfance, on utilise des montures spéciales.
- Même pour les yeux avec IOL, si une hypermétropie résiduelle persiste, le port de lunettes est nécessaire.
- À partir de l’âge scolaire, on peut envisager des lunettes bifocales.
Traitement de l’amblyopie
Section intitulée « Traitement de l’amblyopie »Dans les cas unilatéraux et bilatéraux avec différence interoculaire, une occlusion de l’œil sain est nécessaire. Selon le protocole d’occlusion de l’IATS, jusqu’à l’âge de 8 mois, la durée d’occlusion est égale à l’âge en mois (ex. : 4 mois → 4 heures) ; après 8 mois, elle correspond à environ la moitié du temps d’éveil.
Résultats chirurgicaux de la cataracte congénitale associée à une PFV
Section intitulée « Résultats chirurgicaux de la cataracte congénitale associée à une PFV »Dans l’étude de registre multicentrique du PEDIG (Pediatric Eye Disease Investigator Group), les résultats à 5 ans de 64 yeux avec PFV (48 yeux aphakes, 16 yeux pseudophakes) ont été rapportés1). L’âge médian à la chirurgie pour les yeux aphakes était de 2 mois, et une vitrectomie antérieure a été réalisée dans 96 % des cas. Seulement 10 % (4/42 yeux, IC 95 % 3-23 %) ont atteint une acuité visuelle adaptée à l’âge à 5 ans. Une acuité visuelle meilleure que 20/200 a été obtenue dans 59 % (17/29) des yeux aphakes avec PFV, contre 23 % (3/13) des yeux pseudophakes avec PFV1). Les PFV de type postérieur (avec anomalies du vitré, de la rétine ou du nerf optique) ont montré un pronostic visuel plus défavorable que le type antérieur (acuité visuelle médiane 20/800 vs 20/100)1).
D’après les résultats de l’IATS, l’implantation de LIO avant l’âge de 6 mois ne montre pas de différence d’acuité visuelle par rapport à la gestion par lentilles de contact, mais entraîne davantage de réinterventions pour opacification de l’axe visuel. Par conséquent, l’implantation de LIO à cet âge est réservée à des cas limités. À partir de 2 ans, l’implantation primaire de LIO est généralement choisie. La puissance de la LIO est sélectionnée en visant une hypercorrection pour anticiper la myopie liée à la croissance.
6. Physiopathologie et mécanismes détaillés
Section intitulée « 6. Physiopathologie et mécanismes détaillés »Mécanisme de l’amblyopie par privation de forme
Section intitulée « Mécanisme de l’amblyopie par privation de forme »L’opacité du cristallin provoque une amblyopie par privation de forme en bloquant la lumière sur l’axe visuel. L’absence de stimulation visuelle appropriée pendant la période critique du développement visuel altère le développement du cortex visuel.
La période critique s’étend jusqu’à 6 semaines après la naissance pour les cas unilatéraux et jusqu’à 10 à 12 semaines pour les cas bilatéraux. Une cataracte affectant la fonction visuelle avant la période critique entraîne une amblyopie particulièrement rapide dans les cas unilatéraux. L’acquisition de la fonction visuelle commence pendant la période critique et se termine vers l’âge de 10 ans.
L’amblyopie par privation de forme est plus sévère et plus résistante au traitement que l’amblyopie réfractive ordinaire. C’est la raison pour laquelle une intervention chirurgicale précoce est indispensable.
Mécanisme de la cataracte secondaire (opacification capsulaire postérieure)
Section intitulée « Mécanisme de la cataracte secondaire (opacification capsulaire postérieure) »Chez l’enfant, l’activité des cellules épithéliales du cristallin est élevée, et l’opacification capsulaire postérieure (cataracte secondaire) survient plus fréquemment et plus précocement que chez l’adulte. Les cellules épithéliales résiduelles prolifèrent et migrent sur la capsule postérieure, obstruant l’axe visuel. Pour cette raison, chez les enfants de moins de 6 ans, la technique standard consiste à réaliser une capsulotomie postérieure et une vitrectomie antérieure peropératoires pour prévenir la cataracte secondaire.
Différences selon le type d’opacité et l’impact sur la fonction visuelle
Section intitulée « Différences selon le type d’opacité et l’impact sur la fonction visuelle »L’impact sur la fonction visuelle et l’indication chirurgicale varient selon la localisation et le type d’opacité du cristallin. La cataracte nucléaire produit une opacité dense au centre de l’axe visuel, ce qui entraîne un mauvais pronostic visuel et nécessite une intervention précoce. La cataracte suturale et la cataracte ponctuée affectent rarement le développement visuel et peuvent souvent être surveillées. Le lenticône postérieur est souvent unilatéral, avec une protrusion de la capsule postérieure et une progression de l’opacité, pouvant évoluer vers une cataracte totale.
Développement du cristallin et causes de l’opacité
Section intitulée « Développement du cristallin et causes de l’opacité »La cataracte congénitale résulte d’anomalies au cours du développement embryonnaire du cristallin. Le cristallin se forme à partir de la vésicule cristallinienne différenciée du placode ectodermique ; le noyau est constitué de fibres cristalliniennes primaires (à l’origine de la cataracte nucléaire) et le cortex de fibres secondaires (à l’origine de la cataracte lamellaire et suturale). Les infections intra-utérines comme la rubéole endommagent directement la formation des fibres cristalliniennes embryonnaires. Dans les troubles métaboliques (galactosémie, etc.), l’accumulation excessive de galactitol augmente la pression osmotique dans le cristallin, provoquant une surhydratation et une opacité. Dans les cataractes héréditaires, des anomalies fonctionnelles des protéines cristallines ou des protéines membranaires (connexines, etc.) altèrent le mécanisme de maintien de la transparence du cristallin.
7. Complications postopératoires et pronostic à long terme
Section intitulée « 7. Complications postopératoires et pronostic à long terme »Cataracte secondaire (opacification de l’axe visuel)
Section intitulée « Cataracte secondaire (opacification de l’axe visuel) »Chez les nourrissons opérés, une contraction du bord de la capsulotomie antérieure ou une opacité de type perles d’Elschnig survient dans près de 100 % des cas. Le traitement est le suivant.
- À partir de 1 an : capsulotomie postérieure au laser Nd:YAG possible
- Si le laser est difficile chez les enfants de moins de 6 ans : réaliser une capsulotomie postérieure chirurgicale et une vitrectomie antérieure
L’incidence cumulative à 5 ans de l’opacification de l’axe visuel dans les yeux pseudophakes avec PFV était de 45 % (IC à 95 % : 13 à 66 %) 1). L’incidence de l’opacification de l’axe visuel après vitrectomie antérieure lors de la chirurgie primaire était de 18 % (IC à 95 % : 8 à 28 %), significativement inférieure à celle de 60 % (IC à 95 % : 0 à 84 %) sans vitrectomie antérieure 1).
Glaucome secondaire
Section intitulée « Glaucome secondaire »C’est la complication tardive la plus importante après une chirurgie de cataracte congénitale.
- Incidence : survient chez 18 à 26 % des patients après la chirurgie
- Facteurs de risque : âge jeune au moment de la chirurgie, microphtalmie
- Délai d’apparition : peut survenir même plus de 10 ans après la chirurgie. Un suivi à long terme est essentiel.
L’incidence cumulative à 5 ans des événements indésirables liés au glaucome dans les yeux aphakes avec PFV était de 24 % (IC à 95 % : 9 à 37 %), et dans les yeux pseudophakes de 7 % (IC à 95 % : 0 à 20 %) 1). Il n’y avait pas de différence significative du risque de glaucome entre les yeux avec PFV et sans PFV (HR ajusté sur l’âge = 1,20, IC à 95 % : 0,54 à 2,64, P = 0,66), et le PFV lui-même n’était pas un facteur de risque indépendant de glaucome 1).
Incidence cumulative à 5 ans des complications de la cataracte congénitale associée au PFV
Section intitulée « Incidence cumulative à 5 ans des complications de la cataracte congénitale associée au PFV »| Complication | Œil aphake avec PFV | Œil pseudophake avec PFV |
|---|---|---|
| Événements indésirables liés au glaucome | 24 % (IC à 95 % : 9 à 37 %) | 7 % (IC à 95 % : 0 à 20 %) |
| Opacification de l’axe visuel (avec vitrectomie antérieure) | 18 % (IC à 95 % 8-28 %) | — |
| Opacification de l’axe visuel (sans vitrectomie antérieure) | 60 % (IC à 95 % 0-84 %) | 45 % (IC à 95 % 13-66 %) |
| Décollement de la rétine | 4 % (IC à 95 % 0-10 %) | 7 % (IC à 95 % 0-19 %) |
Autres complications
Section intitulée « Autres complications »- Rétraction capsulaire antérieure : Le bord de la capsulotomie antérieure se rétracte, réduisant l’ouverture capsulaire. Une progression peut entraîner une déficience visuelle.
- Décollement de la rétine : Le risque est particulièrement élevé dans les cas associés à une PFV.
Facteurs influençant le pronostic visuel
Section intitulée « Facteurs influençant le pronostic visuel »- Degré d’amblyopie par privation de forme (la précocité de la chirurgie est le facteur le plus important)
- Présence de complications oculaires associées (microphtalmie et microcornée sont de mauvais pronostic)
- Correction réfractive appropriée et poursuite du traitement de l’amblyopie après la chirurgie
- Compréhension et coopération des parents
Le glaucome secondaire est la complication la plus importante. Il survient chez 18 à 26 % des patients après la chirurgie et peut apparaître même plus de 10 ans après l’opération, nécessitant des contrôles réguliers de la pression intraoculaire même à l’âge adulte. L’opacification de la capsule postérieure (opacité de l’axe visuel) survient dans presque tous les cas de chirurgie chez les nourrissons, mais un traitement au laser YAG est possible chez les enfants de plus d’un an, et une intervention chirurgicale peut être nécessaire chez les moins de 6 ans.
8. Recherches récentes et perspectives futures
Section intitulée « 8. Recherches récentes et perspectives futures »Amélioration de la précision des formules de calcul de la puissance des implants intraoculaires (IOL) chez l’enfant
Section intitulée « Amélioration de la précision des formules de calcul de la puissance des implants intraoculaires (IOL) chez l’enfant »La précision prédictive des formules actuelles de calcul de la puissance des IOL pour enfants est insuffisante par rapport à celle des adultes, et même les formules de nouvelle génération (Kane, Barrett Universal II, etc.) n’ont pas montré de supériorité claire par rapport aux formules traditionnelles (SRK/T, etc.) 2). Le taux de prédiction dans une marge de ±1,00 D n’est que de 35,2 à 43,5 % pour les 8 formules actuelles, contre 93,5 à 100 % chez les adultes, soit une différence significative 2).
Le développement d’algorithmes spécialisés adaptés à la courte longueur axiale, à la courbure cornéenne abrupte, à la faible profondeur de la chambre antérieure et à la croissance oculaire spécifiques aux enfants est nécessaire 2). Il n’y a pas de différence significative dans la précision prédictive selon la technique chirurgicale ou le type d’IOL, et à l’heure actuelle, la correction réfractive active postopératoire et le suivi constituent des mesures complémentaires importantes.
9. Références
Section intitulée « 9. Références »- Haider KM, Repka MX, Sutherland DR, et al. Outcomes and Complications 5 Years After Surgery for Pediatric Cataract Associated With Persistent Fetal Vasculature. Am J Ophthalmol. 2024;261:156-165.
- Jin J, Shen Y, Qu Y, et al. Accuracy of new-generation and traditional intraocular lens power calculation formulas in pediatric primary implantation. J Cataract Refract Surg. 2024.
- Kaur S, Yangzes S, Ram J. Unilateral Congenital Cataract. J Pediatr Ophthalmol Strabismus. 2019;56(1):60-61. PMID: 30673102.
