化學性

新生兒結膜炎(新生兒眼炎)
一目了然的重點
Section titled “一目了然的重點”1. 新生兒結膜炎是什麼
Section titled “1. 新生兒結膜炎是什麼”新生兒結膜炎(ophthalmia neonatorum)是出生後28至30天內發生的結膜炎症。 歷史上,1880年Crede引入1%硝酸銀眼藥水,對預防淋菌性結膜炎有重大貢獻。 目前以抗菌眼藥水預防為主流。
全球發生率為2.04%(95%信賴區間0.705.79%),盛行率為7.79%(95%信賴區間2.9319.10%)。1)
地區差異大,低收入國家為6.90%,高收入國家為1.36%。1)
全球每年估計約有10,000例發生。1)
分娩方式及懷孕週數也會影響發生率。
- 經陰道分娩:發生率4.74%
- 剖腹產:發生率1.88%
- 早產兒:發生率3.08%
- 足月兒:發生率1.16%1)
病因可分為化學性、細菌性及病毒性。 細菌性中以披衣菌最常見,而淋病雙球菌則會導致最嚴重的預後。
全球發生率約為2.04%,估計每年約有10,000例。1)存在地區差異,已開發國家發生率較低(1.36%),而低收入國家則高達6.90%。
2. 主要症狀與臨床表現
Section titled “2. 主要症狀與臨床表現”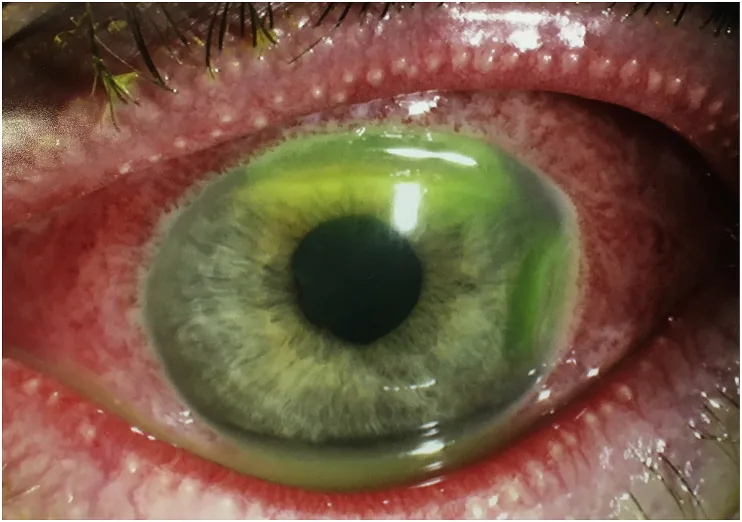
新生兒無法表達症狀。 需由家長或醫療人員客觀觀察。
- 眼分泌物(眼屎):依原因不同,可為漿液性至膿性
- 眼瞼腫脹:嚴重時可能難以確認眼球
- 結膜充血:程度依原因而異
- 流淚:伴隨分泌物增加而出現
- 結膜水腫:重症病例時明顯
新生兒因淚液分泌減少、分泌型IgA缺乏及溶菌酶活性降低,對感染較為脆弱。
發病時間是推測病因最重要的線索。 各原因的特徵性表現如下所示。
淋菌性
披衣菌性
病毒性(HSV)
發病時間:出生後1〜2週
所見:微小樹枝狀・地圖狀角膜潰瘍(新生兒缺乏特徵性所見)
注意:新生兒單純疱疹病毒感染可能進展為全身性感染
莫拉菌屬在出生後7至10天後發病,稱為假淋菌性結膜炎。
發病時間是推測病因最重要的線索。化學性通常在24小時內,淋菌性在出生後1至3天,披衣菌性在出生後3至10天,單純疱疹病毒在出生後1至2週為典型發病時間。但確診仍需微生物學檢查。
3. 原因與風險因素
Section titled “3. 原因與風險因素”產道感染是最常見的感染途徑。 母親的性傳染病是主要的風險因子。
- 淋菌:母子間的傳播率為30〜50%2)
- 披衣菌:未治療的母親其新生兒發病率為30〜40%
- 大腸桿菌:母體帶菌率19.9%,垂直傳播率21.4%8)
其他風險因子如下:
- 母體性傳染病(淋病、披衣菌感染)
- 早期破水
- 早產
- 經陰道分娩
- 出生後立即點眼預防的不足
從Crede法(1%硝酸銀點眼)開始的點眼預防有效,一項包含30項試驗、79,198名新生兒的Cochrane回顧顯示,使用預防藥物可降低所有原因結膜炎的發生率(中等確定性)。2)
WHO推薦的五種預防藥物如下:2)
- 四環黴素1%
- 紅黴素0.5%
- 聚維酮碘2.5%
- 硝酸銀1%
- 氯黴素1%
剖腹產的發生率仍報告為1.88%,無法完全預防。1)因為除了產道感染外,其他途徑(如上行性感染)也可能致病,因此剖腹產後仍需注意。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”根據發病時間進行鑑別診斷最為重要,請參照「臨床表現」一節推測病因。 確診必須進行微生物學檢查。
塗抹鏡檢・染色
Section titled “塗抹鏡檢・染色”發病時間與染色結果的組合是診斷的關鍵。
| 染色法 | 對象 | 觀察所見 |
|---|---|---|
| 革蘭氏染色 | 淋菌 | 被嗜中性球吞噬的革蘭氏陰性雙球菌 |
| 吉姆薩染色 | 披衣菌 | 包涵體(Prowazek小體) |
| 螢光染色 | 角膜病變 | 以鈷藍光檢查上皮缺損 |
培養・基因檢測
Section titled “培養・基因檢測”- 培養(淋菌):使用巧克力瓊脂培養基,在5~10% CO2環境中孵育
- PCR法:靈敏度與特異性高,對披衣菌和淋菌均有用
- 即時PCR、SDA、TMA:作為基因擴增法使用
- 免疫色層分析法:可快速診斷
排除表現類似症狀的疾病很重要。
5. 標準治療方法
Section titled “5. 標準治療方法”治療根據原因選擇。 以日本治療為中心,並補充海外標準治療方案。
日本的标准治疗
Section titled “日本的标准治疗”以下是日本使用的治疗方案。
- 细菌性(一般):贝斯特龙滴眼液0.5%,每日5次
- 淋菌性:贝斯特龙0.5%每日8次 + 罗氏芬静脉滴注1g每日1次
- 披衣菌性:泰利必妥眼藥膏0.3% 每日5次 持續8週,重症病例使用日舒安10mg/kg 連續3天
- 疱疹性:皰疹寧眼藥膏每日5次
海外標準治療
Section titled “海外標準治療”| 原因 | 建議治療 |
|---|---|
| 化學性 | 人工淚液 QID(等待自然消退) |
| 淋菌性 | ceftriaxone 25〜50mg/kg 單次投予 |
| 披衣菌性 | 阿奇黴素20mg/kg 3天4) |
| 單純疱疹病毒 | 阿昔洛韋靜脈注射45mg/kg/日 14~21天 |
口服紅黴素對沙眼衣原體結膜炎的全身治療有效,但需注意其與嬰兒肥厚性幽門狹窄(IHPS)的關聯。
新生兒使用ceftriaxone可能導致高膽紅素血症的風險。3)因此,對於併發眼眶蜂窩組織炎的嚴重病例,建議使用cefotaxime。給藥時,務必確認新生兒的黃疸狀況後再選擇藥物。
6. 病理生理學・詳細發病機制
Section titled “6. 病理生理學・詳細發病機制”新生兒的免疫學脆弱性
Section titled “新生兒的免疫學脆弱性”新生兒的眼睛相較於成人更容易受到感染。 主要原因如下:
- 淚液分泌減少
- 分泌型IgA缺乏
- 溶菌酶活性降低
- 結膜下腺樣組織發育不全(導致偽膜形成的原因之一)
偽膜是纖維蛋白、中性球及發炎滲出物附著於結膜所形成的。 在披衣菌性結膜炎中,由於腺樣組織發育不全,不會形成濾泡(偽膜性結膜炎)。
淋菌的感染機轉
Section titled “淋菌的感染機轉”淋菌是唯一能感染健康角膜上皮的細菌。 其致病性來自以下機制:
- 線毛(pili):媒介對上皮細胞的附著
- 外膜蛋白(OMP):參與細胞侵入
- LOS(脂寡醣·內毒素):引發強烈發炎反應
肯亞報告指出,高達16%的患病兒童會出現角膜病變,2)早期治療至關重要。
披衣菌的感染機轉
Section titled “披衣菌的感染機轉”披衣菌(Chlamydia trachomatis)是絕對細胞內寄生體。在細胞外以感染型的基本小體(EB)存在,在細胞內轉變為複製型的網狀小體(RB)。在感染的上皮細胞內形成封入體(Prowazek小體)。成人型封入體結膜炎在下眼瞼結膜穹窿部可見許多大型實質性濾泡,而新生兒封入體結膜炎則在出生後7天左右發病,因淋巴組織未發育,特徵為無濾泡。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”新興及罕見病原體引起的新生兒結膜炎
Section titled “新興及罕見病原體引起的新生兒結膜炎”除了傳統的主要病原體外,新病原體的報告也逐漸累積。
Mechel等人(2021)報告了首例由SARS-CoV-2引起的新生兒結膜炎,發生於一名4日齡女嬰。7)表現為結膜下出血和黏液膿性分泌物,並在8天內自然消退。
Albuquerque等人(2024)報告指出,Neisseria meningitidis占新生兒結膜炎的1%至2%,其中10%至29%有進展為侵襲性疾病的風險。5)靜脈注射cefotaxime 200mg/kg/日,連續7天,可完全治癒。
Merzouk等人(2025)報告指出,腸道革蘭氏陰性桿菌(如大腸桿菌)在新生兒加護病房相關感染中有增加趨勢。母體大腸桿菌定殖率為19.9%,垂直傳播率為21.4%。8)
Das(2023)報告韓國研究顯示,新生兒結膜炎中1.2%由鮑氏不動桿菌引起,52.4%由金黃色葡萄球菌引起。6)多重耐藥性鮑氏不動桿菌引起的新生兒加護病房院內感染已成為問題。
預防藥物的優化
Section titled “預防藥物的優化”考科藍回顧(Malik and Gilbert 2022)結論指出,目前尚未確立預防藥物種類的優劣,最佳預防藥物的選擇是未來的研究課題。2)
治療延遲與併發症
Section titled “治療延遲與併發症”Law et al.(2024)報告了兩例因治療延遲而進展為眼眶蜂窩織炎的新生兒結膜炎病例。3)這再次顯示了早期診斷和治療介入的重要性。
8. 參考文獻
Section titled “8. 參考文獻”-
Asiamah R, Owusu G, Amoako PT, et al. Epidemiology of ophthalmia neonatorum: a systematic review and meta-analysis. BMC Pediatr. 2025;25:31.
-
Malik ANJ, Gilbert C. Cochrane corner: interventions for preventing ophthalmia neonatorum. Eye. 2022;36:356-357.
-
Law NL, Tan VC, Lim TH, et al. Ophthalmia neonatorum complicated with neonatal orbital cellulitis: A case series. Malays Fam Physician. 2024;19:5.
-
Nwokeji I, Ding K, Ketner S. A Case of Neonatal Chlamydial Conjunctivitis. Cureus. 2024;16(7):e64463.
-
Albuquerque C, Dias ME, Pelicano M, et al. Neisseria meningitidis: The Unforeseen Agent of Acute Neonatal Conjunctivitis. Cureus. 2024;16(7):e65681.
-
Das G. Acinetobacter baumannii ophthalmia neonatorum - A very rare presentation. Indian J Ophthalmol. 2023;71:2595-2597.
-
Mechel E, Trinh M, Kodsi S, et al. Ophthalmia neonatorum as the presenting sign of SARS-CoV-2. J AAPOS. 2021;25:230-231.
-
Merzouk B, Schwartzman K, Yossuck P, et al. A Rare Case of Neonatal Escherichia coli Conjunctivitis With Maternal Asymptomatic Bacteriuria. Cureus. 2025;17(9):e92936.
