Chimique
Moment d’apparition : dans les 24 heures suivant la naissance
Signes : légère rougeur et larmoiement uniquement
Évolution : disparition spontanée en 2 à 4 jours

La conjonctivite néonatale (ophthalmia neonatorum) est une inflammation de la conjonctive survenant dans les 28 à 30 jours suivant la naissance. Historiquement, en 1880, Crede a introduit l’instillation de nitrate d’argent à 1 %, contribuant grandement à la prévention de la conjonctivite gonococcique. Actuellement, la prophylaxie par collyres antibiotiques est la norme.
L’incidence mondiale est de 2,04 % (IC à 95 % 0,70 à 5,79 %) et la prévalence de 7,79 % (IC à 95 % 2,93 à 19,10 %). 1) Il existe d’importantes variations régionales, avec 6,90 % dans les pays à faible revenu et 1,36 % dans les pays à revenu élevé. 1) On estime qu’environ 10 000 cas surviennent chaque année dans le monde. 1)
Le mode d’accouchement et l’âge gestationnel influencent également le taux d’incidence.
Les causes sont classées en chimiques, bactériennes et virales. Parmi les causes bactériennes, le chlamydia est le plus fréquent, tandis que le gonocoque entraîne les conséquences les plus graves.
L’incidence mondiale est d’environ 2,04 %, avec environ 10 000 cas estimés par an.1) Il existe des variations régionales : elle est plus faible dans les pays développés (1,36 %) et atteint 6,90 % dans les pays à faible revenu.
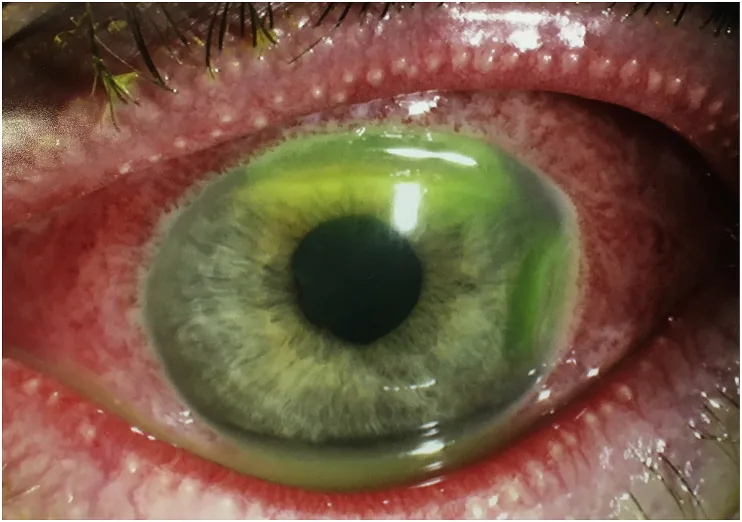
Les nouveau-nés ne peuvent pas exprimer leurs symptômes. Les parents ou les soignants doivent observer objectivement.
Chez le nouveau-né, il existe une diminution de la sécrétion lacrymale, un déficit en IgA sécrétoire et une activité réduite du lysozyme, le rendant vulnérable aux infections.
Le moment d’apparition est l’indice le plus important pour déterminer la cause. Les signes caractéristiques de chaque cause sont présentés ci-dessous.
Chimique
Moment d’apparition : dans les 24 heures suivant la naissance
Signes : légère rougeur et larmoiement uniquement
Évolution : disparition spontanée en 2 à 4 jours
Gonococcique
Âge d’apparition : 1 à 3 jours après la naissance
Signes : écoulement oculaire purulent abondant (blennorrhée), gonflement palpébral important
Caractéristique : seule bactérie capable d’adhérer et de pénétrer l’épithélium cornéen sain. Ulcère cornéen → perforation → risque d’endophtalmie
Chlamydiale
Âge d’apparition : 3 à 10 jours après la naissance
Signes : conjonctivite pseudomembraneuse (sans follicules), hyperhémie veloutée de la conjonctive palpébrale, écoulement oculaire sanglant
Complications : rhinopharyngite et pneumonie dans 10 à 20 % des cas
Virale (HSV)
Âge d’apparition : 1 à 2 semaines après la naissance
Signes : ulcère cornéen dendritique micro-ramifié ou géographique (signes peu caractéristiques chez le nouveau-né)
Attention : l’infection néonatale par le virus de l’herpès simplex peut évoluer vers une infection généralisée
Les espèces de Moraxella se manifestent après 7 à 10 jours de vie et sont appelées conjonctivite pseudogonococcique.
Le moment de l’apparition est l’indice le plus important pour estimer la cause. La conjonctivite chimique survient dans les 24 heures, la conjonctivite gonococcique entre 1 et 3 jours de vie, la conjonctivite à Chlamydia entre 3 et 10 jours, et l’infection par le virus de l’herpès simplex entre 1 et 2 semaines de vie. Cependant, un diagnostic de certitude nécessite un examen microbiologique.
L’infection par voie génitale est la voie de transmission la plus fréquente. Les infections sexuellement transmissibles chez la mère constituent le principal facteur de risque.
Les autres facteurs de risque sont les suivants :
La prophylaxie oculaire débutant par la méthode de Credé (instillation de nitrate d’argent à 1 %) est efficace ; une revue Cochrane portant sur 30 essais et 79 198 nouveau-nés a montré que l’utilisation de médicaments prophylactiques réduit l’incidence des conjonctivites toutes causes confondues (certitude modérée). 2)
Les cinq médicaments prophylactiques recommandés par l’OMS sont les suivants : 2)
Même avec une césarienne, l’incidence rapportée est de 1,88 %, ce qui ne permet pas une prévention complète. 1) D’autres voies que l’infection par voie basse (comme l’infection ascendante) peuvent être en cause, une vigilance est donc nécessaire même après une césarienne.
La distinction selon le moment d’apparition est primordiale ; se référer à la section « Signes cliniques » pour estimer la cause. Un examen microbiologique est indispensable pour le diagnostic définitif.
La combinaison du moment d’apparition et des résultats de coloration est la clé du diagnostic.
| Méthode de coloration | Cible | Observations |
|---|---|---|
| Coloration de Gram | Gonocoque | Diplocoques à Gram négatif phagocytés par les neutrophiles |
| Coloration de Giemsa | Chlamydia | Inclusions (corps de Prowazek) |
| Coloration à la fluorescéine | Lésions cornéennes | Examen des défauts épithéliaux sous lumière bleu cobalt |
Il est important d’exclure les maladies présentant des symptômes similaires.
Le traitement est choisi en fonction de la cause. Nous nous concentrons sur le traitement au Japon et complétons par les protocoles standard internationaux.
Voici le protocole de traitement au Japon.
| Cause | Traitement recommandé |
|---|---|
| Chimique | Larmes artificielles QID (attendre la résolution spontanée) |
| Gonococcique | Ceftriaxone 25-50 mg/kg en dose unique |
| Chlamydia | Azithromycine 20 mg/kg pendant 3 jours4) |
| Virus de l’herpès simplex | Aciclovir IV 45 mg/kg/jour pendant 14 à 21 jours |
L’érythromycine orale est efficace comme traitement systémique de la conjonctivite à Chlamydia, mais il faut être attentif au risque de sténose hypertrophique du pylore chez le nourrisson (IHPS).
Chez les nouveau-nés, l’utilisation de ceftriaxone présente un risque d’hyperbilirubinémie. 3) Par conséquent, dans les cas graves compliqués de cellulite orbitaire, l’utilisation de céfotaxime est recommandée. Il est important de vérifier l’état de la jaunisse du nouveau-né avant de choisir le traitement.
L’œil du nouveau-né est plus vulnérable aux infections que celui de l’adulte. Les principales raisons sont les suivantes :
La pseudomembrane est constituée de fibrine, de neutrophiles et d’exsudat inflammatoire adhérant à la conjonctive. Dans la conjonctivite à Chlamydia, le tissu lymphoïde étant sous-développé, les follicules ne se forment pas (conjonctivite pseudomembraneuse).
Le gonocoque est la seule bactérie capable d’infecter un œil dont l’épithélium cornéen est sain. Sa pathogénicité repose sur les mécanismes suivants.
Au Kenya, il a été rapporté que jusqu’à 16 % des enfants atteints développent des lésions cornéennes, 2) un traitement précoce est essentiel.
Chlamydia trachomatis est un parasite intracellulaire obligatoire. En dehors des cellules, il existe sous forme de corps élémentaires (CE) infectieux, et à l’intérieur des cellules, il se transforme en corps réticulés (CR) réplicatifs. Il forme des inclusions (corps de Prowazek) dans les cellules épithéliales infectées. Dans la conjonctivite à inclusions de l’adulte, on observe de nombreux gros follicules solides dans le fornix conjonctival inférieur, tandis que la conjonctivite à inclusions du nouveau-né survient vers le 7e jour après la naissance et se caractérise par l’absence de follicules en raison du développement incomplet du tissu lymphoïde.
En plus des agents pathogènes principaux traditionnels, des rapports sur de nouveaux agents pathogènes s’accumulent.
Mechel et al. (2021) ont rapporté le premier cas de conjonctivite néonatale due au SARS-CoV-2 chez une fillette de 4 jours. 7) Elle présentait une hémorragie sous-conjonctivale et un écoulement mucopurulent, qui ont disparu spontanément en 8 jours.
Albuquerque et al. (2024) ont rapporté que Neisseria meningitidis représente 1 à 2 % des conjonctivites néonatales, avec un risque de progression vers une maladie invasive dans 10 à 29 % des cas. 5) Un traitement par céfotaxime IV à 200 mg/kg/jour pendant 7 jours a permis une guérison complète.
Merzouk et al. (2025) ont rapporté que les bacilles à Gram négatif entériques (E. coli, etc.) sont en augmentation dans les infections associées aux soins en unité de soins intensifs néonatals (USIN). Le taux de colonisation maternelle par E. coli était de 19,9 % et le taux de transmission verticale de 21,4 %. 8)
Das (2023) a rapporté que, dans une étude coréenne, Acinetobacter baumannii représentait 1,2 % des conjonctivites néonatales et S. aureus 52,4 %. 6) Les infections nosocomiales en USIN dues à A. baumannii multirésistant posent problème.
La revue Cochrane (Malik et Gilbert 2022) conclut qu’aucune supériorité d’un type de prophylaxie par rapport à un autre n’est établie à ce jour, et le choix de la prophylaxie optimale reste un sujet de recherche future. 2)
Law et al. (2024) ont rapporté deux cas de conjonctivite néonatale ayant évolué vers une cellulite orbitaire en raison d’un retard de traitement. 3) L’importance d’un diagnostic et d’une intervention précoces a été une fois de plus démontrée.
Asiamah R, Owusu G, Amoako PT, et al. Epidemiology of ophthalmia neonatorum: a systematic review and meta-analysis. BMC Pediatr. 2025;25:31.
Malik ANJ, Gilbert C. Cochrane corner: interventions for preventing ophthalmia neonatorum. Eye. 2022;36:356-357.
Law NL, Tan VC, Lim TH, et al. Ophthalmia neonatorum complicated with neonatal orbital cellulitis: A case series. Malays Fam Physician. 2024;19:5.
Nwokeji I, Ding K, Ketner S. A Case of Neonatal Chlamydial Conjunctivitis. Cureus. 2024;16(7):e64463.
Albuquerque C, Dias ME, Pelicano M, et al. Neisseria meningitidis: The Unforeseen Agent of Acute Neonatal Conjunctivitis. Cureus. 2024;16(7):e65681.
Das G. Acinetobacter baumannii ophthalmia neonatorum - A very rare presentation. Indian J Ophthalmol. 2023;71:2595-2597.
Mechel E, Trinh M, Kodsi S, et al. Ophthalmia neonatorum as the presenting sign of SARS-CoV-2. J AAPOS. 2021;25:230-231.
Merzouk B, Schwartzman K, Yossuck P, et al. A Rare Case of Neonatal Escherichia coli Conjunctivitis With Maternal Asymptomatic Bacteriuria. Cureus. 2025;17(9):e92936.