萊伯先天性黑矇(LCA)是先天性視網膜 失養症中最嚴重的類型,從出生到嬰兒期即導致重度視覺障礙。
大多數為體染色體隱性遺傳 ,目前已鑑定出約27個致病基因。
眼球震顫 、瞳孔 反應減弱或消失、眼指徵是特徵性臨床表現。視網膜電圖 (ERG )顯示桿體和錐體反應均消失或顯著降低是診斷的關鍵。大部分患者視力 在0.1以下,約三分之一無光感。
針對RPE 65基因突變導致的LCA2的基因治療 藥物(voretigene neparvovec/Luxturna®)於2023年在日本獲批,但僅適用於約8%的LCA患者。
其他類型尚無有效治療方法,主要進行屈光 矯正、視覺訓練和低視力 復健。
萊伯先天性黑矇(Leber congenital amaurosis; LCA)是先天性視網膜 失養症中最嚴重的類型,從出生到嬰兒期即導致重度視覺障礙。它是兒童視覺障礙的主要原因之一,被認為是先天性視覺障礙的代表性疾病。臨床表現多樣。
1869年由德國眼科醫生特奧多爾·卡爾·古斯塔夫·馮·萊伯(Theodor Karl Gustav von Leber, 1840–1917)首次報告。需要注意的是,同一位萊伯於1871年報告的萊伯遺傳性視神經病變 (LHON )是一種粒線體疾病 ,發病年齡在20歲左右,與LCA完全不同。1957年,視網膜電圖 (ERG )波形消失被確認為LCA診斷的共同特徵,疾病名稱得以確立。
估計出生盛行率為每10萬出生人口2~3人(1/30,000~1/81,000)1) 。也有文獻報導為1:80,000~1:200,000,存在差異2) 。LCA約佔所有視網膜 失養症的5%,在盲校就讀的視覺障礙兒童中約20%為LCA1) 。目前已鑑定出約27個LCA相關基因2) ,約70~80%的病例可確定致病基因2) 。遺傳方式主要為體染色體隱性遺傳 ,但也有體染色體顯性遺傳 和X染色體連鎖遺傳的報導。
Q
萊伯先天性黑矇通常在什麼時候被發現?
A
通常在出生後6週左右,家長會注意到眼球震顫 或固視缺失3) 。當出現重度視覺反應不良(完全不能固視或追隨)時,懷疑LCA,並通過視網膜電圖 確診。
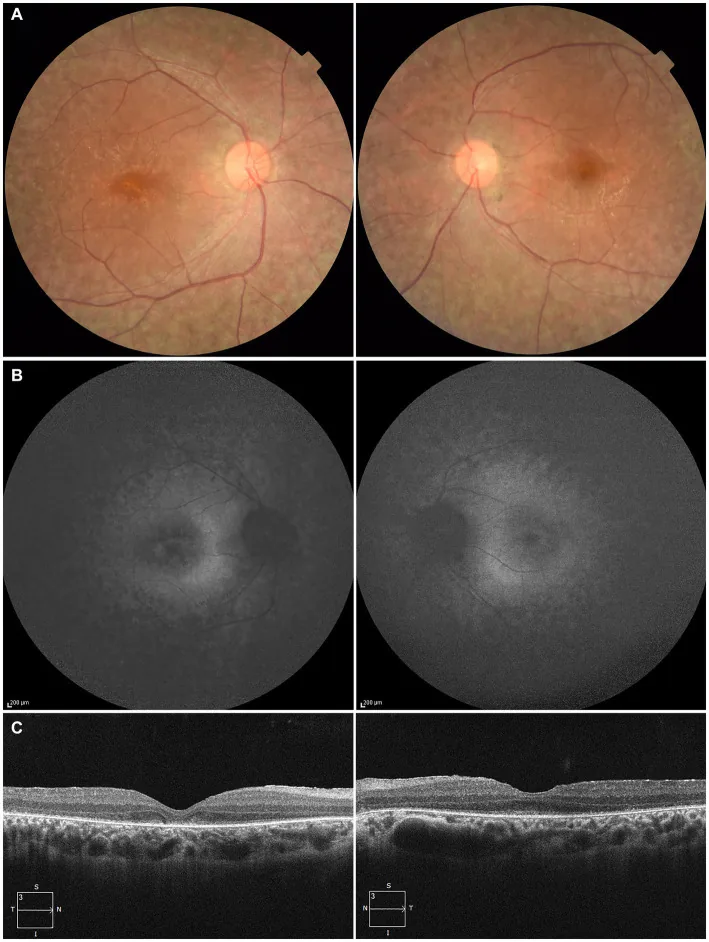
雷伯氏先天性黑矇患者雙眼的眼底照片、眼底自體螢光及OCT,顯示視網膜色素上皮變化與外層視網膜損傷 Higa N, et al. A novel
RPE 65 variant p.(Ala391Asp) in Leber congenital amaurosis: a case report and literature review in Japan. Front Med (Lausanne). 2024. Figure 1. PM
CI D: PMC11446184. License: CC BY.
27歲患者雙眼:(A)眼底照片顯示視網膜色素上皮 脫色素與視網膜 血管變細;(B)眼底自體螢光 顯示病變區域高螢光與訊號減弱;(C)OCT 顯示右眼橢圓體帶(EZ )消失,左眼中心凹僅少量殘留。對應本文「2. 主要症狀與臨床所見」中討論的視網膜色素上皮 變性與視網膜 血管變細。
從出生至出生後早期即存在重度視覺障礙。
視力 下降視力 在0.1以下,約三分之一無光感。視覺障礙通常穩定或進展非常緩慢。畏光 夜盲 :暗處視覺功能進一步下降。
父母常在出生後6週左右因眼震 或固視不良而注意到異常3) 。
眼震 視網膜 營養不良(EOSRD)的重要鑑別點,EOSRD不伴眼震 2) 。瞳孔 反應異常瞳孔 」。眼指徵 :戳、壓或揉眼睛,被認為是透過機械刺激視網膜 來喚起視覺的行為。主要後遺症是因眼眶 脂肪萎縮導致的眼球內陷。屈光 不正遠視 (>5屈光 度),被認為是由早期視覺障礙導致的正視化障礙所致。
嬰兒期眼底常表現正常,但隨後出現多種表現。眼底表現從正常眼底到典型的視網膜色素變性 樣眼底多種多樣。進展期病例視盤蒼白,血管極度變細,整個眼底色調變暗,黃斑 輪狀反射消失。
視神經 盤蒼白視網膜 血管狹細椒鹽樣眼底 :視網膜色素上皮 變性,出現小白斑和脫色素骨針狀色素沉著 和視網膜 下斑點(大理石樣眼底)黃斑 變性Coats樣滲出 色素性錢幣狀病變
OCT 顯示視網膜 外層幾乎消失,橢圓體帶(IS/OS連接)變薄至消失是其特徵。不同基因型表現不同:
CRB1 突變:視網膜 厚度增加的矛盾表現(粗層狀結構)1) RPE 65FAF (眼底自發螢光)消失2) GUCY2D 突變:FAF 正常保留2) NMNAT1 突變:黃斑 萎縮(黃斑 缺損 樣萎縮)
圓錐角膜 、白內障 和青光眼 的發生率隨年齡增長而增加。
LCA分為僅有眼部症狀的單純型 和合併全身疾病的複雜型 。
單純型
僅眼部症狀 :以視力 障礙為主,不伴隨全身異常。
中度至高度遠視 :常見於無全身異常的病例。
複雜型
中樞神經系統異常 :小腦蚓部發育不全、腦幹畸形。
精神發育遲緩 :部分病例伴有智力障礙。
腎臟損害 :可能合併多囊腎。
其他 :聽力喪失、骨骼異常、肝病、代謝異常、癲癇。
Q
眼指徵(揉眼動作)的目的是什麼?
A
這是LCA患者的特徵性行為,被認為是透過用手指戳或按壓眼睛來機械刺激視網膜 ,試圖喚起視覺。長期反覆會導致眼眶 脂肪萎縮,引起眼球凹陷 。
LCA是一組遺傳性視網膜 變性疾病,大多數為體染色體隱性遺傳 2) 。少數病例因CRX 、IMPDH1 或OTX2 突變表現為體染色體顯性遺傳 2) 。也有X染色體連鎖遺傳的報導。
目前已有19種類型(LCA1至LCA19)以及另外8個相關基因被報導2) 。致病基因涉及視網膜 發育和功能的多個路徑,包括光感受器形態發生、光轉導纖毛和視覺週期。
LCA相關基因分為五個主要功能網絡2) :
類視黃醇代謝/視桿細胞 視覺週期 (RPE 65, LRAT, RDH12)視網膜 恆定維持/光受器維持視網膜 發育/形態形成光刺激偵測/視覺感知 (GUCY2D, CNGA3)光受器連接纖毛/外節維持 (CEP290, RP GRIP1, RP GR)
全球最常見的突變基因及其比例如下:
基因 比例 涉及的路徑 CEP290 約15% 纖毛功能 GUCY2D 約12% 光訊息傳導(cGMP合成) CRB1 約10% 細胞極性維持 RPE 65約8% 視黃醇代謝
在日本隊列(34個家系)的NGS分析中,檢出率約為56%,最常見的突變基因報告為CRB1 、NMNAT1 和RP GRIP11) 。
致病基因的鑑定直接關係到治療資格的判斷。特別是確認RPE 65基因治療 (voretigene neparvovec)的適應症判定至關重要2) 。
AIPL1作為磷酸二酯酶6(PDE6)的特異性伴護蛋白,PDE6在光信號傳導中負責cGMP的分解。AIPL1缺失導致PDE6蛋白量急劇減少,引起cGMP代謝紊亂、光感受器變性,最終導致早期失明2) 。AIPL1突變約佔LCA總數的5-10%2) 。
Q
下一個孩子罹患LCA的機率是多少?
A
在體染色體隱性遺傳 中,如果父母雙方都是攜帶者,下一個孩子患病的機率為25%,成為攜帶者的機率為50%,不患病且非攜帶者的機率為25%。如果已知致病基因,可以選擇產前診斷或植入前遺傳學診斷。
LCA的診斷基於臨床,需要通過視網膜電圖 進行確診,並通過基因檢測進行分子遺傳學確認2) 。
當先天性出現顯著的視覺反應不良(缺乏固視和追視)時,應懷疑LCA。對於伴有嚴重視力 障礙和高度遠視 的嬰兒,分子遺傳學檢測LCA是首選4) 。
主要診斷檢查如下所示。
檢查 所見/特徵 視網膜電圖 (ERG )暗適應與明適應均無法引出或顯著降低。必要檢查。 OCT (光學同調斷層掃描 )視網膜 萎縮、外層消失、橢圓體帶消失。FAF (眼底自體螢光 )因亞型而異(RPE 65型消失,GUCY2D型正常)。 基因檢測(NGS等) 確診與亞型鑑定所需。
視網膜電圖 ERG 可排除LCA。OCT 視網膜 外層與橢圓體帶幾乎消失。CRB1 突變表現為反常的視網膜 增厚(粗層狀結構)1) 。手持式OCT 可用於清醒嬰兒或麻醉下幼兒的檢查4) 。FAF GUCY2D 突變自體螢光正常,RPE 652) 。基因檢測 :採用次世代定序(NGS)、DNA微陣列、連鎖分析等方法。整體檢出率約為70-80%2) 。自2023年起,針對82個IRD致病基因的套組檢測(PrismGuide IRD Panel)已納入健保,適用於疑似RPE 65相關IRD的年輕發病患者。
早發型視網膜色素變性 (RP ) :發病比LCA晚,中心視力 保持良好。不伴有眼球震顫 。早發型重度視網膜 營養不良(EOSRD) :出生後1年後出現重度視力 下降,不伴有眼球震顫 2) 。全色盲 (achromatopsia)畏光 和特徵性視網膜電圖 改變。先天性靜止性夜盲 近視 ,視力 優於LCA,並顯示特徵性視網膜電圖 模式。Joubert症候群 視網膜 營養不良。
對於大多數類型的LCA,尚未確立實質性的治療方法。目前的管理如下。
屈光 不正的矯正遠視 等進行適當的屈光 矯正。由於可能存在強屈光 不正,應配鏡並努力進行視覺訓練。視覺訓練 :進行視覺復健 訓練,以最大限度地利用殘餘視功能。視覺替代訓練 :由於視功能嚴重受損,考慮進行點字指導、白手杖行走訓練、使用放大閱讀器等。低視力照護 低視力輔助器具 ,並幫助獲得最佳的教育和就業機會。遺傳諮詢 畏光 處理定期追蹤 :進行包括視網膜電圖 在內的眼科追蹤,必要時轉診至低視力 門診。
2017年,美國FDA批准了**沃雷替基因 奈帕爾沃韋克(voretigene neparvovec-rzyl;商品名Luxturna)**用於治療與雙等位基因RPE 65基因治療 產品。2023年,該藥也在日本獲批(產品名:Luxturna®注射液)。
通過重組腺相關病毒(rAAV2)載體,將正常的RPE 65視網膜 下注射導入視網膜色素上皮 。該手術在玻璃體 手術室進行。
III期301試驗(Russell 2017)5) :
對象:31名RPE 65相關IRD患者
主要終點:MLMT(多亮度移動測試;在不同照度下的行為觀察測試)
在全視野刺激閾值(FST)方面也觀察到顯著改善
I/III期長期結果(Maguire 2019)6) :
治療後6-12個月達到峰值的視網膜 敏感性、視力 和功能性獲益隨後呈進行性下降趨勢
視網膜 敏感性提高有望改善夜盲和視野
國內III期試驗(A11301試驗)(Fujinami 2025)7) :
對象:4名日本RPE 65相關IRD患者
FST(全視野刺激閾值)顯示敏感性顯著提高(定義為敏感性提高超過10倍)
給藥後1年確認視野擴大
主要不良事件:眼部疾病,包括眼痛 (推測與給藥操作相關)
給藥方案:
第二隻眼在第一隻眼給藥後至少6天給藥。
免疫抑制:給藥前3天開始使用類固醇 ,持續至給藥後14天。
然而,RPE 65
Q
基因治療能用於所有LCA患者嗎?
A
目前獲批的基因治療 (voretigene neparvovec / Luxturna®注射液)僅適用於由雙等位基因RPE 65RPE 65
Q
在日本如何接受基因治療?
A
需要確認雙等位基因RPE 65突變,並具有足夠的存活視網膜 細胞。使用基因面板檢測(PrismGuide IRD面板)進行基因診斷是第一步。建議轉診至具有遺傳性視網膜 疾病診療經驗的專業機構。
LCA的病理生理與視覺循環的破壞有關,導致眼睛無法傳遞光信息。
視覺循環是視網膜色素上皮 (RPE )與神經感覺視網膜 之間的一系列酶促反應,代謝飲食中的維生素A以產生11-順式視黃醛,從而生成光色素。沒有11-順式視黃醛,光轉導級聯反應就無法啟動,視覺神經信號就無法傳遞到視覺皮層。編碼該級聯反應中任何蛋白質的基因發生突變,都可能阻斷視覺循環並引起LCA症狀。
組織病理學顯示外視網膜 和光感受器受累,表明LCA是一個退行性過程而非發育不良。
GUCY2D(LCA1) :編碼視網膜 特異性鳥苷酸環化酶(GC-E)。催化cGMP合成,是光訊息傳導的關鍵。已鑑定出140多種疾病相關突變,88%為體染色體隱性LCA的病因。第838號胺基酸是已知的突變熱點2) 。RPE 65(LCA2)2) 。對桿細胞和錐細胞功能均至關重要,近年研究顯示它可能還參與葉黃素向內消旋玉米黃質的異構化2) 。是唯一獲批的基因治療 適應症。CRB1(LCA8) :與果蠅crumbs蛋白同源,表現於光受器內節和Müller細胞。對維持細胞極性重要,位於染色體1q31.31) 。CEP290(LCA10) :參與光受器的纖毛功能。在LCA相關基因中突變頻率最高(約15%)。NMNAT1(LCA9) :編碼NAD(菸鹼醯胺腺嘌呤二核苷酸)生物合成的關鍵酶2) 。LCA5 :編碼lebercilin,參與纖毛功能和纖毛內蛋白質運輸2) 。AIPL1 :作為PDE6(磷酸二酯酶6)的特殊分子伴侶。AIPL1缺失導致PDE6不穩定→cGMP代謝紊亂→通道異常→光受器退化2) 。
voretigene neparvovec的長期追蹤評估(NCT 00481546、NCT 00643747)報告指出,治療後6-12個月出現初始峰值後,包括視網膜 敏感度、視力 和功能獲益在內的臨床益處逐漸下降6) 。PERCEIVE研究(前瞻性登錄研究)報告了真實臨床實踐中的2年安全性和有效性數據,高達50%的病例出現GTAU(基因治療 相關葡萄膜炎 )9) 。
由Editas Medicine公司開發。AAV5載體搭載金黃色葡萄球菌來源的Cas9和兩個引導RNA,靶向CEP290內含子26中的深部內含子突變(c.2991+1655A>G)3) 。首次人體試驗證實了安全性,即使在相對高劑量下也顯示出良好的耐受性3) 。
作為一種非基因依賴性方法,研究正在探索在殘留的內層視網膜 神經元中表達光響應性視紫紅質通道蛋白的技術3) 。該方法可能適用於所有LCA類型(無論基因型),早期臨床試驗正在進行中。
針對GUCY2D 和AIPL1 突變的基因治療 正在動物模型中進行,在拯救視桿和視錐光感受器方面顯示出有希望的結果。
LCA的病程分為三種模式:穩定(約75%)、進行性惡化(約15%)和改善(約10%)。AIPL1 突變與進行性惡化相關,而RP GRIP1基因治療 和再生醫學實現病情停止或治療。
Duan W, Zhou T, Jiang H, Zhang M, Hu M, Zhang L. A novel nonsense variant (c.1499C>G) in CRB1 caused Leber congenital amaurosis-8 in a Chinese family and a literature review. BMC Med Genomics. 2022;15(1):197.
Mordà D, Alibrandi S, Scimone C, et al. Decoding pediatric inherited retinal dystrophies: Bridging genetic complexity and clinical heterogeneity. Prog Retin Eye Res. 2025;109:101405.
Botto C, Rucli M, Tekinsoy MD, et al. Early and late stage gene therapy interventions for inherited retinal degenerations. Prog Retin Eye Res. 2022;86:100975.
Gurnani B, et al. Clinical approach to pediatric nystagmus: a comprehensive diagnostic algorithm. Clin Ophthalmol. 2025;19:1617-1636.
Russell S, Bennett J, Wellman JA, et al. Efficacy and safety of voretigene neparvovec (AAV2-hRPE 65v2) in patients with RPE 65-mediated inherited retinal dystrophy: a randomised, controlled, open-label, phase 3 trial. Lancet. 2017;390:849-860.
Maguire AM, Russell S, Wellman JA, et al. Efficacy, safety, and durability of voretigene neparvovec-rzyl in RPE 65 mutation-associated inherited retinal dystrophy: results of phase 1 and 3 trials. Ophthalmology. 2019;126:1273-1285.
Fujinami K, Akiyama K, Tsunoda K, et al. Efficacy and safety of voretigene neparvovec in RPE 65-retinopathy: results of a phase 3 trial in Japan. Ophthalmol Sci. 2025;5:100876.
Gange WS, Sisk RA, Besirli CG, et al. Perifoveal chorioretinal atrophy after subretinal voretigene neparvovec-rzyl for RPE 65-mediated Leber congenital amaurosis. Ophthalmol Retina. 2022;6:58-64.
Fischer MD, Simonelli F, Sahni J, et al. Real-world safety and effectiveness of voretigene neparvovec: results up to 2 years from the prospective, registry-based PERCEIVE study. Biomolecules. 2024;14:122.