莱伯先天性黑矇(LCA)是先天性视网膜 营养不良中最严重的类型,从出生到婴儿期即导致重度视觉障碍。
大多数为常染色体隐性遗传 ,目前已鉴定出约27个致病基因。
眼球震颤 、瞳孔 反应减弱或消失、眼指征是特征性临床表现。视网膜电图 (ERG )显示杆体和锥体反应均消失或显著降低是诊断的关键。大部分患者视力 在0.1以下,约三分之一无光感。
针对RPE 65基因突变导致的LCA2的基因治疗 药物(voretigene neparvovec/Luxturna®)于2023年在日本获批,但仅适用于约8%的LCA患者。
其他类型尚无有效治疗方法,主要进行屈光 矫正、视觉训练和低视力康复 。
莱伯先天性黑矇(Leber congenital amaurosis; LCA)是先天性视网膜 营养不良中最严重的类型,从出生到婴儿期即导致重度视觉障碍。它是儿童视觉障碍的主要原因之一,被认为是先天性视觉障碍的代表性疾病。临床表现多样。
1869年由德国眼科医生特奥多尔·卡尔·古斯塔夫·冯·莱伯(Theodor Karl Gustav von Leber, 1840–1917)首次报道。需要注意的是,同一位莱伯于1871年报道的莱伯遗传性视神经病变 (LHON )是一种线粒体疾病,发病年龄在20岁左右,与LCA完全不同。1957年,视网膜电图 (ERG )波形消失被确认为LCA诊断的共同特征,疾病名称得以确立。
估计出生患病率为每10万出生人口2~3人(1/30,000~1/81,000)1) 。也有文献报道为1:80,000~1:200,000,存在差异2) 。LCA约占所有视网膜 营养不良的5%,在盲校就读的视觉障碍儿童中约20%为LCA1) 。目前已鉴定出约27个LCA相关基因2) ,约70~80%的病例可确定致病基因2) 。遗传方式主要为常染色体隐性遗传 ,但也有常染色体显性遗传 和X连锁遗传的报道。
Q
莱伯先天性黑矇通常在什么时候被发现?
A
通常在出生后6周左右,家长会注意到眼球震颤 或固视缺失3) 。当出现重度视觉反应不良(完全不能固视或追随)时,怀疑LCA,并通过视网膜电图 确诊。
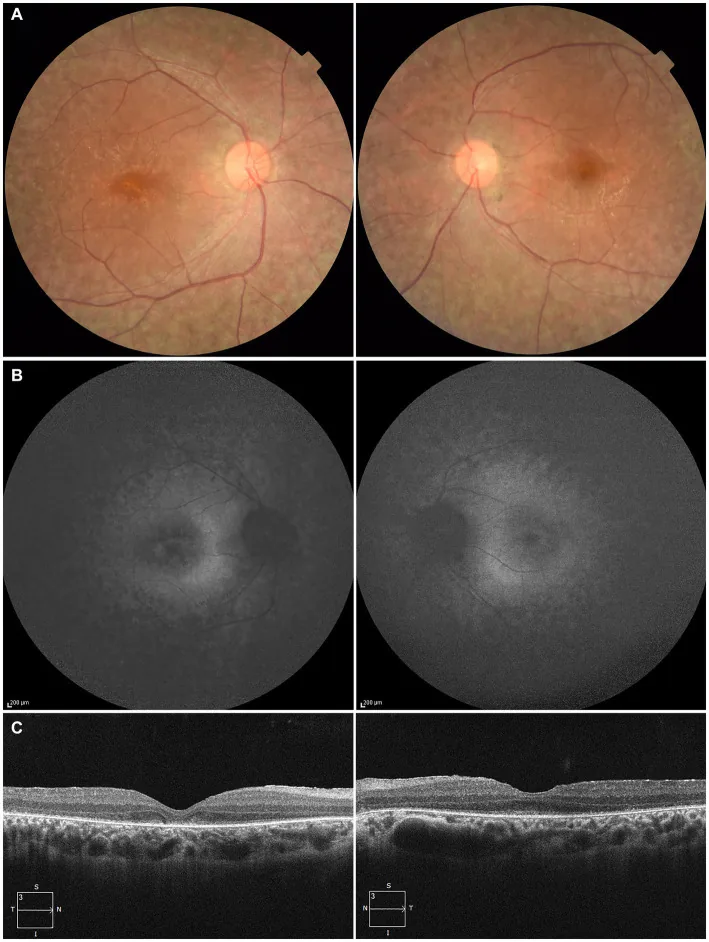
Leber先天性黑矇患者双眼的眼底照片、眼底自发荧光和OCT,显示视网膜色素上皮变化和外层视网膜损伤 Higa N, et al. A novel
RPE 65 variant p.(Ala391Asp) in Leber congenital amaurosis: a case report and literature review in Japan. Front Med (Lausanne). 2024. Figure 1. PM
CI D: PMC11446184. License: CC BY.
27岁患者双眼:(A)眼底照片显示视网膜色素上皮 脱色素和视网膜 血管变细;(B)眼底自发荧光 显示病变区域高荧光和信号减弱;(C)OCT 显示右眼椭圆体带(EZ )消失,左眼中心凹 仅少量残留。对应本文“2. 主要症状和临床所见”中讨论的视网膜色素上皮 变性和视网膜 血管变细。
从出生到出生后早期即存在重度视觉障碍。
视力 下降视力 在0.1以下,约三分之一无光感。视觉障碍通常稳定或进展非常缓慢。畏光 夜盲 :暗处视觉功能进一步下降。
父母常在出生后6周左右因眼震 或固视不良而注意到异常3) 。
眼震 视网膜 营养不良(EOSRD)的重要鉴别点,EOSRD不伴眼震 2) 。瞳孔 反应异常瞳孔 ”。眼指征 :戳、压或揉眼睛,被认为是通过机械刺激视网膜 来唤起视觉的行为。主要后遗症是因眼眶 脂肪萎缩导致的眼球内陷。屈光 不正远视 (>5屈光 度),被认为是由早期视觉障碍导致的正视化障碍所致。
婴儿期眼底常表现正常,但随后出现多种表现。眼底表现从正常眼底到典型的视网膜色素变性 样眼底多种多样。进展期病例视盘苍白,血管极度变细,整个眼底色调变暗,黄斑 轮状反射消失。
视盘苍白 和视网膜 血管变细椒盐样眼底 :视网膜色素上皮 变性,表现为小白斑和脱色素骨细胞样色素沉着 和视网膜 下斑点(大理石样眼底)黄斑 变性Coats样渗出 色素性钱币状病变
OCT 显示视网膜 外层几乎消失,椭圆体带(IS/OS连接)变薄至消失是其特点。不同基因型表现不同:
CRB1 突变:视网膜 厚度增加的矛盾表现(粗层状结构)1) RPE 65FAF (眼底自发荧光 )消失2) GUCY2D 突变:FAF 正常保留2) NMNAT1 突变:黄斑 萎缩(黄斑 缺损 样萎缩)
圆锥角膜 、白内障 和青光眼 的发生率随年龄增长而增加。
LCA分为仅有眼部症状的单纯型 和合并全身疾病的复杂型 。
单纯型
仅眼部症状 :以视力 障碍为主,不伴有全身异常。
中度至高度远视 :常见于无全身异常的病例。
复杂型
中枢神经系统异常 :小脑蚓部发育不全、脑干畸形。
精神发育迟缓 :部分病例伴有智力障碍。
肾脏损害 :可能合并多囊肾。
其他 :听力丧失、骨骼异常、肝病、代谢异常、癫痫。
Q
眼指征(揉眼动作)的目的是什么?
A
这是LCA患者的特征性行为,被认为是通过用手指戳或按压眼睛来机械刺激视网膜 ,试图唤起视觉。长期反复会导致眼眶 脂肪萎缩,引起眼球凹陷 。
LCA是一组遗传性视网膜 变性疾病,大多数为常染色体隐性遗传 2) 。少数病例因CRX 、IMPDH1 或OTX2 突变表现为常染色体显性遗传 2) 。也有X连锁遗传的报道。
目前已有19种类型(LCA1至LCA19)以及另外8个相关基因被报道2) 。致病基因涉及视网膜 发育和功能的多个通路,包括光感受器形态发生、光转导纤毛和视觉周期。
LCA相关基因分为五个主要功能网络2) :
类视黄醇代谢/视杆细胞 视觉周期 (RPE 65, LRAT, RDH12)视网膜 稳态维持/光感受器维持视网膜 发育/形态形成光刺激检测/视觉感知 (GUCY2D, CNGA3)光感受器连接纤毛/外节维持 (CEP290, RP GRIP1, RP GR)
全球范围内最常见的突变基因及其比例如下:
基因 比例 涉及的途径 CEP290 约15% 纤毛功能 GUCY2D 约12% 光信号转导(cGMP合成) CRB1 约10% 细胞极性维持 RPE 65约8% 视黄醇代谢
在日本队列(34个家系)的NGS分析中,检出率约为56%,最常见的突变基因报告为CRB1 、NMNAT1 和RP GRIP11) 。
致病基因的鉴定直接关系到治疗资格的判断。特别是确认RPE 65基因治疗 (voretigene neparvovec)的适应症判定至关重要2) 。
AIPL1作为磷酸二酯酶6(PDE6)的特异性伴侣蛋白,PDE6在光信号传导中负责cGMP的分解。AIPL1缺失导致PDE6蛋白量急剧减少,引起cGMP代谢紊乱、光感受器变性,最终导致早期失明2) 。AIPL1突变约占LCA总数的5-10%2) 。
Q
下一个孩子患LCA的概率是多少?
A
在常染色体隐性遗传 中,如果父母双方都是携带者,下一个孩子患病的概率为25%,成为携带者的概率为50%,不患病且非携带者的概率为25%。如果已知致病基因,可以选择产前诊断或植入前遗传学诊断。
LCA的诊断基于临床,需要通过视网膜电图 进行确诊,并通过基因检测进行分子遗传学确认2) 。
当先天性出现显著的视觉反应不良(缺乏固视和追随)时,应怀疑LCA。对于伴有严重视力 障碍和高度远视 的婴儿,分子遗传学检测LCA是首选4) 。
主要诊断检查如下所示。
检查 所见/特征 视网膜电图 (ERG )暗适应和明适应均无法引出或显著降低。必需检查。 OCT (光学相干断层扫描 )视网膜 萎缩、外层消失、椭圆体带消失。FAF (眼底自发荧光 )因亚型而异(RPE 65型消失,GUCY2D型正常)。 基因检测(NGS等) 确诊和亚型鉴定所需。
视网膜电图 视杆细胞 和视锥细胞 反应均消失或显著降低。正常ERG 可排除LCA。OCT 视网膜 外层和椭圆体带几乎消失。CRB1 突变表现为反常的视网膜 增厚(粗层状结构)1) 。手持式OCT 可用于清醒婴儿或麻醉下幼儿的检查4) 。FAF GUCY2D 突变自发荧光正常,RPE 652) 。基因检测 :采用下一代测序(NGS)、DNA微阵列、连锁分析等方法。总体检出率约为70-80%2) 。自2023年起,针对82个IRD致病基因的panel检测(PrismGuide IRD Panel)已纳入医保,适用于疑似RPE 65相关IRD的年轻发病患者。
早发型视网膜色素变性 (RP ) :发病比LCA晚,中心视力 保持良好。不伴有眼球震颤 。早发型重度视网膜 营养不良(EOSRD) :出生后1年后出现重度视力 下降,不伴有眼球震颤 2) 。全色盲 (achromatopsia)畏光 和特征性视网膜电图 改变。先天性静止性夜盲 近视 ,视力 优于LCA,并显示特征性视网膜电图 模式。Joubert综合征 视网膜 营养不良。
对于大多数类型的LCA,尚未确立实质性的治疗方法。目前的管理如下。
屈光 不正的矫正远视 等进行适当的屈光 矫正。由于可能存在强屈光 不正,应配镜并努力进行视觉训练。视觉训练 :进行视觉康复 训练,以最大限度地利用残余视功能。视觉替代训练 :由于视功能严重受损,考虑进行盲文指导、白杖行走训练、使用放大阅读器等。低视力 护理 :支持使用低视力辅助器具 ,并帮助获得最佳的教育和就业机会。遗传咨询 畏光 处理定期随访 :进行包括视网膜电图 在内的眼科随访,必要时转诊至低视力 门诊。
2017年,美国FDA批准了**沃雷替基因 奈帕尔沃韦克(voretigene neparvovec-rzyl;商品名Luxturna)**用于治疗与双等位基因RPE 65基因治疗 产品。2023年,该药也在日本获批(产品名:Luxturna®注射液)。
通过重组腺相关病毒(rAAV2)载体,将正常的RPE 65视网膜 下注射导入视网膜色素上皮 。该手术在玻璃体 手术室进行。
III期301试验(Russell 2017)5) :
对象:31名RPE 65相关IRD患者
主要终点:MLMT(多亮度移动测试;在不同照度下的行为观察测试)
在全视野刺激阈值(FST)方面也观察到显著改善
I/III期长期结果(Maguire 2019)6) :
治疗后6-12个月达到峰值的视网膜 敏感性、视力 和功能性获益随后呈进行性下降趋势
视网膜 敏感性提高有望改善夜盲和视野
国内III期试验(A11301试验)(Fujinami 2025)7) :
对象:4名日本RPE 65相关IRD患者
FST(全视野刺激阈值)显示敏感性显著提高(定义为敏感性提高超过10倍)
给药后1年确认视野扩大
主要不良事件:眼部疾病,包括眼痛 (推测与给药操作相关)
给药方案:
第二只眼在第一只眼给药后至少6天给药。
免疫抑制:给药前3天开始使用类固醇 ,持续至给药后14天。
然而,RPE 65
Q
基因治疗能用于所有LCA患者吗?
A
目前获批的基因治疗 (voretigene neparvovec / Luxturna®注射液)仅适用于由双等位基因RPE 65RPE 65
Q
在日本如何接受基因治疗?
A
需要确认双等位基因RPE 65突变,并具有足够的存活视网膜 细胞。使用基因面板检测(PrismGuide IRD面板)进行基因诊断是第一步。建议转诊至具有遗传性视网膜 疾病诊疗经验的专业机构。
LCA的病理生理与视觉循环的破坏有关,导致眼睛无法传递光信息。
视觉循环是视网膜色素上皮 (RPE )与神经感觉视网膜 之间的一系列酶促反应,代谢饮食中的维生素A以产生11-顺式视黄醛,从而生成光色素。没有11-顺式视黄醛,光转导级联反应就无法启动,视觉神经信号就无法传递到视觉皮层。编码该级联反应中任何蛋白质的基因发生突变,都可能阻断视觉循环并引起LCA症状。
组织病理学显示外视网膜 和光感受器受累,表明LCA是一个退行性过程而非发育不良。
GUCY2D(LCA1) :编码视网膜 特异性鸟苷酸环化酶(GC-E)。催化cGMP合成,是光信号转导的关键。已鉴定出140多种疾病相关突变,88%为常染色体隐性LCA的病因。第838位氨基酸是已知的突变热点2) 。RPE 65(LCA2)2) 。对杆细胞和锥细胞功能均至关重要,近年研究表明它可能还参与叶黄素向内消旋玉米黄质的异构化2) 。是唯一获批的基因治疗 适应症。CRB1(LCA8) :与果蝇crumbs蛋白同源,表达于光感受器内节和Müller细胞。对维持细胞极性重要,位于染色体1q31.31) 。CEP290(LCA10) :参与光感受器的纤毛功能。在LCA相关基因中突变频率最高(约15%)。NMNAT1(LCA9) :编码NAD(烟酰胺腺嘌呤二核苷酸)生物合成的关键酶2) 。LCA5 :编码lebercilin,参与纤毛功能和纤毛内蛋白运输2) 。AIPL1 :作为PDE6(磷酸二酯酶6)的特殊分子伴侣。AIPL1缺失导致PDE6不稳定→cGMP代谢紊乱→通道异常→光感受器变性2) 。
voretigene neparvovec的长期随访评估(NCT 00481546、NCT 00643747)报告称,治疗后6-12个月出现初始峰值后,包括视网膜 敏感度、视力 和功能获益在内的临床益处逐渐下降6) 。PERCEIVE研究(前瞻性注册研究)报告了真实临床实践中的2年安全性和有效性数据,高达50%的病例出现GTAU(基因治疗 相关葡萄膜炎 )9) 。
由Editas Medicine公司开发。AAV5载体搭载金黄色葡萄球菌来源的Cas9和两个引导RNA,靶向CEP290内含子26中的深部内含子突变(c.2991+1655A>G)3) 。首次人体试验证实了安全性,即使在相对高剂量下也显示出良好的耐受性3) 。
作为一种非基因依赖性方法,研究正在探索在残留的内层视网膜 神经元中表达光响应性视紫红质通道蛋白的技术3) 。该方法可能适用于所有LCA类型(无论基因型),早期临床试验正在进行中。
针对GUCY2D 和AIPL1 突变的基因治疗 正在动物模型中进行,在拯救视杆和视锥光感受器方面显示出有希望的结果。
LCA的病程分为三种模式:稳定(约75%)、进行性恶化(约15%)和改善(约10%)。AIPL1 突变与进行性恶化相关,而RP GRIP1基因治疗 和再生医学实现病情停止或治疗。
Duan W, Zhou T, Jiang H, Zhang M, Hu M, Zhang L. A novel nonsense variant (c.1499C>G) in CRB1 caused Leber congenital amaurosis-8 in a Chinese family and a literature review. BMC Med Genomics. 2022;15(1):197.
Mordà D, Alibrandi S, Scimone C, et al. Decoding pediatric inherited retinal dystrophies: Bridging genetic complexity and clinical heterogeneity. Prog Retin Eye Res. 2025;109:101405.
Botto C, Rucli M, Tekinsoy MD, et al. Early and late stage gene therapy interventions for inherited retinal degenerations. Prog Retin Eye Res. 2022;86:100975.
Gurnani B, et al. Clinical approach to pediatric nystagmus: a comprehensive diagnostic algorithm. Clin Ophthalmol. 2025;19:1617-1636.
Russell S, Bennett J, Wellman JA, et al. Efficacy and safety of voretigene neparvovec (AAV2-hRPE 65v2) in patients with RPE 65-mediated inherited retinal dystrophy: a randomised, controlled, open-label, phase 3 trial. Lancet. 2017;390:849-860.
Maguire AM, Russell S, Wellman JA, et al. Efficacy, safety, and durability of voretigene neparvovec-rzyl in RPE 65 mutation-associated inherited retinal dystrophy: results of phase 1 and 3 trials. Ophthalmology. 2019;126:1273-1285.
Fujinami K, Akiyama K, Tsunoda K, et al. Efficacy and safety of voretigene neparvovec in RPE 65-retinopathy: results of a phase 3 trial in Japan. Ophthalmol Sci. 2025;5:100876.
Gange WS, Sisk RA, Besirli CG, et al. Perifoveal chorioretinal atrophy after subretinal voretigene neparvovec-rzyl for RPE 65-mediated Leber congenital amaurosis. Ophthalmol Retina. 2022;6:58-64.
Fischer MD, Simonelli F, Sahni J, et al. Real-world safety and effectiveness of voretigene neparvovec: results up to 2 years from the prospective, registry-based PERCEIVE study. Biomolecules. 2024;14:122.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。