蒸发过强型干眼

全氟己基辛烷滴眼液
一目了然的要点
Section titled “一目了然的要点”1. 全氟己基辛烷是什么?
Section titled “1. 全氟己基辛烷是什么?”全氟己基辛烷(perfluorohexyloctane, PFHO)滴眼液(商品名:Miebo®,Bausch+Lomb公司)于2023年5月获得FDA批准,用于治疗干眼病(DED)的体征和症状。它是首个针对泪液蒸发的FDA批准处方滴眼液2)。
PFHO是一种两亲性半氟化烷烃(化学式C₁₄H₁₇F₁₃,F6H8),具有亲脂性烃链段和疏脂性氟碳链段3)。该制剂为单一成分、无水、无防腐剂制剂,含100%活性成分4)。在美国作为处方药销售,但在欧洲、澳大利亚和新西兰,它已以EvoTears®/NovaTears®的名称使用多年4)。
干眼是一种多因素疾病,美国有超过1600万人患病,泪液蒸发增强与高达90%的病例相关3)。睑板腺功能障碍(MGD)是蒸发过强型干眼的主要原因1)。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”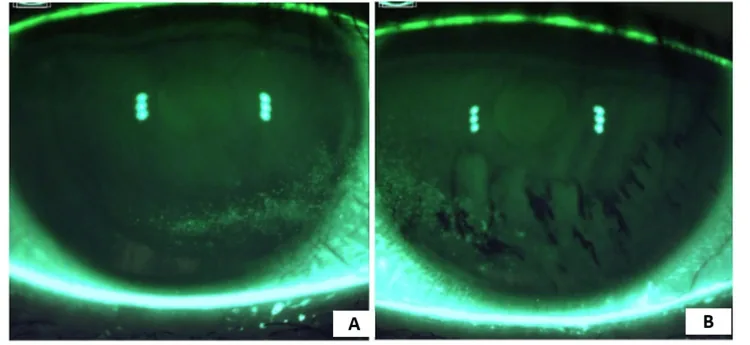
包括蒸发过强型干眼在内的DED的自觉症状如下2)。
- 眼干涩感:最常见的主诉
- 烧灼感、刺痛感:与炎症反应相关
- 异物感:伴随眼表损伤
- 畏光:伴随角膜上皮损伤出现
- 视物模糊:因泪膜不稳定导致一过性视力波动
- 眼疲劳:VDT作业时加重
- 泪膜破裂时间(BUT)缩短:日本诊断标准中BUT≤5秒为确诊条件
- 角膜荧光素染色阳性:反映角膜上皮损伤程度。全角膜荧光素染色评分(tCFS)用于临床试验的主要终点
- 睑板腺功能障碍:腺体开口堵塞、睑板腺分泌物性状改变
- 泪液弯月面减少:反映泪液量减少
- 角结膜上皮损伤:充血、点状表层角膜炎
3. 原因和风险因素
Section titled “3. 原因和风险因素”泪液分泌不足型干眼
- 年龄和性别:患病率随年龄增长而上升。女性更常见,从50岁以下的5.7%增加到75岁及以上的9.8%2)
- 绝经后雌激素治疗:激素波动是干眼的风险因素
- VDT工作:眨眼频率降低导致泪液蒸发增加
- 佩戴隐形眼镜:PFHO需要在滴眼前取下隐形眼镜,并在至少30分钟后重新佩戴
4. 诊断和检查方法
Section titled “4. 诊断和检查方法”干眼的诊断标准
Section titled “干眼的诊断标准”根据日本干眼研究会的诊断标准,同时满足主观症状和泪膜破裂时间(BUT)≤5秒即可确诊。根据TFOS DEWS II的定义,泪膜稳态丧失、泪液渗透压升高、眼表炎症和神经感觉异常也起病因作用。
| 检查 | 评估对象 | 临床试验中的使用 |
|---|---|---|
| tCFS | 角膜上皮损伤 | GOBI和MOJAVE的主要终点 |
| VAS干眼症评分 | 主观症状 | 同上 |
| OSDI问卷 | 生活质量/症状严重程度 | 次要终点 |
- 泪膜破裂时间(BUT):荧光素染色后,测量泪膜首次破裂的时间。
- Schirmer试验:定量评估泪液分泌量。无麻醉下≤5mm提示水液缺乏型干眼。
- 睑板腺评估:评估腺体形态、分泌物排出性和睑板腺脂质质量。
- 泪膜导向诊断(TFOD):通过睁眼后即刻的泪膜破裂模式确定病因层。
PFHO特别适用于伴有MGD的蒸发过强型干眼患者。临床试验中,纳入标准为BUT≤5秒、Schirmer试验≥5mm、MGD评分≥3、tCFS 4-11的患者。对于泪液分泌显著减少的水液缺乏型干眼,免疫调节剂环孢素滴眼液可能适用。
5. 标准治疗方法
Section titled “5. 标准治疗方法”PFHO的用法用量
Section titled “PFHO的用法用量”PFHO是一种不含防腐剂和添加剂的眼科溶液,由100%全氟己基辛烷组成。推荐剂量为每只患眼每日4次,每次1滴。
临床试验结果
Section titled “临床试验结果”两项3期随机双盲试验(GOBI试验和MOJAVE试验)显示,与生理盐水对照相比,PFHO每日四次滴眼在第8周时显著改善了tCFS和VAS干眼感评分这两个主要终点4)。
一项包含4项RCT的荟萃分析(1,814例患者)报告了以下结果1):
PFHO组与对照组相比,tCFS显著改善(MD -1.09;95% CI -1.37至-0.82;P < 0.001;I² = 0%)。眼部不适VAS(MD -9.69;P < 0.01)、OSDI(MD -5.79;P < 0.01)和灼烧感/刺痛感评分(MD -7.16;P < 0.01)也均显著改善,且未观察到异质性1)。
在GOBI试验的延伸试验KALAHARI试验(208例患者,52周)中,tCFS相对于基线的平均变化为-2.1,VAS干眼感评分的平均变化为-33.7,证实了在60周内的持续疗效4)。
| 试验 | 对象 | tCFS改善(LSMD) | VAS改善(LSMD) |
|---|---|---|---|
| GOBI | 597例 | -0.97(P < 0.001) | -7.6(P < 0.001) |
| MOJAVE | 620例 | -1.2(P < 0.001) | -10.2(P < 0.001) |
在第2周(第15天)时,已观察到tCFS和VAS干燥感评分显著改善,并且在单次滴眼后5分钟时也观察到症状改善效果4)。
PFHO滴眼液的安全性良好1)。
- 最常见不良事件:视物模糊(1.3%~3.0%)。轻度且一过性4)
- 眼部不良事件发生率:PFHO组与对照组无显著差异(RR 1.00;95% CI 0.77~1.29;P = 0.999)1)
- 严重眼部不良事件:在GOBI、MOJAVE和KALAHARI试验中均未报告3)
- 停药率:低3)
- 非临床研究已确认其无毒性且无生物蓄积性4)
PFHO目前没有绝对禁忌症,但在孕妇、哺乳期妇女和18岁以下人群中的安全性和有效性尚未确定。
在日本干眼治疗中的定位
Section titled “在日本干眼治疗中的定位”在日本,根据干眼研究会提出的“眼表分层治疗(TFOT)”概念,针对病因层进行治疗。对于脂质层,采用热敷和眼睑清洁;对于水液层,使用透明质酸钠和泪点塞;对于分泌型黏蛋白,使用地夸磷索钠;对于上皮,使用瑞巴派特。PFHO可作为补充脂质层功能、直接抑制泪液蒸发的全新选择。
在临床试验中,单次滴眼后5分钟即可观察到症状改善。第2周(第15天),角膜荧光素染色评分和干涩感评分均显示出显著改善。在KALAHARI延长期试验中,效果持续了52周。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”干眼的恶性循环
Section titled “干眼的恶性循环”干眼病理生理的核心是泪液高渗透压2)。泪液分泌减少或蒸发增加导致泪液渗透压升高,会激活MAP激酶,并引发炎症细胞因子、趋化因子和基质金属蛋白酶的分泌2)。这些炎症介质诱导角膜上皮细胞、结膜细胞和杯状细胞凋亡,导致糖萼损伤、眼表润滑能力下降和泪膜不稳定。结果进一步加重高渗透压,形成“恶性循环”2)。
PFHO的作用机制
Section titled “PFHO的作用机制”PFHO的作用机制提出了几种假说4)。
抑制泪液蒸发是首要机制。PFHO是一种两亲性分子,其氟碳链段(疏油、亲气)和烃链段(亲油)在泪液-空气界面自组装形成有序的单分子层3)。该单分子层物理性地抑制泪液水层的蒸发。体外实验中,将PFHO应用于生理盐水可使蒸发减少约80%2)。
在比较PFHO和PFBP(全氟丁基戊烷)蒸发速率的体外重量分析中,1小时后PFHO的蒸发量不到1.5%,而PFBP蒸发了93%。在离体模型中,1小时后PFHO的角膜残留率为54.5%,约为PFBP(18.6%)的3倍3)。
降低角膜表面温度并激活TRPM8是第二个机制4)。局部应用PFHO可降低角膜表面温度,增加角膜TRPM8冷感受体的活性。这种反应被认为可促进反射性流泪和眨眼,并减轻不适和疼痛。
改善泪液脂质层也有报道。临床前数据显示,PFHO给药7天后,单次滴眼后5分钟脂质层分级即开始改善,重复给药后改善维持5-7天4)。临床试验也在第4周观察到脂质层厚度和泪膜厚度的改善4)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”TFOS DEWS III 2025中的定位
Section titled “TFOS DEWS III 2025中的定位”在2025年发布的TFOS DEWS III管理与治疗报告中,PFHO被定位为基于证据的蒸发过强型干眼(DED)治疗选择4)。一项系统评价(6项RCT)报告,PFHO组在OSDI、脂质层厚度、角膜染色和不良事件等大多数变量上均优于对照组4)。
PFHO与无水环孢素0.1%的比较
Section titled “PFHO与无水环孢素0.1%的比较”PFHO和无水CsA 0.1%(Vevye®)均为含SFA的无水、无防腐剂制剂。但PFHO靶向抑制蒸发,而CsA 0.1%通过免疫调节增加泪液分泌3)。PFHO的临床试验针对蒸发过强型DED(合并MGD),而CsA 0.1%的试验排除了MGD,纳入的是泪液分泌减少的重症病例4)。
临床试验的随访期主要为8周,需要评估长期(超过1年)的有效性和副作用1)。对试验排除的患者群体(如重度DED(tCFS > 11)或隐形眼镜佩戴者)的评估也是未来的挑战1)。期待在日本获得批准。
8. 参考文献
Section titled “8. 参考文献”- Guedes J, Hespanhol LC, Freitas MAA, et al. Efficacy and Safety of Perfluorohexyloctane in Evaporative Dry Eye Disease Associated With Meibomian Gland Dysfunction: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Cureus. 2024;16(8):e67920.
- Azhar A, Taimuri MA, Oduoye MO, et al. MEIBO (perfluorohexyloctane): a novel approach to treating dry eye disease. Ann Med Surg. 2024;86:5292-5298.
- Periman LM, White DE, Katsev D. Differentiating Between Perfluorohexyloctane Ophthalmic Solution and Water-Free Cyclosporine Ophthalmic Solution 0.1% for Dry Eye Disease: A Review of Preclinical and Clinical Characteristics. Ophthalmol Ther. 2025;14(2):283-293.
- TFOS DEWS III Management and Therapy Report. Am J Ophthalmol. 2025;279:289-386.
