증발 항진형 안구건조증

퍼플루오로헥실옥탄 안과용액
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 퍼플루오로헥실옥탄이란?
섹션 제목: “1. 퍼플루오로헥실옥탄이란?”퍼플루오로헥실옥탄(perfluorohexyloctane, PFHO) 안과용액(제품명: Miebo®, Bausch+Lomb)은 2023년 5월 FDA 승인을 받은 안구건조증(DED)의 징후 및 증상 치료제입니다. 눈물 증발을 표적으로 한 최초의 FDA 승인 처방 점안액입니다2).
PFHO는 양친매성 반플루오르화 알칸(화학식 C₁₄H₁₇F₁₃, F6H8)으로, 친유성 탄화수소 세그먼트와 발유성 플루오로카본 세그먼트를 가지고 있습니다3). 본 제제는 100% 유효 성분으로 구성된 단일 성분, 무수, 무방부제 제제입니다4). 미국에서는 처방약으로 판매되지만, 유럽, 호주, 뉴질랜드에서는 EvoTears®/NovaTears®라는 이름으로 수년간 사용되어 왔습니다4).
안구건조증은 미국에서 1,600만 명 이상이 앓고 있는 다인자 질환으로, 눈물 증발 항진이 최대 90%의 사례와 관련됩니다3). 마이봄샘 기능 장애(MGD)가 증발 항진형 안구건조증의 가장 큰 원인입니다1).
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”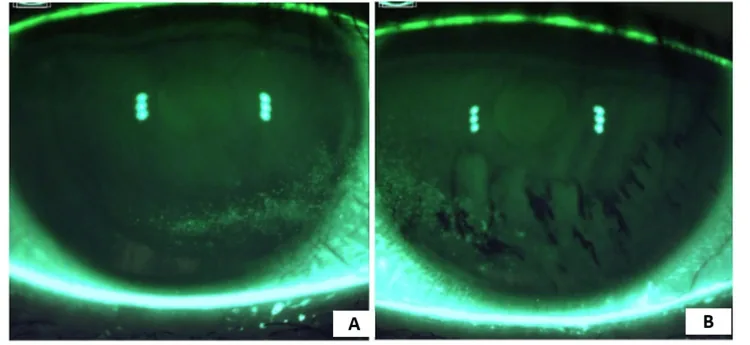
자각 증상
섹션 제목: “자각 증상”증발 항진형 안구건조증을 포함한 DED 전반의 자각 증상은 다음과 같습니다2).
- 안구 건조감: 가장 흔한 주된 호소입니다
- 작열감·찌르는 듯한 통증: 염증 반응과 관련됩니다
- 이물감: 안구 표면 손상에 동반됩니다
- 눈부심: 각막 상피 손상에 따라 나타납니다
- 시야 흐림: 눈물막 불안정으로 일시적인 시력 변동이 발생합니다
- 눈 피로: VDT 작업 시 악화됩니다
임상 소견
섹션 제목: “임상 소견”- 눈물막 파괴 시간(BUT) 단축: 일본 진단 기준에서 BUT 5초 이하가 확정 진단 요건입니다
- 각막 플루오레세인 염색 양성: 각막 상피 손상 정도를 반영합니다. tCFS(전각막 플루오레세인 염색 점수)는 임상 시험의 주요 평가 지표로 사용됩니다
- 마이봄샘 기능 장애: 샘 개구부 폐쇄, 마이봄 분비물 성상 변화를 보입니다
- 눈물 메니스커스 감소: 눈물량 감소를 반영
- 각결막 상피 장애: 충혈, 점상 표층 각막염
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”안구건조증의 분류
섹션 제목: “안구건조증의 분류”눈물 감소형 안구건조증
위험 요인
섹션 제목: “위험 요인”- 연령 및 성별: 유병률은 나이가 들수록 증가합니다. 여성에게 더 흔하며, 50세 미만의 5.7%에서 75세 이상의 9.8%로 증가합니다2)
- 폐경 후 에스트로겐 요법: 호르몬 변동은 안구건조증의 위험 요인입니다
- VDT 작업: 눈 깜빡임 횟수 감소로 눈물 증발이 촉진됩니다
- 콘택트렌즈 착용: PFHO는 점안 전에 콘택트렌즈를 제거하고 최소 30분 후에 다시 착용해야 합니다
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”안구건조증의 진단 기준
섹션 제목: “안구건조증의 진단 기준”일본 안구건조증 연구회의 진단 기준에 따르면, 자각 증상이 있고 눈물막 파괴 시간(BUT)이 5초 이하인 두 가지 조건을 모두 충족하면 확진됩니다. TFOS DEWS II 정의에 따르면, 눈물막 항상성 상실 외에도 눈물 삼투압 상승, 안구 표면 염증, 신경 감각 이상 등도 병인적 역할을 합니다.
주요 검사
섹션 제목: “주요 검사”| 검사 | 평가 대상 | 임상시험에서의 사용 |
|---|---|---|
| tCFS | 각막 상피 손상 | GOBI 및 MOJAVE의 주요 평가변수 |
| VAS 건조감 점수 | 자각 증상 | 상동 |
| OSDI 설문지 | QOL/증상 중증도 | 이차 평가변수 |
- 눈물막 파괴 시간(BUT): 플루오레세인 염색 후 눈물막이 처음으로 파괴될 때까지의 시간을 측정합니다.
- Schirmer 검사: 눈물 분비량을 정량적으로 평가합니다. 마취 없이 5mm 이하이면 눈물 감소형을 시사합니다.
- 마이봄샘 평가: 샘의 형태, 분비물 압출성, 마이봄 질을 평가합니다.
- 눈물막 지향 진단(TFOD): 개안 직후 눈물막 파괴 패턴을 통해 원인층을 확인합니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”PFHO의 용법·용량
섹션 제목: “PFHO의 용법·용량”PFHO는 100% 퍼플루오로헥실옥탄으로 구성된 방부제·첨가물 무첨가 안과용 용액입니다. 권장 용량은 각 환안에 1일 4회, 1회 1방울 점안입니다.
임상 시험 결과
섹션 제목: “임상 시험 결과”2건의 3상 무작위 이중맹검 시험(GOBI 시험 및 MOJAVE 시험)에서 PFHO 1일 4회 점안은 8주째에 생리식염수 대조군과 비교하여 tCFS 및 VAS 건조감 점수 두 가지 주요 평가변수를 유의하게 개선했습니다4).
4건의 RCT를 포함한 메타분석(1,814명)에서 다음과 같은 결과가 보고되었습니다1):
PFHO군은 대조군에 비해 tCFS를 유의하게 개선했습니다(MD -1.09; 95% CI -1.37~-0.82; P < 0.001; I² = 0%). 안구 불편감 VAS(MD -9.69; P < 0.01), OSDI(MD -5.79; P < 0.01), 작열감/따끔거림 점수(MD -7.16; P < 0.01)도 모두 유의하게 개선되었으며 이질성은 관찰되지 않았습니다1).
GOBI 시험의 연장 시험인 KALAHARI 시험(208명, 52주)에서 tCFS의 기준치 대비 평균 변화량은 -2.1, VAS 건조감 점수의 평균 변화량은 -33.7로, 60주에 걸친 지속적인 유효성이 확인되었습니다4).
| 시험 | 대상 | tCFS 개선(LSMD) | VAS 개선(LSMD) |
|---|---|---|---|
| GOBI | 597명 | -0.97 (P < 0.001) | -7.6 (P < 0.001) |
| MOJAVE | 620명 | -1.2 (P < 0.001) | -10.2 (P < 0.001) |
2주째(15일) 시점에서 이미 tCFS와 VAS 건조감 점수의 유의한 개선이 인정되었고, 단회 점안 후 5분 시점에서도 증상 개선 효과가 관찰되었습니다4).
안전성
섹션 제목: “안전성”PFHO 점안액의 안전성은 양호합니다1).
- 가장 흔한 이상반응: 시야 흐림(1.3~3.0%). 경미하고 일과성입니다4)
- 안구 이상반응 발생률: PFHO군과 대조군 간 유의한 차이 없음(RR 1.00; 95% CI 0.77~1.29; P = 0.999)1)
- 중대한 안구 이상반응: GOBI, MOJAVE, KALAHARI 시험 전반에 걸쳐 보고되지 않음3)
- 중단율: 낮음3)
- 비임상 시험에서 비독성 및 비생체축적성이 확인되었습니다4)
PFHO는 현재 절대적 금기는 없지만, 임산부, 수유부, 18세 미만에서의 안전성과 유효성은 확립되지 않았습니다.
일본에서의 안구건조증 치료와의 위치
섹션 제목: “일본에서의 안구건조증 치료와의 위치”일본에서는 안구건조증 연구회가 제창하는 “안구표면 층별 치료(TFOT)” 개념에 기반하여 원인 층에 대한 치료가 이루어집니다. 지질층에는 온찜질과 안검 세척, 액체층에는 히알루론산나트륨과 누점 플러그, 분비형 뮤신에는 디쿠아포솔나트륨, 상피에는 레바미피드가 사용됩니다. PFHO는 지질층 기능을 보완하여 눈물 증발을 직접적으로 억제하는 새로운 선택지가 될 수 있습니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”안구건조증의 악순환
섹션 제목: “안구건조증의 악순환”안구건조증 병태생리의 핵심은 눈물의 고삼투압입니다2). 눈물 분비 감소 또는 증발 증가로 눈물 삼투압이 상승하면 MAP 키나아제 활성화와 염증성 사이토카인, 케모카인, 기질 금속단백분해효소 분비가 유발됩니다2). 이러한 염증 매개체는 각막 상피, 결막, 배상 세포의 세포자멸사를 유도하여 당질외피 손상, 안구 표면 윤활 능력 저하, 눈물막 불안정성을 초래합니다. 그 결과 추가적인 고삼투압이 발생하는 ‘악순환(vicious circle)‘이 형성됩니다2).
PFHO의 작용 기전
섹션 제목: “PFHO의 작용 기전”PFHO의 작용 기전에는 여러 메커니즘이 제안되어 있습니다4).
눈물 증발 억제가 첫 번째 기전입니다. PFHO는 양친매성 분자로, 불소탄소 세그먼트(소유성, 친기성)와 탄화수소 세그먼트(친유성)의 자기 조립을 통해 눈물 표면과 외기 계면에 질서 정연한 단분자막을 형성합니다3). 이 단분자막이 눈물 수성층의 증발을 물리적으로 억제합니다. 시험관 내에서 PFHO를 생리식염수에 적용하면 증발이 약 80% 감소합니다2).
PFHO와 PFBP(퍼플루오로부틸펜탄)의 증발 속도를 비교한 시험관 내 중량 분석에서 1시간 후 PFHO의 증발량은 1.5% 미만인 반면, PFBP는 93%가 증발했습니다. 생체 외 모델에서 1시간 후 PFHO의 각막 잔류율은 54.5%로 PFBP(18.6%)의 약 3배였습니다3).
각막 표면 온도 감소와 TRPM8 활성화가 두 번째 기전입니다4). PFHO의 국소 적용은 각막 표면 온도를 낮추고 각막의 TRPM8 냉각 수용체 활성을 증가시킵니다. 이 반응은 반사성 눈물 분비와 눈 깜빡임 촉진, 불쾌감 및 통증 감소로 이어지는 것으로 생각됩니다.
눈물 지질층 개선도 보고되었습니다. 전임상 데이터에서 PFHO 7일 투여 후 지질층 등급이 단회 점안 후 5분부터 개선되기 시작했으며, 반복 투여로 5~7일 동안 개선이 유지되었습니다4). 임상 시험에서도 4주 시점에 지질층 두께와 눈물막 두께의 개선이 관찰되었습니다4).
7. 최신 연구 및 향후 전망
섹션 제목: “7. 최신 연구 및 향후 전망”TFOS DEWS III 2025에서의 위치
섹션 제목: “TFOS DEWS III 2025에서의 위치”2025년에 발표된 TFOS DEWS III Management and Therapy Report에서 PFHO는 증발 항진형 건성안(DED)에 대한 근거 기반 치료 옵션으로 자리매김하고 있습니다4). 체계적 문헌고찰(6건의 RCT)에서 PFHO군은 OSDI, 지질층 두께, 각막 염색, 이상반응 등 대부분의 변수에서 대조군보다 더 큰 개선을 보였습니다4).
PFHO와 무수 사이클로스포린 0.1%의 비교
섹션 제목: “PFHO와 무수 사이클로스포린 0.1%의 비교”PFHO와 무수 CsA 0.1%(Vevye®)는 모두 SFA 함유 무수·무방부제 제제입니다. 그러나 PFHO는 증발 억제를 표적으로 하는 반면, CsA 0.1%는 면역 조절을 통한 눈물 생성 증가를 표적으로 합니다3). PFHO의 임상시험은 증발 항진형 DED(MGD 동반)를 대상으로 한 반면, CsA 0.1% 시험에서는 MGD를 제외하고 눈물 감소형 중증 사례를 대상으로 했습니다4).
향후 과제
섹션 제목: “향후 과제”임상시험의 추적 기간은 주로 8주였으며, 장기(1년 초과) 유효성 및 부작용 평가가 필요합니다1). 중증 DED(tCFS > 11) 또는 콘택트렌즈 착용자 등 시험에서 제외된 환자군에 대한 평가도 향후 과제입니다1). 한국에서의 승인을 위한 검토도 기대됩니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Guedes J, Hespanhol LC, Freitas MAA, et al. Efficacy and Safety of Perfluorohexyloctane in Evaporative Dry Eye Disease Associated With Meibomian Gland Dysfunction: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Cureus. 2024;16(8):e67920.
- Azhar A, Taimuri MA, Oduoye MO, et al. MEIBO (perfluorohexyloctane): a novel approach to treating dry eye disease. Ann Med Surg. 2024;86:5292-5298.
- Periman LM, White DE, Katsev D. Differentiating Between Perfluorohexyloctane Ophthalmic Solution and Water-Free Cyclosporine Ophthalmic Solution 0.1% for Dry Eye Disease: A Review of Preclinical and Clinical Characteristics. Ophthalmol Ther. 2025;14(2):283-293.
- TFOS DEWS III Management and Therapy Report. Am J Ophthalmol. 2025;279:289-386.
