蒸發亢進型乾眼

全氟己基辛烷眼科溶液
一目瞭然的要點
Section titled “一目瞭然的要點”1. 全氟己基辛烷是什麼?
Section titled “1. 全氟己基辛烷是什麼?”全氟己基辛烷(perfluorohexyloctane, PFHO)眼科溶液(商品名:Miebo®,Bausch+Lomb公司)於2023年5月獲得FDA批准,用於治療乾眼病(DED)的體徵和症狀。它是首個針對淚液蒸發的FDA批准處方眼藥水2)。
PFHO是一種兩親性半氟化烷烴(化學式C₁₄H₁₇F₁₃,F6H8),具有親脂性烴鏈段和疏脂性氟碳鏈段3)。該製劑為單一成分、無水、無防腐劑製劑,含100%活性成分4)。在美國作為處方藥銷售,但在歐洲、澳洲和紐西蘭,它已以EvoTears®/NovaTears®的名稱使用多年4)。
乾眼是一種多因素疾病,美國有超過1600萬人患病,淚液蒸發增強與高達90%的病例相關3)。瞼板腺功能障礙(MGD)是蒸發過強型乾眼的主要原因1)。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”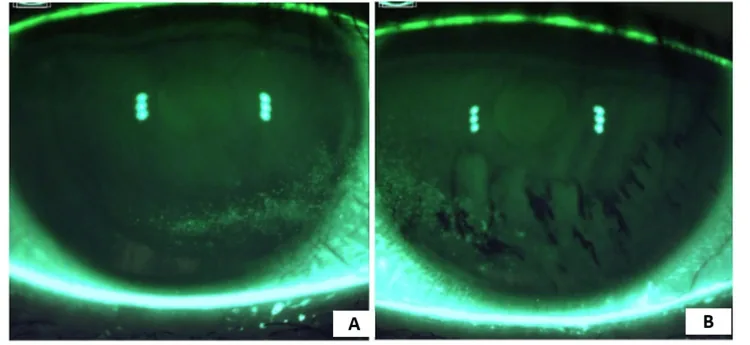
包括蒸發增強型乾眼在內的DED自覺症狀如下2)。
- 眼乾燥感:最常見的主訴
- 灼熱感、刺痛感:與發炎反應相關
- 異物感:伴隨眼表損傷
- 畏光:伴隨角膜上皮損傷出現
- 視物模糊:因淚膜不穩定導致暫時性視力波動
- 眼疲勞:VDT工作時加重
- 淚膜破裂時間(BUT)縮短:日本診斷標準中BUT≤5秒為確診條件
- 角膜螢光素染色陽性:反映角膜上皮損傷程度。全角膜螢光素染色評分(tCFS)用於臨床試驗的主要終點
- 瞼板腺功能障礙:腺體開口阻塞、瞼板腺分泌物性狀改變
- 淚液半月弧減少:反映淚液量減少
- 角結膜上皮損傷:充血、點狀表層角膜炎
3. 原因與風險因素
Section titled “3. 原因與風險因素”淚液分泌不足型乾眼
- 年齡和性別:盛行率隨年齡增長而上升。女性較常見,從50歲以下的5.7%增加到75歲及以上的9.8%2)
- 停經後雌激素治療:荷爾蒙波動是乾眼的風險因素
- VDT工作:眨眼頻率降低導致淚液蒸發增加
- 佩戴隱形眼鏡:PFHO需要在點眼前取下隱形眼鏡,並在至少30分鐘後重新佩戴
4. 診斷和檢查方法
Section titled “4. 診斷和檢查方法”乾眼的診斷標準
Section titled “乾眼的診斷標準”根據日本乾眼研究會的診斷標準,同時滿足主觀症狀和淚膜破裂時間(BUT)≤5秒即可確診。根據TFOS DEWS II的定義,淚膜穩態喪失、淚液滲透壓升高、眼表炎症和神經感覺異常也起病因作用。
| 檢查 | 評估對象 | 臨床試驗中的使用 |
|---|---|---|
| tCFS | 角膜上皮損傷 | GOBI和MOJAVE的主要終點 |
| VAS乾燥感分數 | 自覺症狀 | 同上 |
| OSDI問卷 | 生活品質/症狀嚴重度 | 次要評估指標 |
- 淚膜破裂時間(BUT):螢光素染色後,測量淚膜首次破裂的時間。
- Schirmer試驗:定量評估淚液分泌量。無麻醉下≤5mm表示淚液分泌減少型。
- 瞼板腺評估:評估腺體形態、分泌物可擠出性及瞼板腺脂質品質。
- 淚膜導向診斷(TFOD):透過睜眼後立即的淚膜破裂模式來確定病因層。
PFHO特別適合伴有MGD的蒸發增強型乾眼患者。臨床試驗中,納入標準為BUT≤5秒、Schirmer試驗≥5mm、MGD評分≥3、tCFS 4-11的患者。對於淚液分泌顯著減少的淚液減少型乾眼,免疫調節劑環孢素眼藥水可能適用。
5. 標準治療方法
Section titled “5. 標準治療方法”PFHO的用法與用量
Section titled “PFHO的用法與用量”PFHO是一種不含防腐劑和添加劑的眼科溶液,由100%全氟己基辛烷組成。建議劑量為每隻患眼每日4次,每次1滴。
臨床試驗結果
Section titled “臨床試驗結果”兩項第3期隨機雙盲試驗(GOBI試驗和MOJAVE試驗)顯示,與生理食鹽水對照相比,PFHO每日四次點眼在第8週時顯著改善了tCFS和VAS乾燥感評分這兩個主要終點4)。
一項包含4項RCT的統合分析(1,814例患者)報告了以下結果1):
PFHO組與對照組相比,tCFS顯著改善(MD -1.09;95% CI -1.37至-0.82;P < 0.001;I² = 0%)。眼部不適VAS(MD -9.69;P < 0.01)、OSDI(MD -5.79;P < 0.01)和灼熱感/刺痛感評分(MD -7.16;P < 0.01)也均顯著改善,且未觀察到異質性1)。
在GOBI試驗的延伸試驗KALAHARI試驗(208例患者,52週)中,tCFS相對於基線的平均變化為-2.1,VAS乾燥感評分的平均變化為-33.7,證實了在60週內的持續療效4)。
| 試驗 | 對象 | tCFS改善(LSMD) | VAS改善(LSMD) |
|---|---|---|---|
| GOBI | 597例 | -0.97(P < 0.001) | -7.6(P < 0.001) |
| MOJAVE | 620例 | -1.2(P < 0.001) | -10.2(P < 0.001) |
在第2週(第15天)時,已觀察到tCFS和VAS乾燥感評分顯著改善,並且在單次點眼後5分鐘時也觀察到症狀改善效果4)。
PFHO點眼液的安全性良好1)。
- 最常見不良事件:視力模糊(1.3%~3.0%)。輕度且暫時性4)
- 眼部不良事件發生率:PFHO組與對照組無顯著差異(RR 1.00;95% CI 0.77~1.29;P = 0.999)1)
- 嚴重眼部不良事件:在GOBI、MOJAVE和KALAHARI試驗中均未報告3)
- 停藥率:低3)
- 非臨床研究已確認其無毒性且無生物蓄積性4)
PFHO目前沒有絕對禁忌症,但在孕婦、哺乳期婦女和18歲以下人群中的安全性和有效性尚未確定。
在日本乾眼治療中的定位
Section titled “在日本乾眼治療中的定位”在日本,根據乾眼研究會提出的「眼表分層治療(TFOT)」概念,針對病因層進行治療。對於脂質層,採用熱敷和眼瞼清潔;對於水液層,使用玻尿酸鈉和淚點塞;對於分泌型黏蛋白,使用地夸磷索鈉;對於上皮,使用瑞巴派特。PFHO可作為補充脂質層功能、直接抑制淚液蒸發的全新選擇。
在臨床試驗中,單次點眼後5分鐘即可觀察到症狀改善。第2週(第15天),角膜螢光素染色評分和乾澀感評分均顯示出顯著改善。在KALAHARI延長試驗中,效果持續了52週。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”乾眼的惡性循環
Section titled “乾眼的惡性循環”乾眼病理生理的核心是淚液高滲透壓2)。淚液分泌減少或蒸發增加導致淚液滲透壓升高,會激活MAP激酶,並引發發炎性細胞激素、趨化因子和基質金屬蛋白酶的分泌2)。這些發炎介質誘導角膜上皮細胞、結膜細胞和杯狀細胞凋亡,導致糖萼損傷、眼表潤滑能力下降和淚膜不穩定。結果進一步加重高滲透壓,形成「惡性循環」2)。
PFHO的作用機轉
Section titled “PFHO的作用機轉”PFHO的作用機轉提出了幾種假說4)。
抑制淚液蒸發是首要機轉。PFHO是一種兩親性分子,其氟碳鏈段(疏油、親氣)和烴鏈段(親油)在淚液-空氣界面自組裝形成有序的單分子層3)。該單分子層物理性地抑制淚液水層的蒸發。體外實驗中,將PFHO應用於生理食鹽水可使蒸發減少約80%2)。
在比較PFHO和PFBP(全氟丁基戊烷)蒸發速率的體外重量分析中,1小時後PFHO的蒸發量不到1.5%,而PFBP蒸發了93%。在離體模型中,1小時後PFHO的角膜殘留率為54.5%,約為PFBP(18.6%)的3倍3)。
降低角膜表面溫度並激活TRPM8是第二個機轉4)。局部應用PFHO可降低角膜表面溫度,增加角膜TRPM8冷感受體的活性。這種反應被認為可促進反射性流淚和眨眼,並減輕不適和疼痛。
改善淚液脂質層也有報導。臨床前數據顯示,PFHO給藥7天後,單次點眼後5分鐘脂質層分級即開始改善,重複給藥後改善維持5-7天4)。臨床試驗也在第4週觀察到脂質層厚度和淚膜厚度的改善4)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”TFOS DEWS III 2025中的定位
Section titled “TFOS DEWS III 2025中的定位”在2025年發表的TFOS DEWS III Management and Therapy Report中,PFHO被定位為基於證據的蒸發亢進型乾眼症(DED)治療選擇4)。一項系統性回顧(6項RCT)報告,PFHO組在OSDI、脂質層厚度、角膜染色及不良事件等大多數變數上均優於對照組4)。
PFHO與無水環孢素0.1%的比較
Section titled “PFHO與無水環孢素0.1%的比較”PFHO和無水CsA 0.1%(Vevye®)均為含SFA的無水、無防腐劑製劑。但PFHO針對抑制蒸發,而CsA 0.1%透過免疫調節增加淚液分泌3)。PFHO的臨床試驗針對蒸發亢進型DED(合併MGD),而CsA 0.1%的試驗排除了MGD,納入的是淚液分泌減少的重症病例4)。
臨床試驗的追蹤期主要為8週,需要評估長期(超過1年)的有效性和副作用1)。對試驗排除的患者群體(如重度DED(tCFS > 11)或隱形眼鏡佩戴者)的評估也是未來的挑戰1)。期待在台灣獲得批准。
8. 參考文獻
Section titled “8. 參考文獻”- Guedes J, Hespanhol LC, Freitas MAA, et al. Efficacy and Safety of Perfluorohexyloctane in Evaporative Dry Eye Disease Associated With Meibomian Gland Dysfunction: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Cureus. 2024;16(8):e67920.
- Azhar A, Taimuri MA, Oduoye MO, et al. MEIBO (perfluorohexyloctane): a novel approach to treating dry eye disease. Ann Med Surg. 2024;86:5292-5298.
- Periman LM, White DE, Katsev D. Differentiating Between Perfluorohexyloctane Ophthalmic Solution and Water-Free Cyclosporine Ophthalmic Solution 0.1% for Dry Eye Disease: A Review of Preclinical and Clinical Characteristics. Ophthalmol Ther. 2025;14(2):283-293.
- TFOS DEWS III Management and Therapy Report. Am J Ophthalmol. 2025;279:289-386.
