นิวโรบลาสโตมา (NB) เป็นเนื้องอกแข็งนอกกะโหลกศีรษะที่พบบ่อยที่สุดในเด็ก มีต้นกำเนิดจากนิวรัลครีส คิดเป็นประมาณ 10% ของมะเร็งในเด็ก
ตำแหน่งปฐมภูมิที่พบบ่อยที่สุดคือต่อมหมวกไตและช่องท้อง โดยมีการแพร่กระจายไปยังเบ้าตา ใน 11–56% ของกรณี
ลักษณะเฉพาะของการแพร่กระจายไปยังเบ้าตา ได้แก่ รอยฟกช้ำรอบเบ้าตา (raccoon eyes) ตาโปน และหนังตาตก
บางครั้งอาจพบว่าเป็นสัญญาณพารานีโอพลาสติกของกลุ่มอาการออปโซโคลนัส-ไมโอโคลนัส (OMS )
การตรวจ MIBG scintigraphy เป็นการตรวจทางภาพที่มีประโยชน์มากที่สุดในการระบุตำแหน่งของการแพร่กระจาย
ในกรณีที่มีความเสี่ยงสูง จะใช้การรักษาแบบผสมผสานระหว่างเคมีบำบัดขนาดสูง การปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดด้วยตนเอง และภูมิคุ้มกันบำบัด แต่อัตราการรอดชีวิต 5 ปีต่ำกว่า 50%
อัตราการรอดชีวิต 5 ปีในผู้ป่วยที่มีการแพร่กระจายไปยังเบ้าตา อยู่ที่ 7.6% ซึ่งแย่มาก
นิวโรบลาสโตมา (Neuroblastoma; NB) เป็นเนื้องอกชนิดร้ายที่เกิดจากเซลล์ตั้งต้นของระบบประสาทซิมพาเทติกซึ่งมีต้นกำเนิดจากนิวรัลครีสต์ (neural crest) คิดเป็นประมาณ 10% ของเนื้องอกร้ายในเด็ก และเป็นเนื้องอกแข็งนอกกะโหลกศีรษะที่พบบ่อยที่สุดในเด็ก นอกจากนี้ยังเป็นเนื้องอกร้ายที่พบบ่อยเป็นอันดับสองรองจากมะเร็งเม็ดเลือดขาว
ตำแหน่งปฐมภูมิ ได้แก่ ต่อมหมวกไตประมาณ 46%, ช่องท้อง (นอกต่อมหมวกไต) ประมาณ 18%, เมดิแอสตินัมส่วนหลังประมาณ 14%, เชิงกรานและอื่นๆ ประมาณ 22%4) มากกว่า 60% เกิดขึ้นในช่องท้อง เช่น ต่อมหมวกไตและปมประสาทซิมพาเทติก
ลักษณะทางระบาดวิทยา มีดังนี้:
ประมาณ 700 รายได้รับการวินิจฉัยในแต่ละปีในสหรัฐอเมริกา
อายุเฉลี่ยเมื่อวินิจฉัยคือ 19 เดือน 90% ได้รับการวินิจฉัยก่อนอายุ 5 ปี5)
การเกิดในผู้ใหญ่น้อยมาก คือ 1 รายต่อ 10 ล้านคนต่อปี5)
ทางจักษุวิทยา นิวโรบลาสโตมาสามารถแพร่กระจายไปยังเบ้าตา ได้ 11-56% ลักษณะทางคลินิกมีความหลากหลายตั้งแต่การหายเองตามธรรมชาติไปจนถึงการแพร่กระจายอย่างรุนแรง
ลำดับเหตุการณ์ทางประวัติศาสตร์ มีดังนี้:
พ.ศ. 2407: Virchow รายงานเนื้องอกในช่องท้องครั้งแรกว่าเป็น “glioma”
พ.ศ. 2434: Marchand อธิบายลักษณะที่มาจากต่อมหมวกไตส่วนในและระบบประสาทซิมพาเทติก
พ.ศ. 2444: Pepper รายงานทารกที่มีการแพร่กระจายไปยังตับ (เทียบเท่าระยะ MS ในปัจจุบัน)
พ.ศ. 2453: Homer Wright อธิบาย pseudorosette แบบ Homer-Wright ในไขกระดูก
Q
นิวโรบลาสโตมามักแพร่กระจายไปที่ใด?
A
การแพร่กระจายมักเกิดที่กระดูก ไขกระดูก ต่อมน้ำเหลือง ตับ และผิวหนัง ความถี่ของการแพร่กระจายไปยังเบ้าตา อยู่ที่ 11-56% และอาจมีอาการตาโปนหรือรอยช้ำรอบเบ้าตา (raccoon eyes) เป็นอาการแรกเริ่ม
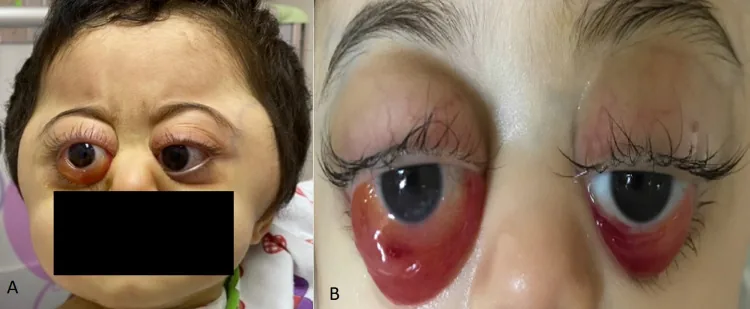
ภาพแสดงอาการของนิวโรบลาสโตมา Rahaf A Mandura. Rapidly Progressive Ocular Proptosis as the First Sign of Neuroblastoma in a 16-Month-Old Child: Case Report and Review of Literature. Cureus. 2022 Jan 6; 14(1):e20982. Figure 1. PM
CI D: PMC8817620. License: CC BY.
รูปที่ 1: ภาพแสดงอาการของนิวโรบลาสโตมาที่ตา
อาการที่ผู้ปกครองหรือตัวผู้ป่วยสังเกตเห็นมีดังนี้
อาการบวมและช้ำรอบดวงตา : ดวงตาบวมเป็นสีน้ำเงินม่วง (raccoon eyes)ตาโปน : ลูกตาข้างหนึ่งยื่นออกมาข้างหน้าเปลือกตาบวม : เปลือกตาบนและล่างบวมน้ำเห็นภาพซ้อน (มองเห็นวัตถุเป็นสองภาพ)การมองเห็น ลดลงอาการทั่วร่างกาย : ปวดท้อง ท้องอืด ปวดกระดูก มีไข้ อ่อนเพลีย ท้องเสีย กล้ามเนื้ออ่อนแรง
แบ่งเป็นอาการแสดงทางจักษุวิทยาที่เกี่ยวข้องกับการแพร่กระจายไปยังเบ้าตา และอาการแสดงทางระบบประสาทจากเนื้องอก
อาการแสดงที่เบ้าตาและรอบดวงตา
เลือดออกใต้ผิวหนังรอบเบ้าตา (raccoon eyes) : อาการแสดงที่พบบ่อยที่สุดในการแพร่กระจายไปยังเบ้าตา ในเด็กอายุต่ำกว่า 2 ปี เกิดจากเลือดออกและเนื้อตายของเนื้องอก มักถูกเข้าใจผิดว่าเป็นการถูกทำร้าย
ตาโปน (proptosis) : การเคลื่อนไปข้างหน้าจากก้อนเนื้องอกในเบ้าตา
อาการบวมน้ำที่เปลือกตาและเยื่อบุตา : อาการบวมน้ำอาจรุนแรงได้
รอยช้ำที่เปลือกตา (ecchymosis) : เป็นลักษณะเฉพาะของ NB และมะเร็งเม็ดเลือดขาว
การทำลายกระดูกเบ้าตา : พบการเปลี่ยนแปลงแบบละลายกระดูกจากการตรวจภาพ
อาการทางระบบประสาทและจอตา
กลุ่มอาการฮอร์เนอร์ ม่านตา หด หนังตาตก และไม่มีเหงื่อ เกิดเมื่อเนื้องอกปฐมภูมิในทรวงอกเกี่ยวข้องกับเส้นประสาทซิมพาเทติก
ม่านตา สองสีกลุ่มอาการฮอร์เนอร์ จาก NB แต่กำเนิดที่ปมประสาทคอ
ภาวะตากระตุก (Opsoclonus) : การเคลื่อนไหวของลูกตาแบบ saccade ความถี่สูง (10-15 Hz) และหลายทิศทาง ร่วมกับกล้ามเนื้อกระตุก (myoclonus)
อัมพาตของกล้ามเนื้อ rectus lateral, ตาเหล่ , ตาเหล่เข้า : เนื่องจากความผิดปกติของการเคลื่อนไหวของลูกตา
ภาวะ papilledema, จอประสาทตา ตกเลือด, เส้นประสาทตา ฝ่อ : เนื่องจากความดันในกะโหลกศีรษะสูงหรือการแทรกซึมโดยตรง
ในเด็กอายุต่ำกว่า 2 ปีที่มีเลือดออกใต้ผิวหนังรอบเบ้าตา (มักเป็นสองข้าง) ต้องนึกถึงการแพร่กระจายของ neuroblastoma มาที่เบ้าตา ในการวินิจฉัยแยกโรคเสมอ เลือดออกใต้ผิวหนังรอบเบ้าตา สองข้างโดยไม่มีประวัติการบาดเจ็บเป็นสัญญาณที่บ่งชี้ถึง neuroblastoma มากกว่าการถูกทารุณกรรม
Q
รอยช้ำรอบดวงตาของเด็กอาจเป็นสัญญาณของ neuroblastoma ได้หรือไม่?
A
รอยฟกช้ำรอบเบ้าตา (raccoon eyes) เป็นอาการที่พบบ่อยที่สุดของการแพร่กระจายไปยังเบ้าตา ในเด็กอายุต่ำกว่า 2 ปี และการมีเลือดออกรอบตาทั้งสองข้างโดยไม่มีประวัติการบาดเจ็บควรทำให้สงสัย neuroblastoma อย่างมาก เนื่องจากมักถูกเข้าใจผิดว่าเป็นการทารุณกรรมเด็ก จึงจำเป็นต้องตรวจร่างกายอย่างละเอียด เช่น อัลตราซาวนด์ช่องท้องและการตรวจ catecholamine ในปัสสาวะเพื่อการวินิจฉัยแยกโรค
Q
Opsoclonus-myoclonus syndrome คืออะไร?
A
เป็นกลุ่มอาการที่มีลักษณะการเคลื่อนไหวของลูกตาแบบ saccadic หลายทิศทางความถี่สูง (10-15 Hz) ร่วมกับ myoclonus ถือเป็น paraneoplastic syndrome ที่เกิดจากแอนติบอดีผิดปกติต่อ RNA ของเซลล์ประสาท พบ neuroblastoma แฝงในผู้ป่วย OMS 48% ดังนั้นจึงจำเป็นต้องตรวจร่างกายอย่างละเอียดในเด็กที่มี OMS
ส่วนใหญ่เป็นแบบประปราย และยังไม่มีการระบุปัจจัยเสี่ยงที่ชัดเจน
ปัจจัยทางพันธุกรรม (ประมาณ 1-2% ของทั้งหมด):
การกลายพันธุ์ในเซลล์สืบพันธุ์ของ ALK : สาเหตุที่พบบ่อยที่สุดของ NB ในครอบครัวความผิดปกติของ PHOX2B : เกี่ยวข้องกับการบกพร่องในการแยกตัวเป็นเซลล์ประสาทที่เจริญเต็มที่ความผิดปกติของ KIF1B และการเพิ่มจำนวนของ MYCN : ส่วนหนึ่งของ NB ในครอบครัวความหลากหลายของจำนวนสำเนา NBPF10 (การสูญเสีย 1p และ 11q) : เกี่ยวข้องกับ NB ที่มีความเสี่ยงสูงการเพิ่มจำนวนของยีน LMO1 : ปัจจัยเสี่ยงของ NB ที่รุกรานความสัมพันธ์กับ NF1 และกลุ่มอาการ Beckwith-Wiedemann : เกิดขึ้นร่วมกันได้ยาก
การกลายพันธุ์ทางพันธุกรรมที่เกี่ยวข้องกับ NB ที่เกิดขึ้นประปราย:
ความแปรผันทางพันธุกรรมที่ 6p22 : มีรายงานความสัมพันธ์กับ NB ที่เกิดขึ้นประปราย
การขยายตัวของ MYCN พบใน 20-25% ของ NB ในเด็ก โดยมีการกระจายแบบสองรูปแบบคือ 3-10 เท่าหรือ 100-300 เท่า เป็นเครื่องหมายระดับโมเลกุลที่สัมพันธ์อย่างมากกับ NB ที่รุกราน5) .
ลักษณะทางอณูชีววิทยาของ NB ในผู้ใหญ่ แตกต่างจากเด็ก โดยการเพิ่มจำนวนของ MYCN นั้นพบได้น้อย การกลายพันธุ์ของ ATRX (11%) การกลายพันธุ์ของ ALK (สูงสุด 14%) และการจัดเรียงใหม่ของ TERT (23%) เป็นลักษณะเฉพาะ 5) .
ปัจจัยเสี่ยงปริกำเนิด (จากการศึกษาแบบย้อนหลังในกลุ่มประชากร):
ทารกอายุครรภ์น้อย: น้ำหนักแรกเกิดสูง, น้ำหนักแม่เพิ่มมากเกินไป, ความดันโลหิตสูงขณะตั้งครรภ์, การคลอดบุตรเมื่ออายุมาก
ทารกอายุมาก: น้ำหนักแรกเกิดต่ำเพิ่มความเสี่ยง
กลุ่มอายุสูง: บุตรคนแรก, การผ่าตัดคลอดครั้งแรก, การคลอดยืดเยื้อ, การแตกของถุงน้ำคร่ำก่อนกำหนด
การใช้ยาของมารดา (ยาขับปัสสาวะ, ยาลดความดันโลหิต), ภาวะโลหิตจางระหว่างตั้งครรภ์, การใช้ยาย้อมผมชั่วคราว
ไม่มีปัจจัยเสี่ยงเฉพาะที่ทราบสำหรับการแพร่กระจายไปยังเบ้าตา
นิวโรบลาสโตมาส่วนใหญ่เกิดขึ้นแบบประปราย และปัจจุบันยังไม่มีวิธีการป้องกันที่ได้รับการยืนยัน หากมีประวัติครอบครัวเป็นนิวโรบลาสโตมา ควรพิจารณาการให้คำปรึกษาทางพันธุกรรม หากพบความผิดปกติ เช่น ก้อนในช่องท้อง เลือดออกรอบดวงตา หรือตาโปนในทารกและเด็กเล็ก ควรพาไปพบกุมารแพทย์และจักษุแพทย์ทันที
คาเทโคลามีนในปัสสาวะ (HVA และ VMA) : เดิมรายงานว่าสูงขึ้นใน 90-95% ของผู้ป่วย แต่การศึกษาล่าสุดพบว่ามีความไวต่ำกว่า ในผู้ใหญ่พบเพียง 40-57% (ตรงกันข้ามกับ 95% ในเด็ก)การตรวจเลือด : การนับเม็ดเลือดสมบูรณ์ การทำงานของตับและไต อิเล็กโทรไลต์ เฟอร์ริติน LDH การทำงานของต่อมไทรอยด์การตรวจชิ้นเนื้อไขกระดูก : ประเมินการแทรกซึมของไขกระดูกโดยการดูดและตัดชิ้นเนื้อจากยอดกระดูกเชิงกรานด้านหลังทั้งสองข้างการตรวจแอนติบอดี : แอนติบอดีต่อต้าน Hu (ANNA-1) มีประโยชน์ในการวินิจฉัยนิวโรบลาสโตมาในเด็กการเจาะน้ำไขสันหลัง : หลีกเลี่ยงเว้นแต่ทราบว่ามีการแพร่กระจายไปยังระบบประสาทส่วนกลาง (มีรายงานการเพิ่มขึ้นของการแพร่กระจายหลังการเจาะ)
ลักษณะเฉพาะของแต่ละวิธีแสดงไว้ด้านล่าง
การตรวจ ลักษณะ ข้อบ่งชี้ ซีทีสแกน ขอบเขตชัด/ไม่ชัด, ค่าความหนาแน่นสูง, หินปูนขนาดเล็ก การประเมินเบื้องต้น, การเปลี่ยนแปลงกระดูกเบ้าตา แบบสลาย เอ็มอาร์ไอ สัญญาณต่ำใน T1, ไม่สม่ำเสมอใน T2, ประเมินการลุกลามเข้าสู่กะโหลกศีรษะ การตรวจละเอียดในกะโหลกศีรษะและเบ้าตา MIBG (123I) เหมาะสมที่สุดในการระบุการแพร่กระจายไปยังเนื้อเยื่ออ่อนและกระดูก การประเมินการแพร่กระจายทั่วร่างกาย PET ความไวและความจำเพาะสูง การวินิจฉัยและติดตามการรักษา
การตรวจ MIBG scintigraphy (123I-MIBG) เหนือกว่า PET/CT ในการระบุการแพร่กระจายไปยังเนื้อเยื่ออ่อนและกระดูก ในการแพร่กระจายไปยังเบ้าตา CT จะแสดงการเปลี่ยนแปลงแบบ lytic ของกระดูก และ MRI จะแสดงสัญญาณ isointense กับกล้ามเนื้อนอกลูกตา ใน T1 และต่ำกว่าไขมัน และสัญญาณ hyperintense กับกล้ามเนื้อนอกลูกตา และไขมันใน T2 การแพร่กระจายมักเกิดขึ้นที่ผนังด้านหลังด้านข้างของเบ้าตา
Q
การตรวจวินิจฉัยทางภาพที่มีประโยชน์มากที่สุดสำหรับนิวโรบลาสโตมาคืออะไร?
A
การตรวจ MIBG scintigraphy (123I-MIBG) ถือว่ามีประโยชน์มากที่สุดในการระบุการแพร่กระจายไปยังเนื้อเยื่ออ่อนและกระดูก และเหนือกว่า PET/CT เนื่องจากสามารถประเมินตำแหน่งแพร่กระจายทั่วร่างกายได้ในครั้งเดียว จึงใช้ทั้งในการแบ่งระยะเริ่มต้นและการประเมินผลการรักษา
ลักษณะของเซลล์เนื้องอก : นิวโรบลาสต์ที่ยังไม่เจริญเต็มที่ (เส้นผ่านศูนย์กลาง 10–15 ไมโครเมตร) นิวเคลียสแบบถุงขนาดใหญ่และมีสีเข้ม ไซโทพลาซึมแบบ eosinophilic น้อยรูปแบบการจัดเรียง : การจัดเรียงแบบแผ่น ก้อน หรือสาย; การสร้าง pseudorosette (แบบ Homer-Wright)อิมมูโนฮิสโตเคมี : ให้ผลบวกต่อซินแนปโตฟิซิน, ให้ผลบวกต่อโครโมกรานิน, ให้ผลบวกต่อ CD56, ให้ผลบวกต่อ NSE4) การจำแนกชิมาดะ (INPC) : การจำแนกทางจุลพยาธิวิทยาเพื่อพยากรณ์โรคที่ดี/ไม่ดีดัชนีการเพิ่มจำนวน Ki-67 : ≥25% สัมพันธ์กับอัตราการรอดชีวิต 3 ปีที่ 34% (76% หาก <25%)5)
การแบ่งระยะตามระบบการจำแนกความเสี่ยงของนิวโรบลาสโตมาระหว่างประเทศ (INRGSS) แสดงไว้ด้านล่าง4) .
L1 : เนื้องอกเฉพาะที่, ไม่มีปัจจัยเสี่ยงที่กำหนดจากภาพ (IDRF), อยู่ในช่องเดียวL2 : เนื้องอกเฉพาะที่ โดยมี IDRF อย่างน้อยหนึ่งรายการM : การแพร่กระจายระยะไกล (ยกเว้น MS )MS
การวินิจฉัยแยกโรคของการแพร่กระจายในเบ้าตา : Ewing sarcoma, มะเร็งเม็ดเลือดขาว (คลอโรมา), rhabdomyosarcomaการวินิจฉัยแยกโรคทั่วร่างกาย : olfactory neuroblastoma, ganglioneuroblastoma, pheochromocytoma, Wilms tumor, rhabdomyosarcoma
การรักษาจะดำเนินการตามการจำแนกความเสี่ยง
กลุ่มความเสี่ยงต่ำ:
การสังเกตอาการ + การตัดออกโดยการผ่าตัด
อัตราการรอดชีวิต 5 ปี: มากกว่า 90%
กลุ่มเสี่ยงสูง (ระยะ M, อายุ ≥ 18 เดือน ฯลฯ):
เคมีบำบัดเหนี่ยวนำ : การใช้ยาหลายชนิดร่วมกัน ได้แก่ cisplatin, cyclophosphamide, doxorubicin, dexrazoxane, etoposide, vincristine 4) การผ่าตัดเอาก้อนเนื้อออก : การนำก้อนเนื้องอกปฐมภูมิออก (เช่น การผ่าตัดต่อมหมวกไต) 4) การรักษาแบบประคอง : เคมีบำบัดขนาดสูง (BuMel: busulfan + melphalan) + การปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดด้วยตนเอง + การฉายรังสี (เนื้องอกปฐมภูมิ 20 Gy/10 ครั้ง, เนื้องอกที่เหลือ 30 Gy/15 ครั้ง) 4) ภูมิคุ้มกันบำบัด : แอนติบอดีต่อต้าน GD2 (dinutuximab) 5) การรักษาแบบประคับประคอง : กรด 13-cis-retinoic (isotretinoin) 160 มก./ตร.ม./วัน, 14 วัน/เดือน, นาน 6 เดือน 4)
อัตราการรอดชีวิต 5 ปีในกลุ่มความเสี่ยงสูงน้อยกว่า 50% 4) .
การตัดออกทั้งหมดไม่ค่อยมีข้อบ่งชี้สำหรับเนื้องอกที่แพร่กระจายไปยังเบ้าตา ให้ทำการรักษาที่มีประสิทธิภาพสำหรับมะเร็งปฐมภูมิ เช่น เคมีบำบัดหรือรังสีรักษา ในเด็ก NB ที่ตอบสนองต่อเคมีบำบัด การพยากรณ์โรคค่อนข้างดี อัตราการรอดชีวิต 5 ปีเมื่อมีการแพร่กระจายไปยังเบ้าตา คือ 7.6% ซึ่งแย่มาก
ไม่มีแนวทางการรักษามาตรฐานที่ชัดเจน และมักจะปรับใช้แนวทางของเด็ก 5) ทำการผ่าตัด (รวมถึงการส่องกล้อง) + เคมีบำบัด (เช่น คาร์โบพลาติน + อีโทโพไซด์) อัตราการรอดชีวิต 5 ปีในผู้ใหญ่อายุมากกว่า 20 ปีคือ 36.3% การพยากรณ์โรคไม่ดี 5) .
ใน NB ความเสี่ยงสูง จำเป็นต้องได้รับการรักษาแบบสหสาขาวิชาที่ผสมผสานเคมีบำบัดขนาดสูง การปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดด้วยตนเอง การฉายรังสี และภูมิคุ้มกันบำบัด และการรักษาในสถานพยาบาลเฉพาะทางเป็นสิ่งที่ขาดไม่ได้
ในระหว่างการให้ 13-cis-retinoic acid (การรักษาแบบประคับประคอง) เนื่องจากมีฤทธิ์ทำให้ทารกพิการ ผู้ป่วยในวัยเจริญพันธุ์จำเป็นต้องคุมกำเนิดอย่างเคร่งครัด
อัตราการรอดชีวิตระยะยาวของกลุ่มความเสี่ยงสูงยังคงอยู่ที่ 40-50% เท่านั้น 2) และจำเป็นต้องติดตามผลระยะยาวหลังการรักษา
Q
การพยากรณ์โรคของนิวโรบลาสโตมาหากมีการแพร่กระจายไปยังเบ้าตาจะเป็นอย่างไร?
A
อัตราการรอดชีวิต 5 ปีของนิวโรบลาสโตมาที่มีการแพร่กระจายไปยังเบ้าตา อยู่ที่ 7.6% ซึ่งแย่มาก การแพร่กระจายไปยังเบ้าตา มักบ่งชี้ถึงการแพร่กระจายระยะไกล (เทียบเท่าระยะ M) และจะได้รับการรักษาแบบสหสาขาวิชาในกลุ่มความเสี่ยงสูง แต่การพยากรณ์โรคที่ดีขึ้นมีจำกัด
NB เกิดจากเซลล์ตั้งต้นของระบบประสาทซิมพาเทติก (sympathoblast) การกลายพันธุ์ของ PHOX2B ทำให้การแยกตัวเป็นเซลล์ประสาทที่เจริญเต็มที่บกพร่อง นำไปสู่การเกิดเนื้องอก การกลายพันธุ์ของ ALK สัมพันธ์กับการเพิ่มจำนวนที่ลดลงและการเพิ่มขึ้นของเซลล์ประสาทซิมพาเทติกที่ยังไม่เจริญเต็มที่
ความผิดปกติของเมแทบอลิซึมของ catecholamine : เนื่องจากข้อบกพร่องในการสังเคราะห์ catecholamine ในเซลล์เนื้องอก ทำให้สารเมแทบอไลต์ตัวกลาง HVA และ VMA สะสมและขับออกทางปัสสาวะ นี่คือพื้นฐานของการตรวจ catecholamine ในปัสสาวะ
การเพิ่มจำนวน MYCN กระตุ้นวิถี polyamine ซึ่งส่งเสริมการเจริญเติบโตของเนื้องอก3)
MYCN (ปัจจัยการถอดรหัสในตระกูล MYC) → เพิ่มการถอดรหัส ODC1 → เพิ่มการสังเคราะห์ polyamine (ornithine → putrescine → spermidine → spermine) → กระตุ้น eIF5A → กระตุ้น LIN28 → ยับยั้ง Let-7 miRNA → ส่งเสริมการเจริญเติบโตของเนื้องอก
กลุ่มอาการออปโซโคลนัส-ไมโอโคลนัส (OMS ) : เกิดจากแอนติบอดีผิดปกติต่ออาร์เอ็นเอของเซลล์ประสาท ถือเป็นอาการพารานีโอพลาสติกจากปฏิกิริยาข้ามกับเนื้อเยื่อกลไกการมองเห็น บกพร่อง (ไม่มีการกดทับโดยตรง) : ปฏิกิริยาภูมิคุ้มกันต่อ NB ทำปฏิกิริยาข้ามกับเนื้อเยื่อ สารเมแทบอไลต์ที่เป็นพิษจากมะเร็งหรือการหยุดชะงักของการขนส่งตามแอกซอนจากเคมีบำบัดอาจเกี่ยวข้องด้วย
NB บางชนิด (โดยเฉพาะระยะ MS ) มีการถดถอยเอง กลไกที่เชื่อว่าเกี่ยวข้อง ได้แก่ การเพิ่มเมทิลเลชันของดีเอ็นเอใต้เทโลเมียร์ การตายของเซลล์แบบอะพอพโทซิส การขาดปัจจัยการเจริญเติบโตของเส้นประสาท (NGF) และปฏิกิริยาภูมิคุ้มกัน
ลักษณะทางพันธุกรรมในเด็กและผู้ใหญ่แตกต่างกันอย่างมาก1) 5) .
ลักษณะ NB ในเด็ก NB ในผู้ใหญ่ การเพิ่มจำนวนของ MYCN 20-25% พบได้น้อย การแสดงออกของ PHOX2B สูง (ความไวและความจำเพาะสูง) 50% เป็นลบ การกลายพันธุ์ ATRX พบได้น้อย 11% การกลายพันธุ์ของ ALK พบได้น้อย สูงสุด 14% การจัดเรียงใหม่ของ TERT พบได้น้อย 23%
การที่ NB ในผู้ใหญ่ 50% มีผลลบต่อ PHOX2B บ่งชี้ถึงความเป็นไปได้ของสายเซลล์ที่แตกต่าง (เช่น ต้นกำเนิดจากต่อมไทมัส) เมื่อเทียบกับชนิดในเด็ก1) .
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
เมื่อวันที่ 13 ธันวาคม 2023 อย.สหรัฐฯ อนุมัติยาใหม่เป็นยาบำรุงรักษาสำหรับ NB ความเสี่ยงสูง 3) .
Jiang & Yu และคณะ (2024) ได้อธิบายรายละเอียดโปรไฟล์ทางเภสัชวิทยาของ eflornithine โดยรายงานว่าเป็นสารยับยั้งแบบไม่ผันกลับ (suicide inhibitor) ของ ODC (ornithine decarboxylase) ซึ่งกำหนดเป้าหมายวิถีโพลีเอมีนใน NB ที่มีการขยายสัญญาณ MYCN 3) การทดลองระยะที่ 2 (NCT 02395666) ในฐานะการบำบัดบำรุงรักษาหลังการบำบัดด้วยภูมิคุ้มกัน (dinutuximab) เสร็จสมบูรณ์ นำไปสู่การอนุมัติของ อย.
คุณสมบัติของยา:
น้ำหนักโมเลกุล: 182.2 กรัม/โมล
เส้นทางการให้ยา: รับประทาน
ครึ่งชีวิต: ประมาณ 3.5 ชั่วโมง (ขับออกทางไต แทบไม่ถูกเมแทบอลิซึม)
ข้อบ่งใช้: การบำรุงรักษาหลังการรักษาด้วยภูมิคุ้มกันสำหรับนิวโรบลาสโตมาความเสี่ยงสูง
ผลข้างเคียงหลัก: ไข้ การติดเชื้อ อาการแพ้ ไอ เยื่อบุตาอักเสบ พิษต่อตับ การได้ยินลดลง ท้องเสีย คลื่นไส้ อาเจียน3)
การพัฒนาวิธีการรักษาแบบใหม่ที่มุ่งเป้าไปที่สภาพแวดล้อมจุลภาคของเนื้องอกซึ่งเกิดจากการกลายพันธุ์ทางพันธุกรรมกำลังดำเนินอยู่
กลยุทธ์การรักษาเฉพาะบุคคลโดยใช้การวางแผนการบำบัดแบบดิจิทัล (เช่น Oncompass™) กำลังอยู่ระหว่างการศึกษา5) .
Q
ยา eflornithine (IWILFIN) คืออะไร?
A
เป็นยารับประทานที่ได้รับการอนุมัติจาก FDA ในเดือนธันวาคม 2023 สำหรับการบำรุงรักษาหลังการรักษาด้วยภูมิคุ้มกันสำหรับนิวโรบลาสโตมาชนิดความเสี่ยงสูง ยับยั้งเอนไซม์ ODC (ornithine decarboxylase) อย่างถาวร ลดการสังเคราะห์โพลีเอมีน และขัดขวางสัญญาณการเจริญเติบโตของเนื้องอกจากการเพิ่มจำนวนของ MYCN3) สถานะการอนุมัติในญี่ปุ่นต้องยืนยันกับแพทย์ผู้รักษา
Collins K, Ulbright TM, Davis JL. Anterior mediastinal neuroblastoma in an adult: an additional case of a rare tumor in an unusual location with review of the literature. Diagn Pathol. 2023;18:127.
Hu J, Xia B, Yuan X, et al. Neuroblastoma with superficial soft tissue mass as the first symptom: case reports with atypical ultrasonic image and literature review. Braz J Med Biol Res. 2023;56:e12975.
Jiang J, Yu Y. Eflornithine for treatment of high-risk neuroblastoma. Trends Pharmacol Sci. 2024;45(6):577-578.
do Amaral-Silva GK, Leite AA, Mariz BALA, et al. Metastatic neuroblastoma to the mandible of children: report of two cases and critical review of the literature. Head Neck Pathol. 2021;15:757-768.
Telecan T, Andras I, Bungardean MR, et al. Adrenal gland primary neuroblastoma in an adult patient: a case report and literature review. Medicina. 2023;59:33.