神経芽細胞腫(NB)は神経堤由来の小児最多の頭蓋外固形腫瘍であり、小児悪性腫瘍の約10%を占める。
原発部位は副腎・腹部が最多で、11〜56%が眼窩 に転移する。
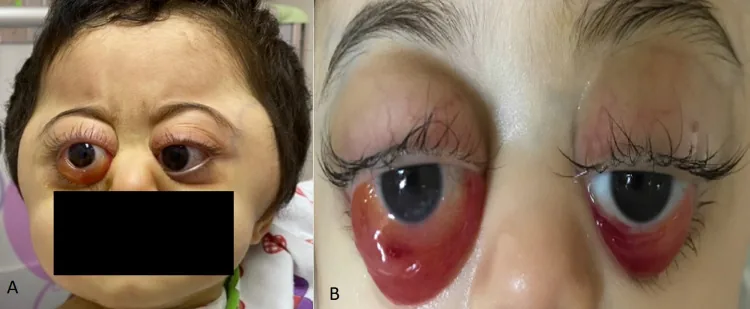
眼窩 転移の特徴的所見は眼窩 周囲皮下出血(raccoon eyes)・眼球突出 ・眼瞼下垂 である。オプソクローヌス・ミオクローヌス症候群 (OMS )の傍腫瘍性徴候として発見されることがある。MIBGシンチグラフィが転移巣の同定に最も有用な画像検査である。
高リスク例では大量化学療法・自家造血幹細胞移植・免疫療法を組み合わせるが、5年全生存率は50%未満である。
眼窩 転移を伴った症例の5年生存率は7.6%と非常に不良である。 神経芽細胞腫(Neuroblastoma; NB)は、神経堤(neural crest)由来の交感神経系前駆細胞から発生する悪性腫瘍である。小児悪性腫瘍の約10%を占め、頭蓋外固形腫瘍としては小児で最多。白血病に次いで多い悪性腫瘍でもある。
原発部位は副腎が約46%、腹部(副腎外)が約18%、後縦隔が約14%、骨盤・その他が約22%を占める4) 。60%以上が副腎や交感神経節などの腹部に発生する。
疫学的特徴 は以下の通りである。
米国で年間約700例が診断される
診断年齢の中央値は19ヶ月。90%が5歳未満で診断される5)
成人での発生は1000万人に1人/年と極めてまれ5)
眼科的には、神経芽細胞腫の11〜56%が眼窩 に転移する。自然退縮から高度転移まで、臨床像は多様である。
歴史的経緯 は以下の通りである。
1864年:Virchowが腹部腫瘍を「神経膠腫」として初報告
1891年:Marchandが副腎髄質・交感神経系由来の特徴を記述
1901年:Pepperが肝転移を伴う乳児例(現在のStage MS 相当)を報告
1910年:Homer Wrightが骨髄中のHomer-Wright型偽ロゼットを記述
Q
神経芽細胞腫はどこに転移しやすいか?
A
骨・骨髄・リンパ節・肝臓・皮膚への転移が多い。眼窩 への転移頻度は11〜56%とされ、眼球突出 や眼窩 周囲皮下出血(raccoon eyes)が初発症状となることがある。
Rahaf A Mandura. Rapidly Progressive Ocular Proptosis as the First Sign of Neuroblastoma in a 16-Month-Old Child: Case Report and Review of Literature. Cureus. 2022 Jan 6; 14(1):e20982. Figure 1. PM
CI D: PMC8817620. License: CC BY.
?????1?????????????????????????????????????????????????????????
保護者や本人が気づく症状は以下の通りである。
眼周囲の腫れ・内出血 :目の周りが青紫色に腫れる(raccoon eyes)眼球突出 眼瞼の腫れ :上下まぶたの浮腫複視 (物が二重に見える)眼球運動障害 による視力 低下全身症状 :腹痛・腹部膨満・骨痛・発熱・倦怠感・下痢・筋力低下
眼窩 転移に伴う眼科所見と、腫瘍による神経学的所見に分けられる。
眼窩・眼周囲所見
眼窩 周囲皮下出血(raccoon eyes)眼窩 転移で最多の所見。腫瘍の出血壊死に由来。虐待と誤認されやすい。
眼球突出 (proptosis)眼窩 内腫瘍塊による前方偏位。
眼瞼・結膜 浮腫 :浮腫が著明になることがある。
眼瞼溢血斑(ecchymosis) :NBと白血病に特徴的な所見。
眼窩 骨の破壊
神経・眼底所見
ホルネル症候群 眼瞼下垂 ・無汗症の三徴。胸部原発腫瘍が交感神経鎖を巻き込む場合に生じる。
虹彩 異色症ホルネル症候群 で認められる。
オプソクローヌス :高頻度(10〜15 Hz)・多方向のサッカード様眼球運動。ミオクローヌスを伴う。
外直筋麻痺・斜視 ・内斜視 :眼球運動障害 による。
うっ血乳頭 ・網膜 出血・視神経萎縮
Q
子どもの目の周りにあざのような内出血があった場合、神経芽細胞腫の可能性はあるか?
A
眼窩 周囲皮下出血(raccoon eyes)は2歳未満の眼窩 転移で最も多い所見であり、外傷歴のない両側性の眼周囲出血では神経芽細胞腫を積極的に疑う必要がある。虐待と誤認されやすいため、鑑別のために腹部超音波・尿中カテコールアミン検査などの全身精査が必要である。
Q
オプソクローヌス・ミオクローヌス症候群とは何か?
A
高頻度(10〜15 Hz)・多方向のサッカード様眼球運動にミオクローヌスを伴う症候群である。神経細胞RNAに対する異常抗体が原因の傍腫瘍性症候と考えられる。OMS 患者の48%に潜在性神経芽細胞腫が存在するとされ、小児のOMS では全身精査が必須である。
大多数は孤発性であり、明確なリスク因子は特定されていない。
遺伝的要因(全体の約1〜2%):
ALK生殖細胞系列変異 :家族性NBの最も多い原因PHOX2B異常 :成熟ニューロンへの分化障害と関連KIF1B異常・MYCN増幅 :家族性NBの一部NBPF10コピー数多型(1p・11q欠失) :高リスクNBとの関連LMO1遺伝子重複 :侵襲性の高いNBのリスク因子NF1 ・Beckwith-Wiedemann症候群との関連
孤発性NBに関連する遺伝子変異:
6p22の遺伝的変異 :孤発性NBとの関連が報告されている
MYCN増幅 は小児NBの20〜25%に認められ、3〜10倍または100〜300倍の二峰性分布を示す。侵襲性の高いNBに強く関連する分子マーカーである5) 。
成人NBの分子生物学的特徴 は小児と異なり、MYCN増幅は稀。ATRX変異(11%)・ALK変異(最大14%)・TERT再構成(23%)が特徴的である5) 。
周産期リスク因子 (後ろ向きコホート研究による):
低月齢乳児:高出生体重・母親の過度な体重増加・妊娠高血圧・高年齢出産
高月齢乳児:低出生体重がリスク増加
高年齢層:第一子・初回帝王切開・遷延分娩・前期破水
母親の薬剤使用(利尿薬・降圧薬)・妊娠中の貧血・一時的染毛剤使用
眼窩 転移に特有のリスク因子は知られていない。
尿中カテコールアミン(HVA・VMA) :以前は90〜95%で上昇と報告されたが、最近の研究では感度はより低い。成人では40〜57%にとどまる(小児95%と対照的)血液検査 :汎血球減少・肝腎機能・電解質・フェリチン・LDH・甲状腺機能骨髄生検 :両側後腸骨稜からの穿刺液・骨芯生検で骨髄浸潤を評価抗体検査 :抗Hu抗体(ANNA-1)が小児NBの診断に有用腰椎穿刺 :CNS転移が判明している場合を除き避けられる(LP後のCNS転移増加の報告あり)
各モダリティの特徴を以下に示す。
検査 特徴 適応 CT 境界明瞭/不明瞭、高吸収値、微小石灰化 初期評価・眼窩 溶骨性変化 MRI T1低信号、T2不均一、頭蓋内進展評価 頭蓋内・眼窩 精査 MIBG(123I) 軟部組織・骨転移の同定に最適 転移の全身評価 PET 高感度・高特異度 診断・治療モニタリング
MIBGシンチグラフィ(123I-MIBG)は軟部組織・骨転移の同定においてPET/CTより優れる。眼窩 転移ではCTで溶骨性変化が認められ、MRIではT1で外眼筋 と等信号・脂肪より低信号、T2で外眼筋 ・脂肪より高信号を示す。眼窩 後外側壁への転移が多い。
Q
神経芽細胞腫の画像診断で最も有用な検査は何か?
A
MIBGシンチグラフィ(123I-MIBG)が軟部組織・骨転移の同定において最も有用であり、PET/CTより優れるとされる。全身の転移巣を一度に評価できるため、初期病期分類と治療効果判定の両方に用いられる。
腫瘍細胞の特徴 :未熟な神経芽細胞(直径10〜15μm)。大きな濃染小胞状核・乏しい嗜酸性細胞質配列パターン :シート状・塊状・索状配列、偽ロゼット(Homer-Wright型)形成免疫組織化学 :synaptophysin陽性・chromogranin陽性・CD56陽性・NSE陽性4) Shimada分類(INPC) :予後良好/不良に分類するための組織学的分類Ki-67増殖指数 :25%以上で3年生存率34%(25%未満では76%)5)
国際神経芽細胞腫リスク分類システム(INRGSS)による病期分類を以下に示す4) 。
L1 :局所腫瘍、画像定義リスク因子(IDRF)なし、1コンパートメント内L2 :局所腫瘍、IDRF1つ以上ありM :遠隔転移(MS を除く)MS
眼窩 転移の鑑別横紋筋肉腫 全身的な鑑別 :嗅神経芽細胞腫・神経節芽細胞腫・褐色細胞腫・Wilms腫瘍・横紋筋肉腫
リスク分類に応じた治療が行われる。
低リスク群:
経過観察 + 外科的切除
5年全生存率:90%以上
高リスク群(Stage M、18ヶ月以上など):
導入化学療法 :cisplatin・cyclophosphamide・doxorubicin・dexrazoxane・etoposide・vincristineの多剤併用4) 外科的切除 :原発巣の摘出(副腎摘出術など)4) 地固め療法 :大量化学療法(BuMel: busulfan + melphalan)+ 自家造血幹細胞移植 + 放射線療法(原発巣20 Gy/10回、残存病変30 Gy/15回)4) 免疫療法 :抗GD2抗体(dinutuximab)5) 維持療法 :13-cis-レチノイン酸(イソトレチノイン)160 mg/m²/日、14日/月、6ヶ月間4)
高リスク群の5年全生存率は50%未満である4) 。
転移性眼窩腫瘍 に対して全摘出が適応となることはほとんどない。化学療法や放射線療法など、原発癌に有効な治療を行う。小児NBで化学療法に反応した場合は生命予後が比較的よい。眼窩 転移を伴った場合の5年生存率は7.6%と非常に不良である。
確立された標準プロトコールはなく、小児プロトコールを適応することが多い5) 。手術(腹腔鏡下含む)+ 化学療法(カルボプラチン+エトポシドなど)が行われる。成人20歳以上の5年全生存率は36.3%と予後不良である5) 。
高リスクNBでは大量化学療法・自家造血幹細胞移植・放射線療法・免疫療法を組み合わせた集学的治療が必要であり、専門施設での治療が不可欠である。
13-cis-レチノイン酸(維持療法)の投与中は催奇形性があるため、生殖可能年齢の患者では厳格な避妊が必要である。
高リスク群の長期生存率は40〜50%にとどまり2) 、治療後も長期的なフォローアップが必要である。
Q
神経芽細胞腫が眼窩に転移した場合の予後はどうなるか?
A
眼窩 転移を伴った神経芽細胞腫の5年生存率は7.6%と非常に不良である。眼窩 への転移は遠隔転移(Stage M相当)を意味することが多く、高リスク群として集学的治療が行われるが、予後改善には限界がある。
NBは交感神経系前駆細胞(交感芽細胞)から発生する。PHOX2B変異により成熟ニューロンへの分化が障害されることで腫瘍化が生じる。ALK変異は増殖低下・未熟交感神経ニューロンの増加と関連する。
カテコールアミン代謝異常 :腫瘍細胞のカテコールアミン合成欠陥により、中間代謝産物であるHVA・VMAが蓄積・尿中排泄される。これが尿中カテコールアミン検査の根拠となる。
MYCN増幅によるポリアミン経路の活性化が腫瘍増殖を促進する3) 。
MYCN(MYCファミリー転写因子)→ ODC1転写亢進 → ポリアミン合成促進(オルニチン → プトレスシン → スペルミジン → スペルミン)→ eIF5A活性化 → LIN28活性化 → Let-7 miRNA抑制 → 腫瘍増殖促進
オプソクローヌス・ミオクローヌス症候群 (OMS )視力 障害の機序(直接圧迫なし)
一部のNB(特にStage MS )では自然退縮が生じる。メカニズムとしてはサブテロメアDNAの過剰メチル化・アポトーシス ・神経成長因子(NGF)欠乏・免疫反応などが関与すると考えられている。
小児と成人では遺伝的特徴が大きく異なる1) 5) 。
特徴 小児NB 成人NB MYCN増幅 20〜25% 稀 PHOX2B発現 高(高感度・高特異度) 50%が陰性 ATRX変異 稀 11% ALK変異 まれ 最大14% TERT再構成 稀 23%
成人NBの50%がPHOX2B陰性であることは、小児型とは異なる細胞系譜(胸腺起源など)の可能性を示唆する1) 。
2023年12月13日、米国FDAが高リスクNBの維持療法として承認した新薬である3) 。
Jiang & Yuら(2024)はエフロルニチンの薬理学的プロファイルを詳述し、ODC(オルニチン脱炭酸酵素)の不可逆的阻害薬(suicide inhibitor)として、MYCN増幅NBにおけるポリアミン経路を標的とすることを報告した3) 。免疫療法(dinutuximab)後の維持療法としてPhase 2試験(NCT 02395666)が完了し、FDA承認に至った。
薬剤特性:
分子量:182.2 g/mol
投与経路:経口
半減期:約3.5時間(腎排泄・ほぼ代謝されない)
適応:高リスクNBの免疫療法後維持療法
主な副作用: 発熱・感染症・アレルギー反応・咳嗽・結膜 充血 ・肝毒性・聴力低下・下痢・悪心・嘔吐3)
遺伝子変異が作り出す腫瘍微小環境を標的とした新規治療法の開発が進んでいる。
デジタルセラピープランニング(OncompassTMなど)を活用した個別化治療戦略の検討が行われている5) 。
Q
エフロルニチン(IWILFIN)とはどのような薬か?
A
高リスク神経芽細胞腫の免疫療法後維持療法として2023年12月にFDA承認された経口薬である。ODC(オルニチン脱炭酸酵素)を不可逆的に阻害することでポリアミン合成を抑制し、MYCN増幅による腫瘍増殖シグナルを遮断する3) 。日本での承認状況については担当医に確認が必要である。
Collins K, Ulbright TM, Davis JL. Anterior mediastinal neuroblastoma in an adult: an additional case of a rare tumor in an unusual location with review of the literature. Diagn Pathol. 2023;18:127. doi:10.1186/s13000-023-01417-6.
Hu J, Xia B, Yuan X, et al. Neuroblastoma with superficial soft tissue mass as the first symptom: case reports with atypical ultrasonic image and literature review. Braz J Med Biol Res. 2023;56:e12975. doi:10.1590/1414-431x2023e12975.
Jiang J, Yu Y. Eflornithine for treatment of high-risk neuroblastoma. Trends in pharmacological sciences. 2024;45(6):577-578. doi:10.1016/j.tips.2024.04.005. PMID:38749882; PMCI D:PMC11162306.
do Amaral-Silva GK, Leite AA, Mariz BALA, et al. Metastatic neuroblastoma to the mandible of children: report of two cases and critical review of the literature. Head Neck Pathol. 2021;15:757-768. doi:10.1007/s12105-020-01277-2.
Telecan T, Andras I, Bungardean MR, et al. Adrenal gland primary neuroblastoma in an adult patient: a case report and literature review. Medicina. 2023;59:33. doi:10.3390/medicina59010033.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください