آستروئیدوزیس زجاجیه (AH)
شکل ذرات: کروی
ترکیب: کلسیم، فسفولیپیدها، موکوپلیساکاریدها
وضعیت زجاجیه: غیرمایع، حفظ حالت ژل
رفتار در حالت سکون: بازگشت به موقعیت اولیه
علائم: معمولاً بدون علامت
زمینه بروز: دژنراسیون وابسته به سن

هیالوزیس ستارهای (Asteroid Hyalosis; AH) یک بیماری دژنراتیو فیبرهای زجاجیه است که معمولاً در افراد مسن بالای 60 سال دیده میشود. تصور میشود اجسام ستارهای (asteroid body; AB) درون فیبرهای کلاژن زجاجیه رسوب کرده و باعث دژنراسیون زجاجیه میشوند. اجسام ستارهای عمدتاً از فسفولیپیدهای حاوی کلسیم، موکوپلیساکارید (یا فسفات کلسیم) تشکیل شده و به صورت ذرات زرد-سفید، کروی و درشت در زجاجیه شناور هستند. با حرکت چشم جابجا میشوند، اما با توقف چشم به جای اولیه برمیگردند.
در سال 1894 توسط آلفرد هیو بنسون برای اولین بار توصیف شد و بعداً لوکزنبرگ و سایم آن را «asteroid hyalosis» نامیدند. این بیماری با سینشیس سینتیلانس (ذوب زجاجیه درخشان) متفاوت است (به بخش تشخیص افتراقی مراجعه کنید).
80% موارد یک طرفه است. شیوع حدود 1-2% است و سه مطالعه بزرگ اپیدمیولوژیک نتایج زیر را گزارش کردهاند:
| مطالعه | شیوع | نکات ویژه |
|---|---|---|
| Beaver Dam Eye Study | 1.2% | 43-54 سال: 0.2% → 75-86 سال: 2.9%. مردان 1.4% در مقابل زنان 0.6%5) |
| مطالعه چشم کوههای آبی | 1.0% | 49-55 سال 0% → 75-97 سال 2.1%6) |
| گروه کالبدشکافی UCLA (10,801 نفر) | 1.96% | تحلیل آسیبشناسی7) |
از نظر جنسیت، مردان (1.4%) بیشتر از زنان (0.6%) مبتلا میشوند و در افراد بالای 60 سال شایعتر است.5)
همراهی با دیابت اغلب مطرح شده است. با این حال، در هیچیک از مطالعات Beaver Dam، Blue Mountains و UCLA ارتباط معنیداری تأیید نشده است.5)6)7) این که اغلب یکطرفه است نیز دلیلی برای تردید در ارتباط با بیماریهای سیستمیک است.
از دیرباز همراهی با دیابت مطرح شده است. با این حال، هر سه مطالعه بزرگ Beaver Dam Eye Study، Blue Mountains Eye Study و گروه کالبدشکافی UCLA ارتباط معنیداری را تأیید نکردهاند.5)6)7) یکطرفه بودن غالب نیز رابطه علّی مستقیم با بیماری سیستمیک را زیر سؤال میبرد.
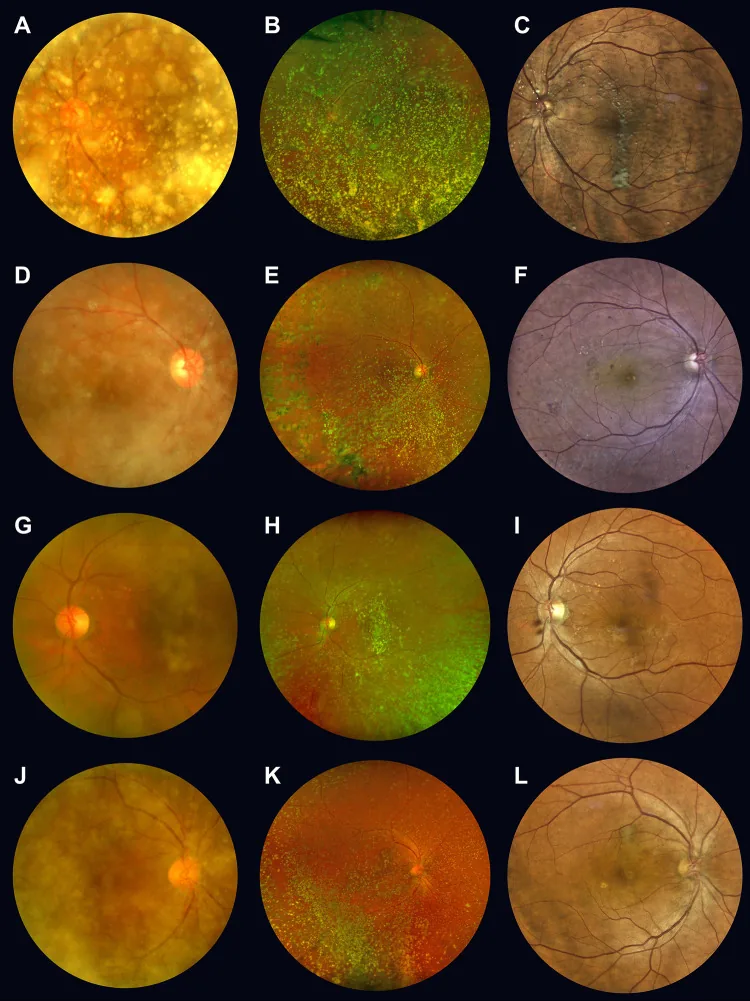
معمولاً بدون علامت است. حتی با کدورت متوسط، بسیاری از بیماران مگسپران را احساس نمیکنند و بینایی خوب است و اغلب نیازی به درمان نیست. حتی با کدورت شدید، بینایی حفظ میشود و حتی در موارد شدید که مشاهده فوندوس دشوار است، بینایی خوب باقی میماند و درمان اغلب ضروری نیست.
به ندرت، به دنبال ایجاد جداشدگی خلفی زجاجیه (PVD)، کاهش حاد بینایی رخ میدهد. مکانیسم آن به این صورت است که اجسام ستارهای در زجاجیه قدامی متمرکز شده و تراکم کدورت در نزدیکی نقطه گرهی (nodal point) چشم افزایش یافته و محور بینایی را مسدود میکند. 3)
در سری 6 چشم از Marlow و همکاران، همه موارد کاهش بینایی حاد یا تحت حاد داشتند. میانگین بهترین دید اصلاحشده (BCVA) قبل از عمل 20/150 (محدوده 20/25 تا 20/2500) بود و میانگین کاهش به دنبال پیشرفت جداشدگی خلفی زجاجیه 0.70 logMAR بود. 3)
بررسی زجاجیه قدامی با میکروسکوپ اسلیت لامپ ضروری است. از بیمار خواسته میشود چشم را حرکت دهد تا حرکت زجاجیه مشاهده شود. در میکروسکوپ اسلیت لامپ، ذرات درشت، کروی و زرد-سفید شناور در زجاجیه دیده میشود.
این ذرات با حرکت چشم جابجا میشوند اما پس از توقف، به موقعیت اولیه بازمیگردند. این پدیده به دلیل عدم مایعشدگی زجاجیه است و اجسام ستارهای به الیاف زجاجیه چسبیده و حرکت را دنبال میکنند. اجسام ستارهای ذرات درشتی هستند و به راحتی از گلبولهای سفید قابل تشخیص هستند.
اغلب مایعشدگی زجاجیه رخ نمیدهد و در بسیاری از موارد جداشدگی خلفی زجاجیه وجود ندارد. چسبندگی قوی به شبکیه باعث میشود جداشدگی خلفی زجاجیه به ندرت ایجاد شود. در صورت بروز جداشدگی خلفی زجاجیه در چشمهای مبتلا به آستروئید هیالوزیس، به دلیل چسبندگی غیرطبیعی زجاجیه-شبکیه، احتمال وتروشیز (vitreoschisis) زیاد است. 3)
در سری Marlow و همکاران، از 6 چشم، 3 چشم جداشدگی کامل خلفی زجاجیه و 3 چشم جداشدگی نسبی (وتروشیز) داشتند. 3)
نکات مهم در کدورت شدید: در موارد رتینوپاتی دیابتی پرولیفراتیو، فتوکوآگولاسیون شبکیه اغلب دشوار است و جراحی زجاجیه نیز ممکن است با دشواری همراه باشد.
معمولاً بدون علامت است، اما به دنبال ایجاد جداشدگی خلفی زجاجیه (PVD) ممکن است کاهش حاد بینایی رخ دهد. دلیل آن تمرکز اجسام ستارهای در زجاجیه قدامی و مسدود شدن محور بینایی است. 3) در گزارش Marlow و همکاران، گروهی که میانگین دید قبل از عمل 20/150 داشتند، پس از ویترکتومی (PPV) ظرف 3 ماه به دید پایه بازگشتند. 3)
افزایش سن بزرگترین عامل خطر است. معمولاً در افراد مسن بالای 60 سال دیده میشود. همچنین ارتباط با عوامل زیر گزارش شده است.
مشاهده زجاجیه قدامی با میکروسکوپ اسلیت لامپ ضروری است. با حرکت دادن چشم بیمار و مشاهده حرکت زجاجیه میتوان تشخیص داد. مشاهده کدورتهای کروی زرد-سفید مشخص در زجاجیه که با حرکت چشم جابجا شده و در حالت استراحت به جای اولیه بازمیگردند، کلید تشخیص است. این ذرات بزرگ از کریستالهای کلسیم هستند و تشخیص نسبتاً آسان است.
ویژگیهای هر آزمایش در زیر آورده شده است.
| روش آزمایش | ویژگی | موقعیتهای مفید |
|---|---|---|
| OCT | تأثیر کم AH (طول موج 830 نانومتر) | ارزیابی سطح مشترک زجاجیه-شبکیه |
| FA | قابل عکسبرداری حتی در حضور AH | موارد همراه با رتینوپاتی دیابتی |
| اولتراسوند B-mode | عدم وجود نقص اکوی خلفی، کانون پراکو | هنگامی که فوندوس قابل مشاهده نیست |
مهمترین تشخیص افتراقی، تمایز از سینکیزیس سینتیلانس (ذوب زجاجیه درخشان) است.
آستروئیدوزیس زجاجیه (AH)
شکل ذرات: کروی
ترکیب: کلسیم، فسفولیپیدها، موکوپلیساکاریدها
وضعیت زجاجیه: غیرمایع، حفظ حالت ژل
رفتار در حالت سکون: بازگشت به موقعیت اولیه
علائم: معمولاً بدون علامت
زمینه بروز: دژنراسیون وابسته به سن
سندرم زجاجیه درخشان (SS)
شکل ذرات: کریستالهای مسطح و نوکتیز (با درخشش طلایی)
ترکیب: کریستالهای کلسترول
وضعیت زجاجیه: مایع شدن (دژنراسیون زجاجیه)
رفتار در حالت سکون: تهنشینی به سمت پایین
علائم: مستعد ایجاد مگسپران
زمینه بروز: پس از ضربه، التهاب، نزدیکبینی شدید
سایر تشخیصهای افتراقی شامل آمیلوئیدوز زجاجیه، خونریزی زجاجیه، التهاب زجاجیه (یووئیت) و لنفوم داخل چشمی است.
در هیالوزیس ستارهای متراکم، دید فوندوس ممکن است دشوار شود. با این حال، میتوان با کمک آزمایشهای کمکی مانند OCT (طول موج 830 نانومتر)، آنژیوگرافی فلورسئین (FA)، خودفلورسانس فوندوس (FAF) و سونوگرافی B-mode اطلاعات فوندوس را به دست آورد. آزمایش FA همچنین برای تشخیص رتینوپاتی دیابتی همراه با هیالوزیس ستارهای مفید است.
معمولاً بیماران از مگسپران (floaters) شکایتی ندارند و بینایی خوب است، بنابراین در بسیاری از موارد نیازی به درمان نیست. حتی اگر کدورت شدید باشد، اغلب بینایی حفظ میشود و به ندرت نیاز به جراحی پیدا میشود.
روند درمان به شرح زیر است:
در صورت ایجاد اختلال بینایی، جراحی اندیکاسیون دارد. اگر کدورت شدید باشد و باعث کاهش بینایی شود، ویترکتومی انجام میشود. در موارد کاهش حاد بینایی ناشی از جداشدگی خلفی زجاجیه، ویترکتومی میتواند به طور درمانی بینایی را بازگرداند. 3)
اندیکاسیونها و نتایج ویترکتومی
اندیکاسیون: کدورت شدید همراه با اختلال بینایی
روش جراحی: ویترکتومی ترانس کونژنکتیوال با گِیج 23 یا 25 3)
روند بهبود بینایی: یک ماه پس از جراحی، دو چشم به بینایی پایه بازگشتند و در سه ماهگی همه چشمها بهبود یافتند 3)
بهترین corrected visual acuity نهایی: میانگین 20/35 (محدوده 20/20 تا 20/200) 3)
عوارض پس از جراحی: گزارشی نشده است3)
نکات احتیاطی در جراحی آب مروارید
خطای اندازهگیری طول محوری و انکسار: ممکن است خطا در اندازهگیری مقادیر انکساری یا طول محوری رخ دهد که در جراحی آب مروارید نیاز به احتیاط دارد
جابجایی به اتاق قدامی (حین عمل): عارضه نادر حرکت اجسام ستارهای به اتاق قدامی در حین دستکاری I/A1)
جابجایی به اتاق قدامی (دیررس پس از عمل): ممکن است به دلیل برگشت زلالیه مانند گلوکوم بدخیم نیز رخ دهد2)
روش درمان: قابل برداشتن با آسپیراسیون I/A و شستشوی اتاق قدامی1)2)
در جراحی زجاجیه چشمهای مبتلا به AH، به دلیل اینکه مایعشدن زجاجیه به ندرت رخ میدهد و چسبندگی بین قشر خلفی زجاجیه و شبکیه به طور پاتولوژیک قوی است، دستکاری دقیق ضروری است. در صورت همراهی با رتینوپاتی دیابتی پرولیفراتیو، انعقاد نوری شبکیه دشوار شده و دشواری جراحی زجاجیه نیز افزایش مییابد.
Saeed و همکاران یک مورد از مرد 70 ساله را گزارش کردند که در حین جراحی آب مروارید (هنگام دستکاری I/A) یک جسم کروی زرد-سفید به اتاق قدامی جابجا شد. بدون پارگی کپسول یا آسیب زونول. با I/A آسپیره و خارج شد و IOL در داخل کپسول قرار داده شد. دید پس از عمل 20/20 بود و پس از 4 سال نیز خوب باقی ماند.1)
Desai و همکاران یک مرد 70 ساله را گزارش کردند که دو ماه پس از جراحی آب مروارید، توده کریستالی زرد در اتاق قدامی، IOP 35 میلیمتر جیوه و اتاق قدامی کم عمق داشت. به عنوان جابجایی AH به اتاق قدامی ناشی از گلوکوم بدخیم تشخیص داده شد. شستشوی اتاق قدامی + بیوپسی زجاجیه + ایریدکتومی-زونولکتومی-ویترکتومی انجام شد و روز بعد IOP به 17 میلیمتر جیوه بهبود یافت. این نشان میدهد که حتی بدون نقص کپسول خلفی یا ضعف زونول، برگشت زلالیه میتواند باعث جابجایی AH به اتاق قدامی شود.2)
از آنجایی که جراحی زجاجیه اجسام ستارهای را همراه با زجاجیه خارج میکند، عود پس از جراحی گزارش نشده است. در تمام 6 چشم از گزارش Marlow و همکاران، دید پایه ظرف 3 ماه پس از جراحی بازگشت و هیچ عارضهای مشاهده نشد.3)
تصور میشود که اجسام ستارهای (asteroid body) درون فیبرهای کلاژن زجاجیه رسوب کرده و باعث تخریب زجاجیه میشوند. اجزای اصلی آن فسفولیپیدهای حاوی کلسیم، موکوپلیساکاریدها (یا فسفات کلسیم) هستند. رسوب در فیبرهای کلاژن زجاجیه پاتولوژی زمینهای است و اگرچه ارتباط با دیابت مطرح شده، اما در مطالعات اپیدمیولوژیک بزرگ رد شده است. 5)6)7)
تصویربرداری طیفسنجی الکترونی توزیع یکنواخت Ca، P و O را نشان میدهد که از نظر ساختاری و عنصری مشابه هیدروکسیآپاتیت است. در میکروسکوپ ایمونوفلورسانس، کندرویتین-۶-سولفات در اطراف اجسام ستارهای شناسایی شده و با نشانگذاری لکتین-طلا، کربوهیدراتهای اختصاصی هیالورونیک اسید به عنوان بخشی از ماتریکس داخلی تأیید شده است. تصور میشود که پروتئوگلیکانها و زنجیرههای جانبی گلیکوزآمینوگلیکان (GAG) در تنظیم فرآیند زیستمعدنیشدن (biomineralization) نقش دارند. 8)
زجاجیه اغلب مایع نشده و چسبندگی محکمی به شبکیه دارد، بنابراین جداشدگی خلفی زجاجیه به ندرت رخ میدهد. اما هنگامی که جداشدگی خلفی زجاجیه رخ میدهد، به دلیل چسبندگی غیرطبیعی زجاجیه-شبکیه، احتمال جداشدگی غیرطبیعی خلفی زجاجیه همراه با ویترئوشیز (vitreoschisis) (جدایی قشر زجاجیه) زیاد است. 3)
در ۳ چشم از ۶ چشم مورد مطالعه مارلو (Marlow) و همکاران، جداشدگی نسبی خلفی زجاجیه (ویترئوشیز) تأیید شد. هنگامی که ویترئوشیز رخ میدهد، زجاجیه قدامی حاوی اجسام ستارهای در نزدیکی نقطه گرهی چشم متمرکز شده و اختلال بینایی آشکار میشود. 3)
در آنالیز پاتولوژیک توپیلو (Topilow) و همکاران، در ۸۱٪ از چشمهای مبتلا به AH، ژل زجاجیه از نظر میکروسکوپی طبیعی بود و در ۱۹٪ مایعشدگی متوسط (سینرزیس) مشاهده شد. 1)
جابجایی AH به اتاق قدامی حین عمل جراحی به دلیل مایعشدگی زجاجیه (سینرزیس) و حرکت قدامی اجسام ستارهای از طریق فضاهای کوچک زونولهای Zinn در نظر گرفته میشود. 1) مکانیسم دیگر برای جابجایی قدامی دیررس پس از عمل، برگشت مایع زلالیه ناشی از گلوکوم بدخیم است. 2) نکته مهم این است که جابجایی AH به اتاق قدامی حتی در غیاب نقص کپسول خلفی یا ضعف زونولها نیز ممکن است رخ دهد. 1)2)
OCT با منبع جاروب (SS-OCT، طول موج مرکزی 1050 نانومتر) در مقایسه با SD-OCT معمولی (840 نانومتر) نفوذ بیشتری دارد و ممکن است به ارزیابی دقیق زجاجیه، مشیمیه و شبکیه در چشمهای مبتلا به آستروئید هیالوزیس کمک کند. انتظار میرود که این روش کمتر تحت تأثیر پراکندگی نور ناشی از اجسام ستارهای قرار گیرد و کاربرد آن در پایش رتینوپاتی دیابتی همراه با آستروئید هیالوزیس و بیماریهای ماکولا در حال بررسی است.
بیومتری با منبع جاروب (مانند IOLMaster 700) از طول موج 1050 نانومتر استفاده میکند، بنابراین میتواند دقت اندازهگیری طول محوری را در چشمهای مبتلا به آستروئید هیالوزیس بهبود بخشد. در بیومتری نوری معمولی، تداخل ناشی از اجسام ستارهای میتواند باعث خطا در طول محوری شود، اما با افزایش طول موج و بهبود پردازش سیگنال، انتظار میرود نرخ موفقیت اندازهگیری افزایش یابد. این روش به عنوان گزینهای برای معاینات دقیق قبل از عمل در بیماران مبتلا به آستروئید هیالوزیس که کاندید جراحی آب مروارید هستند، مورد توجه قرار گرفته است.
آنزیمهای حلکننده زجاجیه مانند اوکریپلاسمین (میکروپلاسمین) برای سندرم کشش زجاجیه-ماکولا و سوراخ ماکولا تأیید شدهاند، اما اندیکاسیون آنها برای آستروئید هیالوزیس ثابت نشده است. از آنجایی که در آستروئید هیالوزیس زجاجیه حالت غیرمایع دارد، اثربخشی و ایمنی رویکرد دارویی در حال حاضر نامشخص است و تحقیقات بیشتری لازم است.