ภาวะแอสเทอรอยด์ไฮอาโลซิส (AH)
รูปร่างอนุภาค: ทรงกลม
ส่วนประกอบ: แคลเซียม ฟอสโฟลิพิด มิวโคโพลีแซ็กคาไรด์
สภาพวุ้นตา: ไม่เหลว ยังคงสภาพเจล
พฤติกรรมเมื่ออยู่นิ่ง: กลับสู่ตำแหน่งเดิม
อาการ: ปกติไม่มีอาการ
ภูมิหลังการเกิด: เสื่อมตามอายุ

โรควุ้นตาดาว (Asteroid Hyalosis; AH) เป็นโรคเสื่อมของเส้นใยวุ้นตาที่มักพบในผู้สูงอายุที่มีอายุมากกว่า 60 ปี เชื่อว่าร่างแหดาว (asteroid body; AB) จะสะสมอยู่ในเส้นใยคอลลาเจนของวุ้นตา ทำให้เกิดการเสื่อมของวุ้นตา ร่างแหดาวประกอบด้วยฟอสโฟลิพิดที่มีแคลเซียมและมิวโคโพลีแซ็กคาไรด์ (หรือแคลเซียมฟอสเฟต) เป็นหลัก เป็นอนุภาคหยาบสีขาวอมเหลืองทรงกลมลอยอยู่ในวุ้นตา มีการเคลื่อนไหวตามการเคลื่อนที่ของลูกตา แต่เมื่อหยุดนิ่งจะกลับสู่ตำแหน่งเดิม
ได้รับการบรรยายครั้งแรกโดย Alfred Hugh Benson ในปี ค.ศ. 1894 และต่อมา Luxenberg และ Sime ได้ตั้งชื่อว่า “asteroid hyalosis” เป็นโรคอิสระที่แตกต่างจากโรควุ้นตาละลายเป็นประกาย (synchysis scintillans) (ดูหัวข้อ การวินิจฉัยแยกโรค)
80% เป็นข้างเดียว ความชุกประมาณ 1-2% และการศึกษาเชิงระบาดวิทยาขนาดใหญ่สามรายงานผลดังนี้
| การศึกษา | ความชุก | ข้อสังเกตพิเศษ |
|---|---|---|
| Beaver Dam Eye Study | 1.2% | 43-54 ปี 0.2% → 75-86 ปี 2.9% เพศชาย 1.4% เทียบกับเพศหญิง 0.6%5) |
| การศึกษา Blue Mountains Eye Study | 1.0% | 49-55 ปี 0% → 75-97 ปี 2.1%6) |
| กลุ่มตัวอย่างชันสูตร UCLA (10,801 คน) | 1.96% | การวิเคราะห์ทางพยาธิวิทยา7) |
ความแตกต่างทางเพศ: ผู้ชาย (1.4%) มากกว่าผู้หญิง (0.6%) และพบบ่อยในผู้สูงอายุที่มีอายุมากกว่า 60 ปี5)
มักมีการกล่าวถึงความสัมพันธ์กับโรคเบาหวาน อย่างไรก็ตาม ไม่พบความสัมพันธ์ที่มีนัยสำคัญในการศึกษา Beaver Dam, Blue Mountains หรือ UCLA5)6)7) การที่โรคนี้มักเป็นข้างเดียวก็เป็นหลักฐานที่ทำให้เกิดข้อสงสัยเกี่ยวกับความสัมพันธ์กับโรคทางระบบ
มีการกล่าวถึงความสัมพันธ์กับโรคเบาหวานมานานแล้ว อย่างไรก็ตาม การศึกษาขนาดใหญ่ทั้งสาม (Beaver Dam Eye Study, Blue Mountains Eye Study และกลุ่มตัวอย่างชันสูตร UCLA) ไม่พบความสัมพันธ์ที่มีนัยสำคัญ5)6)7) การที่โรคนี้มักเป็นข้างเดียวยังทำให้เกิดข้อสงสัยเกี่ยวกับความสัมพันธ์เชิงสาเหตุโดยตรงกับโรคทางระบบ
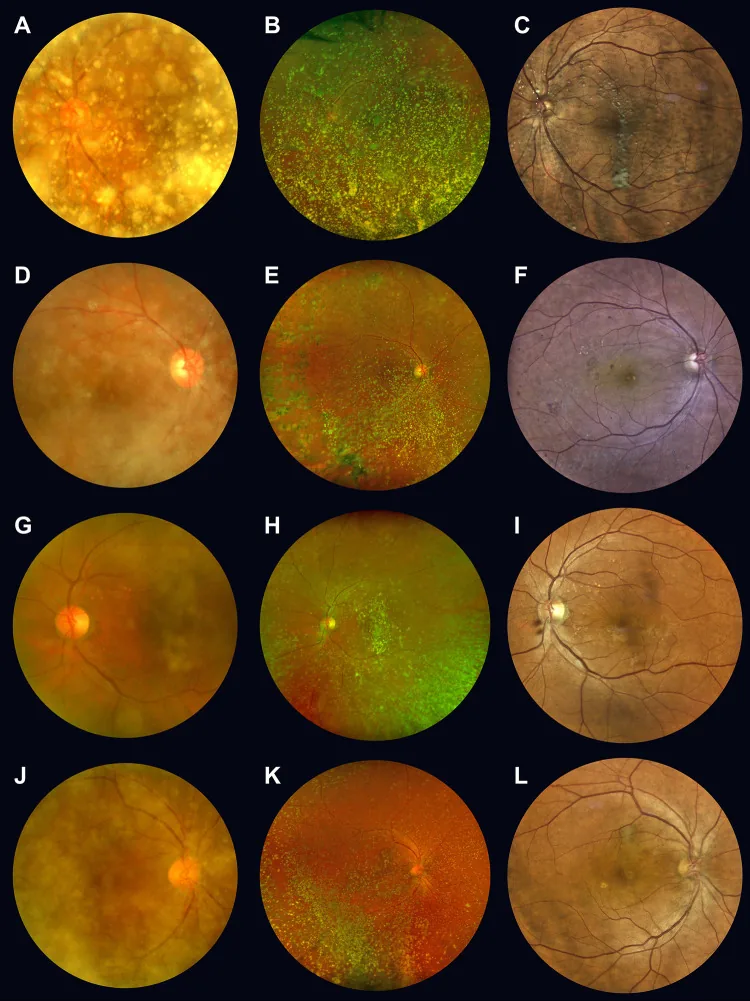
โดยปกติไม่มีอาการ แม้มีความขุ่นปานกลาง ผู้ป่วยมักไม่รู้สึกถึงจุดลอย การมองเห็นดีและไม่จำเป็นต้องรักษา แม้มีความขุ่นรุนแรง การมองเห็นมักยังคงดี ซึ่งเป็นลักษณะเฉพาะ แม้โรคแก้วตาเสื่อมชนิดสเตียรอยด์รุนแรงที่ทำให้การตรวจจอประสาทตาทำได้ยาก ก็มักมีการมองเห็นดีและไม่จำเป็นต้องรักษา
ไม่ค่อยเกิดการมองเห็นลดลงเฉียบพลันจากการเกิดภาวะ Posterior Vitreous Detachment (PVD) กลไกคือ asteroid ไปรวมตัวกันในน้ำวุ้นตาส่วนหน้า ทำให้ความหนาแน่นของความขุ่นใกล้จุด nodal point ของตาเพิ่มขึ้นและขัดขวางแนวแกนการมองเห็น 3)
ในชุดการศึกษา 6 ตาของ Marlow และคณะ ทุกรายมีการมองเห็นลดลงแบบเฉียบพลันหรือกึ่งเฉียบพลัน ค่าเฉลี่ยของ Best Corrected Visual Acuity (BCVA) ก่อนผ่าตัดคือ 20/150 (ช่วง 20/25 ถึง 20/2500) และค่าเฉลี่ยการลดลงที่สัมพันธ์กับการดำเนินของ PVD คือ 0.70 logMAR 3)
การตรวจน้ำวุ้นตาส่วนหน้าด้วยกล้อง Slit Lamp เป็นสิ่งจำเป็น ให้ผู้ป่วยขยับตาเพื่อสังเกตการเคลื่อนไหวของน้ำวุ้นตา กล้อง Slit Lamp จะพบอนุภาคหยาบทรงกลมสีขาวเหลืองลอยอยู่ในน้ำวุ้นตา
อนุภาคเหล่านี้เคลื่อนที่ตามการเคลื่อนไหวของตา แต่จะกลับสู่ตำแหน่งเดิมเมื่ออยู่นิ่ง เนื่องจากน้ำวุ้นตาไม่เหลว และ asteroid ยังคงยึดติดกับเส้นใยน้ำวุ้นตาและเคลื่อนตามไป Asteroid มีขนาดใหญ่และแยกแยะจากเม็ดเลือดขาวได้ง่าย
มักไม่เกิดการเหลวของน้ำวุ้นตา และผู้ป่วยส่วนใหญ่ไม่มี PVD มีการยึดเกาะแน่นกับจอประสาทตาทำให้ PVD เกิดขึ้นได้ยาก เมื่อเกิด PVD ในตาที่มี Asteroid Hyalosis มักมี Vitreoschisis ร่วมด้วยเนื่องจากการยึดเกาะระหว่างน้ำวุ้นตาและจอประสาทตาที่ผิดปกติ 3)
ในชุดของ Marlow และคณะ พบ PVD สมบูรณ์ใน 3 จาก 6 ตา และ PVD บางส่วน (Vitreoschisis) ใน 3 ตา 3)
ข้อควรระวังในกรณีขุ่นมาก: ในผู้ป่วยเบาหวานขึ้นจอประสาทตาระยะ proliferative การจี้แสงจอประสาทตามักทำได้ยาก และการผ่าตัดน้ำวุ้นตาก็อาจมีความท้าทาย
อายุที่มากขึ้นเป็นปัจจัยเสี่ยงที่สำคัญที่สุด มักพบในผู้สูงอายุที่อายุมากกว่า 60 ปี นอกจากนี้ยังมีรายงานความสัมพันธ์กับปัจจัยต่อไปนี้
การตรวจวุ้นตาส่วนหน้าด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp) เป็นสิ่งจำเป็น การวินิจฉัยสามารถทำได้โดยสังเกตการเคลื่อนไหวของวุ้นตาเมื่อผู้ป่วยขยับตา การพบความขุ่นรูปทรงกลมสีเหลืองขาวลักษณะเฉพาะในวุ้นตา ซึ่งเคลื่อนที่ตามการเคลื่อนไหวของลูกตาและกลับสู่ตำแหน่งเดิมเมื่ออยู่นิ่ง เป็นกุญแจสำคัญในการวินิจฉัย อนุภาคขนาดใหญ่ที่มาจากผลึกแคลเซียมทำให้การวินิจฉัยค่อนข้างง่าย
ลักษณะเฉพาะของการตรวจแต่ละวิธีแสดงไว้ด้านล่าง
| วิธีการตรวจ | ลักษณะเฉพาะ | สถานการณ์ที่เป็นประโยชน์ |
|---|---|---|
| OCT | ผลกระทบจาก AH น้อย (ความยาวคลื่น 830 นาโนเมตร) | การประเมินรอยต่อระหว่างวุ้นตาและจอประสาทตา |
| การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA) | สามารถถ่ายภาพได้แม้มี AH | กรณีที่มีจอประสาทตาเสื่อมจากเบาหวานร่วม |
| อัลตราซาวนด์ B-mode | จุดสะท้อนเสียงสูงโดยไม่มีข้อบกพร่องของเสียงสะท้อนด้านหลัง | เมื่อไม่สามารถมองเห็นจอตาได้ |
การวินิจฉัยแยกโรคที่สำคัญที่สุดคือการแยกจากภาวะซินคิซิส ซินทิลแลนส์ (synchysis scintillans)
ภาวะแอสเทอรอยด์ไฮอาโลซิส (AH)
รูปร่างอนุภาค: ทรงกลม
ส่วนประกอบ: แคลเซียม ฟอสโฟลิพิด มิวโคโพลีแซ็กคาไรด์
สภาพวุ้นตา: ไม่เหลว ยังคงสภาพเจล
พฤติกรรมเมื่ออยู่นิ่ง: กลับสู่ตำแหน่งเดิม
อาการ: ปกติไม่มีอาการ
ภูมิหลังการเกิด: เสื่อมตามอายุ
โรควุ้นตาพร่าประกาย (SS)
รูปร่างอนุภาค: ผลึกแบนและแหลม (ประกายทอง)
ส่วนประกอบ: ผลึกคอเลสเตอรอล
สภาพวุ้นตา: เหลว (วุ้นตาเสื่อม)
พฤติกรรมเมื่ออยู่นิ่ง: ตกตะกอนลงด้านล่าง
อาการ: มักรู้สึกเห็นจุดลอย
ภูมิหลังการเกิด: หลังการบาดเจ็บ อักเสบ หรือสายตาสั้นมาก
โรคอื่นที่ต้องวินิจฉัยแยกโรค ได้แก่ โรคอะไมลอยโดซิสในวุ้นตา เลือดออกในวุ้นตา วุ้นตาอักเสบ (ยูเวียอักเสบ) และมะเร็งต่อมน้ำเหลืองในลูกตา
ในกรณี AH ที่หนาแน่น การมองเห็นอวัยวะภายในตาอาจทำได้ยาก อย่างไรก็ตาม สามารถรับข้อมูลอวัยวะภายในตาได้ด้วยการตรวจเสริม เช่น OCT (ความยาวคลื่น 830 นาโนเมตร) การตรวจหลอดเลือดด้วยฟลูออเรสซีน (FA) การเรืองแสงเองของอวัยวะภายในตา (FAF) และอัลตราซาวนด์โหมดบี การตรวจ FA ยังมีประโยชน์ในการวินิจฉัยจอประสาทตาเสื่อมจากเบาหวานที่ร่วมกับ AH
โดยปกติผู้ป่วยไม่รู้สึกถึงอาการจุดลอยและสายตาดี จึงไม่จำเป็นต้องรักษา แม้จะมีขุ่นมัวรุนแรง สายตามักยังคงดี และไม่ค่อยต้องผ่าตัด
ขั้นตอนการรักษามีดังนี้:
การผ่าตัดมีข้อบ่งชี้เมื่อมีสายตาเสีย หากขุ่นมัวรุนแรงทำให้สายตาเสีย ให้ทำการผ่าตัดวุ้นตา ในกรณีที่สายตาลดลงเฉียบพลันจากการหลุดลอกของวุ้นตาส่วนหลัง การผ่าตัดวุ้นตาสามารถฟื้นฟูสายตาได้อย่างหายขาด 3)
ข้อบ่งชี้และผลลัพธ์ของการผ่าตัดวุ้นตา
ข้อบ่งชี้: ขุ่นมัวรุนแรงทำให้สายตาเสีย
วิธีการผ่าตัด: ผ่าตัดวุ้นตาผ่านเยื่อบุตา 23G หรือ 25G 3)
ระยะฟื้นฟูสายตา: สองตาฟื้นสายตาพื้นฐานใน 1 เดือน ทุกตาฟื้นใน 3 เดือน 3)
ค่าสายตาที่ดีที่สุดที่แก้ไขแล้วสุดท้าย: เฉลี่ย 20/35 (ช่วง 20/20 ถึง 20/200) 3)
ภาวะแทรกซ้อนหลังผ่าตัด: ไม่มีรายงาน3)
ข้อควรระวังในการผ่าตัดต้อกระจก
ความคลาดเคลื่อนในการวัดความยาวแกนตาและค่าสายตา: อาจเกิดความคลาดเคลื่อนในการวัดค่าสายตาหรือความยาวแกนตา ต้องระมัดระวังในการผ่าตัดต้อกระจก
การเคลื่อนเข้าสู่ช่องหน้าม่านตา (ระหว่างผ่าตัด): ภาวะแทรกซ้อนที่พบได้น้อยซึ่งร่างแหผลึกดาวเคลื่อนเข้าสู่ช่องหน้าม่านตาระหว่างการทำ I/A1)
การเคลื่อนเข้าสู่ช่องหน้าม่านตา (หลังผ่าตัดระยะปลาย): อาจเกิดจากการไหลย้อนกลับของอารมณ์ขันน้ำ เช่น ในโรคต้อหินชนิดร้าย2)
การจัดการ: สามารถกำจัดออกได้โดยการดูดด้วย I/A และล้างช่องหน้าม่านตา1)2)
ในการผ่าตัดวุ้นตาในตาที่มีภาวะแอสเทอรอยด์ไฮยาโลซิส การกลายเป็นของเหลวของวุ้นตาเกิดขึ้นได้น้อย และการยึดเกาะระหว่างคอร์เทกซ์วุ้นตาส่วนหลังกับจอประสาทตามีความแข็งแรงผิดปกติทางพยาธิวิทยา จึงต้องระมัดระวังในการจัดการ หากมีโรคจอประสาทตาเหตุเบาหวานชนิดเพิ่มจำนวนร่วมด้วย การจี้แสงจอประสาทตาจะทำได้ยาก และความยากของการผ่าตัดวุ้นตาก็เพิ่มขึ้น
Saeed และคณะรายงานผู้ป่วยชายอายุ 70 ปี ซึ่งก้อนกลมสีเหลืองขาวเคลื่อนเข้าสู่ช่องหน้าม่านตาระหว่างการผ่าตัดต้อกระจก (ขณะทำ I/A) ไม่มีการฉีกขาดของแคปซูลหรือความเสียหายของโซนูล ก้อนถูกดูดและกำจัดออกด้วย I/A และใส่เลนส์แก้วตาเทียมในถุงแคปซูล หลังผ่าตัดสายตา 20/20 และยังดีอยู่หลังจาก 4 ปี1)
Desai และคณะรายงานผู้ป่วยชายอายุ 70 ปี ซึ่งมีก้อนผลึกสีเหลืองในช่องหน้าม่านตา ความดันลูกตา 35 มม.ปรอท และช่องหน้าม่านตาตื้น 2 เดือนหลังผ่าตัดต้อกระจก วินิจฉัยว่าเป็นแอสเทอรอยด์ไฮยาโลซิสเคลื่อนเข้าสู่ช่องหน้าม่านตาจากต้อหินชนิดร้าย ทำการล้างช่องหน้าม่านตา + ตรวจชิ้นเนื้อวุ้นตา + ตัดม่านตา-โซนูล-วุ้นตา และความดันลูกตาดีขึ้นเป็น 17 มม.ปรอทในวันถัดไป กรณีนี้แสดงให้เห็นว่าแม้ไม่มีข้อบกพร่องของแคปซูลหลังหรือความอ่อนแอของโซนูล การเคลื่อนของแอสเทอรอยด์ไฮยาโลซิสเข้าสู่ช่องหน้าม่านตาสามารถเกิดขึ้นได้จากการไหลย้อนกลับของอารมณ์ขันน้ำ2)
เนื่องจากการผ่าตัดวุ้นตากำจัดร่างแหผลึกดาวพร้อมกับวุ้นตา จึงไม่มีรายงานการกลับเป็นซ้ำหลังผ่าตัด ใน 6 ตาทั้งหมดในรายงานของ Marlow และคณะ สายตาพื้นฐานฟื้นตัวภายใน 3 เดือนหลังผ่าตัด และไม่พบภาวะแทรกซ้อน3)
เชื่อกันว่าแอสเทอรอยด์บอดี้ (asteroid body) จะสะสมตัวอยู่ในเส้นใยคอลลาเจนของวุ้นตา ทำให้เกิดการเสื่อมของวุ้นตา องค์ประกอบหลักคือฟอสโฟลิพิดที่มีแคลเซียม มิวโคโพลีแซ็กคาไรด์ (หรือแคลเซียมฟอสเฟต) การสะสมบนเส้นใยคอลลาเจนของวุ้นตาเป็นพยาธิสภาพพื้นฐาน และแม้ว่าจะมีความเกี่ยวข้องกับโรคเบาหวาน แต่การศึกษาเชิงระบาดวิทยาขนาดใหญ่ก็ปฏิเสธความสัมพันธ์นี้ 5)6)7)
การถ่ายภาพด้วยอิเล็กตรอนสเปกโทรสโกปีแสดงการกระจายตัวสม่ำเสมอของ Ca, P และ O ซึ่งบ่งชี้ถึงความคล้ายคลึงทางโครงสร้างและองค์ประกอบกับไฮดรอกซีอะพาไทต์ กล้องจุลทรรศน์อิมมูโนฟลูออเรสเซนต์ตรวจพบคอนดรอยติน-6-ซัลเฟตรอบๆ แอสเทอรอยด์บอดี้ และการติดฉลากเลคติน-ทองคำยืนยันว่าคาร์โบไฮเดรตจำเพาะของกรดไฮยาลูโรนิกเป็นส่วนหนึ่งของเมทริกซ์ภายใน เชื่อกันว่าโปรตีโอไกลแคนและสายข้างไกลโคซามิโนไกลแคน (GAG) มีส่วนเกี่ยวข้องในการควบคุมกระบวนการไบโอมิเนอรัลไลเซชัน (biomineralization) 8)
วุ้นตามักไม่เหลว และการยึดเกาะกับจอประสาทตาแน่นมาก ทำให้ PVD เกิดขึ้นได้ยาก อย่างไรก็ตาม เมื่อเกิด PVD ขึ้น การยึดเกาะระหว่างวุ้นตาและจอประสาทตาที่ผิดปกติจะนำไปสู่ PVD ที่ผิดปกติร่วมกับภาวะวุ้นตาฉีกขาด (vitreoschisis) 3)
ใน 3 ใน 6 ตาในการศึกษาของ Marlow และคณะ พบ PVD บางส่วน (vitreoschisis) เมื่อเกิด vitreoschisis วุ้นตาส่วนหน้าที่มีแอสเทอรอยด์บอดี้จะรวมตัวกันใกล้จุดนอดของตา ทำให้เกิดความบกพร่องทางการมองเห็นอย่างชัดเจน 3)
ในการวิเคราะห์ทางพยาธิวิทยาโดย Topilow และคณะ วุ้นตาเจลปกติภายใต้กล้องจุลทรรศน์ใน 81% ของตา AH และพบการเหลวในระดับปานกลาง (syneresis) ใน 19% 1)
การเคลื่อนย้าย AH ไปยังช่องหน้าม่านตาระหว่างการผ่าตัดเชื่อว่าเกิดจากการเหลวของวุ้นตา (syneresis) และการเคลื่อนที่ไปข้างหน้าของแอสเทอรอยด์บอดี้ผ่านช่องว่างเล็กๆ ในเส้นใยซินน์ (zonules) 1) การเคลื่อนที่ไปข้างหน้าที่เกิดขึ้นช้าหลังผ่าตัดอาจเกิดจากกลไกอื่นคือการไหลย้อนกลับของอารมณ์ขันน้ำเนื่องจากต้อหินชนิดร้าย 2) สิ่งสำคัญคือการเคลื่อนย้าย AH ไปยังช่องหน้าม่านตาสามารถเกิดขึ้นได้แม้ไม่มีข้อบกพร่องของแคปซูลหลังหรือความอ่อนแอของเส้นใยซินน์ 1)2)
OCT แบบ Swept-source (SS-OCT, ความยาวคลื่นศูนย์กลาง 1050 นาโนเมตร) มีความลึกทะลุทะลวงสูงกว่าเมื่อเทียบกับ SD-OCT ทั่วไป (840 นาโนเมตร) และอาจมีส่วนช่วยในการประเมินรายละเอียดของวุ้นตา คอรอยด์ และจอประสาทตาในดวงตาที่มีภาวะแอสเทอรอยด์ไฮยาโลซิส คาดว่ามีคุณสมบัติที่ไวต่อการกระเจิงแสงจากร่างแหแอสเทอรอยด์น้อยกว่า และกำลังศึกษาการประยุกต์ใช้ในการติดตามเบาหวานขึ้นจอประสาทตาร่วมกับแอสเทอรอยด์ไฮยาโลซิสและโรคจุดรับภาพ
การวัดทางชีวภาพแบบ Swept-source (เช่น IOLMaster 700) ใช้ความยาวคลื่น 1050 นาโนเมตร จึงสามารถปรับปรุงความแม่นยำในการวัดความยาวแกนในดวงตาที่มีภาวะแอสเทอรอยด์ไฮยาโลซิส ในการวัดทางชีวภาพด้วยแสงแบบดั้งเดิม การรบกวนจากร่างแหแอสเทอรอยด์อาจทำให้เกิดความคลาดเคลื่อนของความยาวแกน แต่ด้วยความยาวคลื่นที่ยาวขึ้นและการปรับปรุงการประมวลผลสัญญาณ คาดว่าอัตราความสำเร็จในการวัดจะเพิ่มขึ้น ซึ่งเป็นทางเลือกที่น่าสนใจสำหรับการตรวจก่อนผ่าตัดที่มีความแม่นยำในผู้ป่วยแอสเทอรอยด์ไฮยาโลซิสที่วางแผนจะผ่าตัดต้อกระจก
เอนไซม์ละลายวุ้นตา เช่น ocriplasmin (microplasmin) ได้รับการอนุมัติสำหรับกลุ่มอาการดึงรั้งวุ้นตาจุดรับภาพและรูที่จุดรับภาพ แต่ยังไม่มีการกำหนดข้อบ่งชี้สำหรับแอสเทอรอยด์ไฮยาโลซิส เนื่องจากวุ้นตาในแอสเทอรอยด์ไฮยาโลซิสไม่กลายเป็นของเหลว ประสิทธิภาพและความปลอดภัยของวิธีการใช้ยายังไม่ทราบในปัจจุบัน และจำเป็นต้องมีการวิจัยเพิ่มเติม