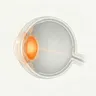
マルファン症候群はFBN1遺伝子変異による常染色体優性遺伝 性結合組織疾患で、発生率は5,000人に1人である。
眼異常はマルファン症候群患者の約80%に発生し、水晶体 異位(ectopia lentis )が最も代表的な眼所見である。
水晶体 亜脱臼は上方・外上方への偏位が多く、瞳孔ブロック 緑内障 の原因となる。白内障 の発症率は一般人口と同程度だが、発症年齢が10〜20年早い傾向がある1) 。チン小帯 の脆弱性により、白内障 手術の難度が高く専門的技術を要する1) 。心血管合併症(大動脈拡張・解離)が生命予後を左右するため、全身管理が必須である。
診断は「改訂ゲント基準」に基づき、眼科・循環器科・整形外科などの多科連携が重要である。
マルファン症候群(Marfan syndrome)は、FBN1遺伝子の変異によって引き起こされる常染色体優性遺伝 性結合組織疾患である。骨形成不全症に次いで2番目に多い遺伝性結合組織疾患であり、世界での発生率は約5,000人に1人と推定される。
男女差はなく、あらゆる人種で発症する。患者の約75%は変異した遺伝子を親から受け継ぐが、約25%は孤発性変異(de novo変異)によるものである。常染色体優性遺伝 のため、患者が子に変異を伝える確率は50%となる。
FBN1遺伝子は第15染色体(15q21.1)に位置し、フィブリリン1(fibrillin-1)タンパク質をコードする。フィブリリン1は微細線維(microfibrils)の主要構成成分であり、チン小帯 (zonular fibers)・大動脈・皮膚・骨格系など全身の結合組織に分布する。変異により結合組織全体の構造的脆弱性が生じる。
1896年にアントワーヌ・マルファンがパリ医学会で初めて正式報告した疾患であり、指定難病に指定されている。
Q
家族にマルファン症候群の人がいない場合、子供は発症しないか?
A
約25%は孤発性変異によって発症するため、家族歴がなくても発症する可能性がある。発症した場合、その子どもへの遺伝確率は50%となる。定期的な遺伝カウンセリング が推奨される。
マルファン症候群は骨格系・心血管系・眼系に影響する多系統疾患であり、眼科領域での主な自覚症状は以下の通りである。
視力 低下・視野のぼやけ水晶体 亜脱臼による屈折 異常、白内障 形成、または緑内障 による視神経 障害に由来する。高度近視 :眼軸長 の延長に伴い、幼少期から強度近視 が生じやすい。単眼複視 ・ゆがみ :水晶体 が瞳孔 をまたぐ位置にある場合、有水晶体 部と無水晶体 部の両方から光が入ることで二重視が生じる。急激な視力 低下 :網膜剥離 の発症時に生じる。眼圧 上昇に伴う症状水晶体 脱臼による瞳孔ブロック 緑内障 では、頭痛・眼痛 ・霧視 が出現することがある。
全身症状として、高身長、クモ状指(蜘蛛指症)、側弯症、漏斗胸、関節過可動性、大動脈拡張・解離が認められる。
眼の異常はマルファン症候群患者の約80%に発生する。最も多い所見は水晶体 異位(ectopia lentis )であり、マルファン症候群患者の50〜80%に認められる。
水晶体偏位
偏位方向 :上方・外上方(上耳側)への偏位が最多。理論的にはあらゆる方向に偏位しうる。
チン小帯 所見虹彩 震顫(iridodonesis)・水晶体 震顫(phacodonesis)を認める。
球状水晶体 水晶体 形状異常を伴う場合がある。
縮瞳時の注意 :縮瞳していると偏位が分かりにくく、散瞳 後に再確認する。
その他の眼所見
高度近視 ・乱視 :眼軸長 延長に伴う軸性近視 が主体。ゲント基準でも≧3Dの近視 は診断スコアに含まれる。
散瞳 不良・小瞳孔 瞳孔 散大筋の発育不全による。
扁平角膜 角膜 曲率の低下を認める。
強膜 菲薄化
網膜剥離 眼軸 延長・硝子体 液化・末梢網膜 変性を基盤とする。水晶体 異位がある場合は8〜38%に網膜剥離 を合併する1) 。
水晶体 が瞳孔 内または前房 内に完全脱臼すると、瞳孔ブロック 緑内障 (pupillary block glaucoma)を引き起こす。また、白内障 はマルファン症候群患者に合併することが多いが、一般人口と比較して発症率が高いわけではなく、発症年齢が10〜20年早い点が特徴的である1) 。40歳未満での白内障 発症例も報告されている1) 。
Q
水晶体がずれていることに自分で気づけるか?
A
軽度の亜脱臼では自覚症状が乏しいことが多い。瞳孔 を水晶体 縁がまたぐ位置まで偏位が進むと複視 が生じる。マルファン症候群患者は定期的な眼科検査で水晶体 位置を確認することが重要である。
マルファン症候群の主な原因はFBN1遺伝子変異であり、フィブリリン1の機能不全によって結合組織全体が脆弱化する1) 。フィブリリン1はチン小帯 (水晶体 を支持する線維)の主要構成成分であり、その欠損が水晶体 異位や眼軸 延長をもたらす1) 。
また、FBN1変異はTGF-β(トランスフォーミング増殖因子β)シグナルの過活性化を引き起こし、細胞外マトリックスの異常なリモデリングを生じる。このTGF-β亢進が大動脈壁の脆弱化や眼軸 の異常延長に関与すると考えられている1) 。
さらに、異常な細胞外マトリックスリモデリングは房水 動態を乱し、眼圧 上昇・緑内障 リスクを高める1) 。
家族歴 :常染色体優性遺伝 のため、患者の子どもへの発症リスクは50%孤発性変異 :約25%は新規変異であり、家族歴がなくても発症しうる変異部位 :FBN1遺伝子内の変異位置が眼症状・全身症状の程度に影響する表現型多様性 :同じ家族内でも症状の程度が異なることがある(多面発現・表現型多様性)
マルファン症候群と診断された場合、眼科・循環器科・整形外科を含む定期検査を継続してください。
眼科検査は最低でも年1回受けてください。水晶体 位置・眼圧 ・眼底の変化を定期的に確認することが重要です。
視力 の急な変化(飛蚊症 の増加・視野の欠け)は網膜剥離 の可能性があります。速やかに眼科を受診してください。激しいコンタクトスポーツや頭部に衝撃を受ける活動は、水晶体 脱臼や網膜剥離 のリスクがあるため注意が必要です。
マルファン症候群の診断は「改訂ゲント基準(Revised Ghent Nosology)」に基づく。主要診断基準として以下を含む。
大動脈バルサルバ洞拡張(Zスコア≧2)
水晶体 異位(ectopia lentis )FBN1遺伝子変異の確認
全身スコア(骨格・皮膚・硬膜所見など)≧7点
水晶体 異位が存在し、かつマルファン症候群の家族歴陽性、または大動脈径のZスコア≧2があれば確定診断となる。
細隙灯顕微鏡検査 (散瞳 下)水晶体偏位 の方向・程度、虹彩 震顫・水晶体 震顫、球状水晶体 を確認する。縮瞳下では偏位の確認が困難なため、散瞳検査 が必須である。屈折 検査水晶体 部・無水晶体 部それぞれの自然瞳孔 下での光学条件を確認する。眼圧測定 緑内障 合併の有無を確認する。水晶体偏位 の程度・方向によって眼圧 変動がある。眼底検査 ・眼底写真網膜 変性・網膜剥離 の早期発見のため定期的に施行する。眼軸長 測定近視 の程度を把握する。
ホモシスチン尿症 水晶体偏位 の方向が下内側である点でマルファン症候群と異なる。知的障害・痙攣・血栓塞栓症を合併する。マルファン様体型だが関節過可動性はない。ワイル・マルケサニ症候群 MS T10変異による。小球状水晶体 が特徴的で、前方脱臼・瞳孔ブロック 緑内障 のリスクが高い。短指・低身長を呈する(マルファン症候群とは対照的な体型)。ロイス・ディーツ症候群 :TGF-β関連遺伝子変異による。水晶体 異位は稀で、頭蓋縫合早期癒合・口蓋裂など頭蓋顔面異常が特徴的。B3GAT 3関連疾患 :B3GAT 3遺伝子変異によるリンケロパチーで、マルファン症候群と誤診されることがある。クモ状指・大動脈基部拡張を呈するが、FBN1変異を認めない2) 。
Q
診断に遺伝子検査は必ず必要か?
A
FBN1遺伝子変異が確認されなくても、臨床所見が改訂ゲント基準を満たせばマルファン症候群と臨床診断できる。ただし、遺伝子検査は確定診断・家族への遺伝カウンセリング ・鑑別診断(B3GAT 3関連疾患など)に有用である。
水晶体 異位の管理:視力 が維持されている場合は、眼鏡またはコンタクトレンズによる屈折 矯正で経過観察する。自然瞳孔 下で有水晶体 部・無水晶体 部いずれを使用しているかを確認し、光学条件に適した矯正を行う。
水晶体 摘出術の適応は以下の通りである(Nemetらの基準)。
水晶体 縁が瞳孔 を二分し光学的矯正が不可能な場合硝子体 腔内への水晶体 脱臼二次性緑内障 を伴う前方転位
白内障 形成による視覚障害
白内障 手術:白内障 手術がマルファン症候群に対する主要な外科的介入である1) 。チン小帯 の脆弱性により、通常の白内障 手術と比較して難度が高い1) 。フェムト秒レーザー支援白内障 手術(femtosecond laser-assisted cataract surgery)は、精度の高い前囊切開・核破砕が可能であり、マルファン症候群患者における有望な治療アプローチとして報告されている1) 。チン小帯 支持器具(カプセルテンションリング、強膜 縫合固定など)を組み合わせた手術も施行されている1) 。
緑内障 の管理:
薬物療法(β遮断薬 点眼、炭酸脱水酵素阻害薬 など)による眼圧 コントロール
瞳孔ブロック 緑内障 には周辺虹彩 切除または水晶体 摘出が有効隅角 異常が高度な例では線維柱帯切開術 ・濾過手術 を要する
網膜剥離 の管理:網膜剥離 に対しては、強膜 バックリング ・硝子体 切除術・シリコンオイル充填などを組み合わせた外科的治療が行われる1) 。対側眼への予防的レーザー治療 が考慮される場合がある。
小児患者の管理:
弱視 の予防のため、水晶体 亜脱臼による屈折 異常・不同視 を早期に矯正する。感受性期間内に視力 育成を促す治療を優先する。
大動脈の監視 :マルファン症候群と診断後は少なくとも年1回の心エコー検査を施行する。大動脈径が急速に変化する場合や手術閾値(成人で4.5cm超)に達した場合は、より頻回の検査が必要である。βブロッカー :大動脈基部拡張の進行予防のため、禁忌がなければ小児・成人とも投与する。大動脈手術 :大動脈瘤・解離に対して外科的修復が行われる。
チン小帯 脆弱例では、白内障 手術中の核落下 ・硝子体 脱出のリスクが高い。必ずマルファン症候群診療経験のある専門施設での手術を受けることが重要である。硝子体手術 の既往・強度近視 例ではさらにチン小帯 脆弱が進むため、白内障 手術前に慎重なリスク評価が必要である。眼内レンズ 計算に影響する眼軸長 の測定は、マルファン症候群患者では眼軸 が長い場合があるため精度の高い検査機器を使用する。
Q
水晶体を摘出した後に眼内レンズ(眼内レンズ)を入れられるか?
A
水晶体偏位 が軽度でチン小帯 が保たれている場合は眼内レンズ 挿入が可能だが、チン小帯 が高度に脆弱な場合は水晶体 摘出のみとなることもある。強膜 縫合固定眼内レンズ などの特殊な眼内レンズ 固定法が選択される場合がある。術前に詳細な検査と医師との十分な相談が必要である。
フィブリリン1(fibrillin-1)は、微細線維の主要構成タンパク質であり、弾性線維の骨格を形成する。眼においては、フィブリリン1はチン小帯 の構成成分として水晶体 を支持する1) 。
FBN1変異が生じると、以下の経路で眼・全身の病態が生じる。
チン小帯 の弱体化チン小帯 の微細線維構造が脆弱化し、水晶体 を正常位置に保てなくなる(水晶体 亜脱臼・脱臼)1) 。TGF-βシグナル亢進 :正常なフィブリリン1は微細線維に結合したTGF-βの活性化を抑制する。変異によりこの抑制が失われ、TGF-βシグナルが過活性化する。この過活性化が眼軸 延長・大動脈壁脆弱化・異常な組織リモデリングをもたらす1) 。房水 動態の乱れ房水 の流出路が障害され、眼圧 上昇・緑内障 リスクが高まる1) 。非色素毛様体 上皮の関与 :眼においてフィブリリン1は非色素毛様体 上皮細胞によって産生される。Fbn1の非色素毛様体 上皮細胞に特異的なノックアウト実験ではチン小帯 に著明な影響が生じ、水晶体 異位・白内障 が発生することが示されている1) 。
Li ら(2022)が報告したB3GAT 3関連疾患の症例では、新生児期よりクモ状指・大動脈基部拡張を認めマルファン症候群が疑われたが、全エクソーム解析でFBN1変異が検出されず、B3GAT 3変異が同定された2) 。マルファン症候群と臨床的に類似する疾患が他にも存在するため、分子診断が確定診断に重要である。
マルファン症候群における変異の位置はFBN1遺伝子内で多岐にわたり、変異の部位と種類が眼症状・全身症状の重症度に関与すると考えられている。新生児マルファン症候群はFBN1遺伝子のエクソン24〜32(新生児領域)の変異と関連し、特に重篤な経過をとり、2歳未満での死亡率が高い2) 。
マルファン症候群の根本的病態であるTGF-β過活性化を標的とした薬物療法の研究が進んでいる。動物モデルにおいて、ロサルタン(アンジオテンシンII受容体拮抗薬)がTGF-βシグナルを抑制し大動脈拡張を軽減することが報告されている。ヒトでの臨床試験も実施されているが、現時点での標準治療はβブロッカーである。
マルファン症候群患者のチン小帯 脆弱例に対するフェムト秒レーザー白内障手術 の適用が積極的に研究されている1) 。カプセルテンションリングとの組み合わせにより、良好な視力 転帰が得られた症例が複数報告されている1) 。ただし、標準化されたプロトコールの確立は今後の課題である。
FBN1遺伝子の根本的修正を目指した遺伝子治療 の基礎研究が行われているが、臨床応用には至っていない。
Adji AS, et al. Ocular complications in Marfan syndrome: A systematic review of case series. Romanian Medical Journal. 2025;72(1):73-81.
Li Y, Zhang C, Zhang H, Feng W, Wang Q, Fan R. Severe phenotypes of B3GAT 3-related disorder caused by two heterozygous variants: a case report and literature review. BMC medical genomics. 2022;15(1):27. doi:10.1186/s12920-022-01160-9. PMID:35151321; PMCI D:PMC8841085.
Coelho SG, Almeida AG. Marfan syndrome revisited: From genetics to the clinic. Rev Port Cardiol (Engl Ed). 2020;39(4):215-226. PMID: 32439107.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください