部分斷離
視力:可能保留一定的視功能。
OCT所見:可見視神經盤深部空洞。RNFL變薄(有報告顳側46μm、上顳側91μm、上鼻側60μm)1)。
病程:神經膠質增生覆蓋離斷空洞。1個月後神經膠質增生變得明顯1)。
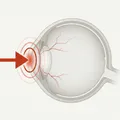
視神經撕脫傷(optic nerve avulsion; ONA)是指外傷導致視神經在篩板水平與眼球分離的病理狀態。也稱為視乳頭撕脫(optic nerve head avulsion),指同一病變。不伴有視神經硬膜鞘或鄰近鞏膜的破裂1)。
視神經撕脫傷中,視神經硬膜的連續性得以保持,而視神經纖維在結構薄弱的篩板無髓鞘部位斷裂。optic nerve evulsion和optic nerve avulsion指同一病變,但詞源上有所區別。
視神經撕脫傷是外傷性視神經病變(traumatic optic neuropathy; TON)的一種類型,屬於前部外傷性視神經病變1)。外傷性視神經病變總體佔頭部外傷的0.5%~5%5),視神經撕脫傷是其中罕見的病變2)。範圍從部分離斷到完全離斷,對視功能的影響可能是毀滅性的1)。
離斷的好發部位為視乳頭(最多)、眼眶尖部和視交叉三處1)。原因以交通事故最多,此外還有運動外傷、跌倒、鬥毆等。Buchwald等人的統合分析顯示,小的鈍性物體或手指佔原因的49%1)。特別是當手指進入眼眶時,施加強大的旋轉外力,容易發生視神經撕脫傷。在拳擊、交通事故或運動相關的鈍性眼外傷中,被視為罕見的嚴重外傷。
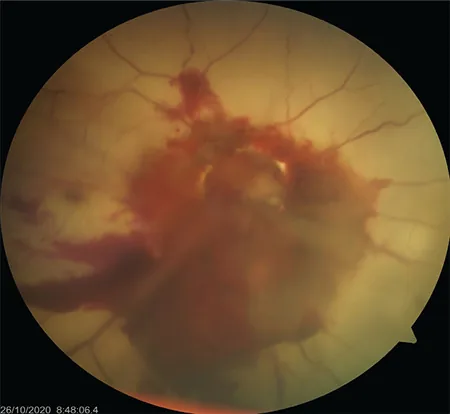
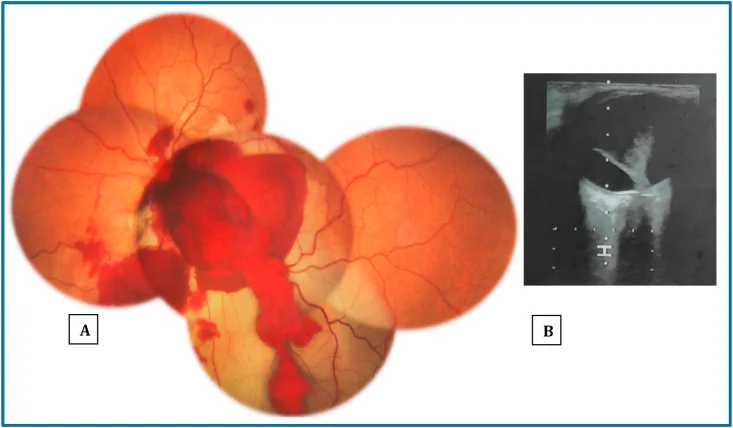
醫師確認的主要所見如下所示。
部分斷離
視力:可能保留一定的視功能。
OCT所見:可見視神經盤深部空洞。RNFL變薄(有報告顳側46μm、上顳側91μm、上鼻側60μm)1)。
病程:神經膠質增生覆蓋離斷空洞。1個月後神經膠質增生變得明顯1)。
完全離斷
視力:無光感(NLP)。
眼底:視神經回縮至硬膜鞘內,形成深部空洞。
預後:視功能恢復幾乎無望。結構性損傷不可逆4)。
OCT所見的時序變化:傷後2週起GCC(神經節細胞複合體)厚度變薄並低於正常範圍。之後約30~50天趨於穩定。螢光眼底攝影可能顯示靜脈分支阻塞和微血管重塑1)。
B型超音波檢查有用。可檢測為與離斷部位相對應的低回音區1)。CT和MRI也可輔助使用。詳見「診斷與檢查方法」一節。
各項影像檢查的特性如下所示。
| 檢查 | 主要用途 | 注意事項 |
|---|---|---|
| CT(薄層) | 骨折、視乳頭斷裂的檢測 | 必須採用0.75~1mm薄層掃描 |
| MRI(STIR/DWI) | 視神經腫脹、斷裂的檢測 | 有金屬異物時禁忌 |
| B型超音波 | 玻璃體出血病例的診斷 | 非侵入性、可快速執行 |
視神經撕脫傷尚無有效的治療方法。早期診斷並避免不必要的治療最為重要。高劑量靜脈注射類固醇未顯示有益,反而有風險 1)。對於篩板處物理性斷裂這一不可逆的結構改變,目前可用的醫療干預無法修復損傷。原則是在正確診斷下避免不必要的侵入性治療,努力維持殘留的視功能。
對於包括撕脫傷以外類型的外傷性視神經病變,考慮以下治療。
Fukumasa 等(2024)對一名因視神經管骨折導致外傷性視神經病變的10歲男童,在傷後6小時行視神經管開放術,術後給予潑尼松龍25 mg/kg/日。術前手動視力在12天後改善至20/30,並在9個月後維持5)。兒童外傷性視神經病變中約80%報告視力改善。
Tachibana 等(2024)對一名70歲男性外傷性視神經病變患者,在甲潑尼龍1 g/日脈衝治療後行內視鏡視神經減壓術。VA從0.2改善至0.8(6個月後)7)。
合併黃斑下出血時:SF6氣體+rtPA 25 μg/0.1 mL玻璃體內注射的氣體移位可能有效。有報告稱透過保持俯臥位3天成功將出血從黃斑下移位1)。
視神經撕脫傷的主要發病機制分為間接損傷和直接損傷。關於鈍性外傷相關的發病機制有多種假說,但無論哪種,均認為在結構脆弱的篩板處視神經無髓神經纖維斷裂,隨後神經纖維在神經鞘內向後方移動。
LSCI(Laser Speckle Contrast Imaging)是一種無創定量評估外傷性視神經病變中視盤血流的技術。
Jallow等人(2025)在一例15歲男性直接型後部外傷性視神經病變患者中,使用LSCI檢測到峰值BFVi(血流速度指數)下降:健眼20.5 a.u.,患眼13.4 a.u.(3週後)9)。6個月後差異仍持續(健眼15.1 a.u.,患眼13.7 a.u.)。其在急性外傷評估中的應用潛力值得關注。
擴散張量成像(DTI)可以量化視神經的微結構變化,可能有助於預測預後4)。
這是一種使用ImageJ巨集對Goldmann視野計進行定量的方法,可以縱向追蹤等敏感線面積的變化7)。已應用於評估外傷性視神經病變的視野變化。
紅血球生成素、腦源性神經營養因子(BDNF)和幹細胞療法等實驗性方法有望用於未來的神經修復4)。
Bayram-Suverza M, Rosano-Barragán M, Ramírez-Estudillo JA. Long-term follow-up of a patient with partial optic nerve avulsion associated with submacular hemorrhage who underwent pneumatic displacement. Am J Ophthalmol Case Rep. 2024;35:102083.
Omari A, Carniciu AL, Desai M, et al. Globe dislocation and optic nerve avulsion following all-terrain vehicle accidents. Am J Ophthalmol Case Rep. 2022;27:101621.
Tenewitz JE, Chen EJ, Cartwright MJ. A rare presentation of direct traumatic optic neuropathy in a patient poked in the eye by an antenna. Cureus. 2021;13(9):e18244.
Naik SN, Nayak DV. Unravelling the unseen: a case series exploring the enigmas of traumatic optic neuropathy. Cureus. 2024;16(12):e75546.
Fukumasa H, Yamaga Y, Miyaoka R, et al. Successful combination therapy of optic canal decompression and steroid administration for traumatic optic neuropathy in a 10-year-old boy. Cureus. 2024;16(9):e70124.
Okui T, Sakamoto T, Morikura I, et al. Feasibility of navigation-assisted endoscopic transnasal optic nerve decompression for the treatment of traumatic optic neuropathy in patients with midfacial fractures. J Korean Assoc Oral Maxillofac Surg. 2024;50:273-284.
Tachibana M, Kanno J, Hashimoto M, et al. Quantification of Goldmann visual fields during resolution of traumatic optic neuropathy. Case Rep Ophthalmol Med. 2024;2024:5560696.
Mehta A, Rathod R, Ahuja C, et al. Hemorrhage in Onodi cell leading to traumatic optic neuropathy. Craniomaxillofac Trauma Reconstr. 2021;14(1):70-73.
Jallow MA, Gholap RS, Asanad S, et al. Laser speckle contrast imaging detects relative blood flow reduction in traumatic optic neuropathy. Am J Ophthalmol Case Rep. 2025;38:102326.