Purtscher斑點
形狀:多邊形、邊界清晰的白濁。
位置:位於小動脈和小靜脈之間的視網膜內層。見於視網膜動脈周圍。
邊界:距血管50μm以內有清晰的邊界。典型的表現為血管周圍視網膜免於白濁(perivascular sparing)。
頻率:約63%的病例可見。
病理生理:毛細血管床的毛細血管前小動脈閉塞導致內層白濁。
1910年,Otmar Purtscher首次報導了一名從樹上墜落導致頭部外傷的中年患者。這是一種罕見疾病,是與外傷相關的視網膜血管閉塞性疾病。它被歸類為遠達性外傷性視網膜病變,由眼外創傷(如頭、頸、胸部挫傷)引起。
與全身性疾病、球後麻醉等手術操作、急性胰臟炎、血栓性血小板減少性紫斑症、腎衰竭或結締組織病相關的類似疾病被區分為Purtscher樣視網膜病變。兩者的眼底表現相同,病理生理相似。
估計發生率為0.24人/百萬人/年,可能存在漏報4)6)。約60%為雙眼,偶有單眼病例。由急性胰臟炎引起時幾乎均為雙眼。病變局限於後極部(視乳頭周圍和黃斑區)佔83-92%。外傷是最常見原因,其次是急性胰臟炎。
Purtscher樣視網膜病變的病因多種多樣。除了急性胰臟炎、腎衰竭、膠原病、妊娠高血壓症候群/HELLP症候群、脂肪栓塞症候群、Valsalva動作、溶血性尿毒症症候群、嬰兒搖晃症候群、球後麻醉、類固醇注射等之外,近年來也有因COVID-19感染1)9)、高血壓急症2)、填充物注射3)、缺血性結腸炎4)、疫苗接種5)和C3腎小球病8)引起的病例報告。
由頭部外傷、胸部壓迫、長骨骨折等外傷引起的病例稱為Purtscher視網膜病變。由急性胰臟炎或腎衰竭等不伴外傷的全身性疾病引起的病例稱為Purtscher樣視網膜病變。兩者的眼底表現相同,治療方針也相同。
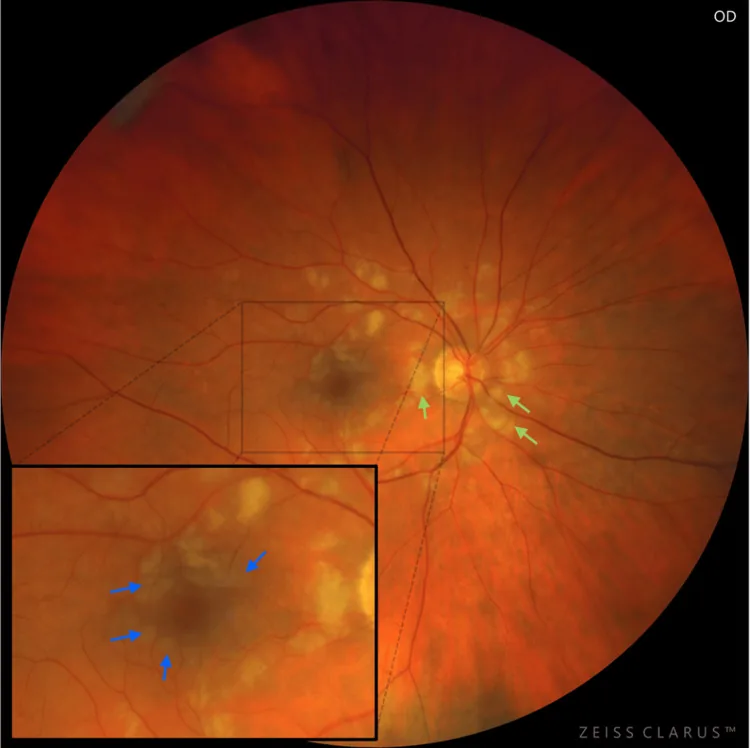
視力障礙在外傷或相關疾病發作後數小時至數天延遲出現。視力障礙的程度從非常輕微到手邊手動不等。也可能伴有視野缺損,表現為中心暗點、旁中心暗點或弓狀暗點。
侷限於後極部(視乳頭周圍與黃斑區域)的所見具有特徵性。
Purtscher斑點
形狀:多邊形、邊界清晰的白濁。
位置:位於小動脈和小靜脈之間的視網膜內層。見於視網膜動脈周圍。
邊界:距血管50μm以內有清晰的邊界。典型的表現為血管周圍視網膜免於白濁(perivascular sparing)。
頻率:約63%的病例可見。
病理生理:毛細血管床的毛細血管前小動脈閉塞導致內層白濁。
軟性滲出(棉絮斑)
形狀:邊界不清的蓬鬆白色斑塊。
位置:神經纖維層(NFL)內的局部梗塞。多見於視盤周圍。
邊界:不清且不規則。
頻率:最常見的表現,93%的病例可見。
病理生理:由NFL內的微梗塞引起。
根據病變範圍分為A、B、C三個區域。三分之二的病例僅涉及A區,C區受累罕見。
| 區域 | 病變範圍 |
|---|---|
| A | 視神經乳頭周圍(乳頭直徑4倍範圍內) |
| B | 後極部(至赤道前) |
| C | 包括周邊部的廣泛範圍 |
發病2個月後的追蹤中,報告如下:眼底正常40%、視神經萎縮64%、RPE虎斑狀變化23%、視網膜變薄14%、視網膜動脈狹窄4%。有時會殘留視神經萎縮和視網膜萎縮。
視力下降通常不是在外傷或全身疾病發病後立即出現,而是在數小時至數天的延遲後發生。無眼痛。如果外傷後視力逐漸變差,需要考慮本病。
Purtscher視網膜病變(外傷性)
頭部外傷:最古老已知的原因。交通事故、墜落、毆打等。
胸部壓迫:因強烈壓迫性外傷導致胸腔內壓急劇升高。擠壓症候群、重物導致的胸部擠壓傷。
長管骨骨折:可能因脂肪栓塞症候群而發病。
Purtscher樣視網膜病變(非外傷性)
急性胰臟炎:最常見的非外傷原因。幾乎均為雙眼性。
腎衰竭 / C3腎小球病:補體替代途徑的活化參與其中 6)8)。
COVID-19感染:即使是輕症,也可能因補體活化和凝血異常而發病 1)9)。
Valsalva動作 / 排便:因胸腔內壓升高導致靜脈回流障礙 7)。
其他非外傷原因包括:膠原病/結締組織疾病(SLE、皮肌炎、硬皮症)、妊娠高血壓症候群/HELLP症候群、脂肪栓塞症候群、溶血性尿毒症症候群、血栓性血小板減少性紫斑症、分娩(羊水栓塞)、球後麻醉、搖晃嬰兒症候群。近年來,也有填充劑注射(包括非臉部)3)、缺血性結腸炎4)、以及帶狀皰疹疫苗(Shingrix)接種後5)的病例報告。
據報導,即使是輕症COVID-19,也可能因補體活化和凝血異常導致視網膜微血管閉塞,從而引發Purtscher樣視網膜病變 1)。也有觀點認為,細胞因子風暴導致的高濃度C5a促進了血栓形成 9)。
使用兩種診斷標準。
Agrawal等人的標準要求滿足以下所有條件:①存在相關疾病,②單眼/雙眼出現Purtscher斑點和/或淺層CWS,③侷限於後極部,④無直接眼外傷,⑤視網膜血管內無栓子,⑥出血極少。
Miguel更新標準(5項標準中符合3項或以上)如下所示4)。
| 標準 | 內容 |
|---|---|
| 標準1 | 存在Purtscher斑 |
| 標準2 | 少量至中度視網膜出血 |
| 標準3 | 軟性滲出(僅限後極部) |
| 標準4 | 存在可解釋的病因 |
| 標準5 | 與診斷一致的輔助檢查結果 |
通過臨床發現和螢光素眼底血管造影進行診斷。
Purtscher flecken呈多邊形,發生在小動脈和小靜脈之間的微血管床,邊界清晰,距離血管50μm以內。軟性滲出是邊界模糊的絮狀白斑,由神經纖維層內的局部梗塞引起2)。兩者可共存於同一眼底。
沒有基於證據的治療指引。多數病例進行觀察,但有時也會使用類固醇治療。治療原發病(如急性胰臟炎、骨折等)是首要任務。
| 治療方法 | 證據 | 主要定位 |
|---|---|---|
| 觀察 | 系統性回顧推薦 | 第一線 |
| 高劑量類固醇 | 前瞻性試驗未確立 | 輔助性 |
| 抗VEGF藥物 | 僅病例報告 | 合併黃斑水腫時 |
即使不治療,多數病例在數個月內會緩解。有時會使用類固醇療法、抗血小板藥物治療、纖溶療法,但效果不明。Miguel等人的系統性回顧顯示,高劑量類固醇組與未治療組在視力改善上無顯著差異。Xia等人(2017)的系統性回顧也認為糖皮質激素療法在視力改善上無差異4)5)。病變傾向在1~3個月內自然消退4)。
高劑量靜脈注射類固醇是最常報告的治療方法,但前瞻性試驗的證據尚未確立。其機轉包括穩定受損的神經膜與微血管通道,以及抑制顆粒球聚集和補體活化。病例報告中使用從prednisolone 60mg開始逐漸減量的劑量1)6)。
多項系統性回顧顯示,類固醇組與未治療組在視力改善方面無顯著差異4)5)。基礎疾病的治療為首要任務,病變通常在1-3個月內自行消退。類固醇治療、抗血小板治療與溶栓治療的療效尚不清楚,前瞻性試驗的證據尚未建立。
主要病因是視網膜小動脈前毛細血管的栓塞導致閉塞。多種因素導致血管內皮損傷參與發病機制。
Purtscher遠達性外傷性視網膜病變的機制推測如下:
栓塞的類型因病因不同而異。已報告的有脂肪(長骨骨折)、胰臟蛋白酶(急性胰臟炎)、白血球聚集(白血球栓塞)、空氣、血小板與纖維蛋白。
根據栓子大小不同,表現各異。大的栓子引起類似視網膜分支動脈阻塞的融合性混濁,小的引起軟性滲出,中等的引起Purtscher斑。
C5和補體的活化伴有繼發性淋巴漏出,扮演重要角色。提示補體活化→白血球聚集(最大50μm)→微血管前阻塞的途徑5)8)。
Purtscher斑由直徑約45μm的微血管前小動脈阻塞引起。視網膜動脈和小動脈兩側50μm的無微血管區形成透明帶。
數據有限。Kincaid等人報告的急性胰臟炎死亡病例中,觀察到視網膜內層局部水腫、囊樣空間和正常結構破壞。小動脈腔內可見蛋白樣物質(推測為再通的血栓),感光細胞外節消失,但RPE和脈絡膜正常。
有病例報告顯示,eculizumab(C5抑制劑)對非典型溶血性尿毒症候群相關的Purtscher樣視網膜病變有效8)。基於C3腎小球病和補體調節異常的共同病理生理學,提示其可能應用於Purtscher樣視網膜病變的治療。
Teru等人(2025年)首次報告了急性缺血性結腸炎後的Purtscher樣視網膜病變4)。一名72歲女性因腹痛、血便住院,次日出現雙眼視力下降。僅通過結腸炎治療(metronidazole和ciprofloxacin),兩週後自然改善。
Pee等人(2023年)報告了首例注射約500 mL乳房玻尿酸填充劑後併發雙眼CF、肺泡出血和腦梗塞的Purtscher樣視網膜病變和PAMM病例3)。SD-OCT顯示內核層高反射帶,10個月後內層視網膜排列異常仍存在。
Shroff等人(2022年)報告了一例COVID-19後單眼Purtscher樣視網膜病變,SS-OCTA顯示血管缺失和血流缺損9)。研究表明急性期的血流缺損在慢性期持續存在,OCTA作為定量評估表層和深層毛細血管叢血管密度的工具受到關注。
關於急性期OCT表現(內層高反射的範圍、程度和深度)與長期視功能預後相關性的研究正在進展中。有報告指出內層萎縮的範圍和黃斑部神經節細胞層的變薄可能是預後不良的指標,期待建立基於OCT的客觀預後預測模型。