Purtscher斑
形状:多边形、边界清晰的白浊。
位置:位于小动脉和小静脉之间的视网膜内层。见于视网膜动脉周围。
边界:距血管50μm以内有清晰的边界。典型的表现为血管周围视网膜免于白浊(perivascular sparing)。
频率:约63%的病例可见。
病理生理:毛细血管床的毛细血管前小动脉闭塞导致内层白浊。
1910年,Otmar Purtscher首次报道了一名从树上坠落导致头部外伤的中年患者。这是一种罕见疾病,是与外伤相关的视网膜血管闭塞性疾病。它被归类为远达性外伤性视网膜病变,由眼外创伤(如头、颈、胸部挫伤)引起。
与全身性疾病、球后麻醉等手术操作、急性胰腺炎、血栓性血小板减少性紫癜、肾功能衰竭或结缔组织病相关的类似疾病被区分为Purtscher样视网膜病变。两者的眼底表现相同,病理生理相似。
估计发病率为0.24/百万人/年,可能存在漏报4)6)。约60%为双眼,偶有单眼病例。由急性胰腺炎引起时几乎均为双眼。病变局限于后极部(视乳头周围和黄斑区)占83-92%。外伤是最常见原因,其次是急性胰腺炎。
Purtscher样视网膜病变的病因多种多样。除急性胰腺炎、肾功能衰竭、胶原病、妊娠高血压综合征/HELLP综合征、脂肪栓塞综合征、Valsalva动作、溶血性尿毒症综合征、摇晃婴儿综合征、球后麻醉、类固醇注射等外,近年来还报告了由COVID-19感染1)9)、高血压急症2)、填充剂注射3)、缺血性结肠炎4)、疫苗接种5)和C3肾小球病8)引起的病例。
由头部外伤、胸部压迫、长骨骨折等外伤引起的病例称为Purtscher视网膜病变。由急性胰腺炎或肾功能衰竭等不伴外伤的全身性疾病引起的病例称为Purtscher样视网膜病变。两者的眼底表现相同,治疗方案也相同。
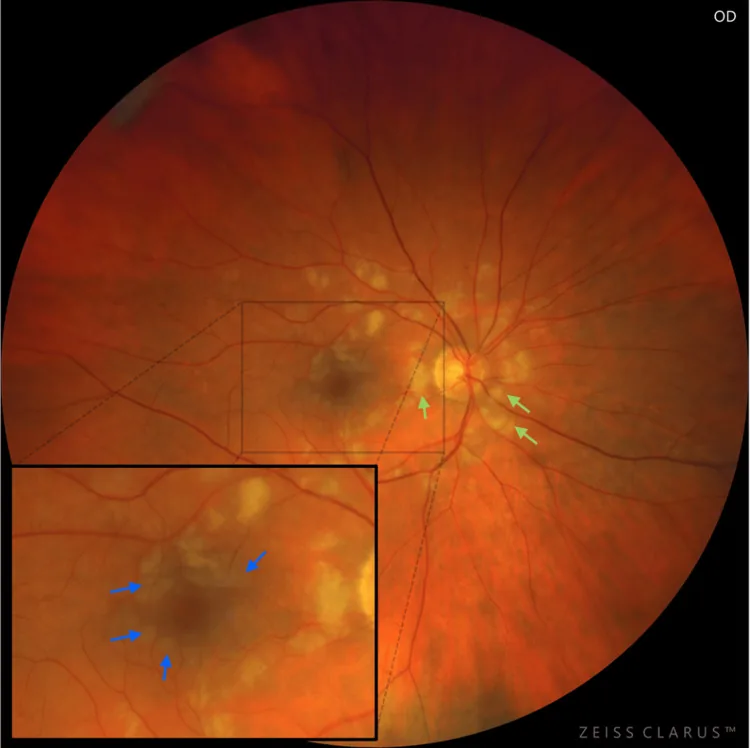
视力障碍在外伤或相关疾病发作后数小时至数天延迟出现。视力障碍的程度从非常轻微到手边手动不等。也可能伴有视野缺损,表现为中心暗点、旁中心暗点或弓形暗点。
局限于后极部(视乳头周围和黄斑区域)的表现具有特征性。
Purtscher斑
形状:多边形、边界清晰的白浊。
位置:位于小动脉和小静脉之间的视网膜内层。见于视网膜动脉周围。
边界:距血管50μm以内有清晰的边界。典型的表现为血管周围视网膜免于白浊(perivascular sparing)。
频率:约63%的病例可见。
病理生理:毛细血管床的毛细血管前小动脉闭塞导致内层白浊。
软性渗出(棉絮斑)
形状:边界不清的蓬松白色斑块。
位置:神经纤维层(NFL)内的局灶性梗死。多见于视盘周围。
边界:不清且不规则。
频率:最常见的表现,93%的病例可见。
病理生理:由NFL内的微梗死引起。
根据病变范围分为A、B、C三个区域。三分之二的病例仅累及A区,C区受累罕见。
| 区域 | 病变范围 |
|---|---|
| A | 视乳头周围(乳头直径4倍范围内) |
| B | 后极部(至赤道前) |
| C | 包括周边部的广泛范围 |
发病2个月后的随访中,报告如下:眼底正常40%、视神经萎缩64%、RPE虎斑状改变23%、视网膜变薄14%、视网膜动脉狭窄4%。有时会残留视神经萎缩和视网膜萎缩。
视力下降通常不是在外伤或全身疾病发病后立即出现,而是在数小时至数天的延迟后发生。无眼痛。如果外伤后视力逐渐变差,需要考虑本病。
Purtscher视网膜病变(外伤性)
头部外伤:最古老已知的原因。交通事故、坠落、殴打等。
胸部压迫:因强烈压迫性外伤导致胸腔内压急剧升高。挤压综合征、重物导致的胸部挤压伤。
长管骨骨折:可能因脂肪栓塞综合征而发病。
Purtscher样视网膜病变(非外伤性)
急性胰腺炎:最常见的非外伤原因。几乎均为双眼性。
肾功能衰竭 / C3肾小球病:补体替代途径的激活参与其中 6)8)。
COVID-19感染:即使是轻症,也可能因补体激活和凝血异常而发病 1)9)。
Valsalva动作 / 排便:因胸腔内压升高导致静脉回流障碍 7)。
其他非外伤原因包括:胶原病/结缔组织病(SLE、皮肌炎、硬皮病)、妊娠高血压综合征/HELLP综合征、脂肪栓塞综合征、溶血性尿毒症综合征、血栓性血小板减少性紫癜、分娩(羊水栓塞)、球后麻醉、摇晃婴儿综合征。近年来,也有填充剂注射(包括非面部)3)、缺血性结肠炎4)、以及带状疱疹疫苗(Shingrix)接种后5)的病例报道。
据报道,即使是轻症COVID-19,也可能因补体激活和凝血异常导致视网膜微血管闭塞,从而引发Purtscher样视网膜病变 1)。也有观点认为,细胞因子风暴导致的高浓度C5a促进了血栓形成 9)。
使用两种诊断标准。
Agrawal等人的标准要求满足以下所有条件:①存在相关疾病,②单眼/双眼出现Purtscher斑点和/或浅层CWS,③局限于后极部,④无直接眼外伤,⑤视网膜血管内无栓子,⑥出血极少。
Miguel更新标准(5项标准中满足3项或以上)如下所示4)。
| 标准 | 内容 |
|---|---|
| 标准1 | 存在Purtscher斑 |
| 标准2 | 少量至中度视网膜出血 |
| 标准3 | 软性渗出(仅限于后极部) |
| 标准4 | 存在可解释的病因 |
| 标准5 | 与诊断一致的辅助检查结果 |
通过临床发现和荧光素眼底血管造影进行诊断。
Purtscher flecken呈多边形,发生在小动脉和小静脉之间的毛细血管床,边界清晰,距离血管50μm以内。软性渗出是边界模糊的絮状白斑,由神经纤维层内的局灶性梗死引起2)。两者可共存于同一眼底。
没有基于证据的治疗指南。多数病例进行观察,但有时也会使用类固醇治疗。治疗原发病(如急性胰腺炎、骨折等)是首要任务。
| 治疗方法 | 证据 | 主要定位 |
|---|---|---|
| 观察 | 系统评价推荐 | 一线选择 |
| 大剂量类固醇 | 前瞻性试验未确立 | 辅助治疗 |
| 抗VEGF药物 | 仅病例报告 | 合并黄斑水肿时 |
即使不治疗,多数病例在数月内缓解。有时会使用类固醇疗法、抗血小板药物疗法、纤溶疗法等,但效果不明。Miguel等人的系统评价显示,大剂量类固醇组与未治疗组在视力改善方面无显著差异。Xia等人(2017)的系统评价也认为糖皮质激素疗法在视力改善方面无差异4)5)。病变倾向于在1~3个月内自然消退4)。
大剂量静脉注射类固醇是最常报道的治疗方法,但前瞻性试验的证据尚未确立。其机制包括稳定受损的神经膜和微血管通道,以及抑制粒细胞聚集和补体激活。病例报告中使用从泼尼松龙60mg开始逐渐减量的剂量1)6)。
多项系统评价显示,类固醇组与未治疗组在视力改善方面无显著差异4)5)。基础疾病的治疗是首要任务,病变通常在1-3个月内自行消退。类固醇治疗、抗血小板治疗和溶栓治疗的疗效尚不清楚,前瞻性试验的证据尚未建立。
主要病因是视网膜小动脉前毛细血管的栓塞导致闭塞。多种因素导致血管内皮损伤参与发病机制。
Purtscher远达性外伤性视网膜病变的机制推测如下:
栓塞的类型因病因不同而异。已报道的有脂肪(长骨骨折)、胰腺蛋白酶(急性胰腺炎)、白细胞聚集(白细胞栓塞)、空气、血小板和纤维蛋白。
根据栓子大小不同,表现各异。大的栓子引起类似视网膜分支动脉阻塞的融合性混浊,小的引起软性渗出,中等大小的引起Purtscher斑。
C5和补体的激活伴有继发性淋巴漏出,起重要作用。提示补体激活→白细胞聚集(最大50μm)→毛细血管前阻塞的途径5)8)。
Purtscher斑由直径约45μm的毛细血管前小动脉阻塞引起。视网膜动脉和小动脉两侧50μm的无毛细血管区形成透明带。
数据有限。Kincaid等报道的急性胰腺炎死亡病例中,观察到视网膜内层局灶性水肿、囊样间隙和正常结构破坏。小动脉腔内可见蛋白样物质(推测为再通的血栓),光感受器外节消失,但RPE和脉络膜正常。
有病例报告显示,依库珠单抗(C5抑制剂)对非典型溶血性尿毒症综合征相关的Purtscher样视网膜病变有效8)。基于C3肾小球病和补体调节异常的共同病理生理学,提示其可能应用于Purtscher样视网膜病变的治疗。
Teru等人(2025年)首次报告了急性缺血性结肠炎后的Purtscher样视网膜病变4)。一名72岁女性因腹痛、血便住院,次日出现双眼视力下降。仅通过结肠炎治疗(甲硝唑和环丙沙星),两周后自然改善。
Pee等人(2023年)报告了首例注射约500 mL乳房透明质酸填充剂后并发双眼CF、肺泡出血和脑梗死的Purtscher样视网膜病变和PAMM病例3)。SD-OCT显示内核层高反射带,10个月后内层视网膜排列异常仍存在。
Shroff等人(2022年)报告了一例COVID-19后单眼Purtscher样视网膜病变,SS-OCTA显示血管缺失和血流缺损9)。研究表明急性期的血流缺损在慢性期持续存在,OCTA作为定量评估浅层和深层毛细血管丛血管密度的工具受到关注。
关于急性期OCT表现(内层高反射的范围、程度和深度)与长期视功能预后相关性的研究正在进展中。有报告指出内层萎缩的范围和黄斑区神经节细胞层变薄可能是预后不良的指标,期待建立基于OCT的客观预后预测模型。