纖維型後發性白內障
後照法所見:邊界不清、多皺褶的混濁。
病理:水晶體上皮細胞轉化為肌纖維母細胞樣細胞,產生以膠原為主的細胞外基質。從前囊和後囊粘連處向後囊上擴展。
對症狀的影響:由於向後散射,損害相對較輕。嚴重時可導致對比敏感度下降和前囊口縮小(前囊收縮)。

後發性白內障(Posterior Capsule Opacification, PCO)是指白內障摘除術後殘留的晶狀體上皮細胞增殖、遷移和分化,導致保留的後囊膜發生繼發性混濁的疾病。也稱為「繼發性白內障」。
廣義的「後發性白內障(after cataract)」是白內障手術後水晶體囊袋內發生的所有組織反應的總稱,包括Elschnig珍珠、後囊膜纖維化和液化後發性白內障等。其中,累及瞳孔區並影響視功能的狀態在臨床上稱為「後囊膜混濁(PCO)」。
術後1年發生率為11.8%,3年為20.7%,5年為28.4%,是白內障手術後最常見的併發症。現代手術技術和人工水晶體設計的進步使其盛行率呈下降趨勢,Nd:YAG雷射後囊膜切開術的執行頻率因報告而異,從不到5%到54%不等1)。儘管如此,它仍然給患者和醫療系統帶來巨大負擔。
兒童和嬰兒的發生率極高,且發病時間早。兒童後發性白內障的發生率最高可達100%,必須早期處理相關的弱視風險。
白內障本身不會復發。摘除的水晶體混濁不會恢復,後發性白內障是最可能的原因之一。如果術後數月至數年出現視力模糊或視力下降,應懷疑後發性白內障,並及時就診眼科。
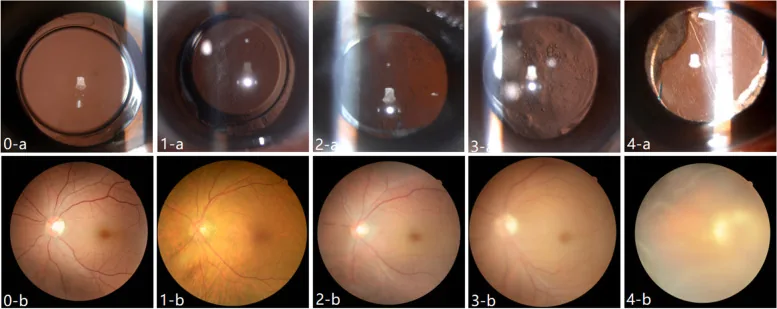
許多患者在順利的白內障手術後數月至數年就診。視功能障礙按「眩光下對比敏感度下降→對比敏感度下降→視力下降」的順序發生,因此早期評估對比敏感度很重要。典型主訴如下。
後發性白內障分為以下4型。
纖維型後發性白內障
後照法所見:邊界不清、多皺褶的混濁。
病理:水晶體上皮細胞轉化為肌纖維母細胞樣細胞,產生以膠原為主的細胞外基質。從前囊和後囊粘連處向後囊上擴展。
對症狀的影響:由於向後散射,損害相對較輕。嚴重時可導致對比敏感度下降和前囊口縮小(前囊收縮)。
珍珠型後發性白內障(Elschnig珍珠型)
徹照法所見:邊界相對清晰的小顆粒狀增生(Elschnig珍珠)。由於向前方散射光線,導致嚴重的視功能障礙。
病理:由水晶體赤道部排列的水晶體上皮細胞不完全分化為水晶體纖維所致。腫脹混濁的膀胱細胞(Wedl細胞)在後囊上積聚。
對症狀的影響:積聚在視軸上會導致顯著的視力下降。如果存在層疊的Elschnig珍珠,通常已經出現視力下降。
Elschnig珍珠呈現出現和消失的動態變化。有報導稱形成和消失可在1週內發生,同一患者左右眼可呈現不同形態。有視軸部珍珠自然消退、視力改善的病例報導,自然消退的機制包括凋亡、脫落至玻璃體腔、巨噬細胞吞噬等。
白內障手術中,切開部分前囊(連續環狀撕囊術:CCC),取出混濁的水晶體組織並植入IOL。殘留的前囊上的水晶體上皮細胞增殖、遷移、分化導致後發性白內障。
術後早期可能開始纖維化,但通常術後較長時間混濁才加重。涉及的細胞因子和生長因子包括TGF-β、FGF-2、肝細胞生長因子(HGF)、基質金屬蛋白酶(MMPs)等。
後發性白內障的診斷基於病史和裂隙燈顯微鏡檢查。診斷步驟如下。
僅憑視力可能難以判斷。如果有模糊主訴但視力未下降,應測量對比敏感度。由於眩光下的對比敏感度、對比敏感度、視力依次受損,因此早期後發性白內障的對比敏感度評估很重要。
排除視力下降的其他原因(黃斑疾病、視神經疾病)後,決定後囊切開的適應症。
Nd:YAG雷射後囊切開的適應症如下1):
基本診斷可透過裂隙燈顯微鏡和徹照法完成。散瞳後徹照後囊,可輕鬆區分Elschnig珍珠和纖維化。使用90D透鏡等觀察眼底透見性也有參考價值。Elschnig珍珠透明,因此僅常規觀察而不徹照時可能漏診。
這是影響視功能的後發性白內障的第一線治療。它是一種非侵入性、快速、有效的治療方法,很少進行外科後囊切開術。
術前處置:為預防眼壓升高,在處置前1小時和處置後立即滴用鹽酸阿普拉可樂定眼藥水。處置前進行散瞳。
切開方法:
| 方法 | 特點 |
|---|---|
| 十字切開 | 後囊片不易漂浮,照射次數少。視軸附近可能出現凹坑或裂紋。 |
| 環形切開 | 避開視軸,安全性高。後囊片可能導致飛蚊症或發炎。 |
切開窗口大小:目標直徑大於瞳孔區,達到4~5mm以上。
多焦點IOL植入眼的注意事項:即使裂隙燈檢查正常,後照法可能發現細微的Elschnig珍珠。後囊切開窗口應設定得較大。由於在低對比度和眩光條件下PCO的功能影響更大,可能比常規更早進行後囊切開術 1)。
散光或不規則散光嚴重的病例:將後囊切開窗口稍做縮小,可透過針孔效應最大化視功能和滿意度。
在幼兒中,無法安全進行Nd:YAG雷射後囊切開術,因此對於後發性白內障導致的視軸混濁,採用經平坦部玻璃體切除術和囊切除術。早期介入對於預防相關弱視尤為重要。
在一般超音波乳化術中,殘留的前囊上的水晶體上皮細胞在術後被活化。這些水晶體上皮細胞透過以下三種現象導致後發性白內障的發生。
在纖維型後發性白內障中,水晶體上皮細胞發生上皮-間質轉化(EMT)成為肌纖維母細胞樣細胞,並產生膠原蛋白等細胞外基質(ECM)。在珍珠型後發性白內障中,殘留的水晶體上皮細胞不完全分化為水晶體纖維,以膀胱細胞(Wedl細胞)的形式在後囊上積聚。
具有直角邊緣(方邊)光學設計的IOL與圓邊IOL相比,後發性白內障發生率較低1)。透過直徑略小於IOL光學部的連續環形撕囊,產生前囊邊緣騎跨在IOL表面的「收縮包裹效應」,將光學部與囊袋周圍房水隔離,從而抑制後發性白內障的發生1)。當前囊切開完全覆蓋整個光學部時,PCO發生率較低1)。
關於IOL材料,2013年的一項統合分析(9項RCT和多項縱向研究)顯示,疏水性銳邊IOL與親水性銳邊IOL相比,PCO發生率和Nd:YAG後囊切開率較低1)。然而,一項為期12年的RCT提示,銳邊疏水性鏡片的保護作用可能只是「延遲」PCO的發生1)。
前囊拋光的影響:前囊拋光對PCO的發生顯示不一致的效果。有報告指出,它可能妨礙IOL光學部後端銳利邊緣與後囊之間的緊密黏附,反而可能促進PCO並增加早期需要Nd:YAG雷射的可能性1)。
為了在不引起周圍眼內組織毒性副作用的情況下清除殘留的晶狀體上皮細胞或抑制其再生,正在研究抗代謝藥物、抗炎藥、低滲透壓藥物和免疫製劑等。
兩項使用免疫毒素(MDX-A)的研究觀察到後發性白內障發生率降低,但尚無確鑿的體內證據表明其他藥物對後發性白內障的發生有顯著影響。手術結束時選擇性損傷晶狀體上皮細胞的「aqueous flush」技術等也在探索中。
一項薈萃分析報告稱,三焦點IOL與雙焦點IOL相比,PCO發生率顯著降低(RR 0.54,95%CI 0.31-0.95)2)。
調節性IOL依賴於柔軟且完整的後囊膜功能,因此預防後發性白內障對這些裝置尤為重要。後囊膜混濁會損害調節功能,因此需要開發更積極的後發性白內障預防措施。