色素性黑色素瘤(70%)
好发部位:约90%发生于球结膜,其中63%位于颞侧象限4, 6)。
外观:黑褐色至茶褐色的隆起性病变。伴有丰富的滋养血管(feeder vessels)朝向肿瘤。
与巩膜的关系:有时可见与巩膜粘连。肿瘤与角膜缘的平均距离为2mm,61%到达角膜缘2)。

结膜恶性黑色素瘤是起源于结膜黑色素细胞的恶性肿瘤。在西方国家常见,但在日本罕见。常起源于原发性获得性黑变病(PAM)。
全球发病率为0.3-0.8/百万人/年,北欧和北美最高。过去50年呈上升趋势。美国每年估计约130例新发病例,欧洲约320例8)。亚洲人的年龄调整发病率为0.15/百万人/年,较低,白种人最常见(91.2%)1, 8)。
平均发病年龄为55-65岁,20岁以下发病极为罕见1, 4, 5, 6)。5年疾病特异性生存率约为82.9%,10年为69.3%8)。
按起源分类:
结膜黑色素瘤是唯一一种被认为与紫外线暴露相关的黏膜黑色素瘤,因为球结膜直接暴露于紫外线4)。
结膜恶性黑色素瘤的发病率为0.3~0.8/百万人/年,是一种罕见疾病,但在过去50年中呈增加趋势。亚洲人的发病风险低于白人,据报道为0.15/百万人/年。儿童病例仅占所有结膜黑色素瘤的1%,20岁以下发病极为罕见。
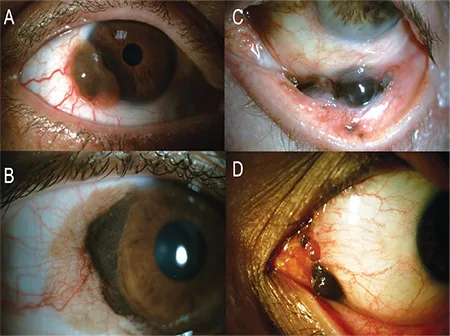
临床上表现为眼球结膜或眼睑结膜的隆起性黑褐色病变,可见丰富的血管向肿瘤分布。
色素性黑色素瘤(70%)
好发部位:约90%发生于球结膜,其中63%位于颞侧象限4, 6)。
外观:黑褐色至茶褐色的隆起性病变。伴有丰富的滋养血管(feeder vessels)朝向肿瘤。
与巩膜的关系:有时可见与巩膜粘连。肿瘤与角膜缘的平均距离为2mm,61%到达角膜缘2)。
无色素性黑色素瘤(30%)
外观:粉红色至红色的肿块,几乎不含色素。
误诊风险:易被误诊为鳞状细胞癌或其他红色结膜肿块3)。
预后:低色素性和无色素性可能与预后不良相关。
影像学评估:
有。约30%的结膜黑色素瘤为无色素性,表现为粉红色至红色肿块。无色素性黑色素瘤外观与鳞状细胞癌等相似,易被误诊,可能导致诊断延迟。对于可疑的结膜肿块,必须通过活检进行病理诊断。
以下因素与转移和死亡风险增加相关1, 4, 5, 6, 8)。
AJCC(美国癌症联合委员会)分期系统与预后密切相关1)。
| 分期 | 5年累积死亡率 |
|---|---|
| cT1 | 2.5% |
| cT2 | 28.6% |
| cT3 | 31.6% |
| cT3c(眼眶浸润) | 100% |
T3肿瘤的5年估计远处转移率为42%,5年死亡率为23%1)。
淋巴道转移是主要途径。颞侧结膜病变易转移至耳前淋巴结,鼻侧结膜病变易转移至颌下淋巴结。远处转移(血行性)可发生于脑、肺、肝、皮肤、肾上腺等6, 1)。淋巴结转移在诊断后中位2.3年时见于15-41%的患者,全身转移在3年时见于9-25%。即使未检测到淋巴结转移,仍有38%发生远处血行性器官转移6)。
主要不良预后因素包括肿瘤厚度(尤其>2mm)、病变部位(泪阜预后最差)、AJCC分期、结节型形态、淋巴管浸润和眼眶浸润。切除的完整性也影响很大,不完全切除病例中约49.3%复发。前哨淋巴结阳性者死亡风险升高。
确诊需要活检。组织病理学表现为含有黑色素、核仁明显、核/质比大的细胞增殖。若黑色素较多,需对病理标本进行脱色素处理。
免疫组织化学染色对确诊和鉴别诊断至关重要。
| 标志物 | 特征 | 备注 |
|---|---|---|
| HMB-45 | 黑色素细胞阳性 | 对诊断有用2, 8) |
| SOX10 | 黑色素细胞系阳性 | 高灵敏度1, 4) |
| Melan-A/MART-1 | 黑色素细胞系阳性 | 通用标记物3, 5, 6) |
| S-100 | 黑色素细胞系阳性 | 灵敏度高但特异性低1) |
| PRAME | 黑色素瘤阳性,痣阴性 | 最有力的鉴别标记物5) |
| Ki-67 | 黑色素瘤中10%~15%以上 | 增殖指数3, 4) |
| p16 | 黑色素瘤中缺失 | 痣中保留5) |
确诊黑色素瘤的病例需要进行系统的全身评估。
手术切除肿瘤及周围组织是基本治疗。术中及术后局部使用MMC或干扰素α-2b也有效。如果肿瘤广泛且明显浸润结膜下,可能需要行眼眶内容物剜除术。
手术治疗
切除边缘:确保3-5mm安全边缘的肿瘤完全切除 4, 8)
无接触技术:避免器械直接接触肿瘤,防止肿瘤细胞播散 4, 8)
干燥技术:不使用灌注液(BSS)进行切除
角膜浸润病例:酒精角膜上皮剥离 + 用角膜刀整块切除 2)
眼眶内容物剜除术:适用于广泛或复发病例(进展期)
眼球摘除术:适用于眼内扩展病例
辅助治疗
冷冻凝固术:采用双冻融方式应用于切除底部和边缘。提起结膜以避免巩膜损伤 3)
MMC局部化疗:
IFNα-2b:不引起角膜缘干细胞缺乏的MMC替代品 3)
放射治疗:近距离放射治疗或外照射3)
前哨淋巴结活检:肿瘤厚度>2mm时考虑7)
广泛切除后的结膜重建采用以下方法4, 5)。
为防止肿瘤细胞播散(局部复发或转移),该技术要求在术中不直接用器械接触肿瘤,并在不使用灌注液(BSS)的干燥环境下切除。整个肿瘤连同3–5mm的安全边界整块切除,以降低因不完全切除导致的复发风险。与常规切除的根本区别在于最大限度地减少肿瘤细胞在结膜上的播散。
结膜黑色素瘤在遗传学上与皮肤黑色素瘤相似,而非葡萄膜黑色素瘤。紫外线相关的驱动突变(C>T转换)主要为BRAF、NF1和RAS。葡萄膜黑色素瘤的标志物(BAP1、GNAQ、GNA11、SF3B1)在结膜黑色素瘤中确认为阴性1)。
Lally等人(2022年)对101例病例的研究中,确定了四种高频突变1)。
NF1突变(33–50%)
频率:最常见的突变。
预后:单独的NF1突变与2年和5年低转移率相关。
特征:可与BRAF突变共存。常与ATRX突变共存8)。
BRAF突变(29–46%)
频率:第二常见的突变。V600E突变占80–90%。
分布:常见于球结膜黑色素瘤(日光暴露部位)4)。
预后:与转移或死亡无显著关联。是靶向治疗(BRAF抑制剂)的治疗靶点。
NRAS突变(11–26%)
频率:第三常见的突变。
预后:转移和死亡风险增加,死亡风险约增加5倍1)。
特征:与BRAF突变互斥。
ATRX突变(25%)
频率:第四常见的突变。
预后:与NF1突变类似,与2年和5年低转移率相关。
特征:常与NF1突变共存8)。
TERT启动子突变(c.-124C>T)影响端粒酶逆转录酶,据报道与转移性结膜黑色素瘤相关1, 8, 6)。在PAM的中度至重度异型中也检测到(约8%),提示其具有原位黑色素瘤的性质6)。还显示与高肿瘤突变负荷相关4)。32-64%的结膜黑色素瘤存在TERT突变,其与预后的关系备受关注8)。
已确认高PD-L1表达和富含免疫相关基因的转录亚型的存在,这为使用免疫检查点抑制剂提供了理论依据。BRAF抑制剂、MEK抑制剂和PD-L1抑制剂的数据有前景,但目前有限。
Chou等人(2023)分析了一名94岁男性T3c结膜黑色素瘤病例的分子谱。他们鉴定出NF1突变和TERT启动子突变(c.-124C>T,VAF 31.4%),BRAF、NRAS和cKIT均为阴性。NF1突变与NRAS阴性的组合被认为有助于相对良好的无转移病程1)。
PD-1抑制剂(pembrolizumab、nivolumab)和CTLA-4抑制剂(ipilimumab)已在转移性和局部晚期结膜黑色素瘤中尝试使用4, 8)。
作为代表性报告,Sagiv等人(2018)报道了对5例患者使用pembrolizumab或nivolumab进行PD-1抑制治疗,部分患者获得完全缓解8)。一项使用axitinib + nivolumab联合治疗的2期试验(针对未经治疗的晚期或转移性黏膜黑色素瘤)正在进行中。
转移性结膜黑色素瘤全身治疗的标准方案尚未确立,需要根据具体病例谨慎判断。
对于BRAF突变阳性病例,已尝试使用BRAF抑制剂单药(vemurafenib)或BRAF/MEK抑制剂联合(dabrafenib + trametinib、encorafenib + binimetinib)4, 8)。
这些药物在部分病例中报告有局部肿瘤缩小效果,但多数为单病例或少数病例报告,长期结果有限。同时靶向MAPK通路和AKT通路可能产生协同效应的可能性也在研究中3)。
利用免疫组织化学组合(PRAME、p16、HMB-45、Ki-67、Cyclin D1),以往被视为“不确定”的病变正在被重新分类5)。C-MIL(结膜黑色素细胞上皮内病变)分类(WHO第5版,2022年)的国际标准化也在推进中。
基于与皮肤黑色素瘤的遗传学相似性(BRAF、NF1、NRAS突变,高PD-L1表达),PD-1抑制剂(pembrolizumab、nivolumab)、CTLA-4抑制剂和BRAF抑制剂已在转移性和局部晚期病例中尝试使用。然而,尚未进行大规模临床试验,目前证据有限,标准治疗方案尚未确立。迫切需要国际多中心合作研究积累大规模数据。