มะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุตา เป็นเนื้องอกร้ายที่เกิดจากเซลล์เมลาโนไซต์ของเยื่อบุตา อุบัติการณ์มีแนวโน้มเพิ่มขึ้น
ประมาณ 60-75% เกิดจาก Primary Acquired Melanosis (PAM )
รอยโรคสีน้ำตาลดำนูนขึ้น มีหลอดเลือดของเนื้องอกมากมาย ชนิดไม่มีเม็ดสีอาจถูกวินิจฉัยผิดเป็นมะเร็งเซลล์สความัส
การตัดออกทางศัลยกรรมทั้งหมด (เทคนิคไม่สัมผัส) และการจี้เย็น เป็นพื้นฐานของการรักษา การให้ MMC เฉพาะที่ระหว่างและหลังผ่าตัดก็มีประสิทธิภาพ
การกลายพันธุ์ของ BRAF, NF1 และ NRAS เป็นตัวขับเคลื่อนหลัก คล้ายคลึงทางพันธุกรรมกับมะเร็งผิวหนังเมลาโนมา
ความหนาของเนื้องอก >2 มม. รอยโรคที่คารันเคิล และชนิดเป็นก้อนเป็นปัจจัยพยากรณ์โรคที่ไม่ดี
อัตราการรอดชีวิตเฉพาะโรค 5 ปีประมาณ 82.9% แต่การพยากรณ์โรคไม่ดีในกรณีที่มีการแพร่กระจาย
มะเร็งเมลาโนมาชนิดร้ายปฐมภูมิของเยื่อบุตา เป็นเนื้องอกร้ายที่เกิดจากเมลาโนไซต์ของเยื่อบุตา พบได้บ่อยในตะวันตกแต่พบน้อยในญี่ปุ่น มักเกิดจาก Primary Acquired Melanosis (PAM )
อุบัติการณ์ทั่วโลกอยู่ที่ 0.3-0.8 ต่อล้านคนต่อปี สูงที่สุดในยุโรปเหนือและอเมริกาเหนือ มีแนวโน้มเพิ่มขึ้นในช่วง 50 ปีที่ผ่านมา ในสหรัฐอเมริกาคาดว่ามีผู้ป่วยรายใหม่ประมาณ 130 รายต่อปี ในยุโรปประมาณ 320 ราย 8) อุบัติการณ์ที่ปรับตามอายุในคนเอเชียต่ำที่ 0.15 ต่อล้านคนต่อปี พบมากที่สุดในคนผิวขาว (91.2%) 1, 8)
อายุเฉลี่ยที่เริ่มป่วยคือ 55-65 ปี การเริ่มป่วยก่อนอายุ 20 ปีพบน้อยมาก 1, 4, 5, 6) อัตราการรอดชีวิตเฉพาะโรค 5 ปีประมาณ 82.9% และ 10 ปี 69.3% 8)
การกระจายตามแหล่งกำเนิด:
จาก PAM (Primary Acquired Melanosis): ประมาณ 60-75% (พบมากที่สุด)
เกิดใหม่ (de novo): ประมาณ 19%
จากปานเยื่อบุตา : 7-20%
เนื่องจากเยื่อบุตา ส่วนลูกตาถูกแสงอัลตราไวโอเลตโดยตรง มะเร็งผิวหนังชนิดเมลาโนมาของเยื่อบุตา เป็นมะเร็งเมลาโนมาของเยื่อเมือกชนิดเดียวที่เชื่อมโยงกับการได้รับรังสีอัลตราไวโอเลต4)
Q
มะเร็งเมลาโนมาชนิดร้ายของเยื่อบุตาพบได้น้อยเพียงใด?
A
อุบัติการณ์ของมะเร็งเมลาโนมาชนิดร้ายของเยื่อบุตา อยู่ที่ 0.3–0.8 ต่อล้านคนต่อปี ซึ่งเป็นโรคที่พบได้น้อย แต่มีแนวโน้มเพิ่มขึ้นในช่วง 50 ปีที่ผ่านมา คนเอเชียมีความเสี่ยงต่ำกว่าคนผิวขาว โดยรายงานอยู่ที่ 0.15 ต่อล้านคนต่อปี ผู้ป่วยเด็กคิดเป็นเพียง 1% ของมะเร็งเมลาโนมาของเยื่อบุตา ทั้งหมด และการเกิดในผู้ที่มีอายุต่ำกว่า 20 ปีพบได้น้อยมาก
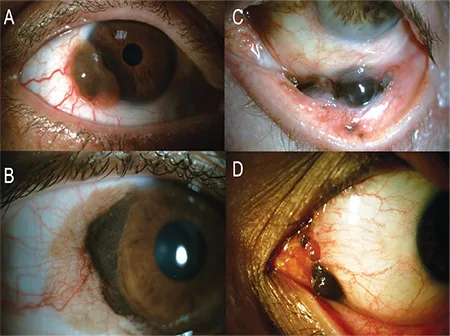
ภาพถ่ายทางคลินิกของส่วนหน้าตาโดยทั่วไปของมะเร็งเมลาโนมาชนิดร้ายของเยื่อบุตา (รอยโรคที่ลิมบัส ฟอร์นิกซ์ และคารันเคิล) Koç İ, Kiratlı H. Current Management of Conjunctival Melanoma Part 1: Clinical Features, Diagnosis and Histopathology. Turk J Ophthalmol. 2020;50(5):293-303. Figure 1. PM
CI D: PMC7610047. License: CC BY.
A) มะเร็งเมลาโนมาของเยื่อบุตา ที่ลิมบัส มีรอยโรคสีเข้มนูนร่วมกับหลอดเลือดเลี้ยงที่อุดมสมบูรณ์ B) มะเร็งเมลาโนมาที่ลิมบัส ขนาดใหญ่ที่เกิดบนพื้นหลังของ PAM แบบกระจาย C) มะเร็งเมลาโนมาที่อยู่เฉพาะที่ในฟอร์นิกซ์ D) ภาพถ่ายส่วนหน้าตาแสดงมะเร็งเมลาโนมาที่ลามไปถึงคารันเคิลและรอยพับกึ่งจันทรา สอดคล้องกับตำแหน่งที่เกิดและรูปแบบทางคลินิกของมะเร็งเมลาโนมาชนิดร้ายของเยื่อบุตา ที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
ผู้ป่วยมักมาพบแพทย์เนื่องจากมีรอยโรคสีเข้มใหม่หรือสังเกตเห็นรอยโรคเดิมมีขนาดใหญ่ขึ้น
รู้สึกเป็นจุดหรือก้อน ระคายเคือง ปวด8)
คัน ตาพร่า การมองเห็น ลดลง (ในกรณีที่มีการลุกลามเข้าไปในกระจกตา )8)
บางครั้งมีเลือดออกเมื่อสัมผัส4)
อาจไม่มีอาการและพบโดยบังเอิญจากการตรวจตามปกติ3)
ทางคลินิก รอยโรคเป็นก้อนนูนสีน้ำตาลดำบนเยื่อบุตา ลูกตาหรือเยื่อบุตา เปลือกตา โดยมีหลอดเลือดจำนวนมากมายังเนื้องอก
มะเร็งเมลาโนมาชนิดมีสี (70%)
ตำแหน่งที่พบบ่อย : ประมาณ 90% เกิดขึ้นที่เยื่อบุลูกตาส่วน bulbar, 63% อยู่บริเวณ quadrant ข้างขมับ 4, 6)
ลักษณะภายนอก : รอยโรคแบบนูนขึ้น สีน้ำตาลดำถึงน้ำตาล ร่วมกับมีหลอดเลือดเลี้ยงจำนวนมาก (feeder vessels) มายังเนื้องอก
ความสัมพันธ์กับตาขาว : อาจพบการยึดติดกับตาขาว ระยะห่างเฉลี่ยจากเนื้องอกถึงขอบกระจกตา 2 มม., 61% ถึงขอบกระจกตา 2)
มะเร็งผิวหนังชนิดไม่มีเม็ดสี (30%)
ลักษณะภายนอก : ก้อนสีชมพูถึงแดง มีเม็ดสีน้อยมากหรือไม่มีเลย
ความเสี่ยงในการวินิจฉัยผิด : มักถูกวินิจฉัยผิดเป็นมะเร็งเซลล์สความัส หรือก้อนเยื่อบุลูกตาสีแดงอื่นๆ 3)
การพยากรณ์โรค : รอยโรคที่มีเม็ดสีน้อยหรือไม่มีเม็ดสีอาจสัมพันธ์กับการพยากรณ์โรคที่ไม่ดี
การประเมินด้วยภาพ:
เครื่องตรวจวินิจฉัยด้วยแสงช่วงหน้าตัด (AS-OCT ) : แสดงเป็นรอยโรคที่มีการสะท้อนแสงสูง สามารถประเมินเยื่อโบว์แมน 2) กล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (UBM ) : วัดความหนาของเนื้องอกและตรวจสอบการลุกลามเข้าตาขาว 3)
สำหรับรอยโรคที่มีเม็ดสีที่เยื่อบุลูกตาซึ่งมีการเปลี่ยนแปลงขนาดหรือสีอย่างรวดเร็ว มีเลือดออก หรือเกิดก้อน ควรไปพบจักษุแพทย์ทันที แม้รอยโรคที่มีเม็ดสีซึ่งเปลี่ยนแปลงน้อยก็แนะนำให้ติดตามผลเป็นระยะ
Q
มีมะเร็งผิวหนังเยื่อบุลูกตาที่ไม่มีเม็ดสีหรือไม่?
A
มี ประมาณ 30% ของมะเร็งผิวหนังเยื่อบุลูกตาเป็นชนิดไม่มีเม็ดสี (amelanotic) ปรากฏเป็นก้อนสีชมพูถึงแดง เนื่องจากมีลักษณะคล้ายกับมะเร็งเซลล์สความัส และชนิดอื่นๆ จึงมักถูกวินิจฉัยผิดทำให้การวินิจฉัยล่าช้า การตัดชิ้นเนื้อเพื่อตรวจทางพยาธิวิทยาเป็นสิ่งจำเป็นสำหรับก้อนเยื่อบุลูกตาที่น่าสงสัย
ปัจจัยต่อไปนี้สัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของการแพร่กระจายและการเสียชีวิต1, 4, 5, 6, 8) .
ความหนาของเนื้องอก >2 มม. : HR 1.20 ต่อการเพิ่มขึ้น 1 มม.การบุกลึก : HR 2.35การบุกรุกท่อน้ำเหลือง : HR 7.49การเกิดแผล : HR 7.01เนื้องอก T3 : HR 17.44มะเร็งผิวหนังชนิดก้อนกลม : RR การแพร่กระจาย 6.00–8.44, RR การเสียชีวิต 25.49–35.49ตำแหน่งรอยโรค : ฟอร์นิกซ์และเยื่อบุตา ที่เปลือกตา > เยื่อบุตา ที่ลูกตา รอยโรคที่คารันเคิลมีอัตราการเสียชีวิต 50% ใน 3 ปี พยากรณ์โรคแย่ที่สุดการบุกรุกเบ้าตา การตัดออกไม่สมบูรณ์ : ประมาณ 49.3% ของกรณีที่ตัดออกไม่สมบูรณ์เกิดการกลับเป็นซ้ำมะเร็งผิวหนังชนิดมีเม็ดสีน้อยหรือไม่มีเม็ดสี การสร้างท่อน้ำเหลืองที่เกี่ยวข้องกับเนื้องอก 3)
การจำแนกระยะ AJCC (คณะกรรมการร่วมโรคมะเร็งแห่งสหรัฐอเมริกา) มีความสัมพันธ์อย่างมากกับการพยากรณ์โรค1) .
ระยะ อัตราการเสียชีวิตสะสม 5 ปี cT1 2.5% cT2 28.6% cT3 31.6% cT3c (การลุกลามเข้าสู่เบ้าตา ) 100%
อัตราการแพร่กระจายระยะไกลโดยประมาณที่ 5 ปีสำหรับเนื้องอก T3 คือ 42% และอัตราการเสียชีวิตที่ 5 ปีคือ 23%1) .
การแพร่กระจายทางน้ำเหลืองเป็นเส้นทางหลัก รอยโรคที่เยื่อบุตา ด้านขมับมีแนวโน้มแพร่กระจายไปยังต่อมน้ำเหลืองหน้าใบหู ส่วนรอยโรคด้านจมูกแพร่กระจายไปยังต่อมน้ำเหลืองใต้ขากรรไกร การแพร่กระจายระยะไกล (ทางเลือด) เกิดขึ้นที่สมอง ปอด ตับ ผิวหนัง และต่อมหมวกไต6, 1) การแพร่กระจายไปยังต่อมน้ำเหลืองตรวจพบใน 15-41% ของผู้ป่วยภายใน 2.3 ปีหลังการวินิจฉัย และการแพร่กระจายทั่วร่างกายเกิดขึ้นใน 9-25% ภายใน 3 ปี แม้ว่าจะตรวจไม่พบการแพร่กระจายไปยังต่อมน้ำเหลือง การแพร่กระจายระยะไกลทางเลือดไปยังอวัยวะยังเกิดขึ้นใน 38% ของผู้ป่วย6) .
Q
ปัจจัยใดที่มีผลต่อการพยากรณ์โรคมากที่สุด?
A
ความหนาของเนื้องอก (โดยเฉพาะ >2 มม.) ตำแหน่งรอยโรค (ต่อมน้ำตาที่ขอบตาด้านในมีการพยากรณ์โรคแย่ที่สุด) ระยะ AJCC ลักษณะเป็นก้อน การบุกรุกของหลอดเลือดน้ำเหลือง และการลุกลามเข้าสู่เบ้าตา เป็นปัจจัยพยากรณ์โรคที่ไม่ดีหลัก ความสมบูรณ์ของการตัดออกก็มีผลอย่างมากเช่นกัน โดยประมาณ 49.3% ของกรณีที่ตัดออกไม่สมบูรณ์เกิดการกลับเป็นซ้ำ กรณีที่ต่อมน้ำเหลืองเซนติเนลเป็นบวกมีความเสี่ยงต่อการเสียชีวิตเพิ่มขึ้น
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit-lamp)เครื่องตรวจภาพตัดขวางด้วยแสงช่วงหน้าตา (AS-OCT ) : ประเมินความลึกของรอยโรคและเยื่อโบว์แมน2) กล้องจุลทรรศน์ชีวภาพด้วยคลื่นเสียงความถี่สูง (UBM ) : วัดความหนาของเนื้องอกและตรวจสอบการลุกลามเข้าไปในตาขาว 3) การพลิกหนังตา : จำเป็นเพื่อตรวจสอบการขยายไปยังเยื่อบุตา เปลือกตาและฟอร์นิกซ์การตัดชิ้นเนื้อแบบแผนที่ (Map biopsy) : ยืนยันขอบเขตของ PAM ทางจุลพยาธิวิทยา
เพื่อการวินิจฉัยที่แน่นอน จำเป็นต้องตัดชิ้นเนื้อ ทางจุลพยาธิวิทยา ประกอบด้วยการเพิ่มจำนวนของเซลล์ขนาดใหญ่ที่มีอัตราส่วนนิวเคลียสต่อไซโทพลาสซึมสูง นิวเคลียสชัดเจน และนิวคลีโอลัสเด่น มีเม็ดสีเมลานิน หากมีเมลานินมาก อาจต้องกำจัดเม็ดสีออกจากชิ้นเนื้อทางพยาธิวิทยา
การย้อมสีอิมมูโนฮิสโตเคมีเป็นสิ่งจำเป็นสำหรับการวินิจฉัยที่แน่นอนและการแยกโรค
เครื่องหมาย ลักษณะ หมายเหตุ HMB-45 ให้ผลบวกในเซลล์เมลาโนไซต์ มีประโยชน์ในการวินิจฉัย2, 8) SOX10 ให้ผลบวกในเซลล์เมลาโนไซต์ ความไวสูง 1, 4) Melan-A/MART-1 ให้ผลบวกในเซลล์เมลาโนไซต์ เครื่องหมายที่ใช้ทั่วไป 3, 5, 6) S-100 ให้ผลบวกในเซลล์เมลาโนไซต์ ความไวสูงแต่ความจำเพาะต่ำ 1) PRAM E ให้ผลบวกในมะเร็งผิวหนังเมลาโนมา ให้ผลลบในปาน เครื่องหมายแยกชนิดที่มีประสิทธิภาพมากที่สุด 5) Ki-67 10-15% หรือมากกว่าในมะเร็งผิวหนังเมลาโนมา ดัชนีการเพิ่มจำนวน 3, 4) p16 หายไปในมะเร็งผิวหนังเมลาโนมา คงอยู่ในปาน5)
ในกรณีที่ยืนยันว่าเป็นมะเร็งผิวหนังเมลาโนมา จำเป็นต้องมีการประเมินทั่วร่างกายอย่างเป็นระบบ
PET/CT: เพื่อค้นหาการแพร่กระจายทั่วร่างกาย1, 8)
MRI สมองและเบ้าตา 1, 4)
อัลตราซาวนด์ช่องท้อง เอกซเรย์ทรวงอก6, 4)
การคลำต่อมน้ำเหลือง (ก่อนหู ใต้ขากรรไกร คอ): ทุกครั้งที่มาตรวจผู้ป่วยนอก
อัลตราซาวนด์ต่อมน้ำเหลืองที่คอ: ปีละครั้ง (ในกรณีรุนแรง)6)
ปานเยื่อบุตา (PAM ): รอยโรคแต่กำเนิดที่มีถุงน้ำ
เมลาโนซิสปฐมภูมิที่ได้มา (PAM ): รอยโรคสีแบน เปลี่ยนแปลงขึ้นลงมะเร็งเซลล์สความัส เยื่อบุตา : การแยกจากมะเร็งผิวหนังเมลาโนมาที่ไม่มีสีมีความสำคัญเป็นพิเศษ3) การสร้างเม็ดสีตามเชื้อชาติและการสร้างเม็ดสีจากภายนอก
การผ่าตัดเอาเนื้องออกรวมถึงเนื้อเยื่อรอบข้างเป็นพื้นฐาน การให้ยา MMC และ interferon α-2b เฉพาะที่ระหว่างและหลังผ่าตัดก็มีประสิทธิภาพเช่นกัน ในกรณีที่เนื้องอกกระจายเป็นบริเวณกว้างและมีการลุกลามใต้เยื่อบุตา อย่างมีนัยสำคัญ อาจจำเป็นต้องผ่าตัดเอาสิ่งในเบ้าตา ออก
การผ่าตัดรักษา
ขอบเขตการตัด : ตัดเนื้องอกออกทั้งหมดโดยมีขอบปลอดภัย 3–5 มม.4, 8)
เทคนิคไม่สัมผัส : หลีกเลี่ยงการสัมผัสเนื้องอกโดยตรงด้วยเครื่องมือเพื่อป้องกันการกระจายของเซลล์เนื้องอก4, 8)
เทคนิคแห้ง : ตัดออกโดยไม่ใช้น้ำยาล้าง (BSS)
กรณีที่มีการลุกลามของกระจกตา : ลอกเยื่อบุกระจกตา ด้วยแอลกอฮอล์ + ตัดออกเป็นชิ้นเดียวด้วยมีดฮอกกี้2)
การผ่าตัดเอาสิ่งในเบ้าตา ออก : เหมาะสำหรับกรณีที่แพร่กระจายเป็นบริเวณกว้างและกลับเป็นซ้ำ (กรณีลุกลาม)
การควักลูกตาออก : เหมาะสำหรับกรณีที่มีการลุกลามเข้าไปในลูกตา
การรักษาเสริม
การจี้เย็น เยื่อบุตา ขึ้นเพื่อหลีกเลี่ยงการบาดเจ็บของตาขาว 3)
เคมีบำบัดเฉพาะที่ด้วย MMC :
ระหว่างผ่าตัด: วาง microsponge MMC 0.02% นาน 180 วินาที2)
หลังผ่าตัด: ยาหยอดตา MMC 0.02% 4 ครั้ง/วัน × 7 วัน × 3 รอบ2)
IFNα-2b : ทางเลือกแทน MMC ที่ไม่ทำให้เกิดความเสียหายต่อสเต็มเซลล์ลิมบัส 3)
การฉายรังสีรักษา : การฝังแร่หรือการฉายรังสีจากภายนอก 3)
การตรวจชิ้นเนื้อต่อมน้ำเหลืองเซนติเนล 7)
สำหรับการสร้างเยื่อบุตา ขึ้นใหม่หลังการตัดออกกว้าง ใช้วิธีการดังต่อไปนี้ 4, 5) .
การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ : มีฤทธิ์ต้านการอักเสบ ต้านการเกิดพังผืด และต้านการสร้างเส้นเลือดใหม่การปลูกถ่ายเยื่อบุช่องปาก
การปลูกถ่ายเยื่อบุตา จากตาข้างตรงข้าม
ผลข้างเคียงหลักของยาหยอดตา MMC:
ผลข้างเคียงเล็กน้อย ได้แก่ การระคายเคืองเฉพาะที่ ตาแดง น้ำตาไหล แพ้ยา เยื่อบุตาอักเสบ และกระจกตา อักเสบ และการสึกกร่อนของกระจกตา ผลข้างเคียงรุนแรง ได้แก่ การตีบของจุดน้ำตา ต้อกระจก เยื่อบุตาอักเสบ และกระจกตา อักเสบเรื้อรัง และภาวะเซลล์ต้นกำเนิดลิมบัส ล้มเหลว (สูงถึง 12%) 3) .
อัตราการกลับเป็นซ้ำ: ยังคงสูง 26-60% ใน 5 ปี และ 31-66.4% ใน 10 ปี 3) ดังนั้นการติดตามผลระยะยาวจึงเป็นสิ่งจำเป็น หลังการผ่าตัด จำเป็นต้องตรวจตาเป็นประจำตลอดชีวิต
Q
เทคนิคไม่สัมผัส (no-touch technique) คืออะไร?
A
เป็นเทคนิคที่เนื้องอกถูกตัดออกโดยไม่สัมผัสโดยตรงกับเครื่องมือในระหว่างการผ่าตัด และในสภาพแวดล้อมที่แห้งโดยไม่ใช้น้ำยาล้าง (BSS) เพื่อป้องกันการแพร่กระจายของเซลล์เนื้องอก (การกลับเป็นซ้ำเฉพาะที่หรือการแพร่กระจาย) เนื้องอกถูกตัดออกทั้งหมดเป็นก้อนเดียวโดยมีขอบปลอดภัย 3-5 มม. เพื่อลดความเสี่ยงของการกลับเป็นซ้ำจากการตัดออกไม่หมด เทคนิคนี้แตกต่างโดยพื้นฐานจากการตัดออกทั่วไปในการลดการแพร่กระจายของเซลล์เนื้องอกไปยังเยื่อบุตา
มะเร็งเยื่อบุตา เมลาโนมามีความคล้ายคลึงทางพันธุกรรมกับมะเร็งผิวหนังเมลาโนมา ไม่ใช่มะเร็งยูเวียลเมลาโนมา การกลายพันธุ์ที่ขับเคลื่อนที่เกี่ยวข้องกับรังสียูวี (การเปลี่ยน C>T) ที่สำคัญ ได้แก่ BRAF, NF1 และ RAS เครื่องหมายของมะเร็งยูเวียลเมลาโนมา (BAP1, GNAQ, GNA11, SF3B1) เป็นลบในมะเร็งเยื่อบุตา เมลาโนมา 1) .
ในการศึกษาโดย Lally et al. (2022) จาก 101 ราย พบการกลายพันธุ์ความถี่สูง 4 ชนิด 1) .
การกลายพันธุ์ NF1 (33-50%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยที่สุด
การพยากรณ์โรค : การกลายพันธุ์ NF1 เพียงอย่างเดียวสัมพันธ์กับอัตราการแพร่กระจายต่ำที่ 2 และ 5 ปี
ลักษณะ : สามารถอยู่ร่วมกับการกลายพันธุ์ BRAF มักอยู่ร่วมกับการกลายพันธุ์ ATRX 8) .
การกลายพันธุ์ BRAF (29-46%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยเป็นอันดับสอง การกลายพันธุ์ V600E คิดเป็น 80-90%
การกระจาย : พบได้บ่อยในมะเร็งผิวหนังชนิดเมลาโนมาของเยื่อบุลูกตาบริเวณลูกตา (บริเวณที่โดนแสงแดด) 4) .
การพยากรณ์โรค : ไม่มีความสัมพันธ์อย่างมีนัยสำคัญกับการแพร่กระจายหรือการเสียชีวิต เป็นเป้าหมายของการรักษาแบบมุ่งเป้า (ยาที่ยับยั้ง BRAF)
การกลายพันธุ์ NRAS (11-26%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยเป็นอันดับสาม
การพยากรณ์โรค : เพิ่มความเสี่ยงของการแพร่กระจายและการเสียชีวิต โดยเฉพาะความเสี่ยงเสียชีวิตสูงขึ้นประมาณ 5 เท่า 1) .
ลักษณะ : แยกกันกับการกลายพันธุ์ BRAF (ไม่เกิดร่วมกัน)
การกลายพันธุ์ ATRX (25%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยเป็นอันดับที่สี่
การพยากรณ์โรค : คล้ายกับการกลายพันธุ์ NF1 สัมพันธ์กับอัตราการแพร่กระจายต่ำใน 2 ปีและ 5 ปี
ลักษณะ : มักเกิดร่วมกับการกลายพันธุ์ NF1 8)
การกลายพันธุ์บริเวณโปรโมเตอร์ TERT (c.-124C>T) ส่งผลต่อเอนไซม์ telomerase reverse transcriptase และมีรายงานความสัมพันธ์กับมะเร็งเยื่อบุตา ชนิดแพร่กระจาย1, 8, 6) นอกจากนี้ยังตรวจพบใน PAM ที่มีความผิดปกติของเซลล์ระดับปานกลางถึงรุนแรง (ประมาณ 8%) ซึ่งบ่งชี้ถึงลักษณะของมะเร็งชนิด in situ6) และยังแสดงให้เห็นความสัมพันธ์กับภาระการกลายพันธุ์ของเนื้องอกที่สูง4) พบการกลายพันธุ์ TERT ในมะเร็งเยื่อบุตา 32-64% และความสัมพันธ์กับการพยากรณ์โรคกำลังได้รับความสนใจ8)
มีการยืนยันการแสดงออกของ PD-L1 สูงและชนิดย่อยของการถอดรหัสที่มียีนที่เกี่ยวข้องกับระบบภูมิคุ้มกันจำนวนมาก ซึ่งเป็นพื้นฐานทางเหตุผลสำหรับการใช้ยา checkpoint inhibitor ข้อมูลของ BRAF inhibitor, MEK inhibitor และ PD-L1 inhibitor มีแนวโน้มที่ดีแต่ยังมีจำกัดในปัจจุบัน
Chou et al. (2023) วิเคราะห์โปรไฟล์โมเลกุลของผู้ป่วยมะเร็งเยื่อบุตา ชนิด T3c ในชายอายุ 94 ปี พบการกลายพันธุ์ NF1 และการกลายพันธุ์โปรโมเตอร์ TERT (c.-124C>T, VAF 31.4%) โดย BRAF, NRAS และ cKIT เป็นลบทั้งหมด การรวมกันของการกลายพันธุ์ NF1 และ NRAS ลบถูกพิจารณาว่าเป็นปัจจัยที่ทำให้เกิดการดำเนินโรคที่ดีโดยไม่มีการแพร่กระจาย1)
ยา PD-1 inhibitor (pembrolizumab, nivolumab) และ CTLA-4 inhibitor (ipilimumab) ได้ถูกทดลองใช้ในมะเร็งเยื่อบุตา ชนิดแพร่กระจายและชนิดลุกลามเฉพาะที่4, 8)
รายงานสำคัญ Sagiv et al. (2018) รายงานการรักษาด้วย PD-1 inhibitor ด้วย pembrolizumab หรือ nivolumab ใน 5 ราย โดยบางรายตอบสนองอย่างสมบูรณ์8) การทดลองระยะที่ 2 โดยใช้ axitinib + nivolumab (ในมะเร็งเยื่อเมือกชนิดแพร่กระจายขั้นสูงที่ไม่เคยรักษามาก่อน) กำลังดำเนินอยู่
สูตรการรักษามาตรฐานสำหรับการรักษาทั่วร่างกายของมะเร็งเยื่อบุตา ชนิดแพร่กระจายยังไม่ได้รับการกำหนด จำเป็นต้องพิจารณาอย่างรอบคอบในแต่ละกรณี
ในผู้ป่วยที่มีการกลายพันธุ์ BRAF เป็นบวก ได้มีการทดลองใช้ยายับยั้ง BRAF เพียงอย่างเดียว (vemurafenib) หรือการใช้ร่วมกันของยายับยั้ง BRAF/MEK (dabrafenib + trametinib, encorafenib + binimetinib) 4, 8)
ยาเหล่านี้บางชนิดมีรายงานว่ามีผลทำให้ก้อนเนื้องอกเฉพาะที่เล็กลง แต่ส่วนใหญ่เป็นรายงานผู้ป่วยเดี่ยวหรือจำนวนน้อย และผลลัพธ์ระยะยาวมีจำกัด กำลังศึกษาความเป็นไปได้ของผลเสริมฤทธิ์จากการมุ่งเป้าทั้งวิถี MAPK และ AKT พร้อมกัน 3)
ด้วยการใช้ชุดตรวจอิมมูโนฮิสโตเคมี (PRAM E, p16, HMB-45, Ki-67, Cyclin D1) ทำให้สามารถจำแนกรอยโรคที่ก่อนหน้านี้ถือว่า “ไม่แน่นอน” ได้อีกครั้ง 5) การกำหนดมาตรฐานสากลของการจำแนก C-MIL (รอยโรคเมลาโนไซต์ในเยื่อบุตา ) (WHO ฉบับที่ 5, 2022) ก็กำลังดำเนินการอยู่
Q
สามารถใช้ภูมิคุ้มกันบำบัดสำหรับมะเร็งเมลาโนมาที่เยื่อบุตาได้หรือไม่?
A
จากความคล้ายคลึงทางพันธุกรรมกับมะเร็งเมลาโนมาที่ผิวหนัง (การกลายพันธุ์ BRAF, NF1 , NRAS, การแสดงออกของ PD-L1 สูง) ได้มีการทดลองใช้ยายับยั้ง PD-1 (pembrolizumab, nivolumab), ยายับยั้ง CTLA-4 และยายับยั้ง BRAF ในผู้ป่วยระยะแพร่กระจายและระยะลุกลามเฉพาะที่ อย่างไรก็ตาม ยังไม่มีการทดลองทางคลินิกขนาดใหญ่ หลักฐานในปัจจุบันมีจำกัด และยังไม่มีการกำหนดสูตรการรักษามาตรฐาน การรวบรวมข้อมูลขนาดใหญ่ผ่านการศึกษาร่วมกันหลายสถาบันในระดับนานาชาติเป็นเรื่องเร่งด่วน
Chou LT, Lozeau DF, Boyle NS. A rare case of a long-standing, extensive and invasive conjunctival melanoma without systemic metastasis. Am J Ophthalmol Case Rep. 2023; PMC10121375.
Englisch CN, Berger T, Flockerzi F, et al. Conjunctival melanoma with pronounced central corneal invasion: one-year relapse free follow-up. Am J Ophthalmol Case Rep. 2024; PMC11403272.
Menna F, Tschopp M, Meyer P, et al. A case of conjunctival melanoma presenting as a squamous cell carcinoma. Case Rep Ophthalmol. 2024; PMC11509494.
Okongwu CC, Adewara BA, Olaofe OO, et al. Malignant melanoma of the conjunctiva metastasizing to the submandibular gland. BMC Ophthalmol. 2025; PMC11905526.
Eder A, Milman T, Mudhar HS , et al. Unusual conjunctival melanocytic proliferations: report of five cases and review of the literature. Surv Ophthalmol. 2024; PMC12208716.
Goemaere J, Lauwers N, de Keizer ROB, et al. Bone metastasis in a case of primary acquired melanosis with atypia resulting from conjunctival melanoma. Am J Ophthalmol Case Rep. 2023; PMC9763362.
Vishnevskia-Dai V, Davidy T, Zloto O. Amelanotic conjunctival melanoma in a child. Am J Ophthalmol Case Rep. 2023; PMC9792290.
Butt K, Hussain R, Coupland SE, Krishna Y. Conjunctival melanoma: a clinical review and update. Cancers. 2023;15(3):922.