เนื้องอกเมลาโนไซต์ของเยื่อบุตาถูกแบ่งออกเป็นสามประเภท: ปานชนิดไม่ร้าย, ภาวะเมลาโนซิสปฐมภูมิที่ได้มา (รอยโรคก่อนมะเร็ง), และมะเร็งเมลาโนมาชนิดร้าย
มะเร็งเมลาโนมาของเยื่อบุตา คิดเป็นประมาณ 2% ของเนื้องอกตาทั้งหมด และอุบัติการณ์มีแนวโน้มเพิ่มขึ้น
ประมาณ 60-75% ของมะเร็งเมลาโนมามีต้นกำเนิดจากภาวะเมลาโนซิสปฐมภูมิที่ได้มา (PAM )
พื้นฐานของการรักษาคือการตัดออกทั้งหมดด้วยเทคนิคไม่สัมผัสร่วมกับการจี้เย็น
ความหนาของเนื้องอก, ตำแหน่งของรอยโรค, และการจัดระยะตาม AJCC มีผลอย่างมากต่อการพยากรณ์โรค; รอยโรคที่คารันเคิลมีการพยากรณ์โรคแย่ที่สุด โดยมีอัตราการเสียชีวิต 50% ใน 3 ปี
ทางพันธุกรรม คล้ายกับมะเร็งเมลาโนมาของผิวหนัง โดยมีการกลายพันธุ์ของ BRAF, NF1 , NRAS และ ATRX เป็นตัวขับเคลื่อนหลัก
ภาวะเมลาโนซิสปฐมภูมิที่ได้มา แสดงรูปแบบ “ขึ้นลง” ดังนั้นการหายไปของเม็ดสีไม่ได้หมายถึงการหายขาด และจำเป็นต้องตรวจทางจุลพยาธิวิทยาเป็นระยะ เนื้องอกเมลาโนไซต์ของเยื่อบุตาคือเนื้องอกชนิดไม่ร้ายและร้ายที่มีต้นกำเนิดจากเมลาโนไซต์ของเยื่อบุตา โดยแบ่งออกเป็นสามประเภทหลัก
ปาน (nevus ) : เนื้องอกชนิดไม่ร้ายแต่กำเนิด เป็นเนื้องอกเมลาโนไซต์ของเยื่อบุตาที่พบบ่อยที่สุด โดยมีความเสี่ยงต่อการเปลี่ยนเป็นมะเร็งประมาณ 1%ภาวะเมลาโนซิสปฐมภูมิที่ได้มา เยื่อบุตา (C-MIL)4) และคะแนน C-MIN ≥5 ถือเป็นมะเร็งเมลาโนมาในระยะเริ่มต้น (melanoma in situ)8) มะเร็งเมลาโนมาของเยื่อบุตา (มะเร็งเมลาโนมาชนิดร้าย) : เนื้องอกร้ายที่คิดเป็นประมาณ 2% ของเนื้องอกตาทั้งหมด และ 5-7% ของมะเร็งเมลาโนมาทางตาทั้งหมด 1, 4, 5, 6)
อุบัติการณ์ทั่วโลกของมะเร็งเมลาโนมาเยื่อบุตา อยู่ที่ประมาณ 0.3-0.8 ต่อประชากร 1 ล้านคนต่อปี สูงที่สุดในยุโรปเหนือและอเมริกาเหนือ อุบัติการณ์เพิ่มขึ้นในช่วง 50 ปีที่ผ่านมา ในสหรัฐอเมริกาคาดว่ามีผู้ป่วยรายใหม่ประมาณ 130 รายต่อปี ในยุโรปประมาณ 320 ราย อุบัติการณ์ที่ปรับตามอายุในคนเอเชียต่ำคือ 0.15 ต่อประชากร 1 ล้านคนต่อปี 2) พบมากที่สุดในคนผิวขาว (91.2%) และเพียง 2.4% ในคนแอฟโฟร-แคริบเบียน
อายุเฉลี่ยที่เริ่มป่วยคือ 55-65 ปี พบน้อยมากในผู้ที่มีอายุต่ำกว่า 20 ปี 5) ผู้ป่วยเด็กคิดเป็นเพียง 1% ของมะเร็งเมลาโนมาเยื่อบุตา ทั้งหมด 9) ภาวะเมลาโนซิสที่ได้มาปฐมภูมิ (PAM ) คิดเป็น 11% ของรอยโรคเยื่อบุตา ทั้งหมด 8) และเป็นต้นกำเนิดที่พบบ่อยที่สุดของมะเร็งเมลาโนมา (ประมาณ 60-75%)
การแบ่งตามต้นกำเนิดของมะเร็งเมลาโนมา:
จากภาวะเมลาโนซิสที่ได้มาปฐมภูมิ: ประมาณ 60-75% (พบบ่อยที่สุด)
เกิดใหม่ (de novo): ประมาณ 19%
จากปาน: 7-20%
มะเร็งเมลาโนมาเยื่อบุตา เป็นมะเร็งเมลาโนมาของเยื่อเมือกชนิดเดียวที่เชื่อมโยงกับการได้รับรังสีอัลตราไวโอเลต เนื่องจากเยื่อบุตา ส่วนลูกตาสัมผัสรังสียูวีโดยตรง 6) เมลานินกรองรังสี UVB ได้ประมาณสองเท่า ซึ่งเป็นสาเหตุที่ทำให้อุบัติการณ์ต่ำในคนผิวสี
Q
เนื้องอกของระบบเมลาโนไซต์เยื่อบุตาพบได้บ่อยแค่ไหน?
A
อุบัติการณ์ของมะเร็งเมลาโนมาเยื่อบุตา คือ 0.3-0.8 ต่อประชากร 1 ล้านคนต่อปี ซึ่งเป็นโรคที่ค่อนข้างหายาก แต่เพิ่มขึ้นในช่วง 50 ปีที่ผ่านมา ในทางกลับกัน ปานเป็นเนื้องอกของระบบเมลาโนไซต์เยื่อบุตา ที่พบบ่อยที่สุด และส่วนใหญ่เป็นชนิดไม่ร้ายแรง
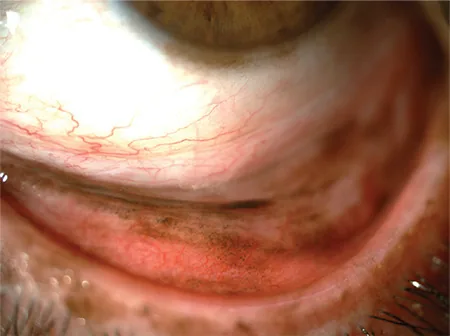
PAM แบบกระจายที่เยื่อบุตาของเปลือกตาล่างและรอยสีที่ขอบกระจกตา Koç İ, et al. Current Management of Conjunctival Melanoma Part 1: Clinical Features, Diagnosis and Histopathology. Turk J Ophthalmol. 2020. Figure 2. PM
CI D: PMC7610047. License: CC BY.
เมื่อพลิกเปลือกตาล่าง จะเห็น PAM แบบกระจายโดยเฉพาะที่เยื่อบุตา ส่วนเปลือกตา และยังสามารถยืนยันรอยสีที่ขอบกระจกตา ได้ ซึ่งสอดคล้องกับภาวะเมลาโนซิสที่ได้มาปฐมภูมิที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
ผู้ป่วยส่วนใหญ่มาพบแพทย์เนื่องจากสังเกตเห็นรอยโรคสีใหม่หรือรอยโรคเดิมมีขนาดใหญ่ขึ้น
รู้สึกมีจุดหรือก้อน ระคายเคือง เจ็บปวด 4)
คัน ตาพร่า สายตาลดลง (ในกรณีที่มีการแทรกซึมของกระจกตา ) 4)
บางครั้งมีเลือดออกเมื่อสัมผัส 6)
อาจไม่มีอาการและพบโดยบังเอิญจากการตรวจสุขภาพหรือการตรวจตามปกติ 5)
เนวัส (Nevus), เมลาโนซิสปฐมภูมิที่ได้มา (Primary Acquired Melanosis) และเมลาโนมา (Melanoma) มีลักษณะทางคลินิกที่แตกต่างกัน
เนวัส (Nevus)
ตำแหน่ง : พบบ่อยที่สุดที่เยื่อบุตา ส่วนลูกตา (bulbar conjunctiva) บริเวณรอยแยกเปลือกตาใกล้ลิมบัส กระจกตา
ซีสต์ : มักมีซีสต์ชนิด inclusion cyst ของเยื่อบุตา ร่วมด้วย (ยืนยันได้ด้วย slit lamp, อัลตราซาวนด์, OCT ส่วนหน้าของลูกตา) การมีซีสต์เป็นสัญญาณสำคัญที่บ่งชี้ถึงความไม่ร้ายแรง
การดำเนินโรค : มีอยู่เป็นเวลานาน (แต่กำเนิด) อาจเปลี่ยนสีและขนาดในช่วงวัยรุ่นเนื่องจากการเปลี่ยนแปลงของฮอร์โมน การเปลี่ยนแปลงอย่างฉับพลันในวัยผู้ใหญ่ทำให้สงสัยว่าจะเป็นมะเร็ง
การแทรกซึมของกระจกตา : พบได้น้อย
เมลาโนซิสปฐมภูมิที่ได้มา (Primary Acquired Melanosis)
ภูมิหลังผู้ป่วย : วัยกลางคนถึงสูงอายุ ส่วนใหญ่เป็นคนผิวขาว มักเป็นข้างเดียวเกือบตลอด
ลักษณะ : รอยโรคสีแบน สีน้ำตาลอ่อนถึงน้ำตาลเข้ม มีหลายเฉดสี
การกระจาย : สามารถเกิดได้ทุกส่วนของเยื่อบุตา ต่อเนื่องหรือไม่ต่อเนื่อง เนื่องจากอาจซ่อนอยู่ในรอยพ้นเยื่อบุตา หรือเยื่อบุตา ส่วนเปลือกตา การพลิกเปลือกตาจึงมีความสำคัญต่อการประเมิน
ดำเนินโรค : อาจแสดงรูปแบบ “wax and wane” (เพิ่มขึ้นและลดลง) การหายไปของเม็ดสีไม่ได้หมายถึงการหายไปของเม็ดสีเมลาโนซิสปฐมภูมิที่ได้มา 8)
มะเร็งเมลาโนมาของเยื่อบุตา
ตำแหน่งที่พบบ่อย : ประมาณ 90% เกิดที่เยื่อบุตา ลูกตา และ 63% อยู่ที่จตุภาคขมับ 4, 6)
ลักษณะ : มีเม็ดสี (70%) หรือไม่มีเม็ดสี (30%) 5) ชนิดไม่มีเม็ดสีจะเป็นก้อนสีชมพูถึงแดง และบางครั้งอาจถูกวินิจฉัยผิดว่าเป็นมะเร็งเซลล์สความัส
ลักษณะเฉพาะ : เป็นก้อนกลมหรือแบน มักมีหลอดเลือดเลี้ยง (feeder vessels) ร่วมด้วย ยึดติดกับตาขาว ระยะห่างเฉลี่ยจากเนื้องอกถึงขอบกระจกตา คือ 2 มม. 61% ถึงขอบกระจกตา 4)
การประเมินด้วยภาพ : ในการตรวจเอกซเรย์การเชื่อมโยงกันด้วยแสงของส่วนหน้า (AS-OCT ) จะเห็นเป็นรอยโรคสะท้อนแสงสูง และสามารถประเมินเยื่อโบว์แมนได้ 4) ในการตรวจกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ (UBM ) สามารถยืนยันความหนาของเนื้องอกและการบุกรุกของตาขาว ได้ 5)
Q
รอยโรคที่มีเม็ดสีที่เยื่อบุตาทั้งหมดเป็นมะเร็งหรือไม่?
A
ไม่ใช่ ในบรรดารอยโรคที่มีเม็ดสีของเยื่อบุตา ปานธรรมดา (nevus ) ที่ไม่เป็นอันตรายพบได้บ่อยที่สุด และความเสี่ยงโดยรวมของการเปลี่ยนเป็นมะเร็งมีเพียงประมาณ 1% เท่านั้น ตำแหน่งของรอยโรค การมีถุงน้ำ เวลาที่เริ่มมีอาการ และรูปแบบการเปลี่ยนแปลงมีความสำคัญในการแยกแยะระหว่างชนิดไม่ร้ายและร้าย หากมีการเปลี่ยนแปลงที่น่าสงสัย แนะนำให้พบผู้เชี่ยวชาญ
ปัจจัยต่อไปนี้สัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของการแพร่กระจายและการเสียชีวิต 1, 4, 5, 6, 8)
ความหนาของเนื้องอก >2 มม. : HR 1.20 ต่อการเพิ่มขึ้น 1 มม.การบุกรุกลึก : HR 2.35การบุกรุกท่อน้ำเหลือง : HR 7.49แผลเปื่อย : HR 7.01เนื้องอก T3 : HR 17.44มะเร็งผิวหนังชนิดปม : ความเสี่ยงการแพร่กระจาย RR 6.00–8.44 ความเสี่ยงเสียชีวิต RR 25.49–35.49ตำแหน่งรอยโรค : ฟอร์นิกซ์และเยื่อบุตา หนังตา > เยื่อบุตา ลูกตา รอยโรคที่คารันเคิลมีการพยากรณ์โรคแย่ที่สุด โดยมีอัตราการเสียชีวิต 50% ใน 3 ปีการลุกลามเข้าสู่เบ้าตา การตัดออกไม่สมบูรณ์ : ประมาณ 49.3% ของกรณีที่ตัดออกไม่สมบูรณ์เกิดการกลับเป็นซ้ำมะเร็งผิวหนังชนิดมีเม็ดสีน้อย/ไม่มีเม็ดสี การสร้างหลอดน้ำเหลืองที่เกี่ยวข้องกับเนื้องอก 5)
การแบ่งระยะตาม AJCC มีความสัมพันธ์อย่างมากกับการพยากรณ์โรค1) .
ระยะ อัตราการเสียชีวิตสะสม 5 ปี cT1 2.5% cT2 28.6% cT3 31.6% cT3c (การลุกลามเข้าสู่เบ้าตา ) 100%
อัตราการแพร่กระจายระยะไกลโดยประมาณที่ 5 ปีสำหรับเนื้องอก T3 คือ 42% และอัตราการเสียชีวิตที่ 5 ปีคือ 23%1) .
การแพร่กระจายทางน้ำเหลืองเป็นเส้นทางหลัก รอยโรคที่เยื่อบุตา บริเวณขมับมีแนวโน้มแพร่กระจายไปยังต่อมน้ำเหลืองหน้าใบหู ส่วนรอยโรคที่เยื่อบุตา บริเวณจมูกมีแนวโน้มแพร่กระจายไปยังต่อมน้ำเหลืองใต้ขากรรไกร การแพร่กระจายระยะไกล (ทางเลือด) เกิดขึ้นที่สมอง ปอด ตับ ผิวหนัง ต่อมหมวกไต หัวใจ เยื่อบุช่องท้อง ตับอ่อน ลำไส้ ไต กระดูก ม้าม เป็นต้น6, 1) พบการแพร่กระจายของต่อมน้ำเหลืองใน 15-41% ของผู้ป่วยภายใน 2.3 ปีหลังการวินิจฉัย และการแพร่กระจายทั่วร่างกายเกิดขึ้นใน 9-25% ภายใน 3 ปี แม้ว่าจะตรวจไม่พบการแพร่กระจายของต่อมน้ำเหลือง แต่การแพร่กระจายทางเลือดไปยังอวัยวะระยะไกลก็เกิดขึ้นใน 38% ของผู้ป่วย8) .
Q
ปัจจัยใดที่มีผลต่อการพยากรณ์โรคของมะเร็งผิวหนังชนิดเมลาโนมาที่เยื่อบุตามากที่สุด?
A
ความหนาของเนื้องอก (โดยเฉพาะ >2 มม.), ตำแหน่งของรอยโรค (ต่อมน้ำตาที่ขอบตามีการพยากรณ์โรคแย่ที่สุด), ระยะ AJCC, ลักษณะเป็นก้อน, การลุกลามเข้าสู่ท่อน้ำเหลืองและหลอดเลือด, และการลุกลามเข้าสู่เบ้าตา เป็นปัจจัยพยากรณ์โรคที่ไม่ดีหลัก ความสมบูรณ์ของการตัดออกก็มีผลอย่างมากเช่นกัน ในกรณีที่ตัดออกไม่สมบูรณ์ ประมาณ 49.3% จะเกิดการกลับเป็นซ้ำ
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit-lamp)การตรวจด้วยเครื่องเอกซเรย์การเชื่อมโยงกันด้วยแสงของส่วนหน้าดวงตา (AS-OCT ) : ประเมินความลึกของรอยโรคและเยื่อโบว์แมน ปรากฏเป็นรอยโรคที่มีการสะท้อนแสงสูง4) การตรวจด้วยกล้องจุลทรรศน์ชีวภาพด้วยคลื่นเสียงความถี่สูง (UBM ) : วัดความหนาของเนื้องอกและตรวจสอบการลุกลามเข้าสู่ตาขาว 5) การตรวจด้วยคลื่นเสียงความถี่สูง : ตรวจหาถุงน้ำในปานการพลิกหนังตา : จำเป็นเนื่องจาก Primary acquired melanosis อาจซ่อนอยู่ใน fornix และเยื่อบุตา หนังตาการบันทึกภาพถ่าย : การประเมินการเปลี่ยนแปลงอย่างเป็นกลางระหว่างการติดตามผล
ในกรณี melanoma ที่ได้รับการยืนยัน จำเป็นต้องมีการประเมินทั่วร่างกายอย่างเป็นระบบ
PET/CT: เพื่อค้นหาการแพร่กระจายทั่วร่างกาย 1, 9)
MRI สมองและเบ้าตา 1, 4)
อัลตราซาวนด์ช่องท้อง, เอกซเรย์ทรวงอก 6, 4)
การคลำต่อมน้ำเหลือง (ก่อนหู, ใต้ขากรรไกร, คอ): ทุกครั้งที่มาพบแพทย์ผู้ป่วยนอก
อัลตราซาวนด์ต่อมน้ำเหลืองที่คอ (ปีละครั้งในกรณี Primary acquired melanosis รุนแรง/melanoma) 8)
เพื่อการวินิจฉัยที่แน่นอน จำเป็นต้องตัดชิ้นเนื้อตรวจ
ผลทางจุลพยาธิวิทยาของปาน:
กลุ่มเซลล์ปานในบริเวณรอยต่อหรือใต้เยื่อบุผิว
ถุงน้ำรวมเยื่อบุตา เป็นลักษณะเฉพาะ
ผลทางจุลพยาธิวิทยาของ Primary acquired melanosis:
ไม่มี atypia: การเพิ่มจำนวนของเมลาโนไซต์น้อยที่สุดในชั้นเบซัลของเยื่อบุผิว
มี atypia: กลุ่มเซลล์เดี่ยว/รวมตัวของเมลาโนไซต์ที่ผิดปกติ, การแพร่กระจายแบบ Pagetoid, เซลล์ขนาดใหญ่ผิดปกติ, นิวคลีโอลัสชัดเจน, อัตราส่วนนิวเคลียสต่อไซโทพลาสซึมสูง, ภาพไมโทซิส
ผลการตรวจทางจุลพยาธิวิทยาของมะเร็งผิวหนังเมลาโนมา:
การบุกรุกของเซลล์เมลาโนมาเข้าสู่ชั้นใต้เยื่อบุผิว
นิวเคลียสเพลโอมอร์ฟิก, นิวเคลียสขนาดใหญ่, นิวคลีโอลัสเด่นชัด, กิจกรรมไมโทติก, ไซโทพลาสซึมมาก5)
การเพิ่มจำนวนแบบ Pagetoid, การแพร่กระจายในแนวรัศมีภายในเยื่อบุผิว, การอักเสบเป็นแถบในชั้นเบซัล5)
อิมมูโนฮิสโตเคมีมีความจำเป็นสำหรับการวินิจฉัยที่แน่ชัดและการแยกความแตกต่างระหว่างชนิดไม่ร้ายแรงและร้ายแรง องค์การอนามัยโลกฉบับที่ 5 ได้นำอิมมูโนฮิสโตเคมีของเครื่องหมายเมลาโนไซต์มาใช้เป็นเกณฑ์การวินิจฉัยที่พึงประสงค์8) .
เครื่องหมาย ปาน เมลาโนมา หมายเหตุ S100 + + พบได้ทั่วไปในสายเมลาโนไซต์1) SOX10 + + ที่พบร่วมในเซลล์เม็ดสี1, 4) HMB45 + + ที่พบร่วมในเซลล์เม็ดสี1, 3, 9) Melan-A/MART-1 + + ที่พบร่วมในเซลล์เม็ดสี3, 5, 6) Ki-67 ต่ำ 10–15% หรือมากกว่า ดัชนีการเพิ่มจำนวน3, 4) p16 คงอยู่ หายไป ยับยั้งเนื้องอก7) PRAM E − + เครื่องหมายแยกชนิดที่ทรงพลังที่สุด7) bcl2 − บวกปานกลางถึงรุนแรง ยับยั้งการตายของเซลล์แบบโปรแกรม 3)
มีรอยโรคที่ไม่สามารถจำแนกได้ชัดเจนว่าเป็นชนิดไม่ร้ายหรือร้าย7) .
ปานเจาะลึก (deep penetrating nevus , DPN) : การกระตุ้นวิถี WNT/β-catenin, การกลายพันธุ์ BRAF V600E บวกทุกราย, การกลายพันธุ์ NRAS ลบ, PRAM E ลบ, Ki-67 ต่ำ. หญิง:ชาย = 1.3:1, อายุเฉลี่ย 25 ปี. ไม่มีรายงานการกลับเป็นซ้ำหรือแพร่กระจายหลังการตัดออก.มะเร็งผิวหนังชนิดเนวอยด์ (nevoid melanoma) : ลักษณะคล้ายปานแต่มีพฤติกรรมร้าย สูญเสีย p16, PRAM E บวก, Ki-67 สูง เกี่ยวข้องกับการยับยั้ง BAP1 การจัดการเหมือนมะเร็งผิวหนัง
รอยดำที่สัมพันธ์กับสีผิว (complexion-associated melanosis)
เอ็นแอ็กเซนเฟลด์ที่มีสี
มะเร็งเซลล์สความัส ของเยื่อบุตา → การแยกจากมะเร็งผิวหนังชนิดไม่มีสีสำคัญเป็นพิเศษ5) รอยดำทุติยภูมิ (รอยดำจากภายนอก เช่น มาสคาร่า)
การลุกลามใต้เยื่อบุตา ของเนื้องอกในลูกตาที่มีสี
โดยปกติเพียงเฝ้าสังเกตรวมถึงบันทึกภาพ พิจารณาตัดออกหากมีการโตหรือเปลี่ยนสี แต่การเปลี่ยนแปลงในวัยรุ่นมักเกิดจากการเปลี่ยนแปลงของฮอร์โมน การอักเสบ หรือถุงน้ำโต การเปลี่ยนแปลงเฉียบพลันในผู้ใหญ่เป็นตัวบ่งชี้ถึงความร้าย
การตัดชิ้นเนื้อ : ทำการตัดชิ้นเนื้อแบบกรีด/ตัดออก/แผนที่อย่างระมัดระวังในรอยโรคที่สงสัยการผ่าตัด : เพิ่มการจี้เย็น ที่ขอบตัดตามบริเวณที่สงสัยทางคลินิกเคมีบำบัดเฉพาะที่ : พิจารณาให้ไมโตมัยซิน C หรืออินเตอร์เฟอรอนอัลฟา-2บีเฉพาะที่สำหรับเมลาโนซิสปฐมภูมิที่ได้มา ซึ่งพิสูจน์แล้วว่ามี atypia ทางจุลพยาธิวิทยา
ไมโตมัยซิน C 0.02%: หลายรอบ 5 ครั้ง/วัน นาน 1 สัปดาห์8)
เฉพาะรอยโรคที่จำกัดอยู่ภายในเยื่อบุผิวเท่านั้นที่เข้าข่าย (ไม่เหมาะสมสำหรับมะเร็งผิวหนังชนิดลุกลาม)
ข้อควรระวังในการติดตามผล : การหายไปของเม็ดสีเนื่องจาก “การขึ้นลง” ของปานสีดำที่ได้มาปฐมภูมิไม่ได้หมายความว่ารอยโรคจะหายไป หลังการรักษาด้วยไมโตมัยซิน ซี ควรยืนยันการกำจัดปานสีดำที่ได้มาปฐมภูมิด้วยการตัดชิ้นเนื้อแบบแผนที่8)
การตัดออกทั้งหมดโดยการผ่าตัดเป็นทางเลือกแรก หลักการต่อไปนี้มีความสำคัญ:
ขอบเขตการตัด : ตัดก้อนเนื้อออกทั้งหมดโดยมีขอบปลอดภัย 3-5 มม. (เอกสารบางฉบับระบุ 2-4 มม.5) )เทคนิคไม่สัมผัส : หลีกเลี่ยงการสัมผัสก้อนเนื้อโดยตรงด้วยเครื่องมือเพื่อป้องกันการแพร่กระจายของเซลล์มะเร็ง5, 9) เทคนิคแห้ง : ตัดออกโดยไม่ใช้น้ำยาล้าง (BSS)กรณีที่มีการลุกลามถึงตาขาว : ทำการตัดตาขาว และเยื่อบุตา ออกกรณีที่มีการลุกลามถึงกระจกตา : แนะนำให้ลอกเยื่อบุกระจกตา ด้วยแอลกอฮอล์ และตัดส่วนกระจกตา ออกเป็นชิ้นเดียวด้วยมีดฮอกกี้4)
การจี้เย็น :เยื่อบุตา ขึ้นเพื่อหลีกเลี่ยงการบาดเจ็บที่ตาขาว 5)
เคมีบำบัดเฉพาะที่ด้วยไมโตมัยซิน ซี:
ระหว่างผ่าตัด: ใช้ไมโครสปองจ์ไมโตมัยซิน ซี 0.02% นาน 180 วินาที4)
หลังผ่าตัด: ยาหยอดตาไมโตมัยซิน ซี 0.02% 4 ครั้ง/วัน นาน 7 วัน พัก 1 สัปดาห์ รวม 3 รอบ4)
ขนาดยามีตั้งแต่ 0.002% ถึง 0.04% ตามรายงาน5)
อัตราการกลับเป็นซ้ำหลังการรักษาเบื้องต้นด้วยไมโตมัยซิน C อยู่ที่ 33–100% และเมื่อเป็นการรักษาเสริมอยู่ที่ 0–66%5)
อินเตอร์เฟอรอน อัลฟา-2บี:
เนื่องจากไม่ทำให้เกิดความเสียหายต่อเซลล์ต้นกำเนิดลิมบัส จึงถือเป็นทางเลือกแทนไมโตมัยซิน C5)
การฉายรังสี:
การฝังแร่ (brachytherapy) หรือการฉายรังสีจากภายนอก5)
สำหรับการสร้างเยื่อบุตา ใหม่หลังการตัดออกกว้าง ใช้วิธีการดังต่อไปนี้4, 5) :
การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ: มีฤทธิ์ต้านการอักเสบ ต้านการเกิดพังผืด และต้านการสร้างเส้นเลือดใหม่การปลูกถ่ายเยื่อบุช่องปาก
การปลูกถ่ายเยื่อบุตา จากตาอีกข้าง
การเอาสิ่งในเบ้าตา ออก: บ่งชี้ในกรณีที่กว้าง/กลับเป็นซ้ำ หลังการตัดออกเพื่อสร้างใหม่ ใช้แผ่นปิด เช่น แผ่นปิดแขนท่อนปลายแนวรัศมีอิสระ แผ่นปิดพังผืดขมับ-ขม่อม และแผ่นปิดต้นขาด้านหน้าด้านข้าง2) การตัดลูกตาออก: บ่งชี้ในกรณีที่มีการลุกลามเข้าไปในลูกตา
ในกรณีที่ความหนาของเนื้องอกมากกว่า 2 มม. ควรพิจารณาทำการตรวจชิ้นเนื้อต่อมน้ำเหลืองเซนทิเนล9)
ผลข้างเคียงหลักของยาหยอดตาไมโตมัยซิน C:
ผลข้างเคียงเล็กน้อย ได้แก่ การระคายเคืองเฉพาะที่ ตาแดง น้ำตาไหล แพ้ยา เยื่อบุตาอักเสบ กระจกตา ถลอก ผลข้างเคียงรุนแรง ได้แก่ การตีบของจุดน้ำตา ต้อกระจก เยื่อบุตาอักเสบ เรื้อรัง ภาวะเซลล์ต้นกำเนิดลิมบัส ล้มเหลว (สูงสุด 12%)5)
อัตราการกลับเป็นซ้ำ: ยังคงสูง 26–60% ใน 5 ปี และ 31–66.4% ใน 10 ปี5) จึงจำเป็นต้องติดตามผลในระยะยาว
Q
เทคนิค "ไม่สัมผัส" ในการผ่าตัดมะเร็งเยื่อบุตาชนิดเมลาโนมาคืออะไร?
A
เพื่อป้องกันการแพร่กระจายของเซลล์เนื้องอก (การกลับเป็นซ้ำเฉพาะที่หรือการแพร่กระจายเนื่องจากการเพาะเชื้อ) เทคนิคนี้ทำโดยไม่สัมผัสเนื้องอกโดยตรงด้วยเครื่องมือระหว่างการผ่าตัด และในสภาพแวดล้อมที่แห้งโดยไม่ใช้น้ำยาล้าง (BSS) เนื้องอกจะถูกตัดออกทั้งหมดเป็นก้อนเดียวโดยมีขอบปลอดภัย 3-5 มม. เพื่อลดความเสี่ยงของการกลับเป็นซ้ำเนื่องจากการตัดออกไม่สมบูรณ์
มะเร็งเยื่อบุตา ชนิดเมลาโนมามีความคล้ายคลึงทางพันธุกรรมกับมะเร็งผิวหนังชนิดเมลาโนมา ไม่ใช่มะเร็งคอรอยด์ ชนิดเมลาโนมา การกลายพันธุ์ขับเคลื่อนที่เกี่ยวข้องกับรังสียูวีส่วนใหญ่คือ BRAF, NF1 และ RAS เครื่องหมายของมะเร็งคอรอยด์ ชนิดเมลาโนมา (BAP1, GNAQ, GNA11, SF3B1) ได้รับการยืนยันว่าเป็นลบในมะเร็งเยื่อบุตา ชนิดเมลาโนมา1)
ในการศึกษาโดย Lally et al. (2022) ใน 101 ราย มีการระบุการกลายพันธุ์ความถี่สูงสี่ชนิด1)
การกลายพันธุ์ NF1 (39%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยที่สุด
การพยากรณ์โรค : การกลายพันธุ์ NF1 เพียงอย่างเดียวสัมพันธ์กับอัตราการแพร่กระจายต่ำที่ 2 และ 5 ปี
ลักษณะ : ไม่มีการแยกกันโดยสมบูรณ์กับการกลายพันธุ์ BRAF (สามารถอยู่ร่วมกันได้)
การกลายพันธุ์ BRAF (31%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยเป็นอันดับสอง การกลายพันธุ์ V600E คิดเป็น 80-90%
การกระจาย : พบได้บ่อยในมะเร็งเยื่อบุตา ชนิดเมลาโนมาที่ลูกตา (บริเวณที่โดนแสงแดด)6)
การพยากรณ์โรค : ไม่มีความสัมพันธ์ที่มีนัยสำคัญกับการแพร่กระจายหรือการเสียชีวิต เป็นเป้าหมายการรักษาสำหรับการรักษาแบบมุ่งเป้า (ยาที่ยับยั้ง BRAF)
การกลายพันธุ์ NRAS (26%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยเป็นอันดับสาม
การพยากรณ์โรค : เพิ่มความเสี่ยงต่อการแพร่กระจายและการเสียชีวิต โดยเฉพาะความเสี่ยงต่อการเสียชีวิตประมาณ 5 เท่า
ลักษณะ : ไม่เกิดร่วมกับการกลายพันธุ์ BRAF
การกลายพันธุ์ ATRX (25%)
ความถี่ : การกลายพันธุ์ที่พบบ่อยเป็นอันดับสี่
การพยากรณ์โรค : เช่นเดียวกับการกลายพันธุ์ NF1 สัมพันธ์กับอัตราการแพร่กระจายต่ำใน 2 ปีและ 5 ปี
การกลายพันธุ์ TERT c.-124C>T ส่งผลต่อเอนไซม์ telomerase reverse transcriptase และมีรายงานว่าเกี่ยวข้องกับมะเร็งเยื่อบุตา ชนิดแพร่กระจาย 1, 8, 6) นอกจากนี้ยังตรวจพบในภาวะเมลาโนซิสที่ได้มาแบบปฐมภูมิที่มีความผิดปกติของเซลล์ระดับปานกลางถึงรุนแรง ซึ่งบ่งชี้ถึงลักษณะของมะเร็งเมลาโนมาในระยะเริ่มต้น (melanoma in situ) 8) และยังแสดงให้เห็นถึงความสัมพันธ์กับภาระการกลายพันธุ์ของเนื้องอกที่สูง 6)
Chou et al. (2023) วิเคราะห์โปรไฟล์โมเลกุลของผู้ป่วยมะเร็งเยื่อบุตา ระยะ T3c ในชายอายุ 94 ปี พวกเขาระบุการกลายพันธุ์ NF1 (c.4339C>T, VAF 31.5%; c.5606T>A, VAF 32.0%) และการกลายพันธุ์โปรโมเตอร์ TERT (c.-124C>T, VAF 31.4%) โดยที่ BRAF, NRAS และ cKIT เป็นลบทั้งหมด การรวมกันของการกลายพันธุ์ NF1 และ NRAS ที่เป็นลบถูกอภิปรายว่าเป็นปัจจัยหนึ่งที่ทำให้เกิดการดำเนินโรคที่ค่อนข้างดีโดยไม่มีการแพร่กระจาย 1)
การแสดงออกของ PD-L1 ที่สูงและการมีอยู่ของชนิดย่อยการถอดรหัสที่อุดมไปด้วยยีนที่เกี่ยวข้องกับระบบภูมิคุ้มกันได้รับการยืนยันแล้ว ซึ่งเป็นเหตุผลทางทฤษฎีสำหรับการใช้สารยับยั้งจุดตรวจภูมิคุ้มกัน ข้อมูลของสารยับยั้ง BRAF สารยับยั้ง MEK และสารยับยั้ง PD-L1 มีแนวโน้มที่ดี แต่ยังมีจำกัดในปัจจุบัน
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
ยับยั้ง PD-1 (pembrolizumab, nivolumab) กำลังถูกทดลองใช้ในมะเร็งเยื่อบุตา ชนิดเมลาโนมาที่มีการแพร่กระจาย 5) นอกจากนี้ยังมีรายงานเกี่ยวกับยับยั้งจุดตรวจภูมิคุ้มกันแบบนีโอแอดจูแวนต์ (ก่อนผ่าตัด) 4)
ในกรณีที่มีการแพร่กระจายไปยังกระดูกจากเมลาโนซิสที่ได้มาแบบปฐมภูมิของ Goemaere et al. (2023) ได้ให้ nivolumab และการฉายรังสีที่กระดูกสันหลัง ตามด้วย paclitaxel + carboplatin และสุดท้ายเปลี่ยนไปสู่การดูแลแบบประคับประคอง 8) ยังไม่มีการกำหนดสูตรมาตรฐานสำหรับการรักษาทั่วร่างกายสำหรับมะเร็งเยื่อบุตา ชนิดเมลาโนมาที่แพร่กระจาย
กำลังทดลองใช้ยับยั้ง BRAF ในกรณีที่มีการกลายพันธุ์ BRAF เป็นบวก กำลังศึกษาความเป็นไปได้ของผลเสริมฤทธิ์กันโดยการกำหนดเป้าหมายวิถี MAPK และ AKT พร้อมกัน 5)
ด้วยการใช้ชุดตรวจอิมมูโนฮิสโตเคมี (PRAM E, p16, HMB45, Ki-67, beta-catenin, Cyclin D1) ทำให้รอยโรคที่ก่อนหน้านี้ถือว่า “ไม่แน่นอน” สามารถจำแนกใหม่ได้ 7)
Eder et al. (2024) ยืนยันโดยการวิเคราะห์ FISH ใน 34 รายของ DPN ว่าทุกกรณีเป็นบวกต่อ BRAF V600E และลบต่อ NRAS Q61R นอกจากนี้ยังมีการเสนอความเป็นไปได้ในการแยกแยะระหว่างชนิดไม่ร้ายและร้ายโดยใช้โปรไฟล์ microRNA 7, 8) การวิเคราะห์ FISH รวมถึงการประเมิน RREB 1 (6p25), CCND1 (11q13), MYB (6q23), MYC (8q24)
Vishnevskia-Dai et al. (2023) รายงานเด็กชายอายุ 7 ปีที่มีเมลาโนมาแบบ de novo ไม่มีสี (8 มม. × 2.5 มม.) ที่เยื่อบุตา ส่วนจมูก ทำการตัดออกด้วยเทคนิคไม่สัมผัสและขอบ 4 มม. การจี้เย็น และการปลูกถ่ายเยื่อหุ้มน้ำคร่ำ โดยไม่มีการกลับเป็นซ้ำนาน 73 เดือน 9) ในผู้ป่วยเด็ก การแยกความแตกต่างทางจุลกายวิภาคจากปาน Spitz มีความสำคัญเป็นพิเศษ
การปลูกถ่ายเยื่อหุ้มน้ำคร่ำหลังการตัดออกกว้างให้การสร้างเยื่อบุผิวที่ดี แต่มีรายงานภาวะพร่องเซลล์ต้นกำเนิดลิมบัส เล็กน้อย เยื่อบุตาอักเสบ และกระจกตา อักเสบแบบเป็นแผลเป็น และการกลับเป็นซ้ำเฉพาะที่ที่พบได้น้อย 5)
Q
สามารถใช้ภูมิคุ้มกันบำบัดสำหรับมะเร็งเยื่อบุตาชนิดเมลาโนมาได้หรือไม่?
A
จากความคล้ายคลึงทางพันธุกรรมกับเมลาโนมาที่ผิวหนัง (การกลายพันธุ์ BRAF, NF1 , NRAS, การแสดงออกของ PD-L1 สูง) ยับยั้ง PD-1 (pembrolizumab, nivolumab ฯลฯ) และยับยั้ง BRAF กำลังถูกทดลองใช้ในกรณีที่มีการแพร่กระจาย อย่างไรก็ตาม ยังไม่มีการทดลองทางคลินิกขนาดใหญ่ หลักฐานในปัจจุบันมีจำกัด และยังไม่มีการกำหนดสูตรการรักษามาตรฐาน
Chou LT, Lozeau DF, Boyle NS. A rare case of a long-standing, extensive and invasive conjunctival melanoma without systemic metastasis. Am J Ophthalmol Case Rep. 2023; PMC10121375.
Tan JA, Khoo ET, Al-Chalabi MM, et al. Orbital exenteration and reconstruction using a free radial forearm flap in conjunctival melanoma. Cureus. 2023; PMC10460132.
Montazer F, Heshmati SM, Asgari S, et al. Conjunctival melanoma: a case presentation. Iran J Pathol. 2023; PMC10646746.
Englisch CN, Berger T, Flockerzi F, et al. Conjunctival melanoma with pronounced central corneal invasion: one-year relapse free follow-up. Am J Ophthalmol Case Rep. 2024; PMC11403272.
Menna F, Tschopp M, Meyer P, et al. A case of conjunctival melanoma presenting as a squamous cell carcinoma. Case Rep Ophthalmol. 2024; PMC11509494.
Okongwu CC, Adewara BA, Olaofe OO, et al. Malignant melanoma of the conjunctiva metastasizing to the submandibular gland. BMC Ophthalmol. 2025; PMC11905526.
Eder A, Milman T, Mudhar HS , et al. Unusual conjunctival melanocytic proliferations: report of five cases and review of the literature. Surv Ophthalmol. 2024; PMC12208716.
Goemaere J, Lauwers N, de Keizer ROB, et al. Bone metastasis in a case of primary acquired melanosis with atypia resulting from conjunctival melanoma. Am J Ophthalmol Case Rep. 2023; PMC9763362.
Vishnevskia-Dai V, Davidy T, Zloto O. Amelanotic conjunctival melanoma in a child. Am J Ophthalmol Case Rep. 2023; PMC9792290.